文档内容
姓 名
机密★启用前
准考证号
高三化学
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需
改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在
本试卷上无效。
3.考试结束后,将本试题卷和答题卡一并交回。
可能用到的相对原子质量:H~1 B~11 C~12 N~14 O~16 Na~23 P~31
S~32 Cl~35.5 V~51 Cu~64 Ag~108
一、选择题(本题共14小题,每小题3分,共42分。每小题只有一个选项符合题目要求)
1.新型材料是支撑现代科技发展的关键基础,在信息、能源、基建等领域应用广泛。下列关于新型
材料与传统材料的说法中,正确的是
A.压电陶瓷能实现机械能与电能的相互转化
B.以黏土和石英为主要原料的普通水泥大量用于建筑和水利工程
C.量子通信材料螺旋碳纳米管属于胶体分散系,该材料具有较强的吸附能力
D.生产集成电路底板的酚醛树脂属于聚酯类化合物
2.下列化学用语表示正确的是
A. SO₃的 VSEPR 的的:
B.对羟基苯甲醛的结构简式:
C.基态Cu⁺的价电子排布图:
D.用电子云轮廓图示意p-pσ键的形成:
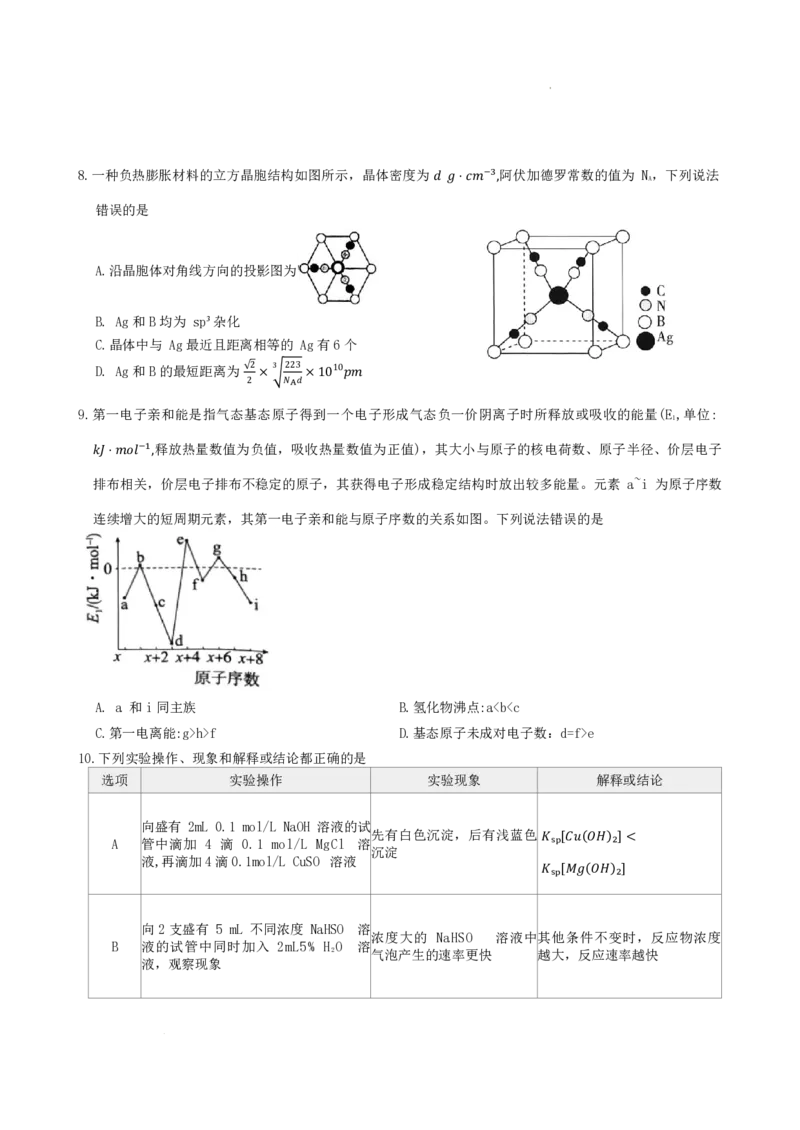
3.下列实验设计或操作合理的是
A.证明非金属性:S> Si B.制备 AlCl₃ 固体 C.吸收尾气 HS D.测定氨水的浓度
2
学科网(北京)股份有限公司4.依据下列事实进行的推测不合理的是
选项 事实 推测
A Na、Al通常用电解法冶炼 Mg通常也可用电解法冶炼
B 室温下 遇浓盐酸生成 室温下 遇浓硝酸生成
C 离子键的百分数:NaCl>NaI 离子键的百分数:
𝑁𝑁𝑁𝑁₃ 𝑁𝑁𝑁𝑁₄𝐶𝐶𝐶𝐶 𝑁𝑁𝑁𝑁₃ 𝑁𝑁𝑁𝑁₄𝑁𝑁𝑁𝑁₃
D 碱性:NaOH>LiOH 碱性:
𝑀𝑀𝑀𝑀𝑁𝑁 > 𝑁𝑁𝑁𝑁₂𝑁𝑁
5.若用 NA表示阿伏加德罗常数的值,下列叙述错误的是 𝑆𝑆𝑆𝑆(𝑁𝑁𝑁𝑁)₂> 𝐶𝐶𝑁𝑁(𝑁𝑁𝑁𝑁)₂
A.10g溶质质量分数为46%的乙醇水溶液中含有的氢原子数目为1.2N
A
和Na HPO₃的 固体混合物中所含阴、阳离子的总数目为3N
2 A
C
𝐵𝐵
.
.
常
14
温
2𝑀𝑀
下
𝑁𝑁
,
𝑁𝑁
p2H
𝑆𝑆
=
𝑁𝑁
14的 H
2
SO₃溶 液中,H⁺的浓度为0.10 mol/L
D.电解精炼铜的过程中,每转移N 个电子时,阳极溶解铜的质量为32g
A
6.下列离子方程式书写正确的是
A.向碳酸氢镁溶液中加入过量澄清石灰水:
2+ − 2+ −
𝑀𝑀𝑀𝑀 +2𝑁𝑁𝐶𝐶𝑁𝑁3 +𝐶𝐶𝑁𝑁 +2𝑁𝑁𝑁𝑁 = 𝐶𝐶𝑁𝑁𝐶𝐶𝑁𝑁3 ↓ +
B.向
2𝑁𝑁
滴2𝑁𝑁 有
+
酚
𝑀𝑀
酞
𝑀𝑀
的
𝐶𝐶𝑁𝑁
3Na
↓2
CO₃溶液中滴入盐酸至红色恰好褪去:
2− +
𝐶𝐶𝑁𝑁3 +2𝑁𝑁 = 𝐶𝐶𝑁𝑁2 ↑ +𝑁𝑁2𝑁𝑁
C.向邻羟基苯甲醛中加入足量浓溴水:
D.将过量 SO₃通入 Ca(ClO)₃ 溶液中: +
2+ − −
C𝑁𝑁 +2𝐶𝐶𝐶𝐶𝑁𝑁 +2𝑆𝑆𝑁𝑁2+2𝑁𝑁2𝑁𝑁 = 𝐶𝐶𝑁𝑁𝑆𝑆𝑁𝑁4 ↓ +2𝐶𝐶𝐶𝐶
2− +
7.化合
𝑆𝑆𝑁𝑁
物4 M
+4
是
𝑁𝑁
一种新型抗生素的中间体,其合成路线如下(略去部分试剂和反应条件)。已知化
合物K 虚线圈内所有原子共平面。下列说法正确的是
A. K中碳氮键可沿键轴旋转
B.形成M时,氮原子与L中碳原子b成键
C. M与足量 H₃加成后的产物分子中有2个手性碳原子
D.不考虑立体异构,Q的同分异构体有7种
学科网(北京)股份有限公司8.一种负热膨胀材料的立方晶胞结构如图所示,晶体密度为 阿伏加德罗常数的值为 N,下列说法
A
−3
错误的是 𝑑𝑑 𝑀𝑀⋅𝑐𝑐𝑚𝑚 ,
A.沿晶胞体对角线方向的投影图为
B. Ag和B均为 sp³杂化
C.晶体中与 Ag最近且距离相等的 Ag有6个
D. Ag和B的最短距离为
√2 3 223 10
2 × �𝑁𝑁A𝑑𝑑×10 𝑝𝑝𝑚𝑚
9.第一电子亲和能是指气态基态原子得到一个电子形成气态负一价阴离子时所释放或吸收的能量(E ,单位:
1
释放热量数值为负值,吸收热量数值为正值),其大小与原子的核电荷数、原子半径、价层电子
−1
𝑘𝑘排𝑘𝑘布⋅𝑚𝑚相𝑚𝑚关𝐶𝐶 ,, 价层电子排布不稳定的原子,其获得电子形成稳定结构时放出较多能量。元素 a~i 为原子序数
连续增大的短周期元素,其第一电子亲和能与原子序数的关系如图。下列说法错误的是
A. a 和i同主族 B.氢化物沸点:ah>f D.基态原子未成对电子数:d=f>e
10.下列实验操作、现象和解释或结论都正确的是
选项 实验操作 实验现象 解释或结论
向盛有 2mL 0.1 mol/L NaOH 溶液的试
先有白色沉淀,后有浅蓝色
A 管中滴加 4 滴 0.1 mol/L MgCl₃ 溶
沉淀
液,再滴加4滴0.1mol/L CuSO₃ 溶液
𝐾𝐾ₛₚ[𝐶𝐶𝐶𝐶(𝑁𝑁𝑁𝑁)₂] <
𝐾𝐾ₛₚ[𝑀𝑀𝑀𝑀(𝑁𝑁𝑁𝑁)₂]
向2支盛有 5 mL 不同浓度 NaHSO₃溶
浓度大的 NaHSO₃ 溶液中其他条件不变时,反应物浓度
B 液的试管中同时加入 2mL5% H O₃溶
2 气泡产生的速率更快 越大,反应速率越快
液,观察现象
学科网(北京)股份有限公司将 溶液加热 K 改变与水解平衡移动共同作
C 溶液的 pH逐渐减小 w
到60℃,用传感器测定溶液pH 用的结果
20°𝐶𝐶 0.5𝑚𝑚𝑚𝑚𝐶𝐶⋅𝐿𝐿⁻ ¹ 𝑁𝑁𝑁𝑁₂𝐶𝐶𝑁𝑁₃
向装有一氯丙烷的试管中加入适量的氢
D 氧化钠溶液,加热一段时间后,用稀硫产生白色沉淀 一氯丙烷中含有氯元素
酸酸化,再滴加硝酸银溶液
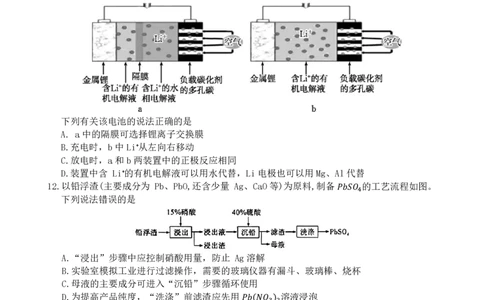
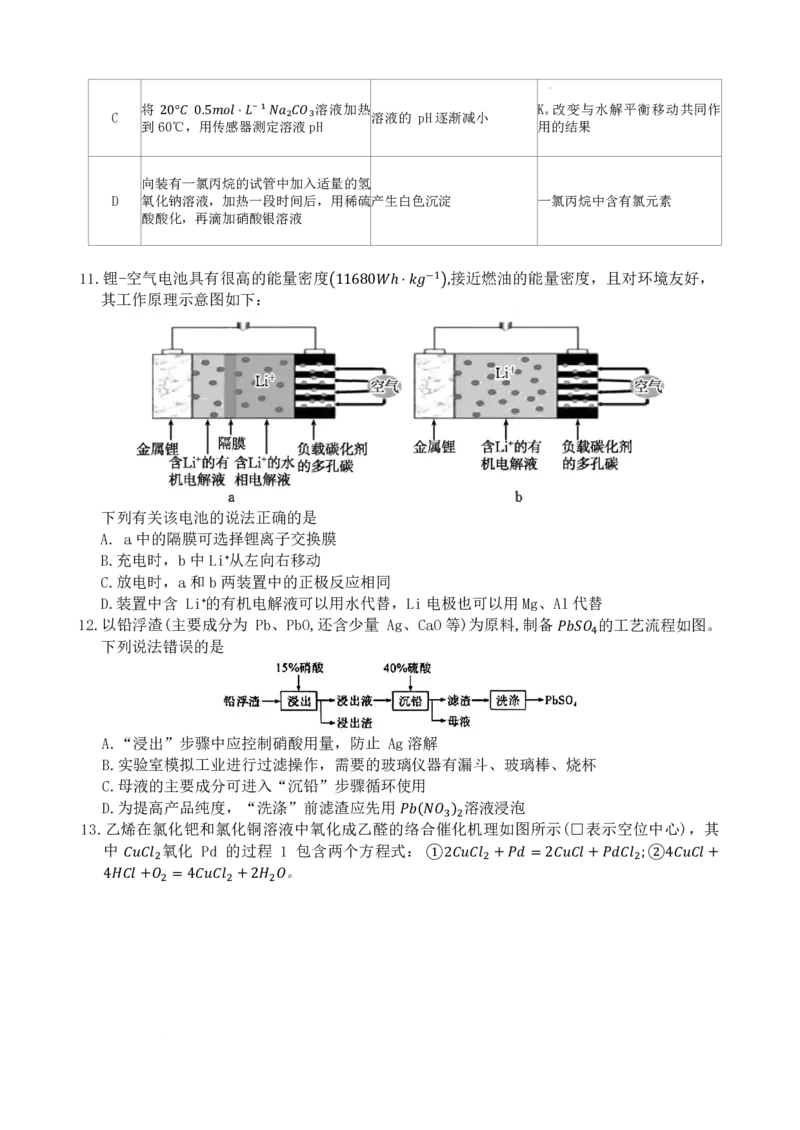
11.锂-空气电池具有很高的能量密度 接近燃油的能量密度,且对环境友好,
其工作原理示意图如下: −1
�11680𝑊𝑊ℎ⋅𝑘𝑘𝑀𝑀 �,
下列有关该电池的说法正确的是
A. a中的隔膜可选择锂离子交换膜
B.充电时,b中Li⁺从左向右移动
C.放电时,a和b两装置中的正极反应相同
D.装置中含 Li⁺的有机电解液可以用水代替,Li电极也可以用Mg、Al代替
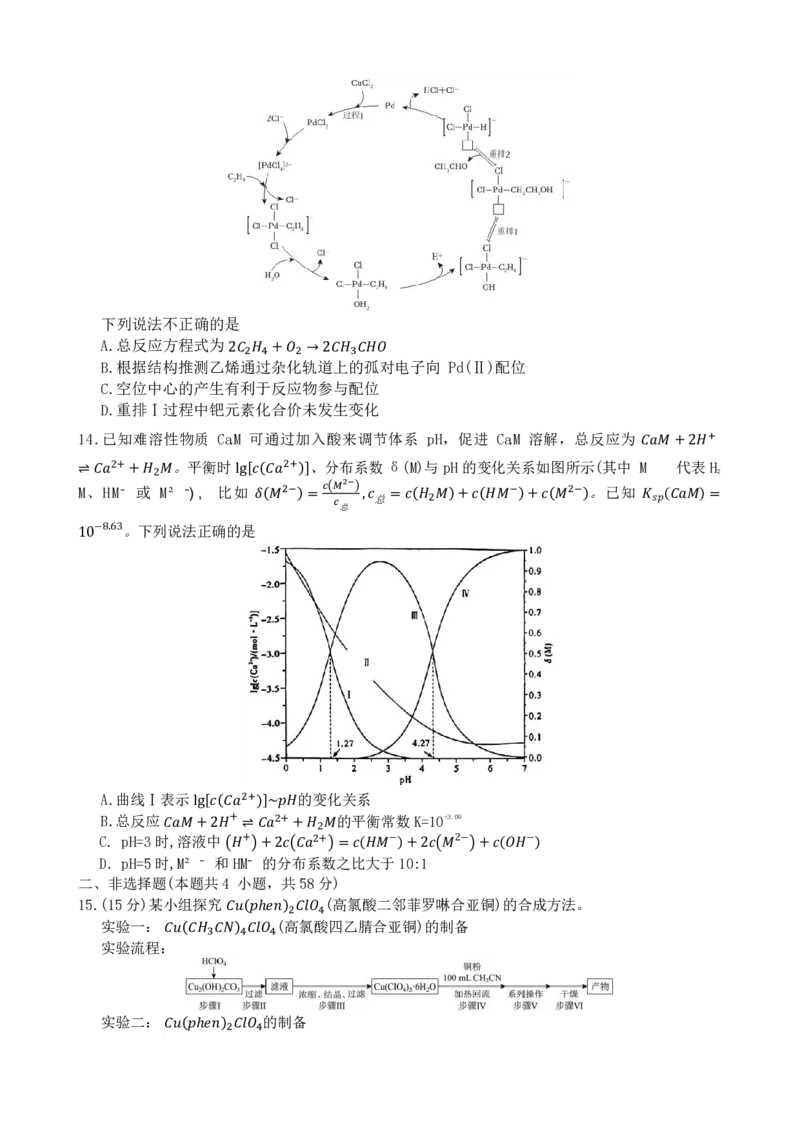
12.以铅浮渣(主要成分为 Pb、PbO,还含少量 Ag、CaO等)为原料,制备 的工艺流程如图。
下列说法错误的是
𝑃𝑃𝑃𝑃𝑆𝑆𝑁𝑁4
A.“浸出”步骤中应控制硝酸用量,防止 Ag溶解
B.实验室模拟工业进行过滤操作,需要的玻璃仪器有漏斗、玻璃棒、烧杯
C.母液的主要成分可进入“沉铅”步骤循环使用
D.为提高产品纯度,“洗涤”前滤渣应先用 溶液浸泡
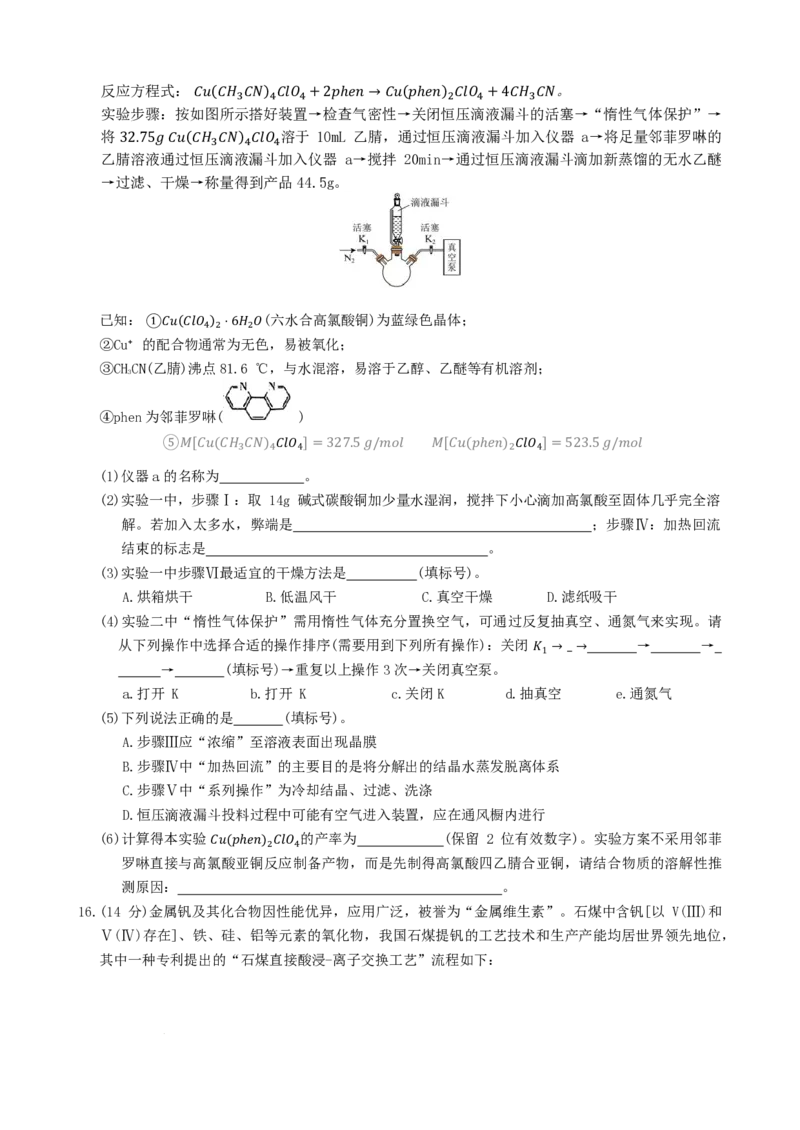
13.乙烯在氯化钯和氯化铜溶液中氧化成乙醛的络合催化机理如图所示(□表示空位中心),其
𝑃𝑃𝑃𝑃(𝑁𝑁𝑁𝑁3)2
中 氧化 Pd 的过程 1 包含两个方程式:
。
𝐶𝐶𝐶𝐶𝐶𝐶𝐶𝐶2 ①2𝐶𝐶𝐶𝐶𝐶𝐶𝐶𝐶2+𝑃𝑃𝑑𝑑 = 2𝐶𝐶𝐶𝐶𝐶𝐶𝐶𝐶+𝑃𝑃𝑑𝑑𝐶𝐶𝐶𝐶2;②4𝐶𝐶𝐶𝐶𝐶𝐶𝐶𝐶+
4𝑁𝑁𝐶𝐶𝐶𝐶 +𝑁𝑁2 = 4𝐶𝐶𝐶𝐶𝐶𝐶𝐶𝐶2+2𝑁𝑁2𝑁𝑁
学科网(北京)股份有限公司下列说法不正确的是
A.总反应方程式为
B.根据结构推测乙烯通过杂化轨道上的孤对电子向 Pd(Ⅱ)配位
2𝐶𝐶2𝑁𝑁4+𝑁𝑁2 →2𝐶𝐶𝑁𝑁3𝐶𝐶𝑁𝑁𝑁𝑁
C.空位中心的产生有利于反应物参与配位
D.重排Ⅰ过程中钯元素化合价未发生变化
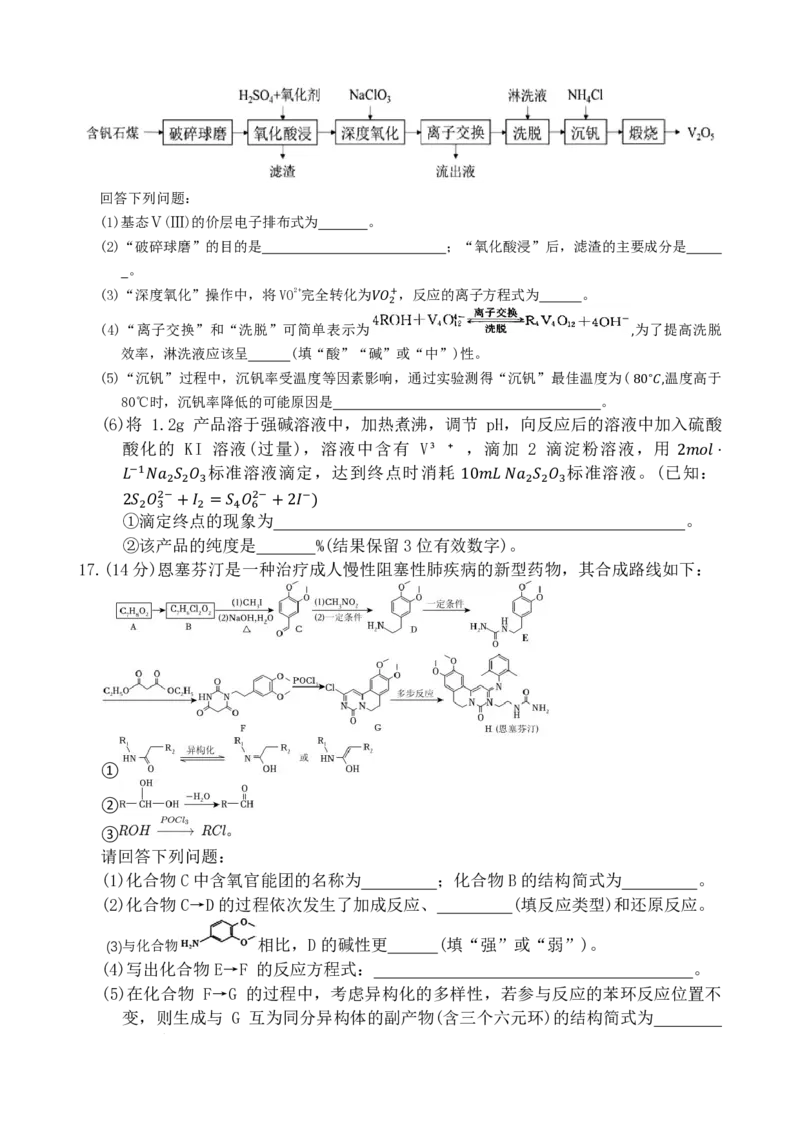
14.已知难溶性物质 CaM 可通过加入酸来调节体系 pH,促进 CaM 溶解,总反应为
+
。平衡时 、分布系数δ(M)与pH的变化关系如图所示(其中 M 代表H
𝐶𝐶𝑁𝑁𝑀𝑀+2𝑁𝑁 2
⇌ M、 𝐶𝐶𝑁𝑁 H2M+ ⁻ + 或 𝑁𝑁2 M 𝑀𝑀 ² ⁻), 比如 lg[ 𝑐𝑐(𝐶𝐶𝑁𝑁 2+ )] 2− 总 。已知
2− 𝑐𝑐�𝑀𝑀总 � − 2−
。下列说法正确的是 𝛿𝛿 (𝑀𝑀 )= 𝑐𝑐 ,𝑐𝑐 = 𝑐𝑐(𝑁𝑁2𝑀𝑀)+𝑐𝑐(𝑁𝑁𝑀𝑀 )+𝑐𝑐(𝑀𝑀 ) 𝐾𝐾𝑠𝑠𝑝𝑝(𝐶𝐶𝑁𝑁𝑀𝑀)=
−8.63
10
A.曲线Ⅰ表示 的变化关系
B.总反应 2+ 的平衡常数K=10-3.09
lg[𝑐𝑐(𝐶𝐶𝑁𝑁 )]~𝑝𝑝𝑁𝑁
C. pH=3时,溶液中 + 2+
𝐶𝐶𝑁𝑁𝑀𝑀+2𝑁𝑁 ⇌𝐶𝐶𝑁𝑁 +𝑁𝑁2𝑀𝑀
D. pH=5时,M² ⁻ 和HM+⁻ 的分布系2+数之比大于−10:1 2− −
�𝑁𝑁 �+2𝑐𝑐�𝐶𝐶𝑁𝑁 �=𝑐𝑐(𝑁𝑁𝑀𝑀 )+2𝑐𝑐�𝑀𝑀 �+𝑐𝑐(𝑁𝑁𝑁𝑁 )
二、非选择题(本题共4 小题,共58分)
15.(15分)某小组探究 (高氯酸二邻菲罗啉合亚铜)的合成方法。
实验一: (高氯酸四乙腈合亚铜)的制备
𝐶𝐶𝐶𝐶(𝑝𝑝ℎ𝑒𝑒𝑒𝑒)2𝐶𝐶𝐶𝐶𝑁𝑁4
实验流程:
𝐶𝐶𝐶𝐶(𝐶𝐶𝑁𝑁3𝐶𝐶𝑁𝑁)4𝐶𝐶𝐶𝐶𝑁𝑁4
实验二: 的制备
𝐶𝐶𝐶𝐶(𝑝𝑝ℎ𝑒𝑒𝑒𝑒)2𝐶𝐶𝐶𝐶𝑁𝑁4
学科网(北京)股份有限公司反应方程式: 。
实验步骤:按如图所示搭好装置→检查气密性→关闭恒压滴液漏斗的活塞→“惰性气体保护”→
𝐶𝐶𝐶𝐶(𝐶𝐶𝑁𝑁3𝐶𝐶𝑁𝑁)4𝐶𝐶𝐶𝐶𝑁𝑁4+2𝑝𝑝ℎ𝑒𝑒𝑒𝑒 → 𝐶𝐶𝐶𝐶(𝑝𝑝ℎ𝑒𝑒𝑒𝑒)2𝐶𝐶𝐶𝐶𝑁𝑁4+4𝐶𝐶𝑁𝑁3𝐶𝐶𝑁𝑁
将 溶于 10mL 乙腈,通过恒压滴液漏斗加入仪器 a→将足量邻菲罗啉的
乙腈溶液通过恒压滴液漏斗加入仪器 a→搅拌 20min→通过恒压滴液漏斗滴加新蒸馏的无水乙醚
32.75𝑀𝑀 𝐶𝐶𝐶𝐶(𝐶𝐶𝑁𝑁3𝐶𝐶𝑁𝑁)4𝐶𝐶𝐶𝐶𝑁𝑁4
→过滤、干燥→称量得到产品44.5g。
已知: (六水合高氯酸铜)为蓝绿色晶体;
②Cu⁺ 的
①
配
𝐶𝐶𝐶𝐶
合
(𝐶𝐶
物
𝐶𝐶𝑁𝑁
通
4)
常
2⋅
为
6𝑁𝑁
无
2𝑁𝑁
色,易被氧化;
③CHCN(乙腈)沸点81.6 ℃,与水混溶,易溶于乙醇、乙醚等有机溶剂;
3
④phen为邻菲罗啉( )
(1)仪器a⑤的名𝑀𝑀称[𝐶𝐶为𝐶𝐶( 𝐶𝐶 𝑁𝑁 3 𝐶𝐶 𝑁𝑁 ) 4 𝐶𝐶 𝐶𝐶𝑁𝑁 4 ]。= 327.5 𝑀𝑀/𝑚𝑚𝑚𝑚𝐶𝐶 𝑀𝑀[𝐶𝐶𝐶𝐶(𝑝𝑝ℎ𝑒𝑒𝑒𝑒)2𝐶𝐶𝐶𝐶𝑁𝑁4 ]=523.5 𝑀𝑀/𝑚𝑚𝑚𝑚𝐶𝐶
(2)实验一中,步骤Ⅰ:取 14g 碱式碳酸铜加少量水湿润,搅拌下小心滴加高氯酸至固体几乎完全溶
解。若加入太多水,弊端是 ;步骤Ⅳ:加热回流
结束的标志是 。
(3)实验一中步骤Ⅵ最适宜的干燥方法是 (填标号)。
A.烘箱烘干 B.低温风干 C.真空干燥 D.滤纸吸干
(4)实验二中“惰性气体保护”需用惰性气体充分置换空气,可通过反复抽真空、通氮气来实现。请
从下列操作中选择合适的操作排序(需要用到下列所有操作):关闭 → →
→ (填标号)→重复以上操作3次→关闭真空泵。
𝐾𝐾1 →_→
a.打开 K₃ b.打开 K₃ c.关闭K₃ d.抽真空 e.通氮气
(5)下列说法正确的是 (填标号)。
A.步骤Ⅲ应“浓缩”至溶液表面出现晶膜
B.步骤Ⅳ中“加热回流”的主要目的是将分解出的结晶水蒸发脱离体系
C.步骤Ⅴ中“系列操作”为冷却结晶、过滤、洗涤
D.恒压滴液漏斗投料过程中可能有空气进入装置,应在通风橱内进行
(6)计算得本实验 的产率为 (保留 2 位有效数字)。实验方案不采用邻菲
罗啉直接与高氯酸亚铜反应制备产物,而是先制得高氯酸四乙腈合亚铜,请结合物质的溶解性推
𝐶𝐶𝐶𝐶(𝑝𝑝ℎ𝑒𝑒𝑒𝑒)2𝐶𝐶𝐶𝐶𝑁𝑁4
测原因: 。
16.(14 分)金属钒及其化合物因性能优异,应用广泛,被誉为“金属维生素”。石煤中含钒[以 V(Ⅲ)和
Ⅴ(Ⅳ)存在]、铁、硅、铝等元素的氧化物,我国石煤提钒的工艺技术和生产产能均居世界领先地位,
其中一种专利提出的“石煤直接酸浸-离子交换工艺”流程如下:
学科网(北京)股份有限公司回答下列问题:
(1)基态Ⅴ(Ⅲ)的价层电子排布式为 。
(2)“破碎球磨”的目的是 ;“氧化酸浸”后,滤渣的主要成分是
。
(3)“深度氧化”操作中,将VO2+完全转化为 ,反应的离子方程式为 。
+
(4)“离子交换”和“洗脱”可简单表示为𝑉𝑉𝑁𝑁2
为了提高洗脱
效率,淋洗液应该呈 (填“酸”“碱”或“中”)性。
,
(5)“沉钒”过程中,沉钒率受温度等因素影响,通过实验测得“沉钒”最佳温度为( 温度高于
80℃时,沉钒率降低的可能原因是 。 ∘
80 𝐶𝐶,
(6)将 1.2g 产品溶于强碱溶液中,加热煮沸,调节 pH,向反应后的溶液中加入硫酸
酸化的 KI 溶液(过量),溶液中含有 V³ ⁺ ,滴加 2 滴淀粉溶液,用
标准溶液滴定,达到终点时消耗 标准溶液。(已知:
2𝑚𝑚𝑚𝑚𝐶𝐶 ⋅
−1
𝐿𝐿 𝑁𝑁𝑁𝑁2𝑆𝑆2𝑁𝑁3 10𝑚𝑚𝐿𝐿 𝑁𝑁𝑁𝑁2𝑆𝑆2𝑁𝑁3
①滴定2−终点的现象2为− − 。
2𝑆𝑆2𝑁𝑁3 +𝐼𝐼2 = 𝑆𝑆4𝑁𝑁6 +2𝐼𝐼 )
②该产品的纯度是 %(结果保留 3 位有效数字)。
17.(14 分)恩塞芬汀是一种治疗成人慢性阻塞性肺疾病的新型药物,其合成路线如下:
①
②
③
请回答下列问题:
(1)化合物 C 中含氧官能团的名称为 ;化合物 B 的结构简式为 。
(2)化合物 C→D 的过程依次发生了加成反应、 (填反应类型)和还原反应。
(3)与化合物 相比,D 的碱性更 (填“强”或“弱”)。
(4)写出化合物 E→F 的反应方程式: 。
(5)在化合物 F→G 的过程中,考虑异构化的多样性,若参与反应的苯环反应位置不
变,则生成与 G 互为同分异构体的副产物(含三个六元环)的结构简式为
学科网(北京)股份有限公司(写出一种即可)。
(6)利用已知信息和流程路线中的相关信息,设计以乙醇、1,3-丙二醇.
为原料合成 的路线(用流程图表示,无机试剂任选)。
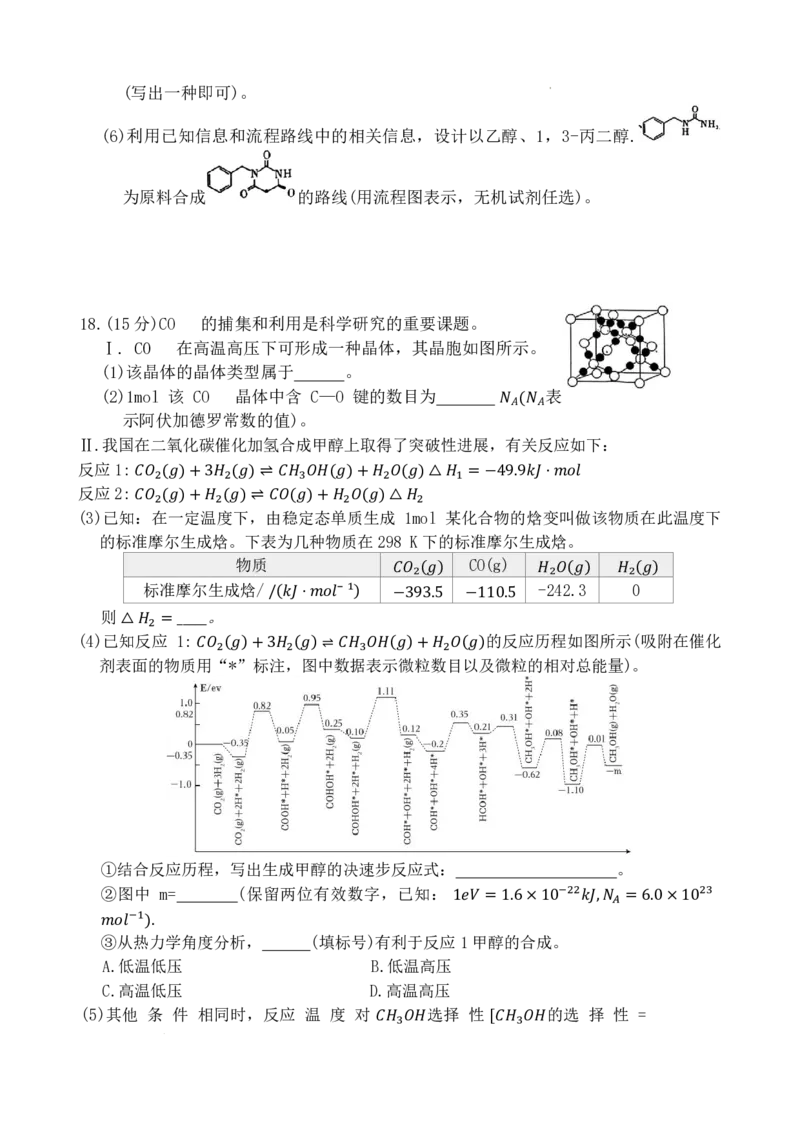
18.(15 分)CO₃ 的捕集和利用是科学研究的重要课题。
Ⅰ. CO₃ 在高温高压下可形成一种晶体,其晶胞如图所示。
(1)该晶体的晶体类型属于 。
(2)1mol 该 CO₃ 晶体中含 C—O 键的数目为 表
示阿伏加德罗常数的值)。
𝑁𝑁𝐴𝐴(𝑁𝑁𝐴𝐴
Ⅱ.我国在二氧化碳催化加氢合成甲醇上取得了突破性进展,有关反应如下:
反应1:
反应2:
𝐶𝐶𝑁𝑁2(𝑀𝑀)+3𝑁𝑁2(𝑀𝑀) ⇌ 𝐶𝐶𝑁𝑁3𝑁𝑁𝑁𝑁(𝑀𝑀)+𝑁𝑁2𝑁𝑁(𝑀𝑀)△𝑁𝑁1 = −49.9𝑘𝑘𝑘𝑘·𝑚𝑚𝑚𝑚𝐶𝐶
(3)已知:在一定温度下,由稳定态单质生成 1mol 某化合物的焓变叫做该物质在此温度下
𝐶𝐶𝑁𝑁2(𝑀𝑀)+𝑁𝑁2(𝑀𝑀) ⇌ 𝐶𝐶𝑁𝑁(𝑀𝑀)+𝑁𝑁2𝑁𝑁(𝑀𝑀)△𝑁𝑁2
的标准摩尔生成焓。下表为几种物质在298 K下的标准摩尔生成焓。
物质 CO(g)
标准摩尔生成焓/ -242.3 0
𝐶𝐶𝑁𝑁₂(𝑀𝑀) 𝑁𝑁₂𝑁𝑁(𝑀𝑀) 𝑁𝑁₂(𝑀𝑀)
则 。
/(𝑘𝑘𝑘𝑘⋅𝑚𝑚𝑚𝑚𝐶𝐶⁻ ¹) −393.5 −110.5
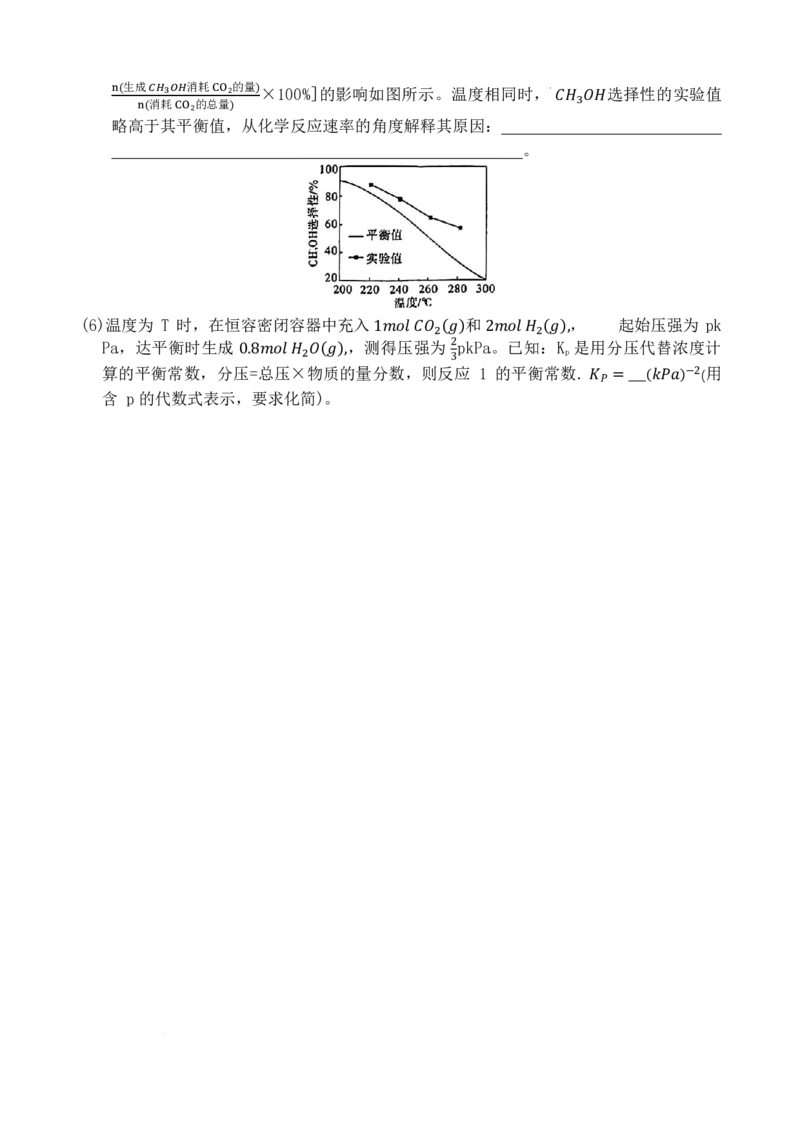
(4)已知反应 1: 的反应历程如图所示(吸附在催化
△𝑁𝑁2 = _____
剂表面的物质用“*”标注,图中数据表示微粒数目以及微粒的相对总能量)。
𝐶𝐶𝑁𝑁2(𝑀𝑀)+3𝑁𝑁2(𝑀𝑀) ⇌ 𝐶𝐶𝑁𝑁3𝑁𝑁𝑁𝑁(𝑀𝑀)+𝑁𝑁2𝑁𝑁(𝑀𝑀)
①结合反应历程,写出生成甲醇的决速步反应式: 。
②图中 m= (保留两位有效数字,已知:
−22 23
1𝑒𝑒𝑉𝑉 = 1.6×10 𝑘𝑘𝑘𝑘,𝑁𝑁𝐴𝐴 = 6.0×10
③从−热1 力学角度分析, (填标号)有利于反应1甲醇的合成。
𝑚𝑚𝑚𝑚𝐶𝐶 ).
A.低温低压 B.低温高压
C.高温低压 D.高温高压
(5)其他 条 件 相同时,反应 温 度 对 选择 性 的选 择 性 =
𝐶𝐶𝑁𝑁3𝑁𝑁𝑁𝑁 [𝐶𝐶𝑁𝑁3𝑁𝑁𝑁𝑁
学科网(北京)股份有限公司生成 消耗 的量
×100%]的影响如图所示。温度相同时, 选择性的实验值
消耗 的总量
n( 𝐶𝐶𝐻𝐻3𝑂𝑂𝐻𝐻 CO₂ )
略高 n 于 ( 其 C 平 O₂ 衡值, ) 从化学反应速率的角度解释其原因: 𝐶𝐶 𝑁𝑁 3𝑁𝑁 𝑁𝑁
。
(6)温度为 T 时,在恒容密闭容器中充入 和 , 起始压强为 pk
Pa,达平衡时生成 ,测得压强为 pkPa。已知:K 是用分压代替浓度计
1𝑚𝑚𝑚𝑚𝐶𝐶 𝐶𝐶𝑁𝑁2(𝑀𝑀) 2𝑚𝑚𝑚𝑚𝐶𝐶 𝑁𝑁2(𝑀𝑀) p ,
算的平衡常数,分压=总压×物质的量分数,则反2应 1 的平衡常数. (用
0.8𝑚𝑚𝑚𝑚𝐶𝐶 𝑁𝑁2𝑁𝑁(𝑀𝑀), 3
含 p的代数式表示,要求化简)。 −2
𝐾𝐾𝑃𝑃 =___(𝑘𝑘𝑃𝑃𝑁𝑁)
学科网(北京)股份有限公司