文档内容
郧阳中学 2025 级高一年级上学期 10 月第一次考试
化学试卷
命题人:贺兴明 审题人:吴锐
本试题卷共8页,29题,全卷满分100分。考试用时75分钟
祝考试顺利★
注意事项:
1.答题前,先将自己的姓名、考号填写在试卷和答题卡上,并将考号条形码粘贴在答题卡上的指
定位置。
2.选择题的作答:每小题选出答案后,用2B 铅笔把答题卡上对应题目的答案标号涂黑。写在试卷
和答题卡上的非答题区域均无效。
3.非选择题的作答:用黑色签字笔直接答在答题卡上对应的答题区域内。写在试卷和答题卡上的
非答题区域均无效。
可能用到的相对原子质量:H1 O 16 Cl 35.5 Fe 56
一、单选题(本题共25小题,每小题2分,共50分。在每小题给出的四个选项中,
只有一项是符合题目要求的。)
1.分类法是化学学习的一种重要方法,物质的分类如图所示。下列说法正确的是
A.图甲表示的是物质的分类
B.图乙表示的分类方法属于树状分类法
C.图丙表示物质分为电解质和非电解质
D.金属氧化物不都属于图丙中的电解质
2.将下列各组物质按酸、碱、盐分类顺次排列,正确的是
A.盐酸、石灰水、碳酸氢钠 B.硝酸、烧碱、五水硫酸铜
C.硫酸、纯碱、孔雀石 D.醋酸、乙醇、硝酸钾
3.下列说法中,正确的是
A.固态的冰不能导电,所以冰不是电解质
B.干冰溶于水能导电,所以干冰是电解质
C.熔融状态的铜能导电,所以铜是电解质
D.硫酸钡虽难溶于水,但硫酸钡是电解质
4.氧化还原反应与四种基本类型的关系如图所示,则下列化学反应属于阴影部分的是
A.Cl +2KBr=Br +2KCl
2 2
B.2NaHCO Na CO +CO ↑+H O
3 2 3 2 2
C.2Na O +2CO =2Na CO +O
2 2 2 2 3 2
D.4Fe(OH) +O +2H O=4Fe(OH)
2 2 2 3
2025级郧阳中学高一10月月考试卷 第1页 共 8页5.下列化合物不能通过化合反应直接一步生成的是
A. NaHCO₃ B.Na O C.Cu(OH) D.Cu (OH) CO
2 2 2 2 2 3
6.中华古文化蕴含丰富的化学知识,以下对古诗词中涉及化学知识解读正确的是
A. “日照香炉生紫烟,遥看瀑布挂前川”中的“烟”是指弥漫在空气中的固体微粒
B.“忽闻海上有仙山,山在虚无缥缈间”涉及自然现象海市蜃楼与胶体知识有关
C.“沧海月明珠有泪,蓝田日暖玉生烟”中的“珠”字对应的化学物质不是电解质
D.“爆竹声中一岁除,春风送暖入屠苏”中的“爆竹声中”没有涉及氧化还原反应
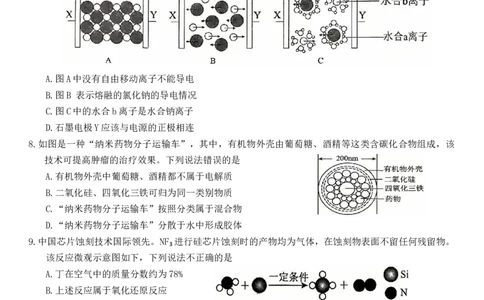
7.图a、b、c分别为氯化钠在不同状态下的导电实验的微观示意图(X、Y均表示石墨电极,且与直流电源连接方式
相同,表示水分子),下列说法不正确的是
A.图A中没有自由移动离子不能导电
B.图B 表示熔融的氯化钠的导电情况
C.图C中的水合b离子是水合钠离子
D.石墨电极Y应该与电源的正极相连
8.如图是一种“纳米药物分子运输车”,其中,有机物外壳由葡萄糖、酒精等这类含碳化合物组成,该
技术可提高肿瘤的治疗效果。下列说法错误的是
A.有机物外壳中葡萄糖、酒精都不属于电解质
B.二氧化硅、四氧化三铁可归为同一类别物质
C.“纳米药物分子运输车”按照分类属于混合物
D.“纳米药物分子运输车”分散于水中形成胶体
9.中国芯片蚀刻技术国际领先。NF₃进行硅芯片蚀刻时的产物均为气体,在蚀刻物表面不留任何残留物。
该反应微观示意图如下,下列说法不正确的是
A.丁在空气中的质量分数约为78%
B.上述反应属于氧化还原反应
C.上述反应中的 NF₃是氧化剂
D.反应后丙和丁的分子数之比为3:2.
10.下列有关金属钠的说法中,不正确的是
A.钠与氧气反应,条件不同所得的产物也不同
B.钠与水反应的现象为“浮、溶、游、响、红”
C.钠着火不能用水而需要用干燥的沙土来灭火
D.实验室中,要把钠保存在石蜡油或煤油中
2025级郧阳中学高--10月月考试卷 第2页 共8页11.下列各组溶液中,反应的离子方程式书写正确的是
A. Na₂O 溶于水: Na O+2H O=2Na++2OH-
2 2
B. NaHCO₃与氢氧化钠溶液混合: HCO-+OH-=H O+CO 个
3 2 2
C. CO₂通入到CaCl₂溶液中: CO +H O+Ca2+=CaCO ↓+2H+
2 2 3
D. NaOH、FeCl₃、NaClO制备 Na FeO :2Fe3++3ClO-+10OH-=2FeO2-+3Cl-+5H O
2 4 a 2
12.下列各组溶液中,反应的离子方程式一定相同的是
A.石灰石上分别滴加稀盐酸、稀硫酸
B.石灰石上分别滴加稀盐酸、稀醋酸
C.澄清的石灰水分别与少量的、足量的 NaHCO₃溶液反应
D.澄清石灰水分别与少量的、足量的(Ca(HCO₃)₂溶液反应
13. 某 无 色 透 明 强 酸 性 溶 液 中 含 有 八 种 离 子
Na+ 、M g2+ 、Al2+ 、Cu2+ 、Ba2+ 、Cl- 、CO2- 、SO2-中的五种 离子 ,该溶液遇
2 4
BaCl₂溶液产生白色沉淀。下列说法正确的是
A.一定不含有 Cu2+ 、Ba2+ 、Al3+离子 B.可能含有 Na+ 、M g2+ 、SO2-等离子
4
C.根据题给信息无法确认5种离子 D. 5种离子个数比可能为1:1:1:2:2
14.粗盐中常含有杂质 M g2+ 、Ca2+ 、SO2-,,为除去杂质得到精盐,同学们设计了如图所
4
示实验步骤。已知实验中所添加的试剂均过量,下列说法正确的是
A. 试剂①②③分别为 Na₂CO₃、BaCl₂、NaOH 三种溶液
B.加入过量的稀盐酸的目的是除去滤液中的CO²⁻和OH⁻
C.蒸发结晶使用的仪器主要有酒精灯、铁架台、锥形瓶、玻璃棒
D.上述步骤中的“过滤”与“稀盐酸”的顺序互换后不影响精盐制备
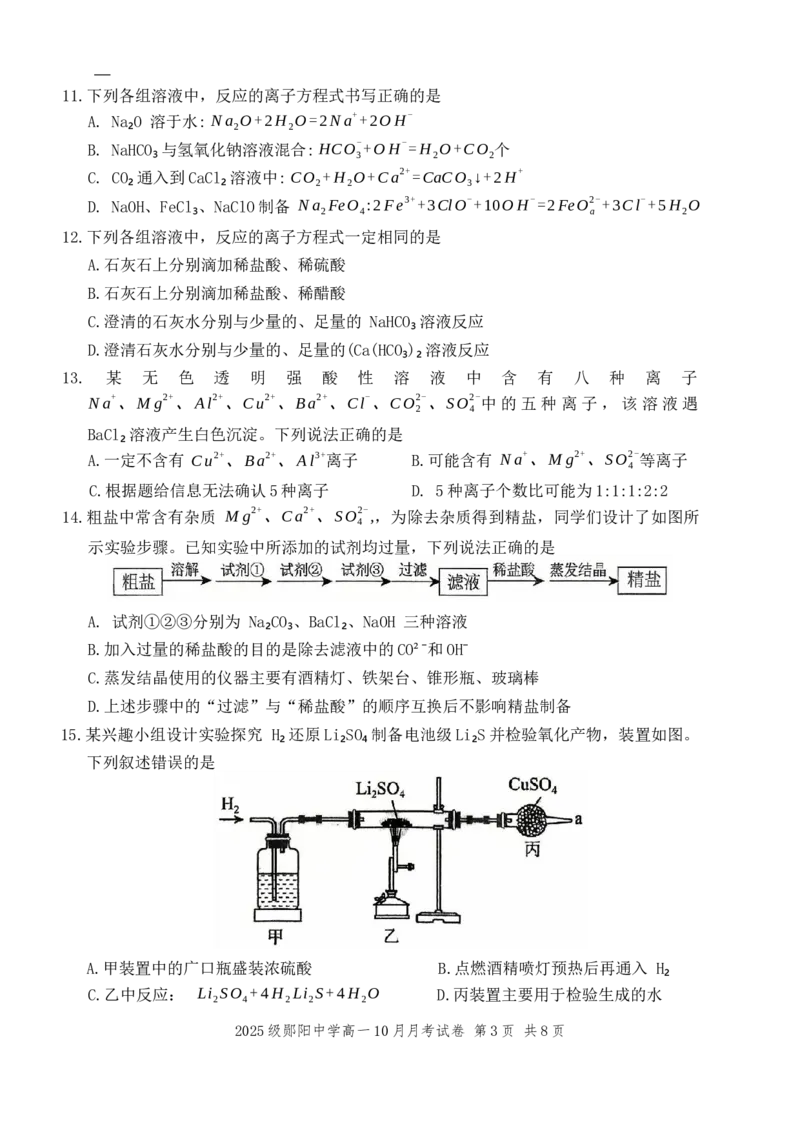
15.某兴趣小组设计实验探究 H₂还原Li₂SO₄制备电池级Li₂S并检验氧化产物,装置如图。
下列叙述错误的是
A.甲装置中的广口瓶盛装浓硫酸 B.点燃酒精喷灯预热后再通入 H₂
C.乙中反应: Li SO +4H Li S+4H O D.丙装置主要用于检验生成的水
2 4 2 2 2
2025级郧阳中学高一10月月考试卷 第3页 共8页16.已知溶液中的反应①~③:
①2FeCl +Cl =2FeCl
2 2 3
②2FeCl +2HI=2FeCl +2HCl+I
3 2 2
③H S+I =S↓+2HI
2 2
根据上述反应,下列有关判断正确的是
A. FeCl₃只是氧化剂和氧化产物 B.氧化性: Cl >Fe3+>I >S
2 2
C.反应②中的还原产物是 FeCl₂、HCl D.还原性: H S>Fe2+>l->Cl-
2
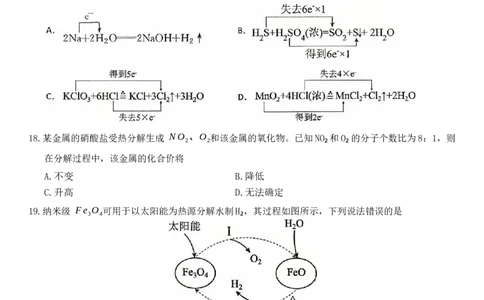
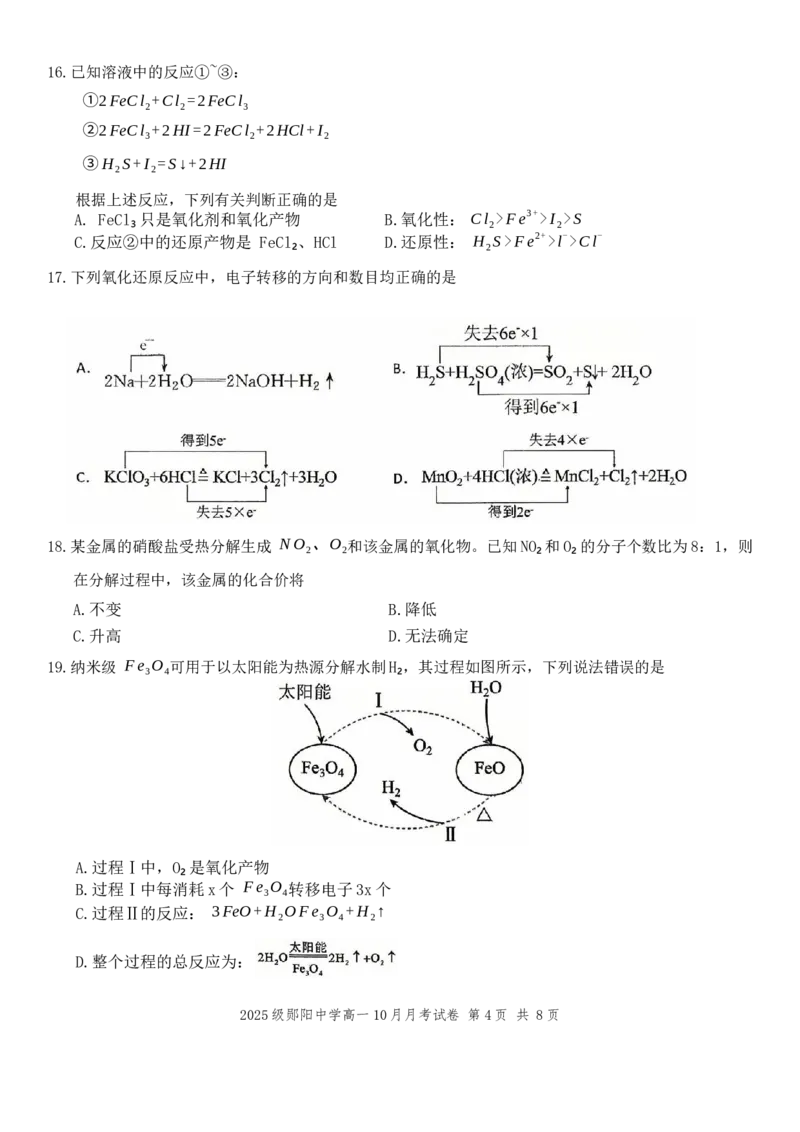
17.下列氧化还原反应中,电子转移的方向和数目均正确的是
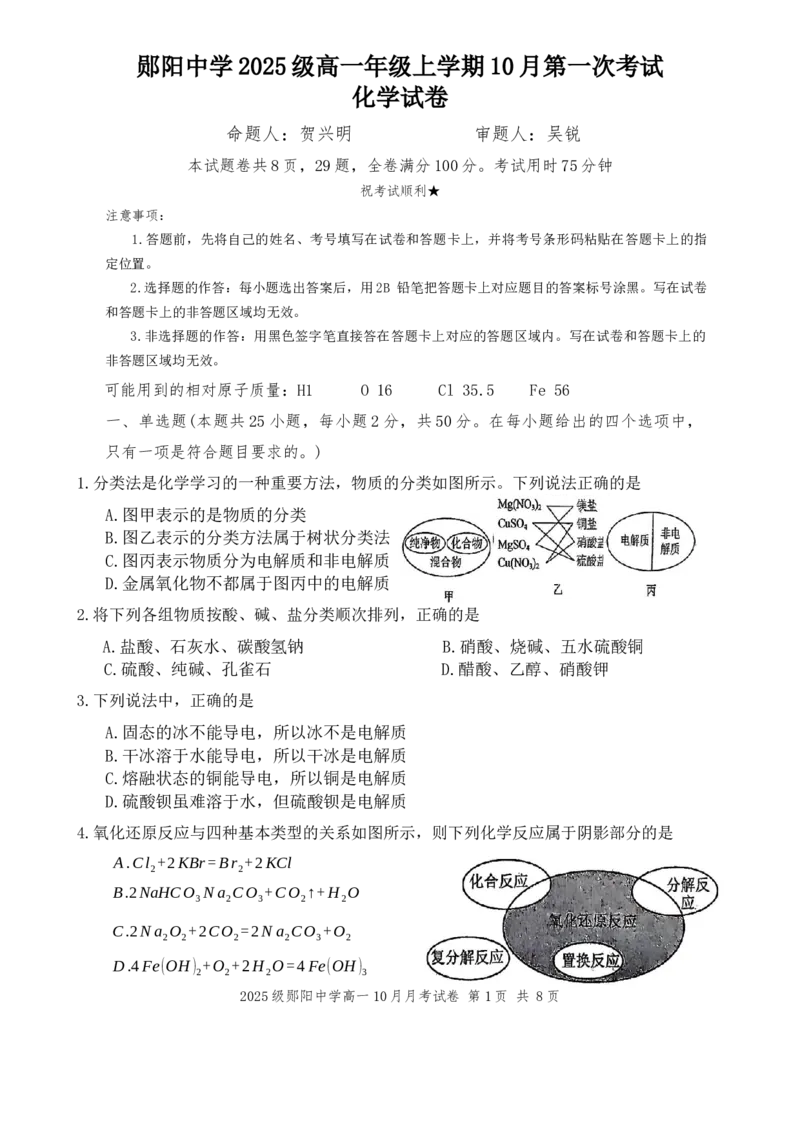
18.某金属的硝酸盐受热分解生成 NO 、O 和该金属的氧化物。已知NO₂和O₂的分子个数比为8:1,则
2 2
在分解过程中,该金属的化合价将
A.不变 B.降低
C.升高 D.无法确定
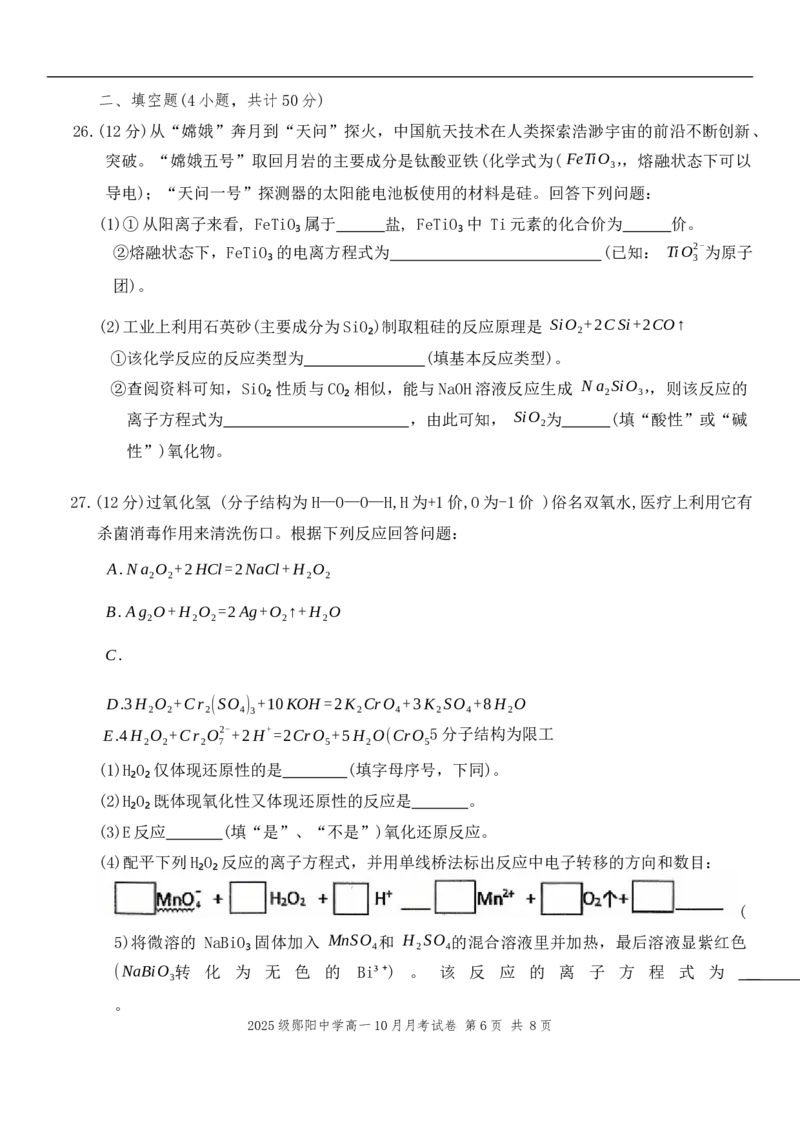
19.纳米级 Fe O 可用于以太阳能为热源分解水制H₂,其过程如图所示,下列说法错误的是
3 4
A.过程Ⅰ中,O₂是氧化产物
B.过程Ⅰ中每消耗x个 Fe O 转移电子3x个
3 4
C.过程Ⅱ的反应: 3FeO+H OFe O +H ↑
2 3 4 2
D.整个过程的总反应为:
2025级郧阳中学高一10月月考试卷 第4页 共 8页20. R₂O⁺在酸性溶液中与MnO₃反应,反应产物为1 RO 、Mn2+ 、H O。已知反应中氧化剂与还
2 2
原剂的离子个数比为2:5,则R₂O*中R的化合价为
A. +4 B.+3 C. +2 D.+1
21.用元素M制备化合物R的反应为 3M2++2Y O2-+O +xOH+=R+Y O2-+2H O。
2 3 2 4 6 2
下列有关叙述中,错误的是
A. x= 4
B.元素 M一定不是非金属元素
C.反应中M²⁺部分被还原
D. R 中 M 元素化合价不止1种
22.实验室用下列方法均可制取 Cl₂:
①MnO +4HCl(浓)MnCl +Cl ↑+2H O
2 2 2 2
②NaClO+2HCl=NaCl+Cl ↑+H O
2 2
③2KMnO₄+16HCl(浓)=2KCl+2MnCl₂+5Cl₂↑+8H₂O
④KClO₃+6HCl(浓) = KCl+3Cl₂个+3H₂O
若上述各反应转移的电子数相同,则①、②、③、④生成的 Cl₂质量之比为
A.1:1:5:3 B.5:10:1:2 C. 5:10:5:3 D.5:10:5:6
23. 一定温度下, 将Cl₂通入 NaOH 溶液中, 得到只含NaCl、NaClO、NaClO₃的混合溶液, 经测
定ClO⁻与ClO₃ ⁻的离子个数之比为1:3,则该应中被还原与被氧化的元素的质量之比为
A. 4:1 B. 3:1 C. 1:3 D. 1:1
24.现有30.4g铁的氧化物FeₓOy(其中 Fe的化合价为+2、+3),先将其完全溶解于一定量的硫酸
溶液中(溶解时 Fe元素的化合价保持不变),再向所得溶液中缓慢通入 7.1gCl₂,恰好将溶
液中的 Fe²⁺完全氧化为Fe³⁺。该铁的氧化物的化学式是
A. Fe₂O₃ B. Fe₃O₄ C. Fe₄O₅ D. Fe₅O₇
25.从矿物学资料查得,一定条件下自然界中存在下面反应:
14CuSO +5FeS +12H O=7Cu S+5FeSO +12H SO (FeSO 中S为-1价, Cu₂S中S
4 2 2 2 4 2 4 2
为-2价)下列说法不正确的是
A.反应中氧化剂与还原剂的个数之比为35:3
B.被氧化与被还原的元素原子个数之比为1:7
C.反应中+2价铜个数与被其氧化的FeS₂个数之比为28:1
D.反应中的 FeS₂ 的个数与转移的电子个数之比为1:4.2
2025级郧阳中学高一10月月考试卷 第5页 共8页二、填空题(4小题,共计50分)
26.(12分)从“嫦娥”奔月到“天问”探火,中国航天技术在人类探索浩渺宇宙的前沿不断创新、
突破。“嫦娥五号”取回月岩的主要成分是钛酸亚铁(化学式为( FeTiO ,,熔融状态下可以
3
导电);“天问一号”探测器的太阳能电池板使用的材料是硅。回答下列问题:
(1)①从阳离子来看, FeTiO₃属于 盐, FeTiO₃中 Ti元素的化合价为 价。
②熔融状态下,FeTiO₃的电离方程式为 (已知: TiO2-为原子
3
团)。
(2)工业上利用石英砂(主要成分为SiO₂)制取粗硅的反应原理是 SiO +2CSi+2CO↑
2
①该化学反应的反应类型为 (填基本反应类型)。
②查阅资料可知,SiO₂性质与CO₂相似,能与NaOH溶液反应生成 Na SiO ,,则该反应的
2 3
离子方程式为 ,由此可知, SiO 为 (填“酸性”或“碱
2
性”)氧化物。
27.(12分)过氧化氢 (分子结构为H—O—O—H,H为+1价,O为-1价 )俗名双氧水,医疗上利用它有
杀菌消毒作用来清洗伤口。根据下列反应回答问题:
A.Na O +2HCl=2NaCl+H O
2 2 2 2
B.Ag O+H O =2Ag+O ↑+H O
2 2 2 2 2
C.
D.3H O +Cr (SO ) +10KOH=2K CrO +3K SO +8H O
2 2 2 4 3 2 4 2 4 2
E.4H O +Cr O2-+2H+=2CrO +5H O(CrO 5分子结构为限工
2 2 2 7 5 2 5
(1)H₂O₂仅体现还原性的是 (填字母序号,下同)。
(2)H₂O₂既体现氧化性又体现还原性的反应是 。
(3)E反应 (填“是”、“不是”)氧化还原反应。
(4)配平下列H₂O₂反应的离子方程式,并用单线桥法标出反应中电子转移的方向和数目:
(
5)将微溶的 NaBiO₃固体加入 MnSO 和 H SO 的混合溶液里并加热,最后溶液显紫红色
4 2 4
(NaBiO 转 化 为 无 色 的 Bi³⁺) 。 该 反 应 的 离 子 方 程 式 为
3
。
2025级郧阳中学高一10月月考试卷 第6页 共 8页28. (14分) 29
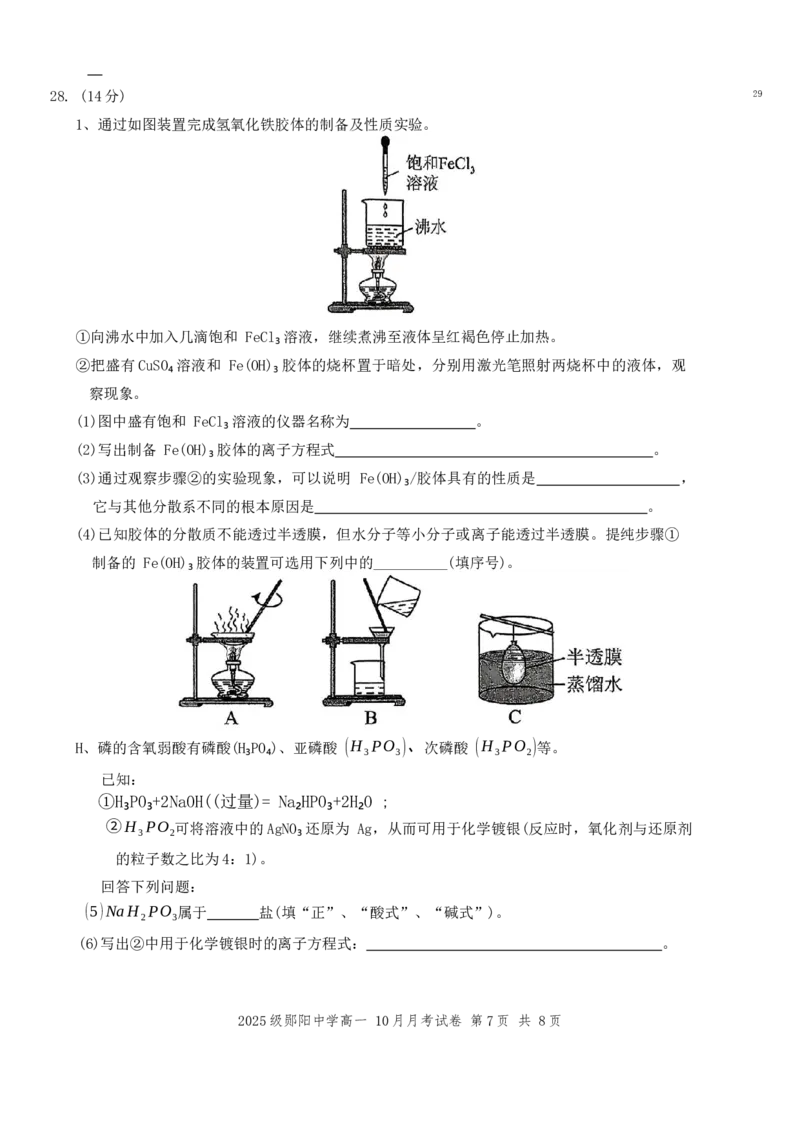
1、通过如图装置完成氢氧化铁胶体的制备及性质实验。
①向沸水中加入几滴饱和 FeCl₃溶液,继续煮沸至液体呈红褐色停止加热。
②把盛有CuSO₄溶液和 Fe(OH)₃胶体的烧杯置于暗处,分别用激光笔照射两烧杯中的液体,观
察现象。
(1)图中盛有饱和 FeCl₃溶液的仪器名称为 。
(2)写出制备 Fe(OH)₃胶体的离子方程式 。
(3)通过观察步骤②的实验现象,可以说明 Fe(OH)₃/胶体具有的性质是 ,
它与其他分散系不同的根本原因是 。
(4)已知胶体的分散质不能透过半透膜,但水分子等小分子或离子能透过半透膜。提纯步骤①
制备的 Fe(OH)₃胶体的装置可选用下列中的 (填序号)。
H、磷的含氧弱酸有磷酸(H₃PO₄)、亚磷酸 (H PO )、次磷酸 (H PO )等。
3 3 3 2
已知:
①H₃PO₃+2NaOH((过量)= Na₂HPO₃+2H₂O ;
②H PO 可将溶液中的AgNO₃还原为 Ag,从而可用于化学镀银(反应时,氧化剂与还原剂
3 2
的粒子数之比为4:1)。
回答下列问题:
(5)NaH PO 属于 盐(填“正”、“酸式”、“碱式”)。
2 3
(6)写出②中用于化学镀银时的离子方程式: 。
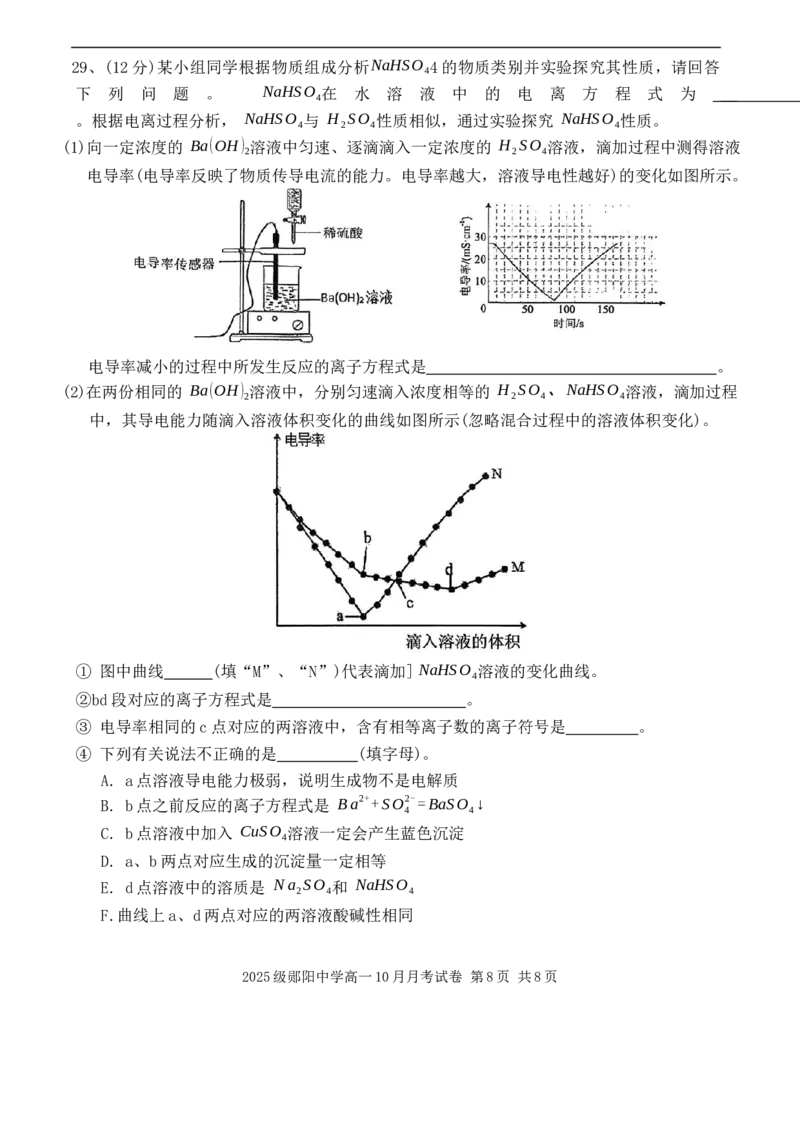
2025级郧阳中学高一 10月月考试卷 第7页 共 8页29、(12分)某小组同学根据物质组成分析NaHSO 4的物质类别并实验探究其性质,请回答
4
下 列 问 题 。 NaHSO 在 水 溶 液 中 的 电 离 方 程 式 为
4
。根据电离过程分析, NaHSO 与 H SO 性质相似,通过实验探究 NaHSO 性质。
4 2 4 4
(1)向一定浓度的 Ba(OH) 溶液中匀速、逐滴滴入一定浓度的 H SO 溶液,滴加过程中测得溶液
2 2 4
电导率(电导率反映了物质传导电流的能力。电导率越大,溶液导电性越好)的变化如图所示。
电导率减小的过程中所发生反应的离子方程式是 。
(2)在两份相同的 Ba(OH) 溶液中,分别匀速滴入浓度相等的 H SO 、NaHSO 溶液,滴加过程
2 2 4 4
中,其导电能力随滴入溶液体积变化的曲线如图所示(忽略混合过程中的溶液体积变化)。
① 图中曲线 (填“M”、“N”)代表滴加] NaHSO 溶液的变化曲线。
4
②bd段对应的离子方程式是 。
③ 电导率相同的c点对应的两溶液中,含有相等离子数的离子符号是 。
④ 下列有关说法不正确的是 (填字母)。
A. a点溶液导电能力极弱,说明生成物不是电解质
B. b点之前反应的离子方程式是 Ba2++SO2-=BaSO ↓
4 4
C. b点溶液中加入 CuSO 溶液一定会产生蓝色沉淀
4
D. a、b两点对应生成的沉淀量一定相等
E. d点溶液中的溶质是 Na SO 和 NaHSO
2 4 4
F.曲线上a、d两点对应的两溶液酸碱性相同
2025级郧阳中学高一10月月考试卷 第8页 共8页