文档内容
南充高中高2024级高一下学期期中考试 5.N
A
为阿伏加德罗常数的值。下列说法正确的是
A.标准状况下,22.4LSO 分子数为N
3 A
化 学 试 题
B.0.1molFe溶解于过量硝酸中,电子转移数目0.2N
A
C.将2molNO与1molO 在密闭容器中混合,容器中分子数为2N
2 A
D.足量金属Zn与100mL18.4mol/L浓硫酸充分反应生成气体的分子数大于0.92N
A
时间:75分钟 总分:100分
6.下列离子方程式书写正确的是
注意事项: A.用氢氟酸刻蚀玻璃:SiO2-+4F-+6H+=SiF +3H O
3 4 2
1.答题前,务必将自己的姓名、班级、考号填写在答题卡规定的位置上。
B.已知:酸性H SO >HClO,向次氯酸钙溶液中通入SO :
2 3 2
2.答选择题时,必须使用2B铅笔将答题卡上对应题目的答案标号涂黑,如需改动,用橡皮擦擦 Ca2++2ClO SO +H O=CaSO 2HClO
2 2 3
干净后,再选涂其它答案标号。
△
C.向NH HCO 溶液中加过量的NaOH溶液并加热: NH +OH- ==== NH ↑ + H O
4 3 4 3 2
3.答非选择题时,将答案书写在答题卡相应位置上,写在本试卷上无效。
D.Zn溶于过量的浓硝酸:Zn+4H++2NO-=Zn2++2NO +2H O
可能用到的相对原子质量:H—1 N—14 O—16 S—32 3 2 2
7.用下列实验装置完成对应实验,能达到实验目的的是
一、选择题:(本大题共15小题,每题只有一个选项符合题意,每题3分,共45分)
1.化学与生活密切相关,下列说法正确的是
A.碳化硅(SiC)具有优异的高温抗氧化性能,可用作耐高温的半导体材料
B.SO 可用于丝织品漂白是由于其能氧化丝织品中的有色成分
2
C.维生素C可用于水果罐头的抗氧化剂是由于其难以被氧化
D.新能源汽车所使用的三元锂电池和磷酸铁锂电池都属于一次电池
2.下列变化属于放热反应的是 A B C D
A.CO 通过炽热的炭层 B.浓硫酸溶于水
2
A.制取并收集少量氨气 B.比较KMnO、Cl、S的氧化性强弱
4 2
C.氢气与氯气反应 D.碳酸氢钠与稀盐酸反应
C.用于验证反应是否有CO 生成 D.探究Fe3+、Cu2+对H O 分解速率的影响
2 2 2
3.下列实验过程中,始
.
终
.
无
.
明显现象的是
8.硫和氮元素的类别与化合价的对应关系,下列说法错
.
误
.
的是
A.NO 通入FeSO 溶液中 B.CO 通入CaCl 溶液中
2 4 2 2
C.NH 通入AlCl 溶液中 D.SO 通入Ba(NO ) 溶液中
3 3 2 3 2
4.下列有关化学用语表示正确的是
A.二氧化碳分子结构模型:
B.离子结构示意图 ,可以表示32S2,又可以表示34S2 A.c与a的水溶液反应生成b,体现c的氧化性
B.g的浓水溶液可检验输送氯气的管道是否泄漏
C.加热条件下,Cu能与e的浓溶液发生反应,结束后向剩余溶液加水呈蓝色,可证明生成
C.氯化铵的电子式:
了f点对应的铜盐
D.次溴酸的结构式:H—Br—O D.f与l可能是同一种物质
南充高中高2024级高一下学期期中 化学试题 第1页 共8页 南充高中高2024级高一下学期期中 化学试题 第2页 共8页9. 对下列有关装置的说法正确的是 12.甲烷与氧气反应过程中的能量变化如图所示。下列有关说法中正确的是
A.装置Ⅰ中镁为原电池的负极
A.1mol CH (g)的能量大于1mol CO (g)和2mol H O(g)的能量总和
4 2 2
B.装置Ⅱ在工作时正负极质量均增加
B.该反应可以设计成燃料电池,将CH 和O 储存在电池内部
4 2
C.装置Ⅲ能构成原电池
C.若破坏1mol O (g)中的化学键需吸收热量493kJ,则破坏1mol C-H键需吸收热量415kJ
2
D.装置Ⅳ工作时,锌筒作负极,发生还原反应,锌筒会变薄
D.1mol CH (g)在O (g)中完全燃烧生成2mol H O(l)向外界释放800kJ的能量
4 2 2
10.某温度下,将等物质的量的气体A、B混合于2L的恒容密闭容器中,发生如下反应:A(g)
13.在恒容密闭容器中投入1molC和1molBaSO ,一定温度下发生反应:
4
+3B(g) 2C(g)+2D(g),经2min后测得B的物质的量分数为25%,以D表示的反应速率
3C(s)+BaSO (s) BaS(s)+2CO(g)+CO (g)。下列情况下表明该反应达到限度(平衡状态)的是
4 2
v(D)=0.25mol/(L·min),下列说法正确的是 A.混合气体平均摩尔质量不再变化 B.CO的体积分数不再变化
A.2min时,B的浓度为1.5mol/L C. 硫酸钡浓度不再变化 D.混合气体密度不再变化
B.反应时,向容器中通入氦气,容器内压强增大,化学反应速率加快 14.某原电池装置如图所示,电池总反应为2Ag+Cl
2
===2AgCl。下列说法正确的是
C.A、B起始物质的量均为3mol
D.若混合气体的平均相对分子质量不变,则表明该反应已达到平衡状态
11.某化学兴趣小组同学设计了三组实验,探究反应温度、反应物浓度对化学反应速率的影响,
具体情况如表所示。
A.正极反应为AgCl+e-===Ag+Cl-
B.放电时,交换膜右侧溶液中有大量白色沉淀生成
C.若用NaCl溶液代替盐酸,则电池总反应随之改变
D.当电路中转移0.01mole-时,交换膜左侧溶液中约减少0.02mol离子
15.利用空气催化氧化法除掉电石渣浆(含CaO)上清液中的S2,制取石膏CaSO 2H O的过程
4 2
如图,下列说法错误的是
..
下列有关说法错误的是( )
..
A.
A.CaSO 2H O属于盐类和纯净物
B. 4 2
=0
B.将10L上清液中的S2(S2浓度为480mgL1)转化为SO2,理论上共需要0.15molO
C.实验1和实验3是探究反应温度对反应速率的影响 4 2
= =10
C.过程I后溶液碱性减弱
D.实验1中发生反应的离子方程式为
− − − 2− +
D.过程Ⅱ中,反应的离子方程式为2S24MnO29H O4Mn(OH) S O210OH
3HSO3 +ClO3 =Cl +3SO4 +3H 3 2 2 2 3
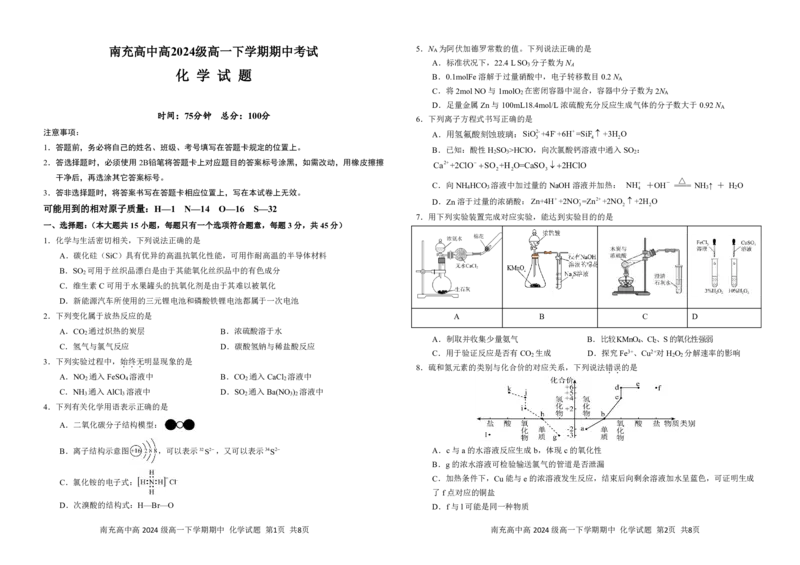
南充高中高2024级高一下学期期中 化学试题 第3页 共8页 南充高中高2024级高一下学期期中 化学试题 第4页 共8页二、非选择题:(本大题共 4个小题,共 55分) 17.(13分)肼N H 常用作火箭的燃料,实验室模拟氨和次氯酸钠反应制备肼,装置如图所示,
2 4
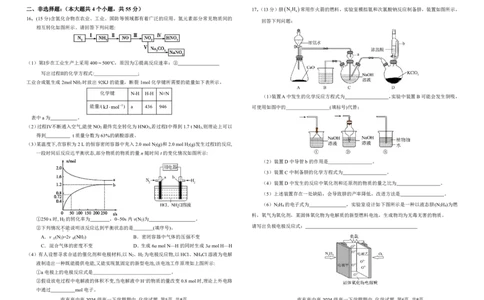
16.(15分)含氮化合物在农业、工业、国防等领域都有着广泛的应用。氮元素部分常见物质间的
回答下列问题:
相互转化如图所示。请回答下列问题:
(1)第Ⅰ步在工业生产上采用400~500℃,原因为①提高反应速率:②
写出过程Ⅱ的化学方程式: ;
工业合成氨生成2molNH 时放出92KJ的能量,断裂1mol化学键所需要的能量如下表所示,
3
化学键 N-H H-H N≡N
(1)装置A中发生的化学反应方程式为 ,实验中装置B可能会发生倒吸,
能量/(kJmol1) a 436 946 可使用如图中的 (填标号)代替;
表中a为 。
(2)过程Ⅳ不断通入空气,能使NO 最终完全转化为HNO ,若过程Ⅰ中得到1.7tNH ,则理论上可以
2 3 3
得到 t质量分数为63%的硝酸溶液。
(3)某温度下,在容积为2L的恒容密闭容器中充入2.0molN (g)和2.0molH (g)发生过程Ⅰ的反应,
2 2
一段时间后反应达平衡状态,部分物质的物质的量n随时间t的变化情况如图所示:
(2)装置D中导管b的作用是 。
(3)装置C中制备肼的化学方程式为 。
(4)装置D中发生的反应中氧化剂和还原剂的物质的量之比为 。
(5)上述装置存在一处缺陷,会导致肼的产率降低,改进方法是 。
(6)N H 的电子式为 ,实验室设计如下图所示是一种以液态肼(N H )为燃
2 4 2 4
料,氧气为氧化剂,某固体氧化物为电解质的新型燃料电池,生成物均为无毒无害的物质。
①250s时,H 的转化率为 ,0~50s内v(N )为 。
2 2
请写出负极电极反应式:
②下列情况不
.
能
.
说明该反应达到平衡状态的是 (填序号)。
A.v (N )=2v (NH ) B.密闭容器中气体的压强不变
正 2 逆 3
C.混合气体的密度不变 D.生成6amolN—H的同时生成3amolH—H
(4)有人设想寻求合适的催化剂和电极材料,以N 、H 为电极反应物,以HCl、NH Cl溶液为电解
2 2 4
液制造出一种既能提供电能,又能实现氮固定的新型电池,该电池工作原理如上图所示:
①a电极上的电极反应式是 。
②假设放电过程中电解液的体积不变,当电解液中H+的物质的量改变0.8mol时,理论上外电路
中通过 mol电子。
南充高中高2024级高一下学期期中 化学试题 第5页 共8页 南充高中高2024级高一下学期期中 化学试题 第6页 共8页18. (14分)从失效的废银催化剂中回收银具有极高的社会、经济价值。废银催化剂主要由银和
(4)某同学利用NaOH溶液研究和处理NOx ,主要反应为NO+NO +2OH 2NO H O、
α-氧化铝及少量二氧化硅组成,其回收工艺流程如下: 2 2 2
2NO +2OH NO NO H O
2 2 3 2
①下列措施能提高NO和NO 去除率的有 (填字母)。
2
A.采用气、液逆流的方式吸收尾气
B.加快通入尾气的速率
已知:α-氧化铝不溶于硝酸;AgCl能与Cl-反应生成溶于水的[AgCl ]-、[AgCl ]2-等离子。
2 3 C.吸收尾气过程中定期补加适量NaOH溶液
回答下列问题:
D.升高反应温度
(1)酸浸时,反应的离子方程式为________________________________________;
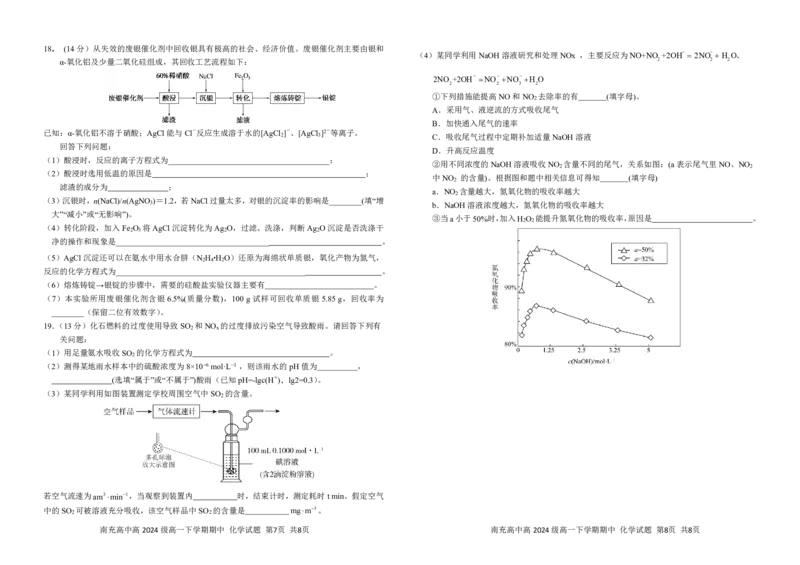
②用不同浓度的NaOH溶液吸收NO 含量不同的尾气,关系如图:(a表示尾气里NO、NO
2 2
(2)酸浸时选用低温的原因是 ;
中NO 的含量)。根据图和题中相关信息可得知 (填字母)
2
滤渣的成分为 ;
a.NO 含量越大,氮氧化物的吸收率越大
2
(3)沉银时,n(NaCl)/n(AgNO )=1.2,若NaCl过量太多,对银的沉淀率的影响是________(填“增
3 b.NaOH溶液浓度越大,氮氧化物的吸收率越大
大”“减小”或“无影响”)。
③当a小于50%时,加入H O 能提升氮氧化物的吸收率,原因是 。
2 2
(4)转化阶段,加入Fe O 将AgCl沉淀转化为Ag O,过滤、洗涤,判断Ag O沉淀是否洗涤干
2 3 2 2
净的操作和现象是______________________________________ 。
(5)AgCl沉淀还可以在氨水中用水合肼(N H . H O)还原为海绵状单质银,氧化产物为氮气,
2 4 2
反应的化学方程式为_______________________________________________ 。
(6)熔炼铸锭→银锭的步骤中,需要的硅酸盐实验仪器主要有 。
(7)本实验所用废银催化剂含银6.5%(质量分数),100 g 试样可回收单质银 5.85g,回收率为
________(保留二位有效数字)。
19.(13分)化石燃料的过度使用导致SO 和NO 的过度排放污染空气导致酸雨。请回答下列有
2 x
关问题:
(1)用足量氨水吸收SO 的化学方程式为 。
2
(2)测得某地雨水样本中的硫酸浓度为8×10−6mol·L−1 ,则该雨水的pH值为 ,
(选填“属于”或“不属于”)酸雨(已知pH=-lgc(H+),lg2=0.3)。
(3)某同学利用如图装置测定学校周围空气中SO 的含量。
2
若空气流速为am3min1,当观察到装置内 时,结束计时,测定耗时tmin。假定空气
中的SO 可被溶液充分吸收,该空气样品中SO 的含量是 mgm3。
2 2
南充高中高2024级高一下学期期中 化学试题 第7页 共8页 南充高中高2024级高一下学期期中 化学试题 第8页 共8页