文档内容
微信公众号:上海通优教案资料中心
初三年级学业质量抽样调研
化学学科
相对原子质量:H-1 C-12 O-16 S-32 Cu-64
一、制作酸菜(10分)
我国制作酸菜的历史颇为悠久,制作酸菜的初衷是为了延长蔬菜保存时间。制作过程中会产生大量乳
酸,赋予酸菜独特的风味。蔬菜中含有硝酸盐,它对人体无直接危害,但会转化成亚硝酸盐。若食物中的
亚硝酸盐含量过高会危害人体健康,应严格控制其含量。
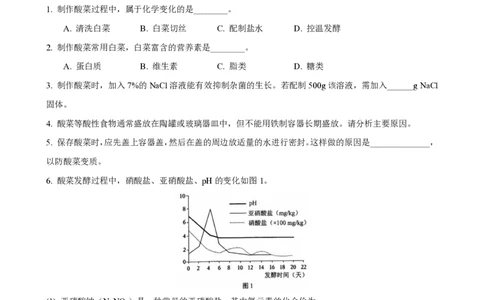
1. 制作酸菜过程中,属于化学变化的是________。
A. 清洗白菜 B. 白菜切丝 C. 配制盐水 D. 控温发酵
2. 制作酸菜常用白菜,白菜富含的营养素是________。
A. 蛋白质 B. 维生素 C. 脂类 D. 糖类
3. 制作酸菜时,加入7%的NaCl溶液能有效抑制杂菌的生长。若配制500g该溶液,需加入______g NaCl
固体。
4. 酸菜等酸性食物通常盛放在陶罐或玻璃器皿中,但不能用铁制容器长期盛放。请分析主要原因。
5. 保存酸菜时,应先盖上容器盖,然后在盖的周边放适量的水进行密封。这样做的原因是______________,
以防酸菜变质。
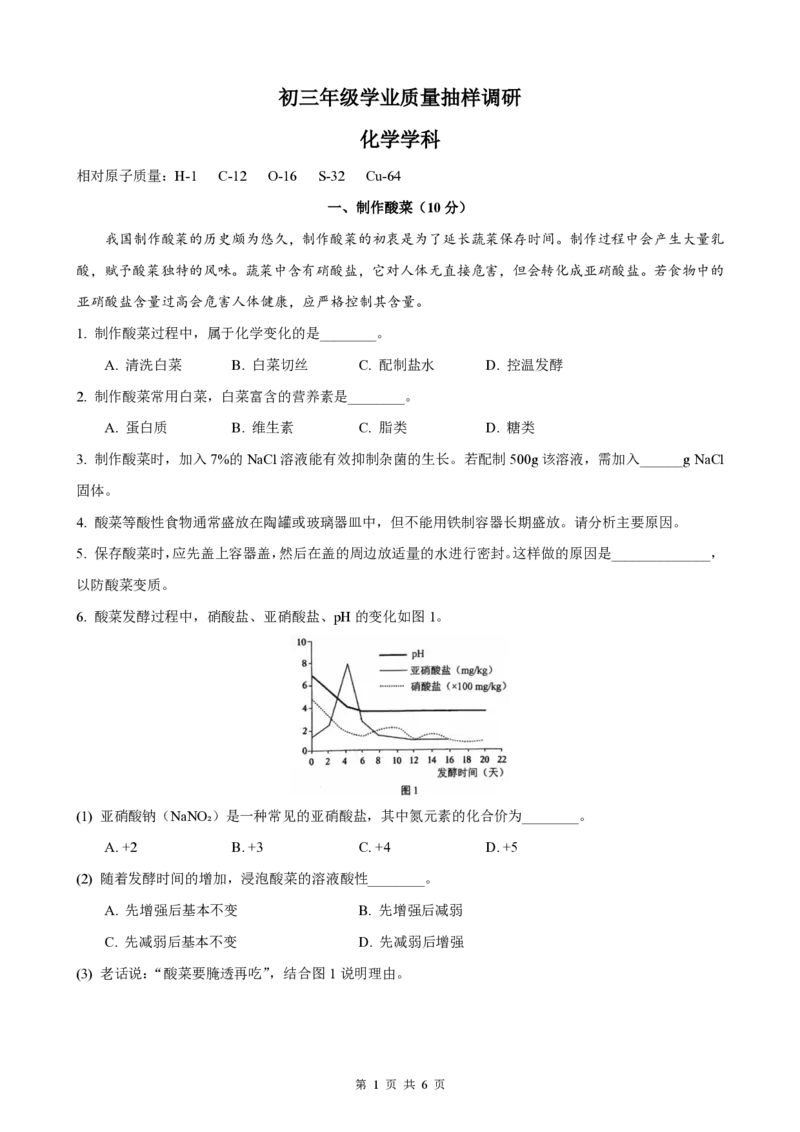
6. 酸菜发酵过程中,硝酸盐、亚硝酸盐、pH的变化如图1。
(1) 亚硝酸钠(NaNO₂)是一种常见的亚硝酸盐,其中氮元素的化合价为________。
A. +2 B. +3 C. +4 D. +5
(2) 随着发酵时间的增加,浸泡酸菜的溶液酸性________。
A. 先增强后基本不变 B. 先增强后减弱
C. 先减弱后基本不变 D. 先减弱后增强
(3) 老话说:“酸菜要腌透再吃”,结合图1说明理由。
第 1 页 共 6 页微信公众号:上海通优教案资料中心
二、汽车能源的变迁(10分)
由于化石燃料消耗很快且不可再生,使用过程中还会对环境造成污染。因此,汽车从依赖化石燃料的
传统类型,逐渐向多元化的新能源汽车发展。技术的进步,正持续推动着能源利用方式的变迁。
7. 传统汽车是将汽油(主要成分 C₈H₁₈)先喷成雾状再送入气缸中燃烧,目的是________。
A. 提供充足的空气 B. 减少二氧化碳的排放
C. 增大氧气的浓度 D. 增大可燃物与空气的接触面积
8. 粮食等生物质原料在微生物作用下,经发酵可以得到乙醇(C₂H₆O)。在汽油中加入适量的乙醇可以制成
车用乙醇汽油。
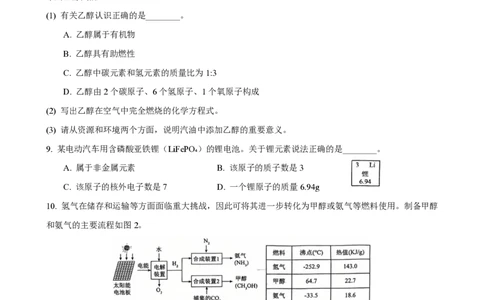
(1) 有关乙醇认识正确的是________。
A. 乙醇属于有机物
B. 乙醇具有助燃性
C. 乙醇中碳元素和氢元素的质量比为1:3
D. 乙醇由2个碳原子、6个氢原子、1个氧原子构成
(2) 写出乙醇在空气中完全燃烧的化学方程式。
(3) 请从资源和环境两个方面,说明汽油中添加乙醇的重要意义。
9. 某电动汽车用含磷酸亚铁锂(LiFePO₄)的锂电池。关于锂元素说法正确的是________。
A. 属于非金属元素 B. 该原子的质子数是3
C. 该原子的核外电子数是7 D. 一个锂原子的质量6.94g
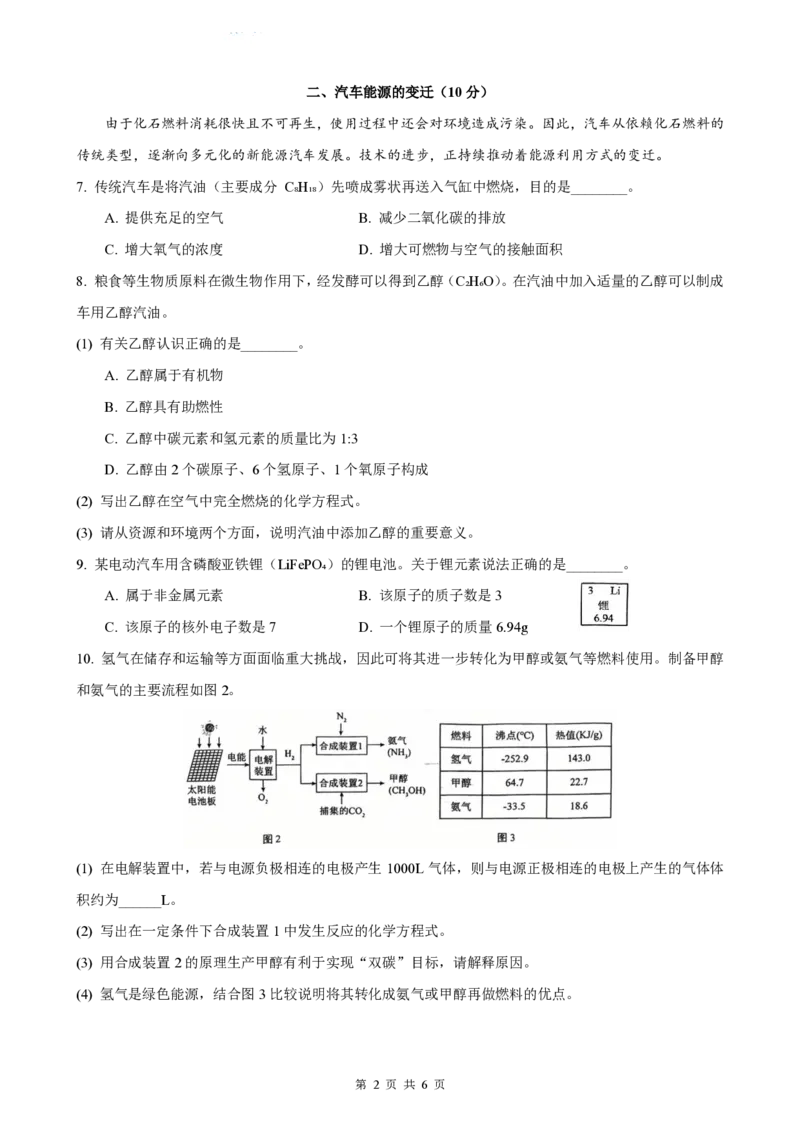
10. 氢气在储存和运输等方面面临重大挑战,因此可将其进一步转化为甲醇或氨气等燃料使用。制备甲醇
和氨气的主要流程如图2。
(1) 在电解装置中,若与电源负极相连的电极产生 1000L 气体,则与电源正极相连的电极上产生的气体体
积约为______L。
(2) 写出在一定条件下合成装置1中发生反应的化学方程式。
(3) 用合成装置2的原理生产甲醇有利于实现“双碳”目标,请解释原因。
(4) 氢气是绿色能源,结合图3比较说明将其转化成氨气或甲醇再做燃料的优点。
第 2 页 共 6 页微信公众号:上海通优教案资料中心
三、制氧机(8分)
制氧机常用于医疗氧疗与保健供氧。
11. 富氧膜制氧机是利用不同气体在特殊膜中渗透速率的差异对气体进行分离。在压力驱动下,氧气比氮
气更快透过膜,在膜的另一侧富集成氧气浓度为25%~40%的富氧空气。
(1) 空气中氧气的体积分数约为______%。
(2) 分子动力学直径是导致分子渗透速率差异的主要因素。动力学直径小的分子能更快的渗透通过膜材料,
实现不同气体的分离和富集。推测O₂动力学直径______(填 “大于”或 “小于”)N₂动力学直径。
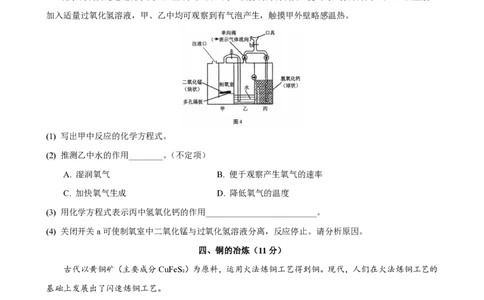
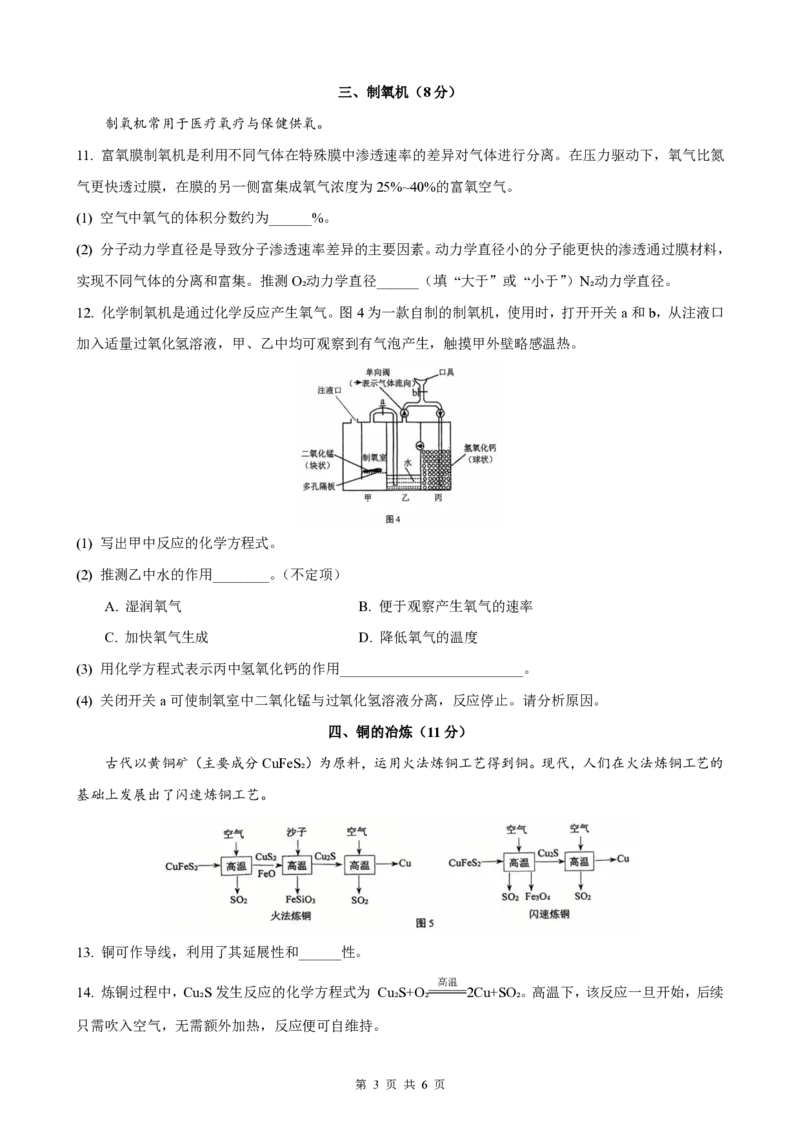
12. 化学制氧机是通过化学反应产生氧气。图4为一款自制的制氧机,使用时,打开开关a和b,从注液口
加入适量过氧化氢溶液,甲、乙中均可观察到有气泡产生,触摸甲外壁略感温热。
(1) 写出甲中反应的化学方程式。
(2) 推测乙中水的作用________。(不定项)
A. 湿润氧气 B. 便于观察产生氧气的速率
C. 加快氧气生成 D. 降低氧气的温度
(3) 用化学方程式表示丙中氢氧化钙的作用__________________________。
(4) 关闭开关a可使制氧室中二氧化锰与过氧化氢溶液分离,反应停止。请分析原因。
四、铜的冶炼(11分)
古代以黄铜矿(主要成分CuFeS₂)为原料,运用火法炼铜工艺得到铜。现代,人们在火法炼铜工艺的
基础上发展出了闪速炼铜工艺。
13. 铜可作导线,利用了其延展性和______性。
高温
14. 炼铜过程中,Cu₂S发生反应的化学方程式为 Cu₂S+O₂ 2Cu+SO₂。高温下,该反应一旦开始,后续
只需吹入空气,无需额外加热,反应便可自维持。
第 3 页 共 6 页微信公众号:上海通优教案资料中心
(1) 该反应的基本反应类型是_______。
A. 化合反应 B. 分解反应 C. 复分解反应 D. 置换反应
(2) 推测该反应是______(填“放热”或“吸热”)反应。
(3) 若将1600g Cu₂S完全转化成铜,计算理论上需要氧气的质量。(根据化学方程式列式计算)
(4) 分析说明上述反应中通入空气的量对产物的影响。
高温
15. 闪速炼铜中回收Fe₃O₄的原理是:2C+Fe₃O₄ 3Fe+2X,X的化学式是______。
16. 对比火法炼铜,闪速炼铜的优势有______。(不定项)
A. 原料种类更少 B. 无污染
C. 得到的铜更多 D. 工艺流程简单
五、碳酸钙的提纯(11分)
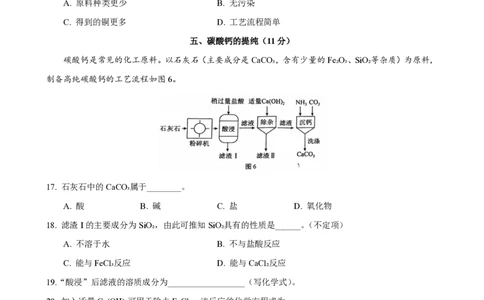
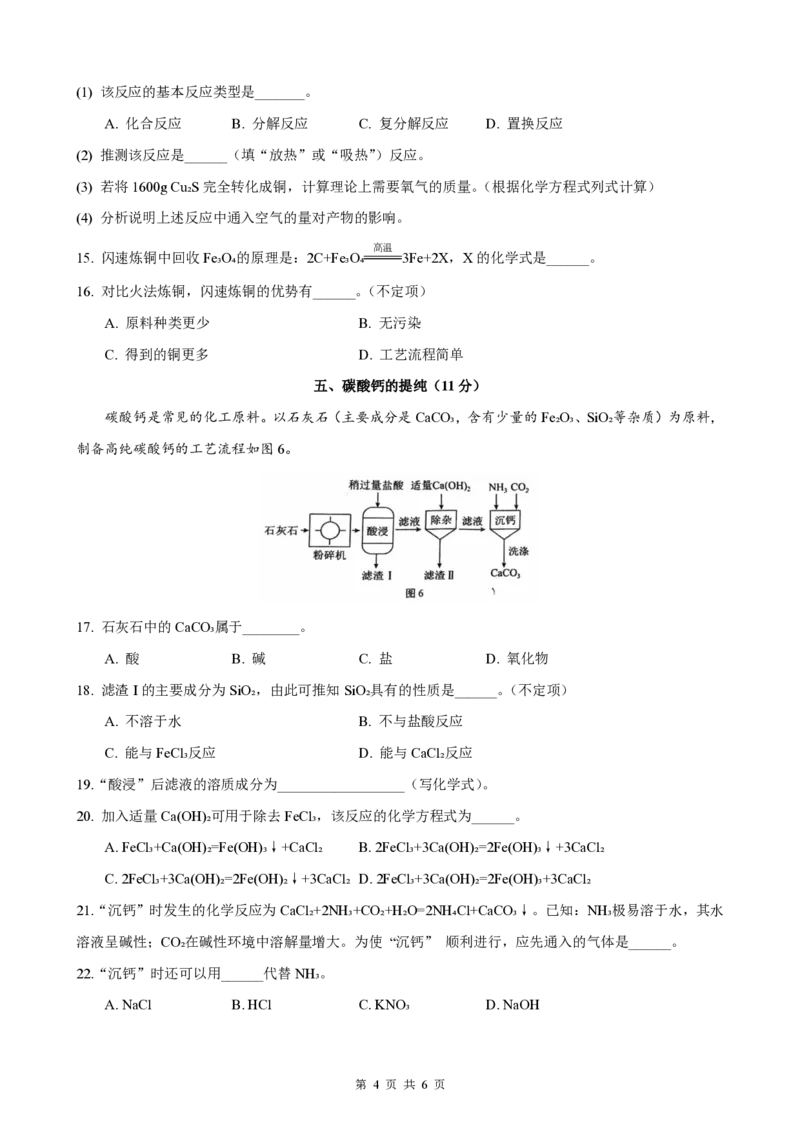
碳酸钙是常见的化工原料。以石灰石(主要成分是CaCO₃,含有少量的Fe₂O₃、SiO₂等杂质)为原料,
制备高纯碳酸钙的工艺流程如图6。
17. 石灰石中的CaCO₃属于________。
A. 酸 B. 碱 C. 盐 D. 氧化物
18. 滤渣I的主要成分为SiO₂,由此可推知SiO₂具有的性质是______。(不定项)
A. 不溶于水 B. 不与盐酸反应
C. 能与FeCl₃反应 D. 能与CaCl₂反应
19.“酸浸”后滤液的溶质成分为__________________(写化学式)。
20. 加入适量Ca(OH)₂可用于除去FeCl₃,该反应的化学方程式为______。
A. FeCl₃+Ca(OH)₂=Fe(OH)₃↓+CaCl₂ B. 2FeCl₃+3Ca(OH)₂=2Fe(OH)₃↓+3CaCl₂
C. 2FeCl₃+3Ca(OH)₂=2Fe(OH)₂↓+3CaCl₂ D. 2FeCl₃+3Ca(OH)₂=2Fe(OH)₃+3CaCl₂
21.“沉钙”时发生的化学反应为CaCl₂+2NH₃+CO₂+H₂O=2NH₄Cl+CaCO₃↓。已知:NH₃极易溶于水,其水
溶液呈碱性;CO₂在碱性环境中溶解量增大。为使 “沉钙” 顺利进行,应先通入的气体是______。
22.“沉钙”时还可以用______代替NH₃。
A. NaCl B. HCl C. KNO₃ D. NaOH
第 4 页 共 6 页微信公众号:上海通优教案资料中心
参考答案
一、制作酸菜(10分)
1. D
2. B
3. 35
4. 酸菜呈酸性,铁能与酸反应,会腐蚀容器且污染食物
5. 隔绝氧气(空气),防止酸菜被氧化
6. (1) B
(2) A
(3) 腌透后亚硝酸盐含量降低,达到安全值,食用更健康
二、汽车能源的变迁(10分)
7. D
8. (1) A
点燃
(2) C H O+3O 2CO +3H O
2 6 2 2 2
(3) 资源:可再生,节约化石能源;环境:污染更小,更环保
9. B
10. (1) 500
一定条件
(2) N +3H 2NH
2 2 3
(3) 消耗CO₂,减少碳排放
(4) 沸点更高,更容易液化,便于储存和运输
三、制氧机(8分)
11. (1) 21
(2) 小于
12. (1) 2H O
MnO2
2H O+O ↑
2 2 2 2
(2) ABD
(3) CO +Ca(OH) =CaCO ↓+H O
2 2 3 2
(4) 关闭a,装置内压强增大,将液体压回,固液分离,反应停止
四、铜的冶炼(11分)
13. 导电
14. (1) D
第 5 页 共 6 页微信公众号:上海通优教案资料中心
(2) 放热
(3) 320g
(4) 空气不足,产物含Cu₂S;空气充足,生成Cu
15. CO
2
16. AD
五、碳酸钙的提纯(11分)
17. C
18. AB
19. CaCl₂、FeCl₃、HCl
20. B
21. NH₃
22. D
第 6 页 共 6 页