文档内容
2021 年上海等级性考试化学试卷
一、选择题(本大题共20小题)
1.实施碳达峰,碳中和是应对国际新变局、构建新发展格局、落实新发展理念的重大战略
布局,上海自2013年起作为全国7个试点城市之一开展碳交易试点,以下符合碳中和目
的的是( )
A.完全不排放CO B.CO 排放量相对为零
2 2
C.只用风能、太阳能等清洁能源 D.用碱吸收所有生成的CO
2
2.以下关于氚的说法正确的是( )
A.质子数为2 B.电子数为3
C.质量数为4 D.氚原子和1H化学性质相似
3.石油是工业的血液,以下关于石油说法正确的是( )
A.密度比水大 B.属于纯净物
C.分馏得到汽油 D.石油全是由芳香烃组成
4.以下关于合金说法不正确的是( )
A.熔点比组分中的纯金属高 B.具有金属的一般特性
C.硬度比组分中的纯金属高 D.运用范围比单一金属广泛
5.下列物质的三态变化只与分子间作用力有关的是( )
A.CCl B. NaCl C.AI D. KCIO
4 3
6.以下哪个既含氯离子又含氯分子( )
A.液氯 B.氯水 C.氯化钙 D.盐酸
7.下列化合物中有非极性共价键的是( )
A.KOH B.SiO C. HCOOCH D. Na O
2 3 2 2
8.下列使用稀硫酸或浓硫酸的方法正确的是( )
A.浓硫酸和乙醇加热到170℃制乙烯 B.常温下浓硫酸和铁制硫酸铁
C.稀硫酸和铜加热制二氧化硫 D.稀硫酸和氯化钠固体共热制备氯化氢
9.关于二氯甲烷,以下说法错误的是( )
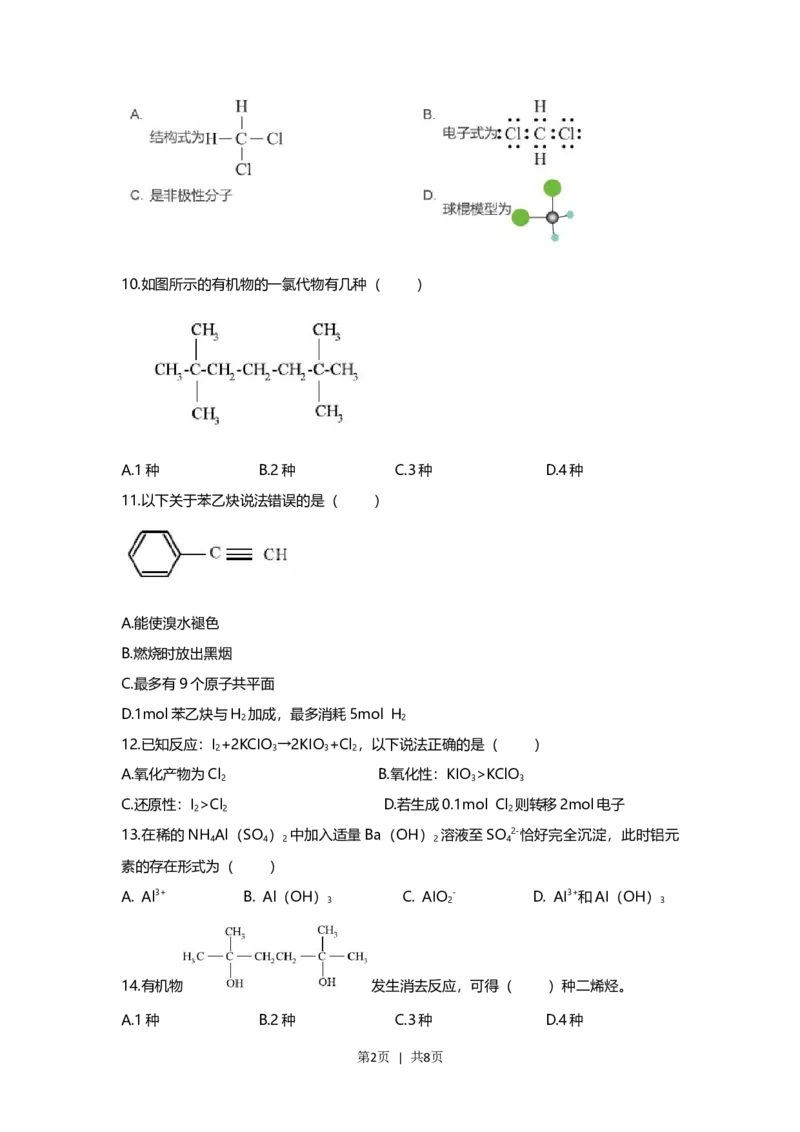
第1页 | 共8页10.如图所示的有机物的一氯代物有几种( )
A.1种 B.2种 C.3种 D.4种
11.以下关于苯乙炔说法错误的是( )
A.能使溴水褪色
B.燃烧时放出黑烟
C.最多有9个原子共平面
D.1mol苯乙炔与H 加成,最多消耗5mol H
2 2
12.已知反应:I +2KCIO →2KIO +Cl ,以下说法正确的是( )
2 3 3 2
A.氧化产物为Cl B.氧化性:KIO >KClO
2 3 3
C.还原性:I >Cl D.若生成0.1mol Cl 则转移2mol电子
2 2 2
13.在稀的NH Al(SO ) 中加入适量Ba(OH) 溶液至SO 2-恰好完全沉淀,此时铝元
4 4 2 2 4
素的存在形式为( )
A. Al3+ B. Al(OH) C. AIO - D. AI3+和AI(OH)
3 2 3
14.有机物 发生消去反应,可得( )种二烯烃。
A.1种 B.2种 C.3种 D.4种
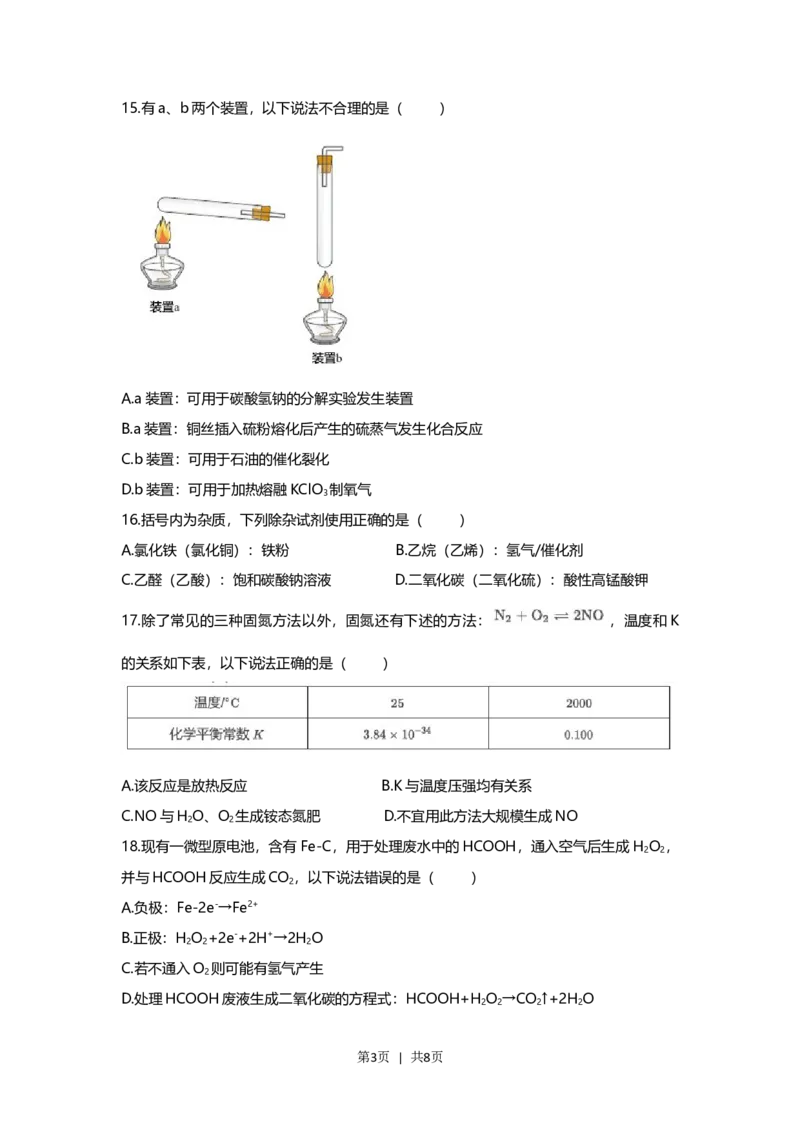
第2页 | 共8页15.有a、b两个装置,以下说法不合理的是( )
A.a装置:可用于碳酸氢钠的分解实验发生装置
B.a装置:铜丝插入硫粉熔化后产生的硫蒸气发生化合反应
C.b装置:可用于石油的催化裂化
D.b装置:可用于加热熔融KClO 制氧气
3
16.括号内为杂质,下列除杂试剂使用正确的是( )
A.氯化铁(氯化铜):铁粉 B.乙烷(乙烯):氢气/催化剂
C.乙醛(乙酸):饱和碳酸钠溶液 D.二氧化碳(二氧化硫):酸性高锰酸钾
17.除了常见的三种固氮方法以外,固氮还有下述的方法: ,温度和K
的关系如下表,以下说法正确的是( )
A.该反应是放热反应 B.K与温度压强均有关系
C.NO与H O、O 生成铵态氮肥 D.不宜用此方法大规模生成NO
2 2
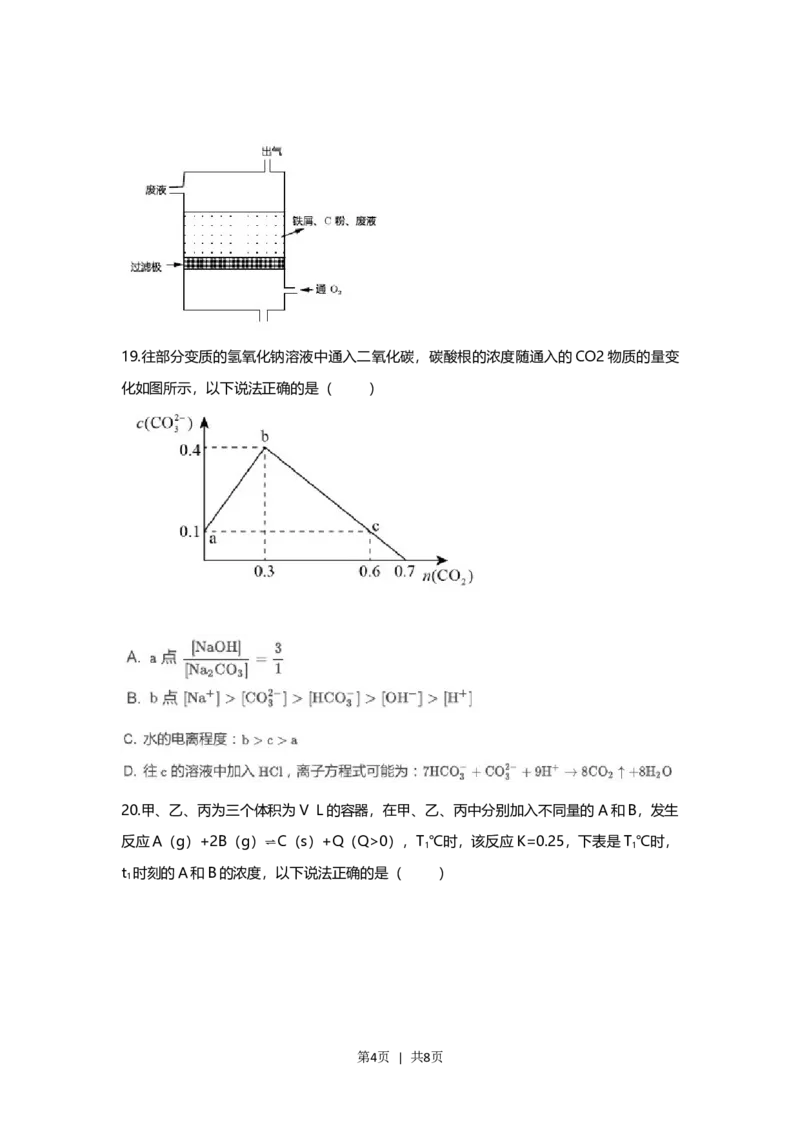
18.现有一微型原电池,含有Fe-C,用于处理废水中的HCOOH,通入空气后生成H O ,
2 2
并与HCOOH反应生成CO ,以下说法错误的是( )
2
A.负极:Fe-2e-→Fe2+
B.正极:H O +2e-+2H+→2H O
2 2 2
C.若不通入O 则可能有氢气产生
2
D.处理HCOOH废液生成二氧化碳的方程式:HCOOH+H O →CO ↑+2H O
2 2 2 2
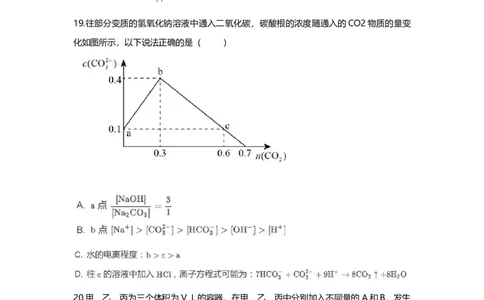
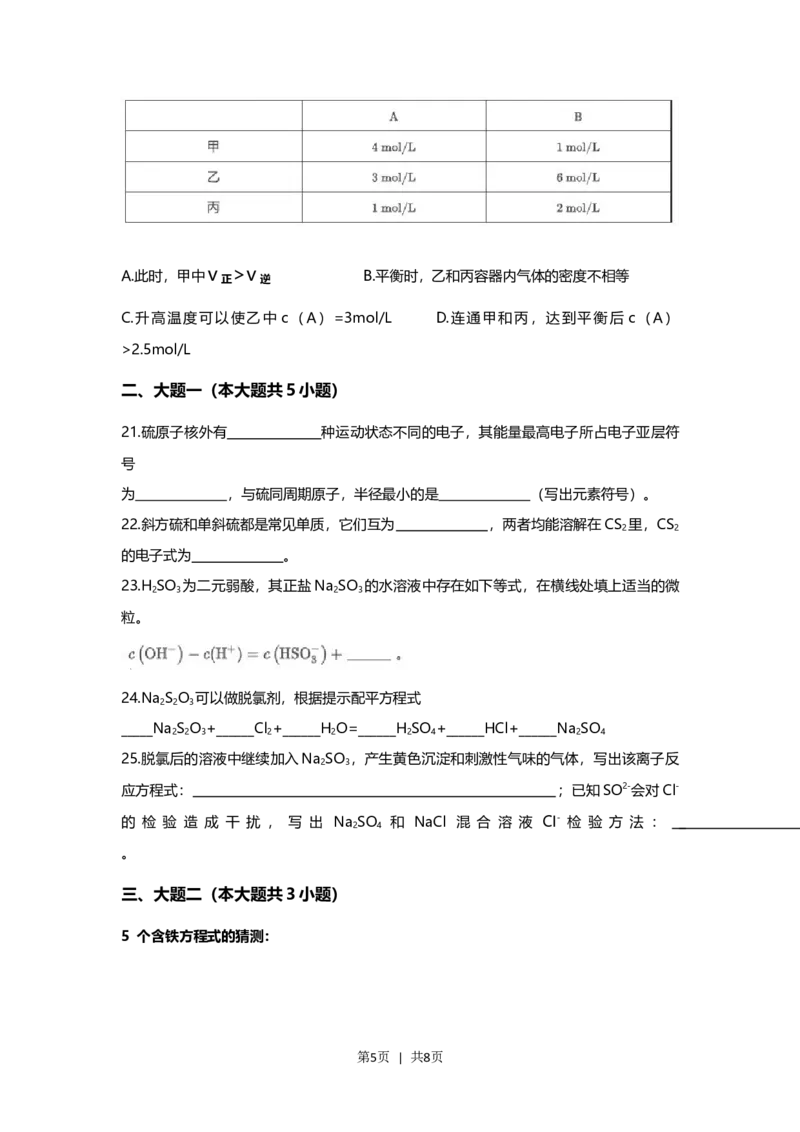
第3页 | 共8页19.往部分变质的氢氧化钠溶液中通入二氧化碳,碳酸根的浓度随通入的CO2物质的量变
化如图所示,以下说法正确的是( )
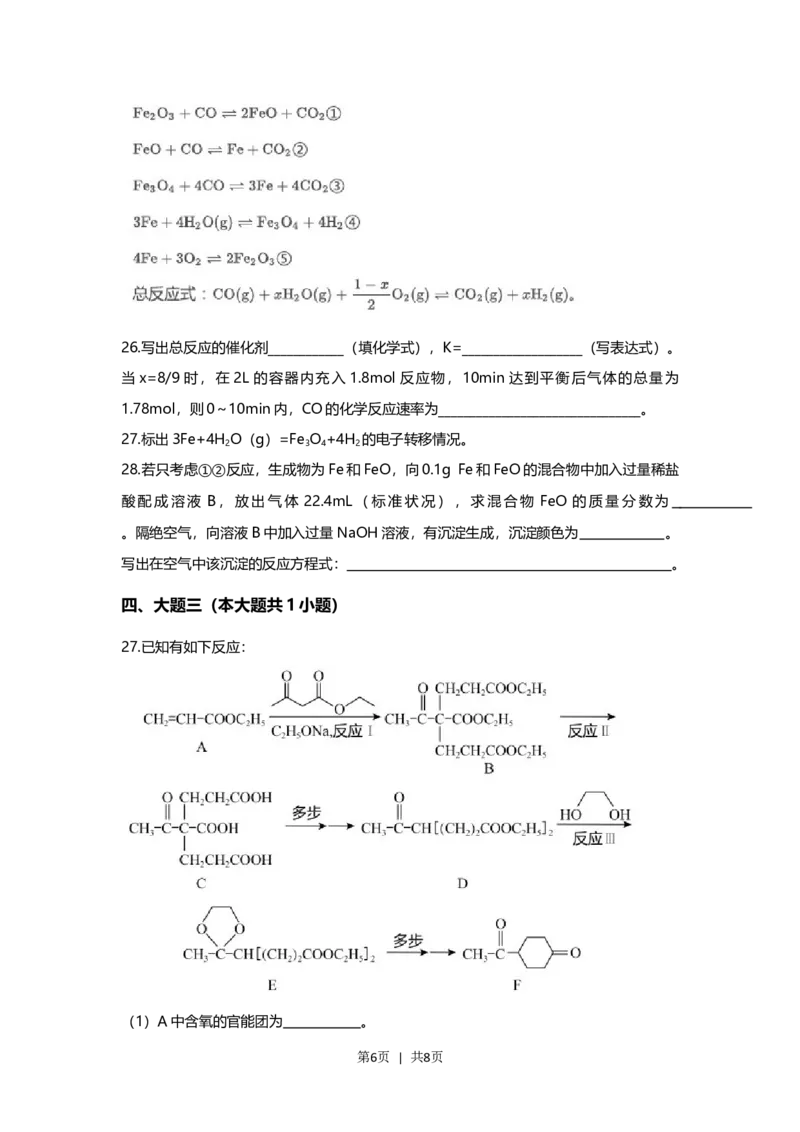
20.甲、乙、丙为三个体积为V L的容器,在甲、乙、丙中分别加入不同量的A和B,发生
反应A(g)+2B(g)⇌C(s)+Q(Q>0),T
1
℃时,该反应K=0.25,下表是T
1
℃时,
t 时刻的A和B的浓度,以下说法正确的是( )
1
第4页 | 共8页A.此时,甲中v >v B.平衡时,乙和丙容器内气体的密度不相等
正 逆
C.升高温度可以使乙中 c(A)=3mol/L D.连通甲和丙,达到平衡后 c(A)
>2.5mol/L
二、大题一(本大题共5小题)
21.硫原子核外有 种运动状态不同的电子,其能量最高电子所占电子亚层符
号
为 ,与硫同周期原子,半径最小的是 (写出元素符号)。
22.斜方硫和单斜硫都是常见单质,它们互为 ,两者均能溶解在CS 里,CS
2 2
的电子式为 。
23.H SO 为二元弱酸,其正盐Na SO 的水溶液中存在如下等式,在横线处填上适当的微
2 3 2 3
粒。
24.Na S O 可以做脱氯剂,根据提示配平方程式
2 2 3
_____Na S O +______Cl +______H O=______H SO +______HCl+______Na SO
2 2 3 2 2 2 4 2 4
25.脱氯后的溶液中继续加入Na SO ,产生黄色沉淀和刺激性气味的气体,写出该离子反
2 3
应方程式: ;已知SO2-会对Cl-
的 检 验 造 成 干 扰 , 写 出 Na SO 和 NaCl 混 合 溶 液 CI- 检 验 方 法 :
2 4
。
三、大题二(本大题共3小题)
5 个含铁方程式的猜测:
第5页 | 共8页26.写出总反应的催化剂____________(填化学式),K=___________________(写表达式)。
当 x=8/9 时,在 2L 的容器内充入 1.8mol 反应物,10min 达到平衡后气体的总量为
1.78mol,则0~10min内,CO的化学反应速率为________________________________。
27.标出3Fe+4H O(g)=Fe O +4H 的电子转移情况。
2 3 4 2
28.若只考虑①②反应,生成物为Fe和FeO,向0.1g Fe和FeO的混合物中加入过量稀盐
酸配成溶液 B,放出气体 22.4mL(标准状况),求混合物 FeO 的质量分数为
。隔绝空气,向溶液B中加入过量NaOH溶液,有沉淀生成,沉淀颜色为 。
写出在空气中该沉淀的反应方程式: 。
四、大题三(本大题共1小题)
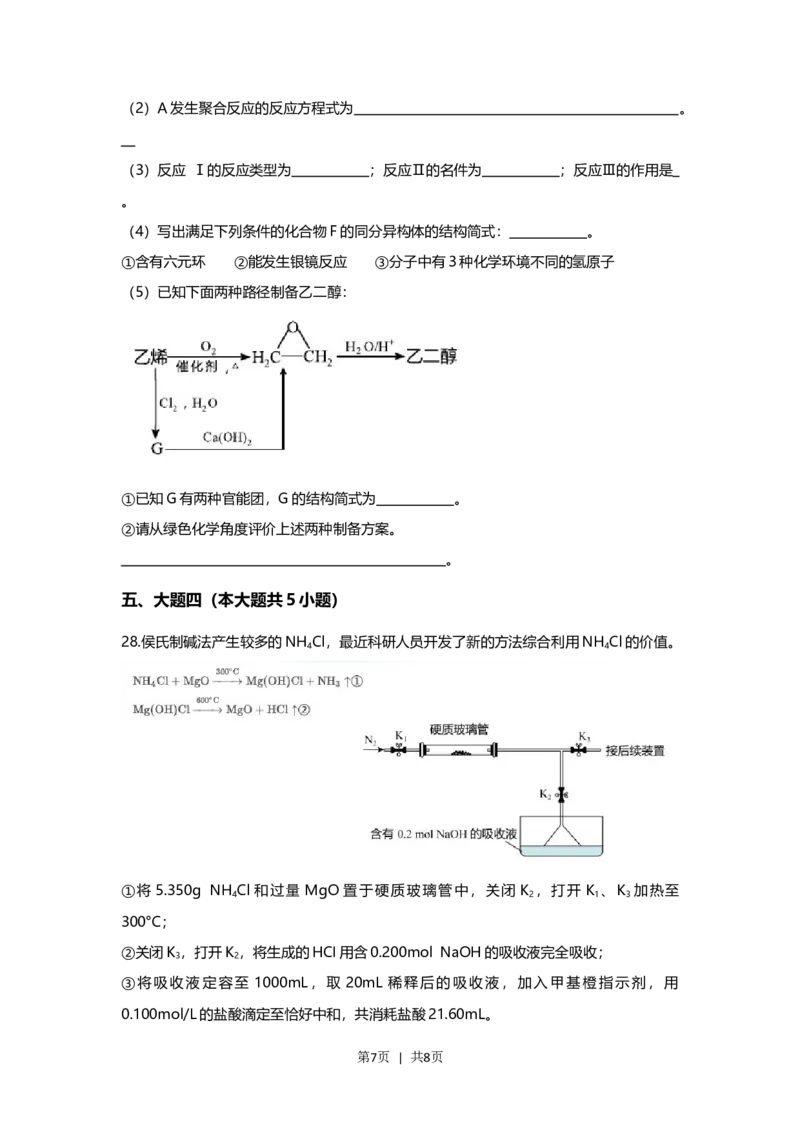
27.已知有如下反应:
(1)A中含氧的官能团为 。
第6页 | 共8页(2)A发生聚合反应的反应方程式为 。
(3)反应 Ⅰ的反应类型为 ;反应Ⅱ的名件为 ;反应Ⅲ的作用是
。
(4)写出满足下列条件的化合物F的同分异构体的结构简式: 。
①含有六元环 ②能发生银镜反应 ③分子中有3种化学环境不同的氢原子
(5)已知下面两种路径制备乙二醇:
①已知G有两种官能团,G的结构简式为 。
②请从绿色化学角度评价上述两种制备方案。
。
五、大题四(本大题共5小题)
28.侯氏制碱法产生较多的NH Cl,最近科研人员开发了新的方法综合利用NH Cl的价值。
4 4
①将 5.350g NH Cl 和过量 MgO 置于硬质玻璃管中,关闭 K ,打开 K 、K 加热至
4 2 1 3
300°C;
②关闭K ,打开K ,将生成的HCI用含0.200mol NaOH的吸收液完全吸收;
3 2
③将吸收液定容至 1000mL,取 20mL 稀释后的吸收液,加入甲基橙指示剂,用
0.100mol/L的盐酸滴定至恰好中和,共消耗盐酸21.60mL。
第7页 | 共8页( 1 ) . 实 验 室 不 能 通 过 直 接 加 热 NH Cl 制 取 NH 和 HCl , 原 因 是
4 3
__________________________。
(2).若要检查NH 是否被完全释放,应在A口处_____________________________________。
3
(3).步骤③中使用的定量仪器有__________________;滴定终点的溶液由 色变为
________色,并保持30s不变色。
(4).HCl的释放率用α表示,α=n(释放的HCl)/n(NH Cl的总量),即α(HCI)
4
=n(HCl)/nNH Cl),试计算 α=____________;若 HCl 未被吸收完全,则 α 值将会
4
___________(填“偏大”、“偏小”或“不变”)。
(5).试评价这种利用NH Cl综合价值的方法。
4
第8页 | 共8页