《北京市DCT项目管理体系文件要点专家共识》正式落地,15项模块规范全流程

文末可领取完整版PDF

重磅引领,范式确立
《北京市去中心化临床试验(DCT)项目管理体系文件要点专家共识》正式发布,为机构开展项目提供了清晰指引。
变革不止,DCT 学院即将发布《DCT 机构实践审查要点》《DCT 实施决策树》两大行业共识,聚焦 DCT 规模化落地痛点,敬请期待!
01
背景与意义
随着数字医疗技术的深度融合与创新应用,去中心化临床试验(DecentralizedClinicalTrials,DCT)正引领全球药物研发模式向更加高效、包容与以患者为中心的方向转型。
为积极应对这一变革,系统规范DCT在本市的科学、有序开展,北京市药品监督管理局前瞻性地组织十家试点机构,历经深入的实践探索与多轮研讨,共同制定了覆盖DCT全流程、全要素的《北京市DCT项目管理体系文件共识》
本共识体系由15项具体管理文件构成,旨在构建一个权责清晰、操作可行、质量可控的标准化管理框架。它不仅是将传统临床试验质量管理规范(GCP)原则成功适配于DCT研究场景的关键举措,更是本市在新药研发领域推动治理能力现代化、形成可复制推广的”北京经验”的一项重要制度性成果。现就核心管理要点达成如下共识,以供各相关机构遵照执行。
02
核心管理体系与实施要点
(一)项目启动与设计
DCT的开展需要严谨的设计与审慎的评估。本阶段需着重确保试验方案的科学性与远程模式的适用性、合规性。
方案设计:方案设计是确保试验科学性与远程操作可行性的基石。DCT方案设计遵循合规性基础,全面评估远程模式带来的便利性与潜在风险,重视提升试验参与者体验,利用数字化技术确保数据实时与准确,并明确界定可在机构外实施的环节及其技术要求。其具体规范与设计要求,详见附件《去中心化临床试验(DCT)中的方案设计》
立项审查:机构立项环节需评估DCT所使用的技术平台和工具在机构使用的可行性,确保相关技术的工作流程符合GCP要求。并审查DCT环节的试验参与者权益保护。详见:《去中心化临床试验(DCT)中的立项审查》
伦理审查:伦理审查需考虑到远程场景下的特有风险。重点关注电子知情同意的有效性、隐私保护的充分性、数据安全的措施及弱势群体可及性。详见:《去中心化临床试验(DCT)中的伦理审查》
(二)项目实施与执行:
DCT的执行质量依赖于对远程环节的精准管理和对关键流程的标准化控制。
远程招募:应利用合规的渠道进行招募,并确保宣传材料真实、易懂。重点关注招募过程的公平性与隐私保护。详见:《去中心化临床试验(DCT)中的远程招募》
电子知情同意:应采用可靠技术平台,确保试验参与者充分理解、自主决策,且过程全程记录、法律效力完整。重点关注电子知情同意流程的易用性、验证身份的有效性及文档的不可篡改性。详见:《去中心化临床试验(DCT)中的电子知情同意》
试验参与者培训和教育:应为试验参与者提供针对远程参与方式的专项培训。重点关注培训内容的易懂性、远程平台使用的熟练度及问题反馈渠道的畅通性。详见:《去中心化临床试验(DCT)中的试验参与者培训和教育》
药物直达试验参与者:应建立涵盖药品存储、运输、交接及用药指导的全链条标准化操作与追溯体系。重点关注药品质量受控、用药依从性核实、评估持续用药和药品回收机制。详见:《去中心化临床试验(DCT)中的药物直达管理》
就近使用医疗资源:应预先建立并验证本地医疗协作网络,以应对试验参与者的紧急医疗需求或需线下完成的检查。重点关注协作机构的资质、响应流程与数据共享机制。详见:《去中心化临床试验(DCT)中的就近使用医疗资源》
远程访视:研究者通过实时音视频等技术进行访视,应确保环境私密、沟通充分、医疗判断准确且记录完整。重点关注访视的规范性、远程访视的记录与紧急情况识别。详见:《去中心化临床试验(DCT)中的远程访视》
远程监查:监查员应基于风险,对电子化源数据和关键流程进行远程监查访问。重点关注系统安全与隔离、隐私保护与合规和权限分级管理。详见:《去中心化临床试验(DCT)中的远程监查》
安全性事件的管理:应建立高效的远程不良事件(AE)与严重不良事件(SAE)收集、评估与报告通路。重点关注试验参与者报告便捷性、研究者获知及时性与上报合规性。详见:《去中心化临床试验(DCT)中的安全性事件的管理》
(三)体系支撑与质量保障:
稳健的支撑体系是DCT项目数据可靠与质量可持续的根本。
质量管理体系:应建立基于风险的、适应DCT特点的全面质量管理体系。需制定融合DCT要素的管理文件、配备经过充分培训的专职质量管理人员以及对研究团队及受试者实施针对性培训等。详见:《去中心化临床试验(DCT)中的质量管理》
数据管理:在数据采集与传输环节,源数据系统需经验证,传输过程应加密。重点关注电子数据采集系统的安全、合规、可追溯及数据交接的完整性。详见:《去中心化临床试验(DCT)中的数据管理》
电子支付:试验参与者补贴等支付应采用安全、可追溯的电子化方式进行。重点关注支付流程的合规性、试验参与者个人信息保护与财务记录准确性。详见:《去中心化临床试验(DCT)中的电子支付》
档案管理:所有试验相关文件,包括电子源数据、电子知情同意记录等,均须完整保存,确保长期可读、安全可靠。重点关注档案的归档及时性、存储安全性与查阅权限控制。详见:《去中心化临床试验(DCT)中的档案管理》
03
总结与展望
本共识系统集成了前期试点工作的宝贵经验,将分散的管理要求整合为有机统一的操作体系。共识的发布与实施,旨在为各机构提供一套清晰、完整的DCT项目管理”工具箱”,降低探索成本,统一实施标准,最终保障试验参与者权益与试验数据质量。
我们相信,通过此共识的广泛应用与持续完善,必将有力推动DCT模式在本市乃至全国的规范化、规模化发展,为加快新药创制、满足患者需求贡献坚实的”北京智慧”与”北京方案”。
扫码领取完整版

添加DCT学院小助手
备注“姓名+公司+职务”
即可领取《北京市去中心化临床试验(DCT)
项目管体系文件要点专家共识》PDF文档
让我们携手共进,
将愿景化为行动,将挑战变为机遇。
共同推动中国DCT的创新发展,
为中国医药创新贡献坚实力量!
DCT学院,引领变革,定义未来。

关于DCT学院
DCT学院 (DCT Academy) 是一个专注于DCT 领域的专业社区。
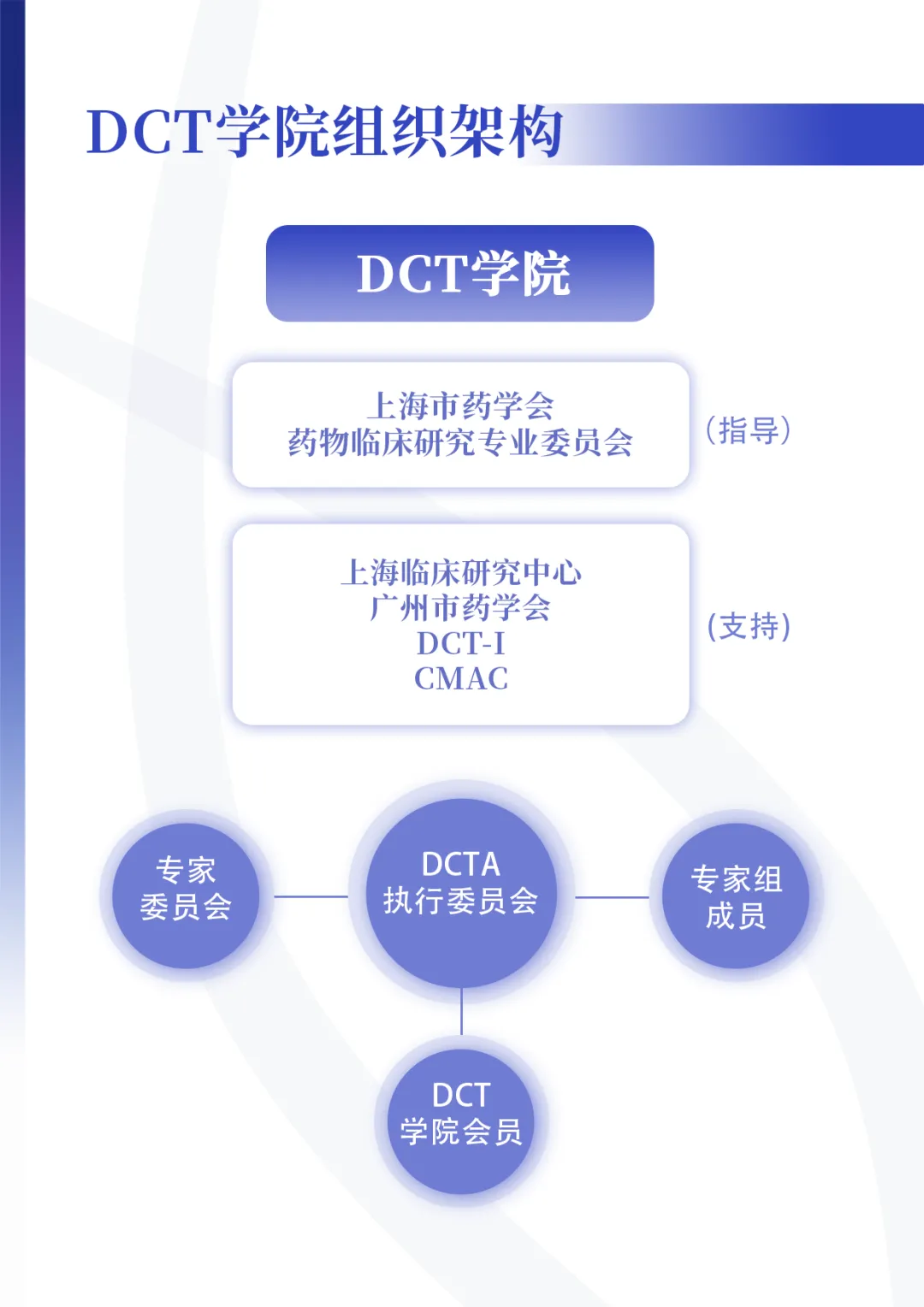
学院由上海市药学会药物临床研究专业委员会指导,并由上海临床研究中心、广州市药学会、DIA(DCT-I)及CMAC支持,由DCTA执行委员会负责具体运营。
学院借鉴商学院的会员制模式,携手国内外DCT实战专家,提供聚焦于方案设计、项目运营与合规管理的实战培训。我们摒弃空泛理论,通过深度案例剖析与沙盘演练,帮助会员将所学应用于实践,以应对真实世界中的各种挑战。
 夜雨聆风
夜雨聆风





