配位数+配体数+配位键数(Word)

部分内容展示
说明:本文介绍了配位化合物的基本概念和构成要素,包括中心离子/原子、配体、配位键和外界离子。解释了配位体的定义、特征以及单齿和多齿配位体的区别。阐述了配位数的计算方法,即中心离子周围配位原子的总数。同时,介绍了配体数和配位键数的计算,强调了配位键数等于配位数。什么是配位化合物?
配位化合物是中心离子或原子通过配位键结合一定数目的配位体,即提供孤对电子的分子或离子,形成的稳定化合物,配位化合物也叫配合物。
核心构成
1.中心离子/原子:通常是过渡金属离子,如Cu²⁺、Fe³⁺、Co³⁺,也可以是主族金属离子,如Al³⁺或中性原子,如Ni、Fe,核心是提供空轨道接纳电子对。
2.配体:与中心离子结合的分子或离子,如NH₃、H₂O、CN⁻、EDTA等,必须含1个及以上“配位原子”,如N、O、C、Cl⁻等,能提供孤对电子。
3.配位键:连接中心离子与配体的特殊共价键,电子对仅由配体单方面提供,中心离子提供空轨道共享,是配合物稳定存在的关键。
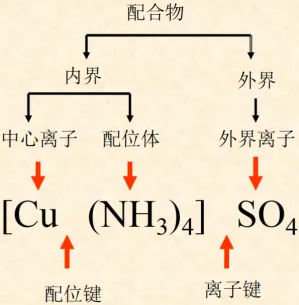
4.外界离子:若配位单元,即中心离子+配体,带电荷,会与相反电荷的离子结合维持电中性,这部分离子为外界离子,如[Cu(NH₃)₄]SO₄中的SO₄²⁻。
配位数+配体数+配位键数(Word),下载方式如下:
(1)关注公众号:化学教学社;
(2)内容分享在夸克网盘,复制如下链接内容,打开“夸克APP”,即可查看、保存、下载。
链接:https://pan.quark.cn/s/ead299ff5389
本公众号重在分享,尊重原创,版权归原作者或原刊发平台所有。本公众号志在为更多老师、学生及家长提供学习与交流的平台,转载内容不代表本公众号的立场,如侵犯到您的权益,烦请留言联系我们,我们将在24小时内删除。
 夜雨聆风
夜雨聆风





