救命神器还是心脏杀手?深度解析T细胞免疫疗法的心毒性机制与临床管理

🔖 原标题:Cardiotoxicity of T cell immunotherapies
🔖 中文标题:T细胞免疫疗法的心血管毒性
🏛️ 发表期刊: Nature Reviews Cardiology(Nat Rev Cardiol)
📅 发表时间:2026年2月23日
T细胞免疫疗法为癌症治疗提供了新途径,其中嵌合抗原受体T细胞疗法应用最广。此外,双特异性抗体、T细胞受体工程T细胞和肿瘤浸润淋巴细胞也是新兴的有效T细胞疗法。T细胞激活可导致大量细胞因子释放和过度炎症,即细胞因子释放综合征。与其他炎症综合征类似,CRS可导致心血管并发症,包括心律失常、心肌梗死和心力衰竭,在发生高级别CRS的患者中,心血管事件的发生率高达20%。本综述总结了T细胞疗法相关CRS及其后续心脏毒性的机制、流行病学和管理。并探讨了对CAR-T疗法及其他新兴T细胞疗法理解的加深,将如何为不良心血管事件的预防和管理提供信息。
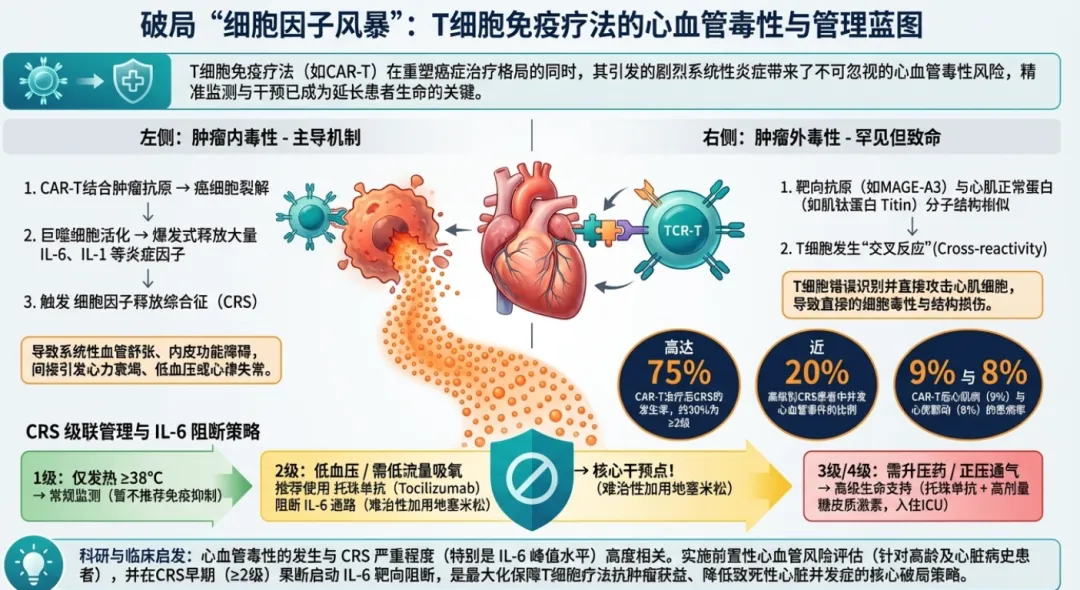


本文是一篇综述,系统性地回顾和总结了T细胞免疫疗法(特别是CAR-T疗法)相关心血管毒性的现有文献。研究方法包括:
-
文献检索与整合: 作者检索并整合了关于T细胞疗法(CAR-T, BsAb, TCR-T, TIL)的作用机制、毒性机制(特别是CRS)、CRS及心脏毒性的流行病学数据、以及当前预防和管理策略的相关研究。
-
机制阐述: 详细解析了CAR的结构(胞外结合域、铰链域、跨膜域、胞内信号域)如何影响其功能与毒性,并对比了不同T细胞疗法(CAR-T, BsAb, TCR-T, TIL)在作用机制和毒性驱动因子(如IL-6, IL-2)上的差异。
-
数据分析: 回顾了多项回顾性队列研究、荟萃分析和FDA不良事件报告系统的数据,总结了CRS和心血管事件(如心肌病、心律失常、心力衰竭、心血管死亡)的发生率、危险因素(如基线肾病、高级别CRS、CD28共刺激域、IL-6水平等)及其对预后的影响。
-
临床指南与专家共识整合: 基于现有的临床指南(如ASCO指南)和专家意见,梳理了T细胞疗法前后的心血管评估、监测和管理流程。

-
心脏毒性机制:
-
肿瘤上毒性: 这是最常见的心脏毒性机制。CAR-T细胞与肿瘤细胞结合后,引发大量T细胞和巨噬细胞等释放细胞因子(IL-1, IL-6, IFNγ等),导致CRS。CRS的全身性炎症反应可导致血流动力学不稳定(低血压、缺氧),进而诱发心律失常、心肌梗死和心力衰竭。IL-6是介导CAR-T相关心脏毒性的关键因子,它能导致内皮和心肌功能障碍。对于TCR-T和TIL疗法,心脏毒性与辅助使用的IL-2密切相关,高剂量IL-2本身即可导致严重低血压和心律失常。
-
肿瘤外毒性: 包括靶向肿瘤外毒性(CAR-T细胞攻击表达相同抗原的健康组织)和脱靶肿瘤外毒性(CAR-T或TCR-T细胞错误识别了健康组织中结构相似的抗原)。目前尚无T细胞疗法导致心脏靶向肿瘤外毒性的确诊病例,但有两例TCR-T疗法因T细胞错误识别心肌细胞中的肌联蛋白而导致致命性心脏毒性的报道。
-
流行病学数据:
-
CAR-T疗法: CRS发生率可高达75%,其中三分之一为≥2级。约70%的心血管事件发生在CRS背景下。CRS的严重程度是心脏毒性的最强预测因子。心血管事件发生率在4%-28%之间。2024年一项荟萃分析显示,心肌病(包括心力衰竭)的汇总患病率为9%,房性心律失常为8%,心肌梗死、室性心律失常和心血管死亡均<1%。低血压发生率高达53%。危险因素包括:基线慢性肾病、高级别CRS、肌钙蛋白升高、既往存在心血管疾病、高龄(>65岁)、以及使用含CD28共刺激域的CAR产品(与更强的炎症反应相关)。
-
双特异性抗体: CRS发生率似乎低于CAR-T疗法。FAERS数据分析显示,约20%的BsAb相关不良事件为心血管事件,且更可能是致命性的,如心肌炎、低血压和休克。
-
TCR-T和TIL疗法: 心脏毒性主要由IL-2驱动。低剂量IL-2方案下,≥3级CRS和低血压/心律失常发生率较低。高剂量IL-2仍与约50%的低血压和10%的心律失常发生率相关。
-
预防与管理策略:
-
治疗前评估: 尚无特定指南,但基于专家意见,建议对高风险患者进行基线心电图和超声心动图检查,以发现潜在的结构性或节律性问题。对有心脏毒性药物(如蒽环类药物)暴露史者,心脏影像检查尤为重要。优化已有的心血管疾病(如心力衰竭患者的容量状态、血压控制)是准备工作的核心。T细胞疗法本身没有绝对的心脏禁忌症,但患者需能够耐受CRS可能带来的血流动力学波动。
-
CRS与心脏毒性监测: 密切监测生命体征至关重要。诊断CRS需结合临床症状,而非仅依赖炎症标志物(如CRP、铁蛋白、IL-6)升高。不推荐常规监测生物标志物(如BNP、肌钙蛋白),但对于高危患者可考虑基线检测。心脏毒性的诊断应基于具体的心血管终点事件(如心律失常、心肌梗死、心肌病),而非CRS相关的非特异性表现(如低血压、心动过速)。
-
CRS管理: 靶向IL-6是核心策略。托珠单抗(IL-6受体抗体)被ASCO指南推荐用于≥2级CRS的患者。研究表明,CRS onset后每延迟12小时使用托珠单抗,主要心血管事件风险增加近70%。糖皮质激素作为难治性或严重CRS的二线治疗。其他策略如IL-1受体拮抗剂(阿那白滞素)在临床前和早期临床研究中显示可减轻CRS和神经毒性,但其对心脏保护的作用有待进一步研究。

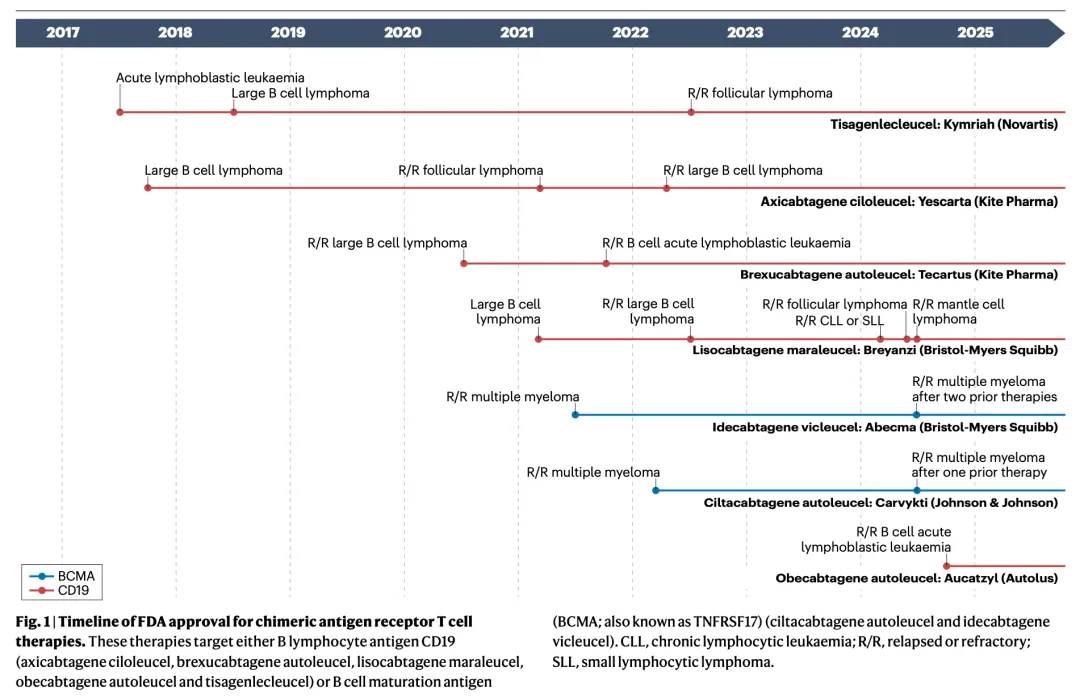
图1 | FDA批准嵌合抗原受体T细胞疗法的时间线: 该图以时间轴形式展示了从2017年至2025年间,FDA批准的7种CAR-T疗法。图中清晰标示了每种药物的商品名、所属公司及其获批的适应症,主要靶向B淋巴细胞抗原CD19或B细胞成熟抗原。
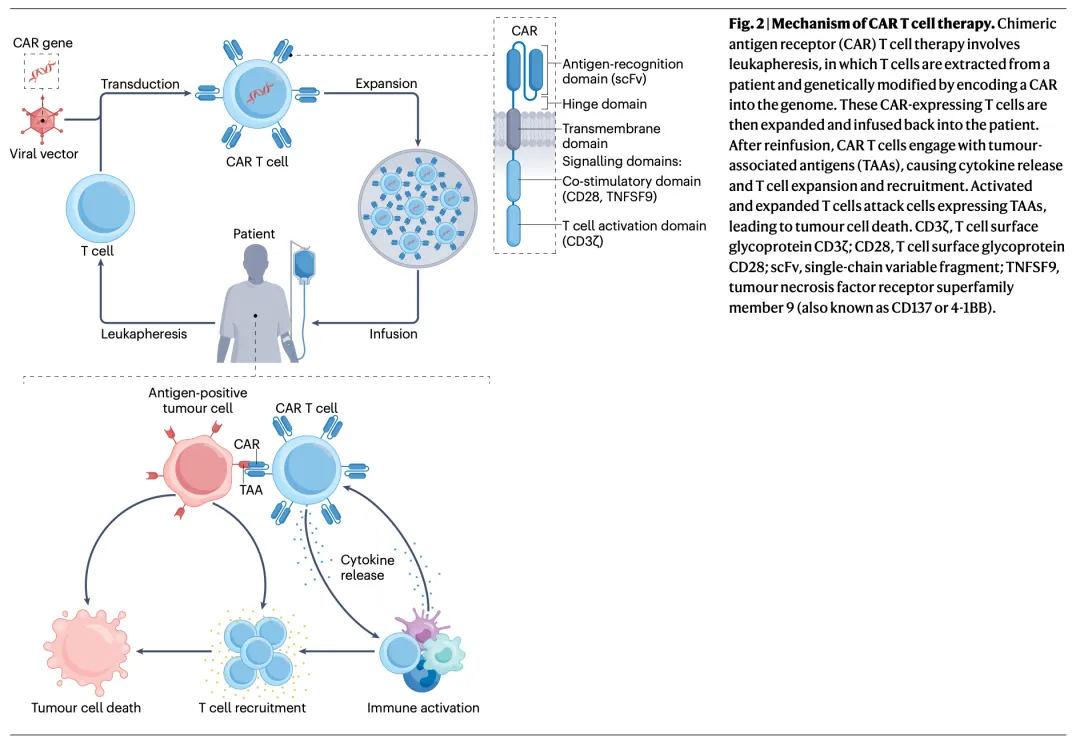
图2 | CAR-T细胞疗法的作用机制: 该流程图详细展示了CAR-T疗法的全过程:从患者体内进行白细胞分离术提取T细胞,到通过基因工程技术将CAR编码进入T细胞基因组,再到CAR-T细胞的体外扩增和回输患者体内。回输后,CAR-T细胞与表达特定肿瘤相关抗原的肿瘤细胞结合,引发细胞因子释放、T细胞扩增和募集,最终导致肿瘤细胞死亡。图中还标注了CAR结构的四个关键部分:单链可变片段、铰链域、跨膜域和胞内信号域(包含CD3ζ和共刺激分子如CD28或4-1BB)。
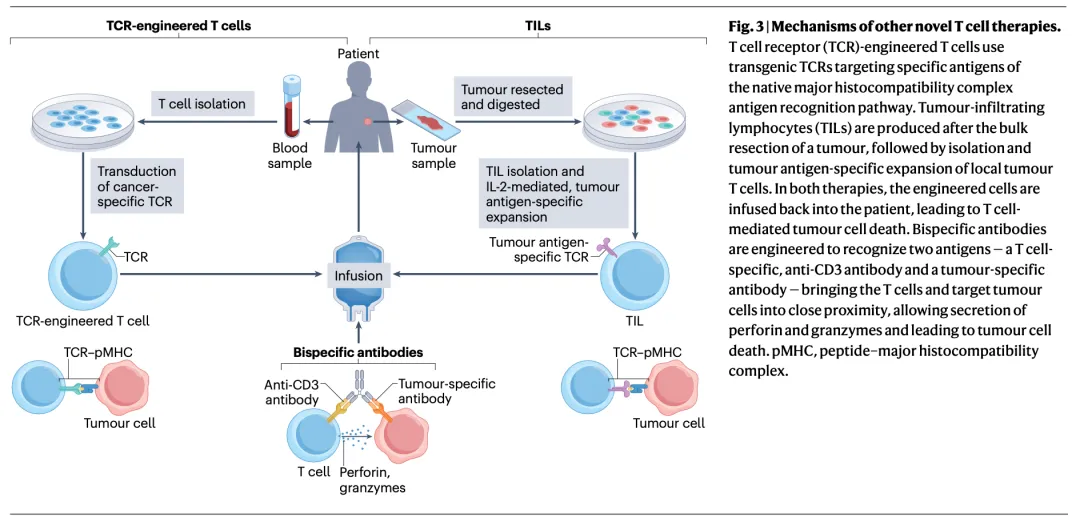
图3 | 其他新型T细胞疗法的机制: 该图通过三个并列的示意图,分别阐述了T细胞受体工程T细胞、肿瘤浸润淋巴细胞和双特异性抗体的作用机制。TCR-T利用转基因TCR识别由主要组织相容性复合体呈递的细胞内抗原。TIL疗法通过切除肿瘤、分离并扩增其中的肿瘤抗原特异性T细胞后回输。BsAb则通过同时结合T细胞上的CD3和肿瘤细胞上的特异性抗原,将两者拉近,从而激活T细胞杀伤肿瘤。
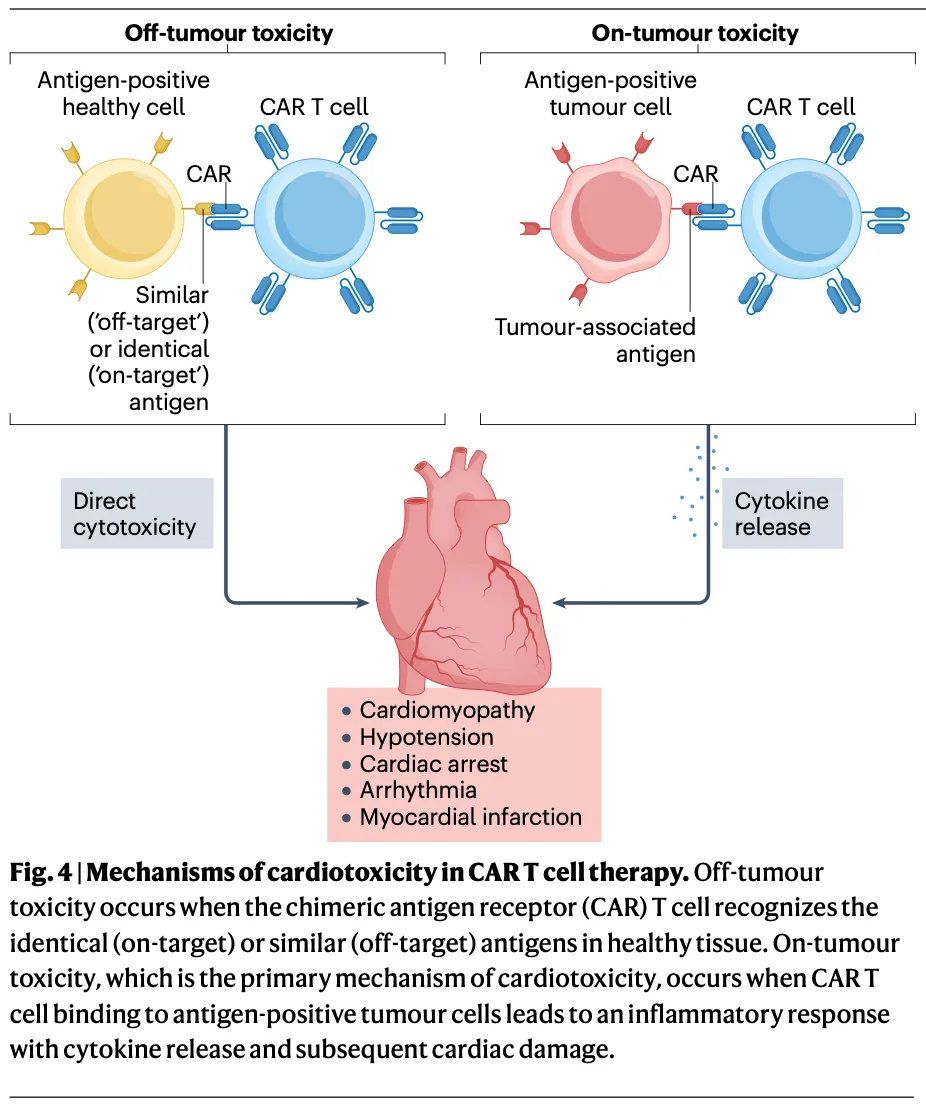
图4 | CAR-T细胞疗法中心脏毒性的机制: 该图清晰地对比了“肿瘤上毒性”和“肿瘤外毒性”。左侧显示“肿瘤上毒性”是心脏毒性的主要机制:CAR-T细胞与抗原阳性的肿瘤细胞结合,引发炎症反应和细胞因子释放,继而导致心脏损伤。右侧显示了“肿瘤外毒性”,即CAR-T细胞识别了健康组织(包括心脏)中相同(靶向)或相似(脱靶)的抗原,直接造成损伤。但目前尚无心脏“靶向肿瘤外毒性”的确诊病例。
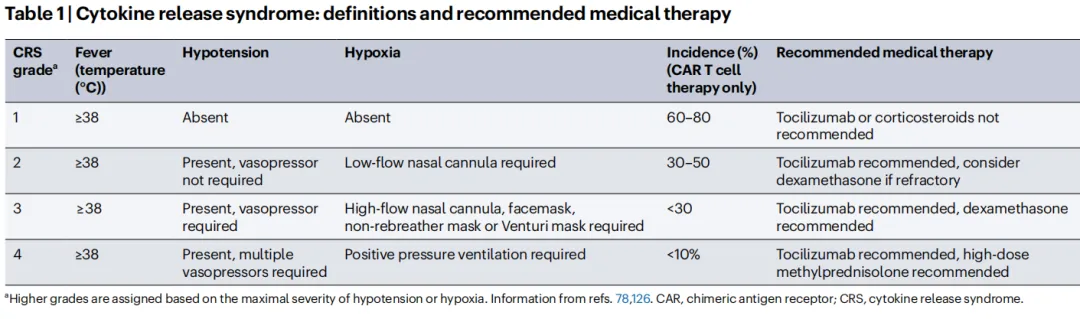
表1 | 细胞因子释放综合征:定义与推荐药物治疗: 该表根据美国移植与细胞治疗学会的共识,对CRS进行了1-4级的分级。分级依据是发热、低血压(是否需要以及需要何种血管加压药)和缺氧(需要何种给氧方式)的严重程度。表中还列出了各级CRS在CAR-T疗法中的大致发生率,并给出了相应的推荐治疗方案,核心是托珠单抗和糖皮质激素的阶梯式使用。
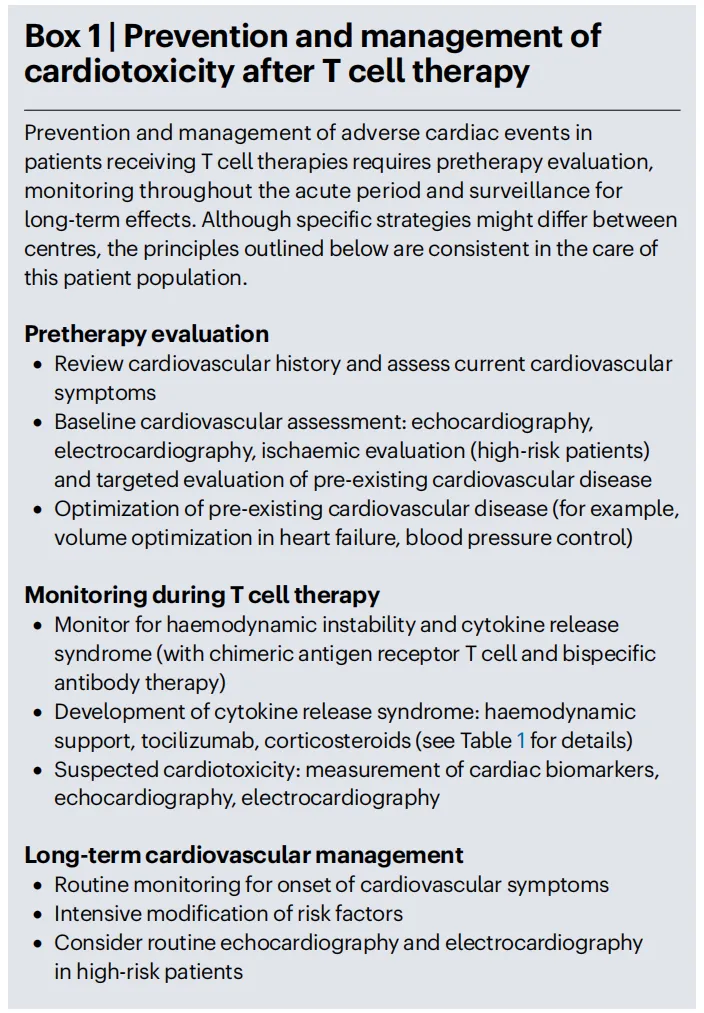
文本框1 | T细胞疗法后心脏毒性的预防和管理: 该流程图概括了从治疗前到长期随访的全程管理策略。治疗前阶段包括心血管病史评估、基线检查和优化。治疗中阶段强调监测血流动力学和CRS,并针对CRS和疑似心脏毒性进行处理。长期管理阶段则关注心血管症状监测、危险因素强化控制和影像学复查。


本综述为临床医生(尤其是肿瘤科和心脏科医生)提供了关于T细胞免疫疗法心血管毒性的全面和最新认识。其临床意义在于:
-
提高认知与警惕: 促使临床医生认识到T细胞疗法(不仅是CAR-T)可能引发严重心血管事件,特别是在CRS背景下。
-
指导风险评估与分层: 明确了心血管毒性的危险因素,如高龄、基础心血管病、高肿瘤负荷、高级别CRS等,有助于在治疗前识别高危患者,进行个体化评估和准备。
-
优化监测策略: 强调了CRS与心脏毒性的密切关系,将心脏监测整合到CRS的常规管理流程中,建议对高危患者进行基线心脏影像学和生物标志物检查。
-
提供管理框架: 提供了基于循证证据和专家共识的CRS和心脏毒性管理策略,特别是IL-6拮抗剂在预防和治疗中的核心地位,以及及时干预的重要性。
-
推动多学科协作: 强调了肿瘤心脏病学团队在患者筛选、治疗中监测和长期随访中的关键作用,以最大程度地减少心血管并发症,改善患者预后。

-
数据异质性: 目前关于CAR-T相关心脏毒性的研究多为回顾性、观察性研究,且各研究对“心血管事件”的定义缺乏标准化,导致报道的发生率差异较大。
-
样本量有限: 针对TCR-T和TIL疗法心脏毒性的前瞻性研究数据较少,多为小样本研究或病例报告,难以得出确切结论。
-
机制研究不足: 虽然IL-6在CAR-T相关心脏毒性中的核心作用较为明确,但其他细胞因子和免疫细胞的具体作用,以及IL-2在其他疗法中的剂量-毒性关系,仍需更深入的机制研究。
-
缺乏预测工具: 目前尚无经过验证的风险预测模型或生物标志物能够准确识别哪些患者会发生严重心脏毒性。
-
管理策略证据等级低: 针对心脏毒性的具体治疗方案(如心律失常、心力衰竭的管理)多借鉴于非T细胞疗法相关的心脏病学指南,缺乏专门针对T细胞疗法后心脏事件的RCT研究证据。
-
长期随访数据缺乏: 关于T细胞疗法后心脏毒性的长期影响,如心功能不全的恢复情况、迟发性心血管事件风险等,尚缺乏充分的长期随访数据。


Raddatz, Michael A., et al. “Cardiotoxicity of T cell immunotherapies.” Nature Reviews Cardiology, 23 Feb. 2026, https://doi.org/10.1038/s41569-026-01265-z.
本资讯专为医疗卫生专业人士提供疾病领域最新进展,内容可能涉及未在中国批准的适应症,使用药物时请遵循国家药品监督管理局批准的说明书。本资讯非广告,不构成药物推广或诊疗推荐,提供信息不替代专业医疗指导,不作为任何诊疗建议。若相关信息被用于除了解资讯以外的其他用途,本公众号及作者不承担法律责任。未经授权,禁止转载或他用。引用资料均已发表,若涉版权请联系删除。
 夜雨聆风
夜雨聆风




