可编程支架介导的组装调控工具用于多酶生物催化剂动态控制

Programmable Scaffold-Mediated Assembly Regulation
Tool for Dynamic Control of a Multienzyme Biocatalyst


研究背景
表面展示全细胞生物催化方法相较于传统胞内酶催化方法具有显著优势,能够减少传质限制,甚至处理膜不透性分子,并可整合胞内与胞外催化过程。但当前表面展示系统主要面临三大挑战:一是仅适用于简单反应,缺乏功能分配与动态行为调控能力,限制了其在复杂多酶级联过程中的应用;二是常用宿主菌(如大肠杆菌、枯草芽孢杆菌)需要两阶段培养以达到特定生理状态和形成相应生物被膜支架,且细胞完整性差、支架展示水平低;三是现有方法通常需要分别培养支架宿主和酶宿主,增加了时间、劳动力和资源需求,降低了过程效率和成本效益。因此开发一种可编程的支架介导表面展示平台,实现对多酶系统的动态控制,成为解决上述挑战的关键方向。

研究摘要
表面展示全细胞生物催化相较于传统基于胞内酶的方法具有显著优势,但在复杂多酶过程中仍面临效率偏低等挑战。本文构建了支架介导组装调控工具(Scaffold-Mediated Assembly Regulation Tool, SMART),这一可编程平台可在谷氨酸棒状杆菌表面实现多酶生物催化剂的动态调控。SMART 将正交交联支架与双组分 Catcher/Tag 配对(SpyCatcher/SpyTag 与 SnoopCatcher/SnoopTag)相结合,具备分子比例可控、负载量高的特点,可根据需求实现酶的定制化组装。我们通过计算建模与实验验证对 SMART 系统进行优化,构建了双功能支架与长串联重复序列以实现最优酶负载。通过在双酶级联反应中实现共展示与化学计量比可调,证明了 SMART 的通用性,可显著提高麦芽糊精向海藻糖的转化效率。此外,我们整合了基于Bxb1 重组酶的状态机(RSM)遗传线路,实现单细胞内酶与支架表达的时序调控。最后,以低成本蔗糖合成异麦芽酮糖为例验证了该系统的应用潜力。SMART 设计是表面展示生物催化领域的重要进展,为复杂多酶反应提供了可编程平台,在多种工业相关生物催化体系中具有广阔应用前景。

研究内容
内容一:谷氨酸棒杆菌正交表面展示系统的构建与锚定蛋白筛选
为实现可编程支架介导的组装调控工具(SMART),研究者首先在谷氨酸棒杆菌中构建了正交表面展示系统。研究选取了内源性孔蛋白基因PorB、PorC、PorH、Ncgl1337以及来自枯草芽孢杆菌的异源PgsA基因作为候选锚定基序,通过柔性连接子(GGGGS)3与SpyCatcher结构域融合,并在C端添加Flag标签。激光共聚焦显微镜和流式细胞术分析显示,以PorB、PorC和Ncgl1337为锚定基序的细胞呈现明显的远红特异性荧光,而PorH和PgsA则无荧光信号。SDS-PAGE分析证实,与PorB、PorC和Ncgl1337融合的SpyCatcher结构域能够有效穿透细胞膜并稳定锚定于外膜上。进一步利用SpyTag-eGFP探针验证表明,PorB-SpyCatcher展示系统具有最高的荧光强度,5000个细胞全部能够有效募集绿色荧光探针,而PorC和Ncgl1337的阳性细胞比例分别为60.8%和50.1%。单细胞平均荧光强度分析显示,PorB、PorC和Ncgl1337的荧光值分别为4832、4219和3810,远高于对照菌株的253。基于PorB的优异表现,研究确定其为SMART系统的最佳锚定蛋白,为后续精确酶组装提供了稳定高效的平台。
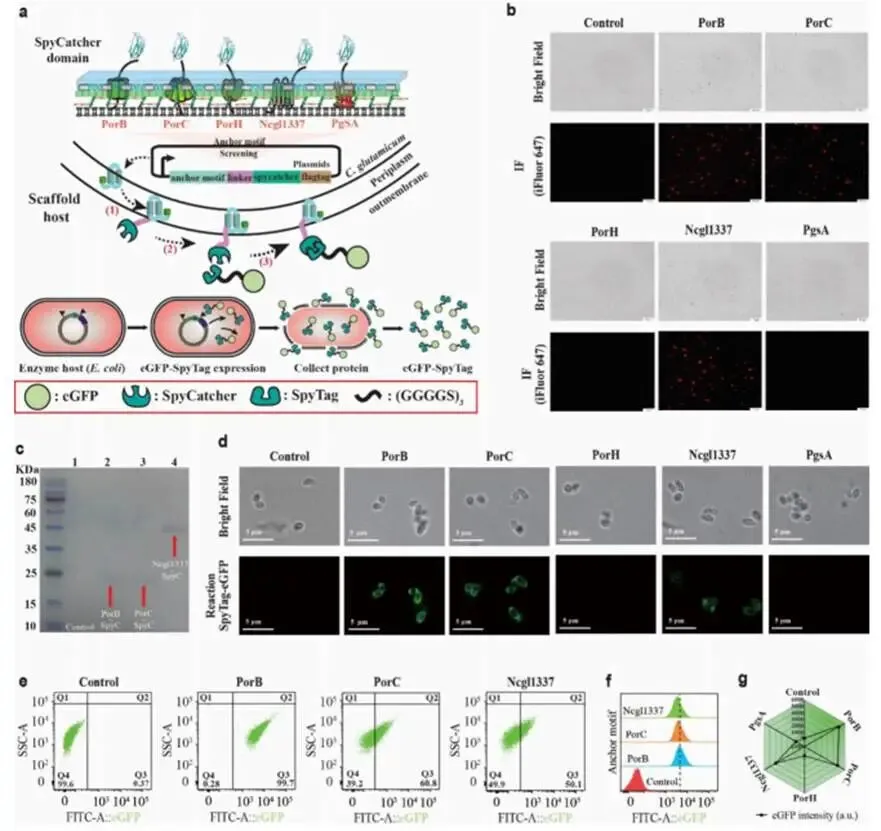
图1系统展示了SMART系统的构建流程。
图1a:表面展示系统示意图;图1b:免疫荧光染色后的激光共聚焦图像,显示PorB、PorC、Ncgl1337成功锚定;图1c:SDS-PAGE分析确认锚定蛋白表达;图1d:SpyTag-eGFP探针功能验证;图1e-g:流式细胞术定量分析,证实PorB具有最高的展示效率和结合能力。
内容二:双功能展示支架的理性设计与计算机辅助优化
为增强SMART系统的多功能性,研究者将SpyCatcher和SnoopCatcher两个正交结构域融合,构建双功能展示支架。初始采用(GGGGS)3连接子时,只有第一个结构域(SpyCatcher)能有效结合其对应探针,而第二个结构域(SnoopCatcher)完全丧失结合能力。通过AlphaFold2-Monomer算法进行结构模拟发现,(GGGGS)3连接子会在SnoopCatcher的关键催化残基天冬酰胺(Asn)上方形成环状结构,阻碍其活性中心与SnoopTag-mCherry的相互作用。研究进一步筛选了10种不同连接子,包括柔性连接子和刚性连接子变体。结构分析表明,L2-L10连接子倾向于在关键催化残基(SpyCatcher的赖氨酸和SnoopCatcher的天冬酰胺)上方形成环状结构,可能损害其活性。相比之下,源自核糖体蛋白L9的17个氨基酸α–螺旋连接子(L1)能够保持SpyCatcher和SnoopCatcher结构域之间的空间独立性,防止功能相互干扰。替换为α–螺旋连接子后,双功能支架成功实现了与SpyTag-eGFP和SnoopTag-mCherry的双正交结合,激光共聚焦显微镜证实两种荧光探针同时锚定于细胞表面。PorB作为锚定基序的双功能支架展示效率仍高于PorC,进一步确认了PorB的优越性。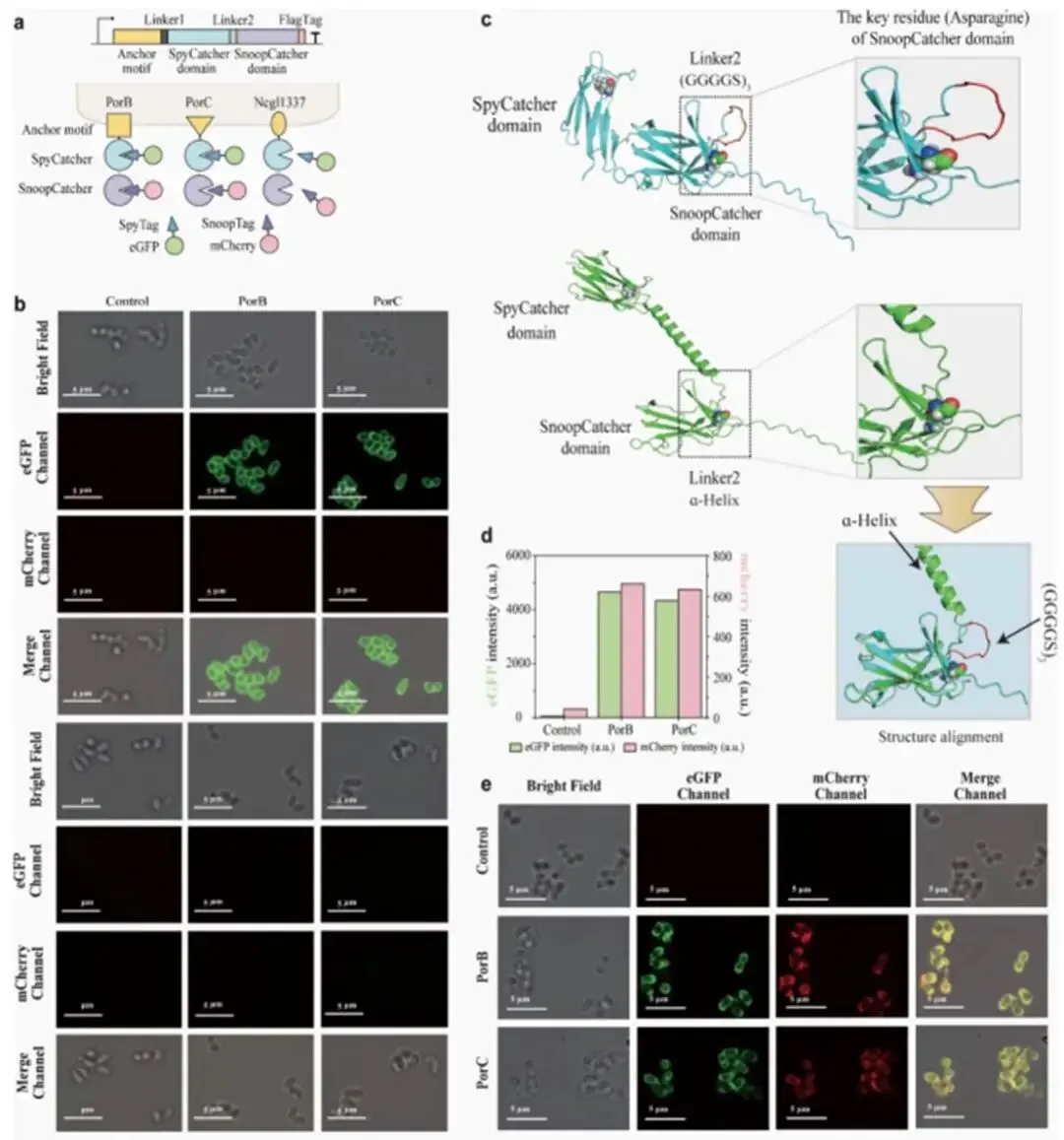
图2a:双功能展示支架示意图;图2b:(GGGGS)3连接子下只有SpyCatcher能结合探针;图2c:AlphaFold2模拟结构,揭示(GGGGS)3连接子对SnoopCatcher活性位点的空间位阻;图2d:荧光强度定量分析;图2e:α–螺旋连接子优化后双功能支架的成功展示,两种荧光探针同时锚定于细胞表面。
内容三:高负载膜支架的设计与表面展示优化
为提高SMART系统的催化效率,研究者采用两种并行策略增强支架在谷氨酸棒杆菌表面的负载量。第一种策略通过敲除内源性孔蛋白基因构建更精简的底盘细胞。研究构建了PorB、PorC、Ncgl1337的单敲除、双敲除和三敲除突变株,共获得7种不同底盘细胞。虽然这些突变株未见明显形态改变或生长缺陷(图3b),但其募集SpyTag-eGFP的能力反而低于亲本菌株(图3c),表明酶组装效率受到细胞表面过量支架拥挤的阻碍。因此,亲本菌株仍为SMART系统的最适底盘细胞。第二种策略构建了含1-6个SpyCatcher结构域的长串联重复(LTR)支架(Scaf-1X至6X)。随着SpyCatcher结构域数量的增加,支架结构复杂度增加,可能影响其分泌和锚定效率。免疫荧光分析显示,Scaf-1X在Q2区域的远红荧光阳性比例最高(93.9%),结构域数量少于4个时阳性比例均超过90.1%,但当结构域数量增至6个时阳性比例骤降至70.0%。流式细胞术分析表明,几乎所有LTR支架都能有效结合SpyTag-eGFP探针,结合率接近100%。单位细胞绿色荧光强度分析显示,Scaf-2X至Scaf-6X的相对荧光强度为Scaf-1X的1.2-2.0倍。综合考虑支架表达水平和饱和程度,Scaf-4X被选为SMART系统最适的高负载支架,特别适用于需要高酶负载或复杂多酶级联的应用场景。
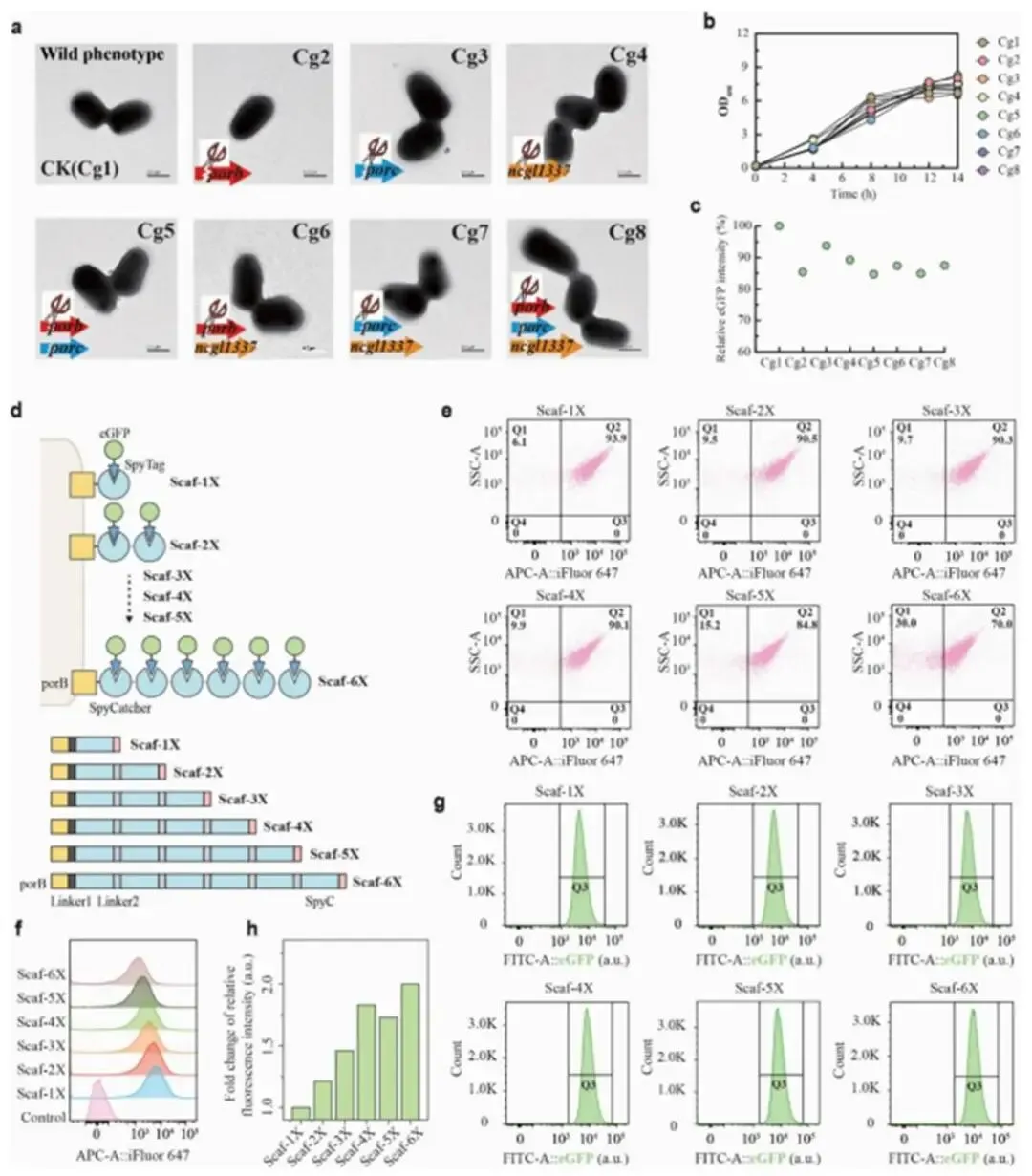
图3a:透射电镜图像显示敲除突变株的形态;图3b:生长曲线;图3c:敲除突变株结合能力反而降低;图3d:高负载支架示意图;图3e-f:流式细胞术分析不同LTR支架的展示水平;图3g-h:SpyTag-eGFP结合能力定量分析,Scaf-4X被选为最优高负载支架。
内容四:可编程SMART实现可调计量比的连续酶级联共展示
在多酶级联反应中,各酶催化活性的差异会显著影响整体催化效率。研究利用SMART的模块化特性,开发了可调计量比的连续酶级联共展示策略。构建了SpyCatcher:SnoopCatcher比例分别为1:1、2:1和3:1的嵌合支架,命名为Scaf-I、Scaf-II和Scaf-III。SDS-PAGE和免疫染色分析证实三种支架均成功锚定于谷氨酸棒杆菌表面,展示水平相近(53-54%)。使用双荧光探针分析表明,随着SpyCatcher结构域比例增加,SpyTag-eGFP的结合量逐渐增强,Scaf-I、Scaf-II、Scaf-III的相对荧光强度分别达到Scaf-III的44.6%、79.4%和99.7%;而SnoopTag-mCherry的结合量因SnoopCatcher结构域比例恒定而基本不变。将源于节杆菌的双酶AstreY和AstreZ分别与SpyTag和SnoopTag融合,锚定于蛋白支架上,实现从多糖麦芽糊精到二糖海藻糖的转化。与游离酶系统(16.7 g/L/h)相比,Scaf-I系统实现了更高的生产效率(20.4 g/L/h)。Scaf-II系统进一步将生产效率提升了67.8%,而Scaf-III系统的生产效率与Scaf-II基本持平,这可能是由于第二步酶的负载已达到饱和。经条件优化后,在5 L发酵罐中放大生产,麦芽糊精在15 h内快速转化,转化率达71.8%,海藻糖效价达215.4 g/L,生产效率为14.4 g/L/h。
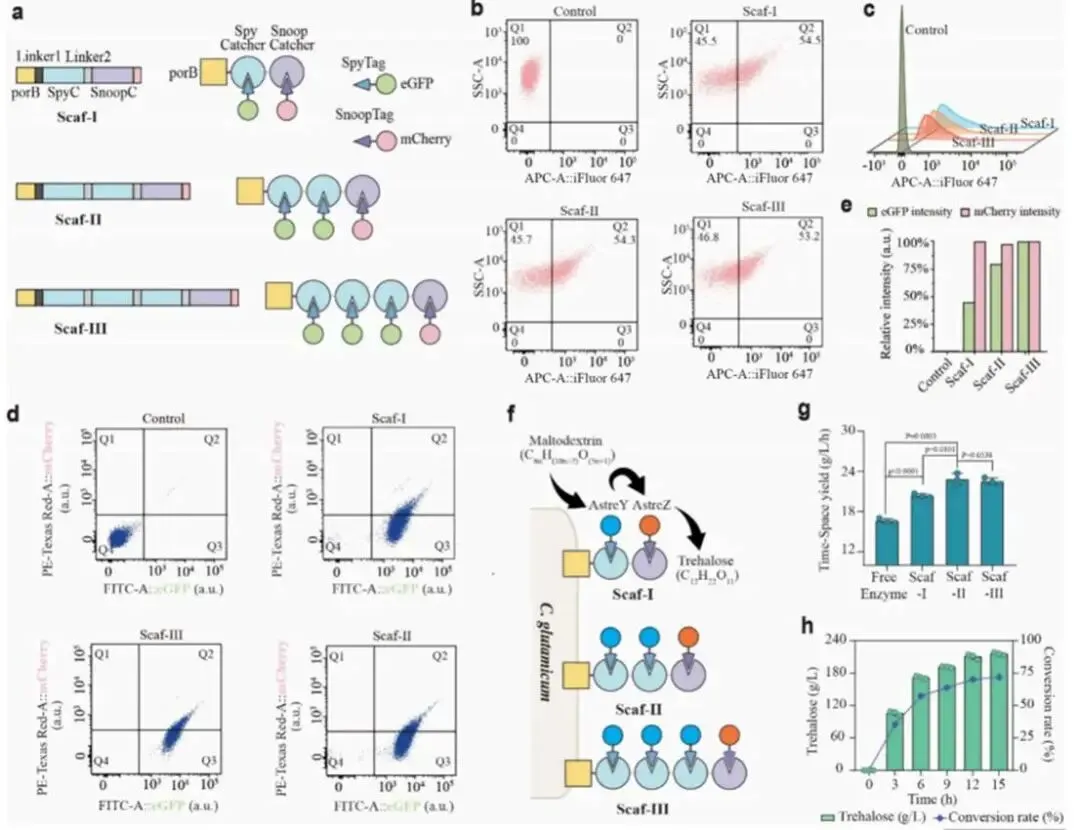
图4a:可调计量比共展示支架示意图;图4b-c:免疫染色分析显示不同支架展示水平相近;图4d-e:双探针结合定量分析,证实SpyCatcher比例可调;图4f:海藻糖合成途径示意图;图4g:SMART系统与游离酶系统生产效率对比;图4h:5 L发酵罐中海藻糖生产的时间进程。
内容五:基因电路整合实现单细胞内酶与支架表达的时序调控
为进一步增强SMART的通用性和动态控制能力,研究者整合了Bxb1重组酶状态机遗传电路,实现了表面展示酶的自组装。该系统采用双质粒设计:输入质粒携带受乳糖诱导型启动子Ptac调控的Bxb1重组酶;输出质粒基于pECXK99E骨架,包含反向排列的attB-attP位点和强组成型启动子Peffu。当乳糖诱导Bxb1表达时,重组酶识别并剪切attB/attP位点,使Peffu启动子方向反转,开启eGFP表达同时关闭mCherry表达。初始系统存在基础泄漏表达问题,Western blot证实Bxb1在谷氨酸棒杆菌中有明显本底表达。通过优化Bxb1的降解和翻译速率解决此问题:在Bxb1 C端融合不同SsrA降解标签,筛选出含LAA标签的Bxb1使动态反转率有效降低,OFF和ON状态荧光变化分别达21.6倍和15.9倍;缩短Shine-Dalgarno区间隔序列下调Bxb1翻译水平,筛选出的间隔序列5使mCherry荧光强度提升29.7倍,ON状态达20.3倍变化。将优化后的电路与高负载支架Scaf-4X和SpyTag-PDSI整合,构建单宿主系统转化糖蜜中蔗糖为异麦芽酮糖。HPLC分析证实,经8 h生物催化,糖蜜中蔗糖基本转化为异麦芽酮糖。自组装系统的异麦芽酮糖产量达到游离酶系统的4.99倍。经条件优化后,在5 L发酵罐中,使用含204.0 g/L蔗糖的50%(v/v)糖蜜,12 h内异麦芽酮糖效价达178.5 g/L,产率87.3%(g/g蔗糖),生产效率14.9 g/L/h。连续10批次发酵中,催化活性逐渐下降,转化率降至80.2%,最终批次因细胞裂解溶解进一步降至57.4%。
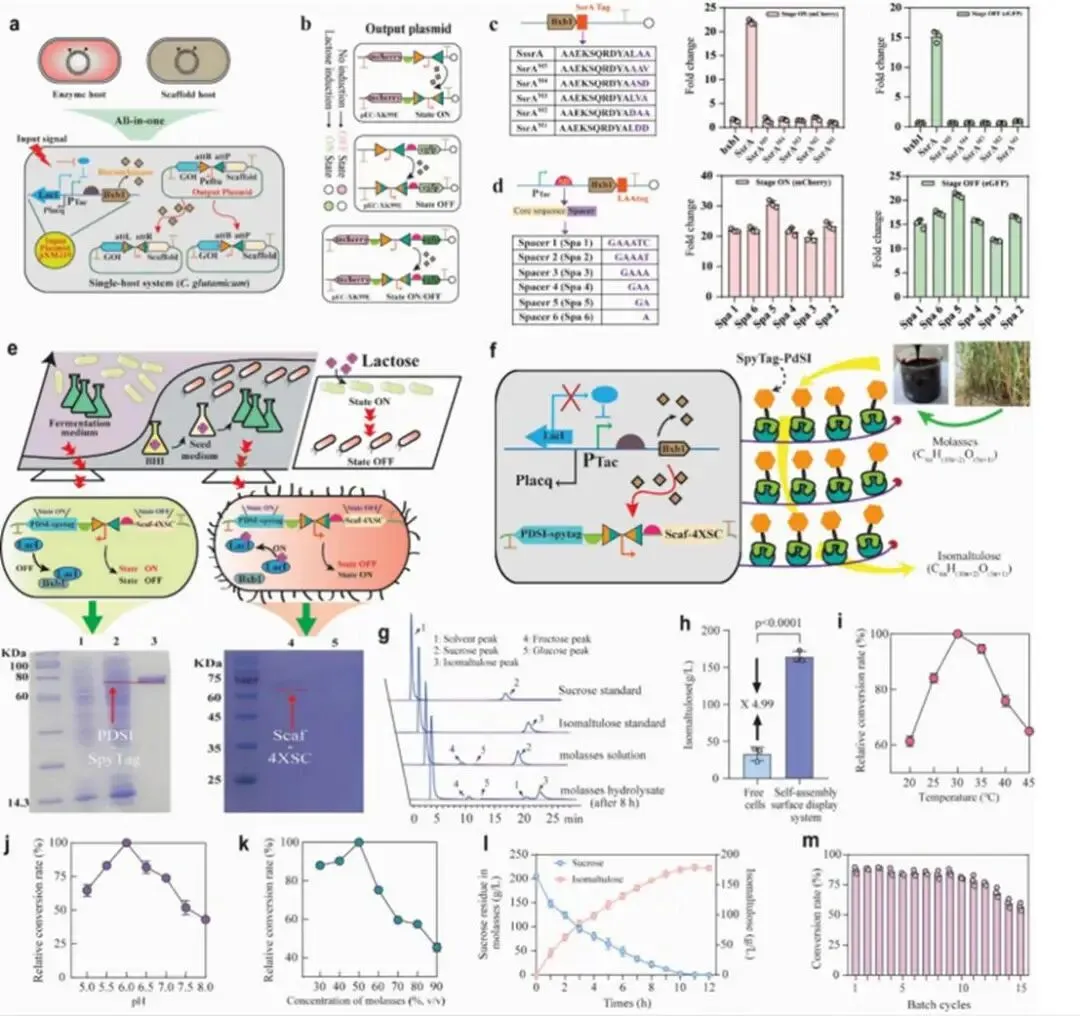
本研究成功建立了一种可编程的支架介导组装调控工具(SMART),能够在谷氨酸棒杆菌外膜上展示可调控比例和高负载能力的多结构域蛋白。与游离细胞相比,SMART的模块化的特征在现有表面展示系统中独具特色,为构建响应性全细胞生物催化剂开辟了新途径。SMART与工业相关菌株谷氨酸棒杆菌的兼容性为其在规模化生物过程中的应用奠定了基础。未来,可进一步整合合成生物学方法和机器学习,优化支架设计、预测酶相互作用、精细调控反应参数;开发更复杂的基因电路,使SMART能够处理更复杂的反应,响应复杂环境信号或代谢状态,最终构建高度响应和高效的生物催化系统,应对更具挑战性的工业和生物技术需求。
撰稿:丁瑞桐
校稿:曹少攀



关注我们了解
更多
微信号:
BioChemWorld

 夜雨聆风
夜雨聆风




