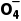【2026版三维高考设计高中化学人教版培优讲义word电子版第46讲离子平衡图像中粒子浓度的“动态分析”
 “动态分析”
“动态分析”
课标要求
1.进一步加深对电离平衡、水解平衡的理解与应用。
2.能正确辨析图像,并根据图像中的关键点、变化趋势,计算各种平衡常数,判断粒子浓度的大小关系。
3.能利用沉淀溶解平衡原理,分析图像中粒子浓度的关系。

类型一中和滴定曲线分析

抓住关键“五点”,突破中和滴定曲线
|
抓反应的“起始”点 |
判断酸、碱的相对强弱 |
|
抓反应的“一半”点 |
判断是哪些溶质的等量混合 |
|
抓溶液的“中性”点 |
判断溶液中溶质的成分及哪种物质过量或不足 |
|
抓“恰好反应”点 |
判断生成的溶质成分及溶液的酸碱性 |
|
抓反应的“过量”点 |
判断溶液中的溶质及哪种物质过量 |
|
关键点 |
溶液中溶质成分及粒子浓度大小关系 |
|
|
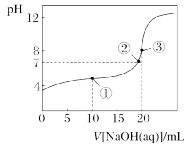
常温下,用0.100 0 mol·L-1 NaOH溶液滴定20.00 mL 0.100 0 mol·L-1 CH3COOH溶液
|
起点V[NaOH(aq)]=0(0点) |
溶质是 ,粒子浓度大小关系: |
|
一半点V[NaOH(aq)]= 10 mL(点①) |
溶质是等物质的量的和 ,粒子浓度大小关系:;元素守恒:c(CH3COOH)+c(CH3COO-)= |
|
|
中性点pH=7(点②) |
溶质是和少量的 ,粒子浓度大小关系: |
|
|
恰好反应点V[NaOH(aq)]= 20 mL(点③) |
溶质是 ,粒子浓度大小关系: |
|
|
过量1倍点V[NaOH(aq)]=40 mL |
溶质是等物质的量的和 ,粒子浓度大小关系: |

|
一 |
一元弱电解质的滴定曲线 |
1.常温下,用0.100 0 mol·L-1的盐酸分别滴定20.00 mL浓度均为0.100 0 mol·L-1的三种一元弱酸的钠盐(NaX、NaY、NaZ)溶液,滴定曲线如图所示。下列判断错误的是()
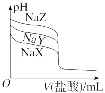
A.NaX溶液中:c(Na+)>c(X-)>c(OH-)>c(H+)
B.三种一元弱酸的电离常数:Ka(HX)>Ka(HY)>Ka(HZ)
C.当pH=7时,三种溶液中:c(X-)=c(Y-)=c(Z-)
D.分别滴加20.00 mL盐酸后,再将三种溶液混合:c(X-)+c(Y-)+c(Z-)=c(H+)-c(OH-)
2.25 ℃时,向20 mL 0.1 mol·L-1NaOH溶液中逐滴加入0.2 mol·L-1醋酸溶液,曲线如图所示。下列有关粒子浓度关系的比较中,不正确的是()
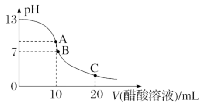
A.在A点:c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
B.在B点:c(OH-)=c(H+),c(Na+)=c(CH3COO-)
C.在C点:c(CH3COO-)>c(H+)>c(Na+)>c(OH-)
D.在C点:c(CH3COO-)+c(CH3COOH)=2c(Na+)
|
二 |
二元弱电解质的滴定曲线 |
3.已知pKa=-lg Ka,25 ℃时,H2A的pKa1=1.85,pKa2=7.19。常温下,用0.1 mol·L-1 NaOH溶液滴定20 mL 0.1 mol·L-1 H2A溶液的滴定曲线如图所示。下列说法错误的是()
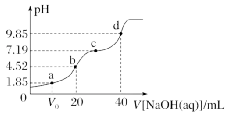
A.a点加入NaOH溶液的体积V0>10 mL
B.a、b、c、d四点所得溶液均满足:2c(A2-)+c(HA-)+c(OH-)=c(H+)+c(Na+)
C.当加入NaOH溶液的体积为80 mL时,有c(OH-)>c(A2-)
D.a、b、c、d四点对应的溶液中水的电离程度:a<b<c<d
类型二分布系数曲线分析

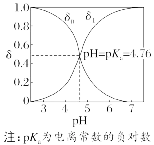
1.认识分布系数δ(X)与pH曲线
分布系数曲线是指以pH为横坐标、分布系数(即组分的平衡浓度占总浓度的分数)为纵坐标的关系曲线。
|
一元弱酸(以CH3COOH为例) |
二元弱酸(以H2C2O4为例) |
|
|
|
|
δ0为CH3COOH的分布系数,δ1为CH3COO-的分布系数 |
δ0为H2C2O4的分布系数,δ1为HC2 |
2.读图解题要领
(1)读“曲线”——每条曲线所代表的粒子及变化趋势(以上图中H2C2O4为例)
随pH增大,δ只减不增的为H2C2O4曲线,δ先增后减的为HC2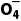 曲线,δ只增不减的为C2
曲线,δ只增不减的为C2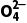 曲线。
曲线。
(2)用“交点”——交点是某两种粒子浓度相等的点,可计算电离常数K:
①图中M点:c(HC2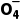 )=c(H2C2O4),其pH为pH1,Ka1(H2C2O4)=
)=c(H2C2O4),其pH为pH1,Ka1(H2C2O4)=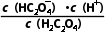 =
=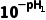 。
。
②同理图中N点:c(HC2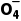 )=c(C2
)=c(C2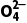 ),对应pH为pH2,Ka2=
),对应pH为pH2,Ka2=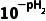 。
。
③图中O点,c(H2C2O4)=c(C2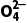 ),此时c(HC2
),此时c(HC2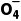 )最大,对应溶液pH为pH3,则pH3=
)最大,对应溶液pH为pH3,则pH3=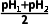 。
。

1.某弱酸HA溶液中主要成分的分布分数随pH的变化如图所示。下列说法错误的是()

A.该酸-lg Ka≈4.7
B.NaA的水解平衡常数Kh=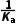
C.当该溶液的pH=7.0时,c(HA)<c(A-)
D.某c(HA)∶c(A-)=4∶1的缓冲溶液,pH≈4
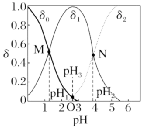
2.(2024·山西运城模拟)草酸(H2C2O4)是一种二元弱酸。向草酸溶液中滴加稀NaOH溶液,H2C2O4、HC2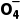 和C2
和C2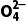 的分布系数δ与溶液pH的变化关系如图所示。下列说法正确的是()
的分布系数δ与溶液pH的变化关系如图所示。下列说法正确的是()
[比如C2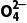 的分布系数:δ(C2
的分布系数:δ(C2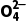 )=
)=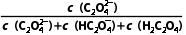 ]
]
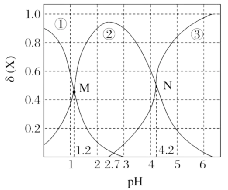
A.草酸Ka2的数量级为10-5
B.NaHC2O4溶液中c(OH-)>c(H+)
C.水的电离程度:N点<M点
D.pH=5时,溶液中c(H+)=c(HC2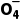 )+2c(C2
)+2c(C2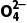 )+c(OH-)
)+c(OH-)

通过网盘分享的文件:word讲义
链接: https://pan.baidu.com/s/136tUpK67Q1V3PV2VsUIuPw?pwd=4321 提取码: 4321
–来自百度网盘超级会员v8的分享
 夜雨聆风
夜雨聆风