【2026版三维高考设计高中化学人教版培优讲义word电子版第44讲盐类的水解
课标要求
1.认识盐类水解的原理及其一般规律,掌握盐类水解离子方程式的书写。
2.认识影响盐类水解程度的主要因素。
3.了解盐类水解的应用。

考点一盐类水解及其规律

(一)盐类的水解

(二)盐类的水解规律
1.根据相关物质的电离常数(25 ℃),回答下列问题:
CH3COOH Ka=1.8×10-5
HCN Ka=4.9×10-10
H2CO3Ka1=4.3×10-7、Ka2=5.6×10-11
(1)相同物质的量浓度的①CH3COONa、②Na2CO3、③NaHCO3、④NaCN溶液,pH由大到小的顺序: ,水的电离程度由大到小的顺序:。
(2)相同pH的①CH3COONa、②Na2CO3、③NaHCO3、④NaCN溶液,物质的量浓度由大到小的顺序:。
(3)常温下,NH3·H2O的Kb=1.8×10-5,则CH3COONH4溶液显(填“酸”“碱”或“中”,下同)性,NH4HCO3溶液显性。
2.水解规律
|
强酸强碱盐不水解 |
呈中性 |
|
强酸弱碱盐水解 |
呈酸性 |
|
弱酸强碱盐水解 |
呈碱性 |
|
弱酸弱碱盐水解 |
可能呈酸性、碱性或中性,如NH4F溶液呈酸性、CH3COONH4溶液呈中性 |
|
有弱才水解,越弱越水解;谁强显谁性,同强显中性 |
(三)盐类水解离子方程式的书写
1.书写要求
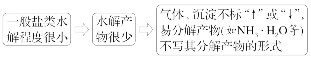
2.书写原则
(1)多元弱酸根离子的水解分步进行,水解以第一步为主。
(2)多元弱碱阳离子水解反应过程复杂,在中学阶段只要求一步书写完成。
(3)弱酸弱碱中阴、阳离子水解相互促进。
①N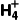 与S2-、HC
与S2-、HC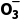 、C
、C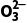 、CH3COO-等组成的盐虽然水解相互促进,但水解程度较小,书写仍用“
、CH3COO-等组成的盐虽然水解相互促进,但水解程度较小,书写仍用“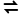 ”表示。
”表示。
②Al3+与C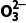 、HC
、HC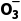 、S2-、HS-、[Al(OH)4]-以及Fe3+与C
、S2-、HS-、[Al(OH)4]-以及Fe3+与C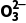 、HC
、HC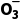 等组成的盐水解相互促进非常彻底,生成气体和沉淀,书写时用“
等组成的盐水解相互促进非常彻底,生成气体和沉淀,书写时用“ ”表示。
”表示。
3.写出下列盐溶液水解的离子方程式。
(1)NH4Cl:。
(2)Na2CO3:、。
(3)FeCl3:。
(4)CH3COONH4:。
(5)Al2S3:。
(6)AlCl3溶液和NaHCO3溶液混合:。

判断正误(正确的打“√”,错误的打“×”)。
(1)溶液呈中性的盐一定是强酸、强碱生成的盐。()
(2)pH相同的盐酸和氯化铵溶液中由水电离出的c(H+)相同。()
(3)Na2CO3溶液呈碱性的原因是C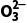 +H2O
+H2O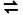 HC
HC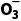 +OH-。()
+OH-。()
(4)KHC2O4溶液呈酸性的原因是HC2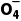 的电离程度大于其水解程度。()
的电离程度大于其水解程度。()
(5)FeCl3溶液与Na2CO3溶液混合:2Fe3++3C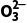 +3H2O
+3H2O 2Fe(OH)3↓+3CO2↑。()
2Fe(OH)3↓+3CO2↑。()
(6)N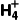 与CH3COO-在水解时相互促进,故在溶液中不能大量共存。()
与CH3COO-在水解时相互促进,故在溶液中不能大量共存。()

|
一 |
盐类水解的原理和规律 |
1.根据表中信息,判断0.10 mol·L-1的下列各物质的溶液pH最大的是()
|
酸 |
电离常数(常温下) |
|
CH3COOH |
Ka=1.75×10-5 |
|
H2CO3 |
Ka1=4.5×10-7,Ka2=4.7×10-11 |
|
H2S |
Ka1=1.1×10-7,Ka2=1.3×10-13 |
A.CH3COONaB.Na2CO3C.NaHCO3D.Na2S
2.常温下,浓度均为0.1 mol·L-1的下列四种盐溶液,测得其pH如表所示:
|
序号 |
① |
② |
③ |
④ |
|
溶液 |
CH3COONa |
NaHCO3 |
Na2CO3 |
NaClO |
|
pH |
8.8 |
9.7 |
11.6 |
10.3 |
下列说法正确的是()
A.四种溶液中,水的电离程度:③>④>②>①
B.Na2CO3和NaHCO3溶液中,粒子种类不相同
C.等物质的量浓度的CH3COOH和HClO溶液相比较,pH小的是HClO
D.Na2CO3水解的离子方程式:C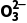 +H2O
+H2O HC
HC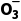 +OH-
+OH-
|
二 |
水解产物的判断及水解方程式的书写 |
3.物质与水发生的复分解反应称为水解反应。例如:Mg3N2+6H2O 3Mg(OH)2↓+2NH3↑。在一定条件下,BrCl、CuCl2、Mg2C3和K3P均可以发生水解。根据上述观点,下列说法不正确的是()
3Mg(OH)2↓+2NH3↑。在一定条件下,BrCl、CuCl2、Mg2C3和K3P均可以发生水解。根据上述观点,下列说法不正确的是()
A.BrCl的水解产物是HBrO和HCl
B.K3P的水解产物是KOH和H3PO4
C.Mg2C3的水解产物是Mg(OH)2和C3H4
D.CuCl2的水解产物是Cu(OH)2和HCl
4.用离子方程式表示下列事实。
(1)铁盐净水:。
(2)NaHS溶液呈碱性:。
(3)Na2C2O4溶液呈碱性:。
(4)FeCl3溶液与NaHCO3溶液混合产生大量泡沫:。

酸式盐溶液酸碱性的判断
(1)强酸的酸式盐只电离,不水解,溶液一定显酸性;如NaHSO4 Na++H++S
Na++H++S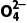 。
。
(2)弱酸的酸式盐溶液的酸碱性,取决于酸式酸根离子的电离程度和水解程度的相对大小。
①电离程度大于水解程度时呈酸性,如NaHSO3、NaHC2O4。
②电离程度小于水解程度时呈碱性,如NaHCO3、NaHS。
考点二盐类水解的影响因素及应用

1.影响盐类水解的因素
(1)内因:形成盐的酸或碱越弱,其盐就越易水解,例如,由酸性:CH3COOH>H2CO3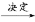 3、CH3COONa溶液的pH:NaHCO3(填“>”“=”或“<”)CH3COONa。
3、CH3COONa溶液的pH:NaHCO3(填“>”“=”或“<”)CH3COONa。

通过网盘分享的文件:word讲义
链接: https://pan.baidu.com/s/136tUpK67Q1V3PV2VsUIuPw?pwd=4321 提取码: 4321
–来自百度网盘超级会员v8的分享
 夜雨聆风
夜雨聆风




