《物质的量》易错题提升练(可下载word版)

对于资料下载,敬请点击:
【友情提示】本公众号使用说明书
为便于友友们阅读,现将各个合集的代表作展示如下,欢迎赐教:
(1)《氧化还原反应》合集:【热点提升】信息化氧化还原反应方程式如何破解(可下载word版)
(2)《物质的量》合集:雾点警示:你知道摩尔命题有哪些魔坑吗
(3)《物质结构、元素周期律》合集:【专题突破】《物质结构与性质》综合性难点如何考查(可下载word版)
(4)《电化学》合集:【专题突破】如何弄懂电化学中的那些膜(可下载word版)
(5)《化学平衡、化学反应速率》合集:【专题破解】化学平衡图像题的分析技巧(可下载wod版)
(6)《电解质溶液》合集:【解题指导】电解质溶液两类特异图像的解题技巧
(7)《化学实验》合集:热点提升:常见两类实验,破解设计方案
(8)《有机化学》合集:【解密高考】有机化学命题意图有哪些
(9)《我的育人理念》合集:考后寄语:高考,人生的跳板而已
(10)《我的文学作品》合集:周末驿站:那个中午,我收到了3封情书
(11)《诗歌》合集:教师节抒怀诗词两首
百度网盘:《物质的量》易错题提升练(可下载word版).docx
链接: https://pan.baidu.com/s/17E8dxdTcjCYxFxk0tGjYCA
提取码: cb25
课程标准
1.了解物质的量、摩尔质量、气体摩尔体积、阿伏加德罗常数的含义;
2.掌握物质的量与微粒数目、物质的质量、气体体积(标准状况下)、溶液的体积等之间的相互关系及有关计算;
3.了解阿伏加德罗定律。
一、常考易错选择题选项需排查
1、化学计量
正误判断,正确的打“√”,错误的打“×”
(1)考查气体摩尔体积适用条件及物质的聚集状态
①常温常压下,14 g由N2与CO组成的混合气体含有的原子数目为NA( )
②常温常压下,2.24 L CO和CO2混合气体中含有的碳原子数目为0.1NA( )
③标准状况下,22.4 L二氯甲烷的分子数约为4NA个( )
【答案】①√ ②× ③×
(2)考查物质的组成和结构
①1 mol羟基与1 mol的氢氧根所含电子数均为9NA( )
②28 g乙烯和环丁烷(C4H8)的混合气体中含有的碳原子数为2NA( )
③1 mol Na2O 与1 mol Na2O2的固体中含有的阴离子数均为NA( )
④1.7 g H2O2中含有电子数为0.9NA( )
⑤1 mol NaCl中含有6.02×1023个NaCl分子( )
【答案】①× ②√ ③√ ④√ ⑤×
(3)考查氧化还原反应电子转移数目
①标准状况下,0.1 mol Cl2溶于水,转移的电子数目为0.1NA( )
②1 mol Na与足量O2反应,生成Na2O和Na2O2的混合物,钠失去NA个电子( )
③常温常压下,Na2O2与足量H2O反应,共生成0.2 mol O2,转移电子的数目为0.4NA( )
④1 mol Cl2与足量Fe反应,转移的电子数为3NA( )
【答案】 ①× ②√ ③√ ④×
(4)考查电解质溶液中粒子的数目
①1 L 1 mol·L-1的NaClO溶液中含有ClO-的数目为NA( )
②1 L 0.1 mol·L-1氨水含有0.1NA个OH-( )
③常温下,10 L pH=1的硫酸溶液中含有的H+的数目为2NA( )
④常温下,10 L pH=13的NaOH溶液中含有的OH-的数目为NA( )
⑤1.0 L 1.0 mol·L-1的NaAlO2水溶液中含有的氧原子数为2NA( )
⑥1 mol·L-1NaCl溶液含有NA个Na+( )
【答案】 ①× ②× ③× ④√ ⑤× ⑥×
(5)考查化学反应前后微粒数目的变化
①50 mL 18.4 mol·L-1浓硫酸与足量铜微热反应,生成SO2分子的数目为0.46NA( )
②某密闭容器盛有0.1 mol N2和0.3 mol H2,在一定条件下充分反应,转移电子的数目为0.6NA( )
③1 mol Cu和足量稀硝酸反应产生NA个NO分子( )
④0.1 mol H2与0.1 mol I2蒸气在密闭容器中充分反应后,分子总数为0.2NA( )
⑤常温常压下,将0.1 mol NH3与0.1 mol HCl混合充分反应后,分子总数为0.2NA( )
【答案】 ①× ②× ③× ④√ ⑤×
2、溶液配制
正误判断,正确的打“√”,错误的打“×”
(1)10 mL质量分数为98%的H2SO4,用10 mL水稀释后,H2SO4的质量分数大于49%( )
(2)在标况下,将22.4 L氨气溶于1 L水中,得到1 mol·L-1的氨水( )
(3)实验室用蔗糖配制100.0 g溶质的质量分数为10%的蔗糖溶液,必须用到:100 mL的容量瓶、托盘天平、玻璃棒、烧杯和胶头滴管( )
(4)配制0.1 mol·L-1的Na2CO3溶液480 mL,需用500 mL容量瓶( )
(5)配制0.1000 mol·L-1碳酸钠溶液,将溶液转移到容量瓶中需用玻璃棒引流( )
(6)用容量瓶配制溶液时,若加水超过刻度线,立即用滴管吸出多余液体( )
(7)用pH=1的盐酸配制100 mL pH=2的盐酸只需要100 mL容量瓶、烧杯、玻璃棒、胶头滴管( )
(8)用容量瓶配制溶液,定容时俯视刻度线,所配溶液浓度偏小( )
(9)配制浓度为0.010 mol·L-1的KMnO4溶液时,称取KMnO4固体0.158 g,放入100 mL容量瓶中,加水溶解并稀释至刻度 ( )
【答案】 (1)√ (2)× (3)× (4)√ (5)√ (6)× (7)× (8)× (9)×
对于该考点更详尽的应用,敬请阅读:
二、常考简答题答题语言要规范
1.实验室需要0.5 mol·L-1的NaOH溶液470 mL,配制时应称量__________g NaOH,称量时需要__________、________、________(填仪器名称)。
【答案】 10.0 托盘天平 小烧杯 药匙
2.检查容量瓶是否漏水的方法: ______________________。
【答案】 向容量瓶中加入适量水,盖好瓶塞,右手食指顶住瓶塞,左手托住瓶底,将容量瓶倒转过来看瓶口处是否有水渗出,若没有,将容量瓶倒立,将瓶塞旋转180度,重复上述操作,如果瓶口仍无水渗出,则此容量瓶不漏水
3.配制一定物质的量浓度溶液定容时的操作是______________________。
【答案】 往容量瓶中缓慢加蒸馏水,等液面离容量瓶瓶颈刻度线1~2 cm时,改用胶头滴管滴加蒸馏水至凹液面与刻度线相切
4.某医疗小分队用溶质质量分数为0.5%的过氧乙酸溶液对灾民的居住环境进行消毒。要配制溶质质量分数为0.5%的过氧乙酸溶液300 kg,需溶质质量分数为15%的过氧乙酸溶液________kg,配制的主要步骤是________、________、________。
【答案】 10 计算 称量(量取) 溶解(稀释)
【解析】 稀释前后溶液中溶质的质量不变,设需要溶质质量分数为15%的过氧乙酸溶液的质量为x,则15%×x=
300 kg×0.5%,x=10 kg;配制的主要步骤:首先根据溶质的质量=溶液的质量×溶质的质量分数计算需要过氧乙酸溶液的质量和水的质量,再换算为体积,并进行称量、量取,然后混合溶解。
5.为测定镁铝合金中铝的含量,设计如下图所示的实验:
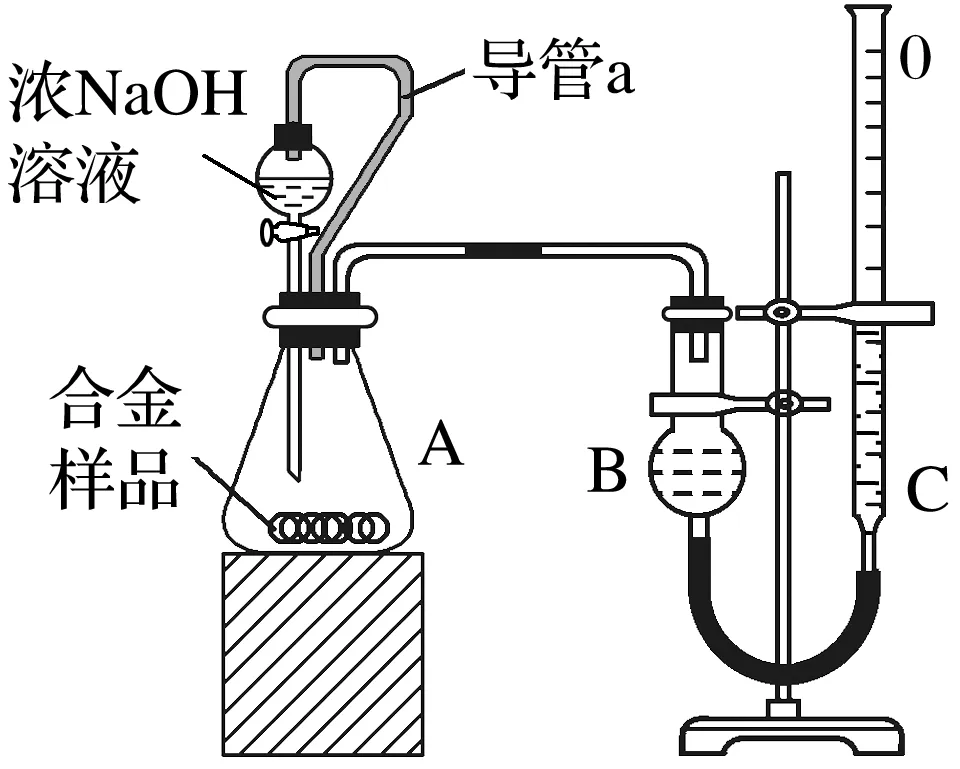
(1)锥形瓶中反应的化学方程式: ________________________。
(2)读数前调平B、C装置液面的方法是______________________,
其目的是________________________________________。
(3)若拆去实验中导管a,使测得气体体积________(填“偏大”“偏小”或“无影响”)。
【答案】(1)2Al+2NaOH+6H2O===6Na[Al(OH)4]+3H2↑
(2)上下缓慢移动量气管C 使B内的气压等于外界大气压
(3)偏大
特别提示:点击“合集”(操作方法见精选文章《本公众号使用说明书》)可以得到某合集所有考点的word版。

 夜雨聆风
夜雨聆风




