【2026年南方台江苏专用教辅电子版化学培优word讲义第12讲练习1氮气氮的氧化物
 12讲 氮及其化合物
12讲 氮及其化合物
练习1 氮气 氮的氧化物
1. (2022·江苏卷)氮及其化合物的转化具有重要应用。下列说法错误的是(A)
A. 自然固氮、人工固氮都是将N2转化为NH3
B. 侯氏制碱法以H2O、NH3、CO2、NaCl为原料制备NaHCO3和NH4Cl
C. 工业上通过NH3催化氧化等反应过程生产HNO3
D. 多种形态的氮及其化合物间的转化形成了自然界的“氮循环”
【解析】 自然固氮和人工固氮得到的氮的化合物不一定是NH3,如自然固氮中N2与O2放电生成NO,A错误。
2. (2023·前黄中学)氨气经氧化等步骤制得硝酸。利用石灰乳、尿素等吸收硝酸工业的尾气(含NO、NO2),石灰乳吸收时主要反应为NO2+NO+Ca(OH)2===Ca(NO2)2+H2O。下列关于氮氧化物的形成、吸收等说法正确的是(D)
A. 汽车尾气中含氮氧化物,主要来源于烃类燃料
B. 用石灰乳吸收NO和NO2,增加气体流速可提高氮氧化物的吸收率
C. 收集NO2气体时采用排水法,可提高NO2气体的纯度
D. 用CO(NH2)2可将NO2转化为N2,是利用了CO(NH2)2的还原性
【解析】 汽车尾气中的氮氧化物主要由空气中的N2和O2在气缸中高温条件下生成,A错误;减慢气体流速可提高氮氧化物与石灰乳的接触时间,提高氮氧化物的吸收率,B错误;NO2能溶于水且能与水反应,不能用排水法收集,C错误;CO(NH2)2+NO2→N2,CO(NH2)2中N由-3价升至0价,CO(NH2)2作还原剂,D正确。
阅读下列材料,完成第3题。
N、P为第ⅤA族元素。NH3是氮的常见氢化物,液氨可部分电离产生NH-2和NH+4,氨水与Ag+形成Ag(NH3)2OH;NH3可转化为NO、NO2、HNO3等。磷单质主要有红磷、白磷和黑磷,黑磷具有类似石墨的片状结构,称之为“金属磷”;PCl5为离子晶体,其晶胞结构如图所示,PCl5溶于水生成两种常见的酸。
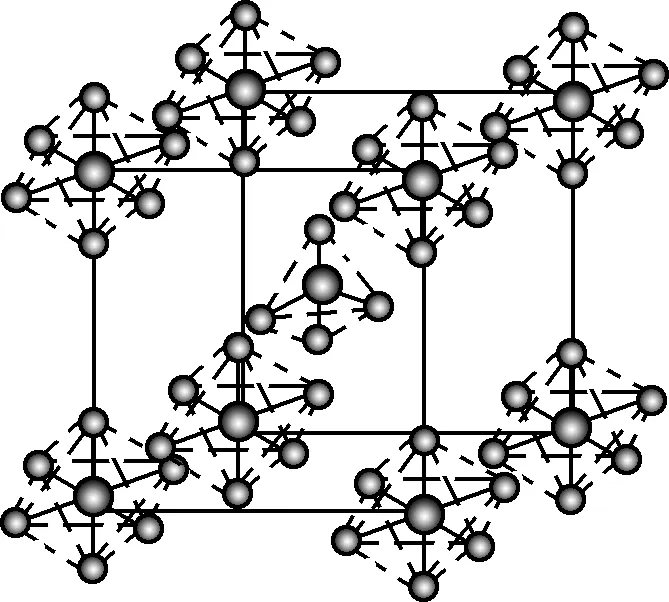
PCl5晶胞结构图
3. (2024·镇江期末)下列说法错误的是(D)
A. NH+4键角约为109.5°
B. 液氨电离可表示为2NH3NH+4+NH-2
C. PCl5晶胞中含有PCl-6与PCl+4两种离子
D. 红磷、白磷、黑磷互为同分异构体
【解析】 NH+4空间结构为正四面体形,键角约为109.5°,A正确;由题给信息可知液氨可部分电离产生NH-2和NH+4,B正确;PCl5晶胞中位于顶点的正八面体为PCl-6、位于体心的正四面体为PCl+4,C正确;红磷、白磷、黑磷互为同素异形体,D错误。
4. (2024·江苏各地模拟)下列叙述正确的是(C)
A. 氨气催化氧化制取NO属于氮的固定中的一种
B. 1 mol SO3和1 mol NO2分别通入1 L水中可产生相同浓度的H2SO4和HNO3
C. NO2尾气可用Na2CO3溶液吸收
D. 用下图装置收集NO气体
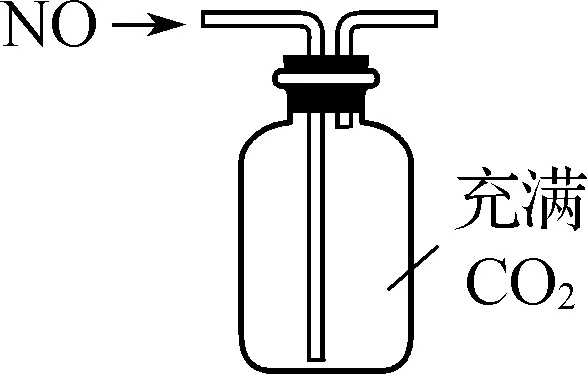
【解析】 氮的固定是指将N2转化为氮的化合物,A错误;1 mol SO3和1 mol NO2分别通入1 L水中最终溶液体积未知,无法计算所得溶液的物质的量浓度,B错误;NO2在碱性溶液中发生歧化反应,并促进CO2-3水解,总反应为2NO2+CO2-3===NO-3+NO-2+CO2,可以用Na2CO3溶液吸收NO2尾气,C正确;NO密度小于CO2,应短管进气,长管出气,D错误。
5. (2023·苏锡常镇二模)下列化学反应表示正确的是(B)
A. 用水吸收二氧化氮制硝酸:2NO2+H2O===HNO3+NO
B. 用烧碱溶液吸收硝酸工业尾气:NO+NO2+2OH-===2NO-2+H2O
C. 雷雨天气空气中的氮气和氧气反应:N2+2O2放电2NO2
D. 铜粉和稀硝酸反应:4H++2NO-3+Cu===Cu2++2NO2↑+2H2O
【解析】 H、O原子均不守恒,A错误;雷雨天气中,N2与O2反应生成NO,C错误;铜粉与稀硝酸反应生成的气体是NO,D错误。
6. (2023·华罗庚中学)下列选项所示的物质间转化均能实现的是(B)
A. N2――→O2放电NO2
B. NO2Na2CO3NaNO2
C. HNO3(aq)少量Fe粉Fe(NO3)2
D. NO――→SO2H2OHNO3
【解析】 氮气和氧气在闪电作用下只能生成NO,A错误;2NO2+Na2CO3===NaNO2+NaNO3+CO2↑,B正确;稀硝酸与少量铁粉生成Fe(NO3)3,C错误;SO2主要表现还原性,不能将NO氧化为HNO3,D错误。
7. (2023·连云港期末)常温下NaNO2与H2SO4反应能生成NO和NO2。实验室探究NaNO2与H2SO4反应及气体产物的成分。下列实验装置和操作不能达到实验目的的是(D)
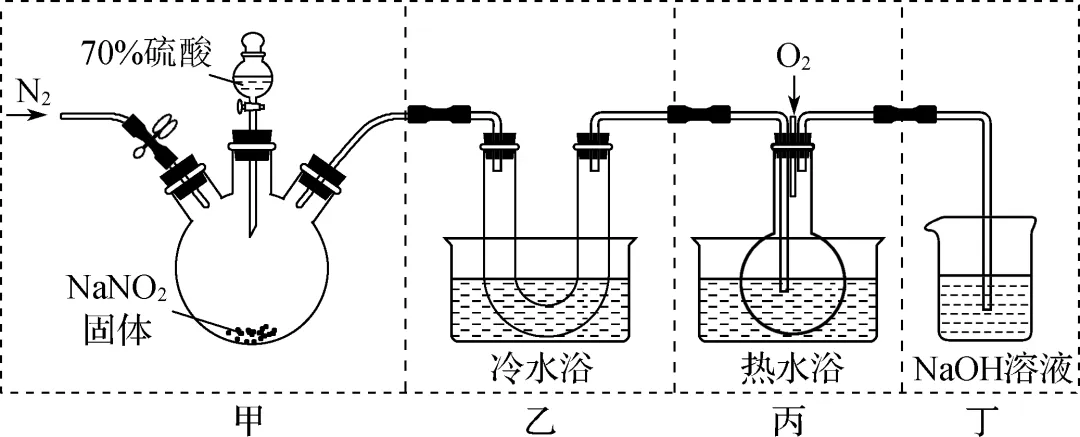
A. 用装置甲制取气体
B. 用装置乙收集生成的NO2
C. 用装置丙检验NO生成
D. 蒸发丁中所得溶液得到纯净NaNO3晶体
【解析】 NaNO2与硫酸常温下反应生成NO和NO2,A正确;冷水可以将NO2液化,达到收集NO2的目的,B正确;NO是无色气体,通入O2后变为红棕色NO2,C正确;NO2与NaOH溶液生成NaNO3、NaNO2和水,D错误。
8. N2O、NO和NO2等氮氧化物是空气污染物,含有氮氧化物的尾气需处理后才能排放。
(1) N2O的处理。N2O是硝酸生产中氨催化氧化的副产物,用特种催化剂能使N2O分解。NH3与O2在加热和催化剂作用下生成N2O的化学方程式:2NH3+2O2=====催化剂△N2O+3H2O。
(2) NO和NO2的处理。已除去N2O的硝酸尾气可用NaOH溶液吸收,主要反应:
NO+NO2+2OH-===2NO-2+H2O
2NO2+2OH-===NO-2+NO-3+H2O
①下列措施能提高尾气中NO和NO2去除率的有BC(填字母)。
A. 加快通入尾气的速率
B. 采用气、液逆流的方式吸收尾气
C. 吸收尾气过程中定期补加适量NaOH溶液
②吸收后的溶液经浓缩、结晶、过滤,得到NaNO2晶体,该晶体中的主要杂质是NaNO3(填化学式);吸收后排放的尾气中含量较高的氮氧化物是NO(填化学式)。
(3) NO的氧化吸收。用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。其他条件相同,NO转化为NO-3的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示:
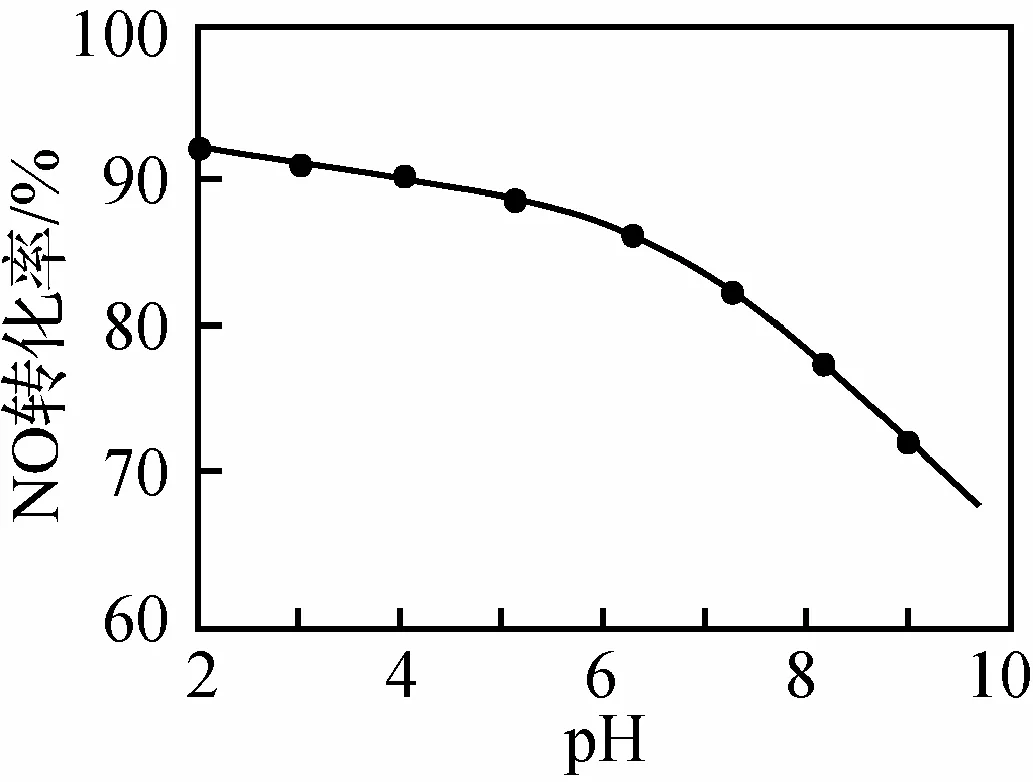
①在酸性NaClO溶液中,HClO氧化NO生成Cl-和NO-3,其离子方程式:3HClO+2NO+H2O===3Cl-+2NO-3+5H+。
② NaClO溶液的初始pH越小,NO转化率越高。其原因是溶液pH越小,溶液中HClO的浓度越大,氧化NO的能力越强。
通过网盘分享的文件:南方凤凰台·2026全国一轮电子稿等7个文件
链接: https://pan.baidu.com/s/1Q8yIZ6J_EF4Bq61Fj8yz8w?pwd=4321 提取码: 4321
–来自百度网盘超级会员v8的分享
 夜雨聆风
夜雨聆风




