【2026年南方台江苏专用教辅电子版化学培优word讲义第1讲练习2物质的量

1. (2023·徐州期初)设NA为阿伏加德罗常数的值。下列说法正确的是(B)
A.一定条件下3.2 g SO2与足量O2反应转移电子数为0.1NA
B.2.9 g异丁烷和正丁烷混合物含有C—H数目为0.5NA
C.50 mL 12 mol/L浓盐酸与足量MnO2共热转移电子数0.3NA
D.标准状况下,3.36 L三氯甲烷中含有氯原子数目为0.45NA
【解析】 SO2与O2的反应是可逆反应,3.2 g SO2(即0.05 mol),与足量O2反应转移电子少于0.05 mol×2=0.1 mol,A错误;正丁烷和异丁烷分子中均含有10个C—H,2.9 g(0.05 mol)正丁烷和异丁烷混合物中含有的C—H数目为0.5 NA,B正确;随着反应进行,盐酸由浓变稀,MnO2与稀盐酸不反应,无法计算转移的电子数,C错误;标准状况下三氯甲烷为液态,不能根据气体摩尔体积来计算其物质的量,D错误。
2. (2024·贵州卷)二氧化氯(ClO2)可用于自来水消毒。实验室用草酸(H2C2O4)和KClO3制取ClO2的反应为H2C2O4+2KClO3+H2SO4===2ClO2↑+2CO2↑+K2SO4+2H2O,设NA为阿伏加德罗常数的值。下列说法正确的是(D)
A. 0.1 mol H182O中含有的中子数为1.2NA
B. 每生成67.5 g ClO2,转移电子数为2.0NA
C. 0.1 mol/L H2C2O4溶液中含有的H+数目为0.2NA
D. 标准状况下,22.4 L CO2中含σ键数目为2.0NA
【解析】 H182O中子数为10,0.1 mol H182O中含有的中子数为NA,A错误;反应中每生成2 mol ClO2转移2 mol e-,则每生成67.5 g ClO2(即1 mol),转移1 mol e-,B错误;缺少溶液的体积和该温度下H2C2O4的电离平衡常数,无法计算H+数目,C错误。
3. (2024·常州期末)下列有关配制一定物质的量浓度溶液的操作(图中箭头表示运动方向)正确的是(A)
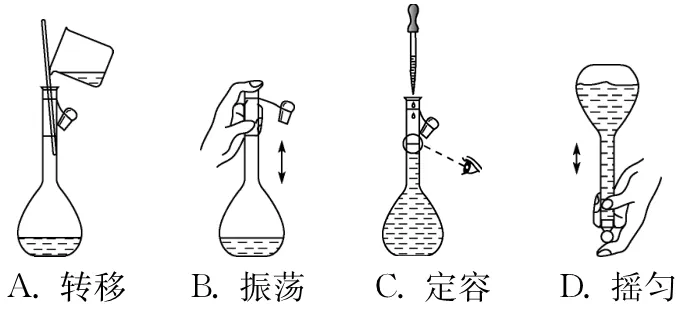
【解析】 振荡时,应塞紧容量瓶的瓶塞,B错误;定容时,应平视刻度线,C错误;摇匀时,应盖好瓶塞,用食指顶住瓶塞,用另一只手托住瓶底,把容量瓶反复倒转多次,摇匀,D错误。
4. (1) (2024·如东、姜堰中学联考)用亚硫酸钠固体配制250 mL 0.2 mol/L Na2SO3溶液,下列仪器无需使用的是分液漏斗、冷凝管(或球形冷凝管)(填仪器名称)。

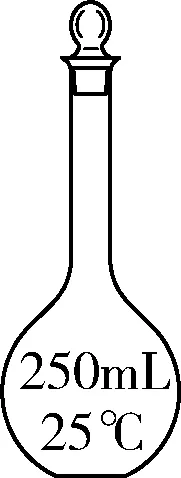
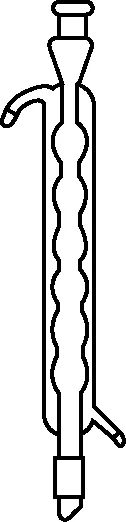
(2) (2023·南京六校期初)由浓硫酸配制250 mL 1.0 mol/L H2SO4溶液,需要用到的玻璃仪器有烧杯、玻璃棒、量筒、250 mL容量瓶、胶头滴管。
(3) (2023·如皋期初)10 L密度为1.83 g/mL、质量分数为98%的浓硫酸,其中所含H2SO4的物质的量为183 mol。
【解析】 (3) m(浓硫酸)=ρV=1.83 g/mL×10 000 mL=18 300 g,n(H2SO4)=mM=18 300 g×98%98 g/mol=183 mol。
5. (1)(2022·海南卷)现有浓磷酸质量分数为85%,密度为1.7 g/mL。若实验需100 mL 1.7 mol/L H3PO4溶液,则需浓磷酸11.5mL(保留一位小数)。
(2) (2024·前黄中学)处理100 m3含NaCN 10.3 mg/L的废水,实际至少需NaClO 14 900 g(实际用量应为理论值的4倍),才能使NaCN含量低于0.5 mg/L,达到排放标准[反应的离子方程式为2CN-+5ClO-+H2O===2CO2↑+N2↑+5Cl-+2OH-]。
【解析】 (1) 溶液稀释前后溶质的物质的量不变,列式为1 000×1.7×85%98 mol/L×V=100 mL×1.7 mol/L,解得V≈11.5 mL。(2) NaCN含量由10.3 mg/L降到0.5 mg/L,NaCN减少的浓度为9.8 mg/L=9.8×10-3 g/L,根据离子方程式可得关系式:2CN-~5NaClO,实际需要NaClO质量=9.8×10-3 g/L×100×103 L49 g/mol×52×74.5 g/mol×4=14 900 g。
6. (2023·如皋期初)以绿矾(FeSO4·7H2O)为原料,可以制取铁铬氧体Cr2Fe20O27(Cr为+3价)。制取的方法如下:向含1 mol CrO2-4的溶液中,加入10 mol FeSO4·7H2O,充分反应后向溶液中边通入空气边滴加NaOH溶液,反应后过滤得到铁铬氧体。反应共消耗O2的物质的量为0.25 mol。
【解析】 根据化合物中各元素化合价代数和为0可得Cr2Fe20O27中Fe元素平均化合价为+2.4。反应中Cr元素化合价降低了3,Fe元素化合价升高了0.4,则1 mol CrO2-4在反应中得到3 mol电子、10 mol 的FeSO4·7H2O在反应中失去4 mol电子,根据得失电子相等可知O2得1 mol电子,反应共消耗O2的物质的量为0.25 mol。
7. 草酸钙沉淀经稀硫酸处理后,用KMnO4标准溶液滴定,通过测定草酸的量可间接获知钙的含量,滴定反应为MnO-4+H++H2C2O4―→Mn2++CO2↑+H2O。实验中称取0.400 g水泥样品,滴定时消耗了0.050 0 mol/L KMnO4溶液36.00 mL,则该水泥样品中钙的质量分数为45.0%。
【解析】 配平离子方程式为2MnO-4+5H2C2O4+6H+===2Mn2++10CO2↑+8H2O,根据关系式:2KMnO4~5H2C2O4~5Ca2+,n(Ca2+)=52n(KMnO4)=52×0.050 0 mol/L×36.00×10-3 L=4.50×10-3 mol,水泥样品中钙的质量分数=4.50×10-3 mol×40.0 g/mol0.400 g×100%=45.0%。
8. 为测定某碘水(其溶质为I2)中碘单质的浓度,取该碘水10.00 mL,加入淀粉溶液作为指示剂,用0.01 mol/L Na2S2O3滴定此碘水,当溶液由蓝色变为无色时,消耗Na2S2O3的体积为20.00 mL。已知Na2S2O3被氧化为Na2SO4,则碘单质的浓度为(A)
A. 0.08 mol/L B. 0.16 mol/L
C. 0.04 mmol/L D. 0.06 mol/L
【解析】 设碘水中碘的浓度为x,S元素的化合价由+2升高为+6,I元素的化合价由0降低为-1,由得失电子守恒可知10.00×10-3 L×x×2×(1-0)=20.00×10-3 L×0.01 mol/L×2×(6-2),解得x=0.08 mol/L,故选A。
9. (2024·海安中学)PbO2受热分解为Pb的+4价和+2价的混合氧化物,+4价的Pb能氧化浓盐酸生成Cl2。现将1 mol PbO2加热分解得到O2,向“剩余固体”中加入足量的浓盐酸得到Cl2。生成的O2和Cl2的物质的量相等。“剩余固体”中Pb、O原子个数之比为3∶4。
【解析】 PbO2受热分解生成Pb的混合氧化物和O2,混合氧化物再与HCl反应生成Cl2。设产生x mol O2,则Cl2也为x mol,根据得失电子守恒得4x mol+2x mol=2 mol,x=13。即1 mol PbO2分解生成13 mol O2,则混合氧化物中n(O)=2 mol-13 mol×2=43 mol,而n(Pb)=1 mol,则n(Pb)∶n(O)=1∶43=3∶4。
10. (2023·泰州中学)用下列实验可以测定LixCoO2的组成:
实验1.准确称取一定质量的LixCoO2样品,加入盐酸,加热至固体完全溶解(溶液中的金属离子只存在Li+和Co2+),冷却后转移到容量瓶中并定容至100 mL。
实验2.移取25.00 mL实验1容量瓶中溶液,加入指示剂,用0.010 00 mol/L EDTA(Na2H2Y)溶液滴定至终点(滴定反应为Co2++Y4-===CoY2-),平行滴定3次,平均消耗EDTA溶液25.00 mL。
实验3.准确称取与实验1中等质量的LixCoO2样品,加入一定量的硝酸和H2O2溶液,加热至固体完全溶解。冷却后转移到容量瓶中并定容至100 mL。移取10.00 mL溶液,通过火焰原子吸收光谱法测定其中Li+浓度为6.000×10-3mol/L。计算化学式LixCoO2中x的值,并写出计算过程。
样品中n(Co2+)=n(Y4-)=0.010 0 mol/L×25.00×10-3 L×100 mL25.00 mL=1×10-3 mol,
样品中n(Li+)=6.000×10-3 mol/L×10.00×10-3 L×100 mL10.00 mL=6×10-4 mol,
故n(Li+)∶n(Co2+)=x∶1=6×10-4∶1×10-3,x=0.6
11. 实验室需要0.5 mol/L硫酸溶液480 mL。现在用浓硫酸配制该溶液,回答下列问题:
(1) 实验中需要质量分数为98%、密度为1.84 g/cm3的浓硫酸13.6 mL。
(2) 配制溶液时需要用到的玻璃仪器有烧杯、量筒、胶头滴管和500 mL容量瓶、玻璃棒(填仪器名称)。
(3) 在量取浓硫酸后,进行了下列操作:
① 等稀释的浓硫酸的温度与室温一致后,沿玻璃棒注入容量瓶中。
② 向容量瓶中小心加蒸馏水且边加边振荡均匀,加蒸馏水至液面离容量瓶刻度线1~2 cm时,改用胶头滴管加蒸馏水,使溶液的凹液面与刻度线相切。
③ 在盛有一定体积的蒸馏水的烧杯中注入浓硫酸,并用玻璃棒搅动,使其混合均匀。
④ 用蒸馏水洗涤烧杯和玻璃棒2~3次,并将洗涤液全部注入容量瓶。
上述操作中,正确的顺序是③①④②(填序号)。
(4) 若实验过程遇到下列情况,对硫酸物质的量浓度有何影响(填“偏高”“偏低”或“不变”)?
① 容量瓶洗涤,瓶底有少量蒸馏水,未干燥:不变;
② 定容时俯视观察液面:偏高。
通过网盘分享的文件:南方凤凰台·2026全国一轮电子稿等7个文件
链接: https://pan.baidu.com/s/1Q8yIZ6J_EF4Bq61Fj8yz8w?pwd=4321 提取码: 4321
–来自百度网盘超级会员v8的分享
 夜雨聆风
夜雨聆风




