NBT| 可控分体碱基编辑器实现体内癌症功能筛选
细胞是一座城。基因是图纸,蛋白是工人。而癌细胞最狡猾的地方是:它们往往不是把整栋楼拆掉,而只是悄悄拧松了某一颗螺丝……
问题来了——我们过去做基因功能筛选,常常擅长判断“这栋楼没了会怎样”,却不容易看清“到底是哪颗螺丝松了,才让整栋楼出问题”。
4月15日,Nature Biotechnology 发表了美国宾夕法尼亚大学Junwei Shi实验室领衔的一项新工作,论文题目是 Inducible, split base editors for in vivo cancer functional genomics。论文第一作者是 Diqiu Ren 和 Shangshang Wang。这项研究做的事情很漂亮:他们把传统碱基编辑器改造成了一种可诱导、可控、能在体内做大规模筛选的新系统,用来更精细地寻找癌症中的关键突变位点和治疗靶点。

为什么传统碱基编辑器不够理想?
碱基编辑器这些年很火,因为它不像经典CRISPR那样直接把DNA切断,而是更像“定点改字”,把一个碱基改成另一个碱基。对于研究癌症来说,这特别有吸引力:因为癌症里大量真正有意义的变化,往往不是基因整段消失,而是一个氨基酸被改了,一个功能位点被扰乱了,甚至出现显性负效应。
但问题也很现实。传统碱基编辑器里,负责“化学改字”的脱氨酶是完整存在的,它有时候并不老老实实等Cas9带路,自己也会乱动手,造成非特异性编辑、细胞毒性、转录扰动。这在体外就已经麻烦,在体内做筛选更是难上加难。某种意义上,这就像你请来一个修表师傅,但他在修指针之前,先把整个钟表铺都敲了一遍。
这篇文章的巧思:把编辑器“拆开”,再用小分子打开
这项工作的核心思路很有工程美感。研究团队没有继续使用完整的脱氨酶,而是把它拆成两半,平时两部分都处于“失活”状态;只有在加入特定小分子后,这两半才会重新组合,恢复编辑活性。作者把这类系统称为 split-engineered base editors,简称 seBEs。
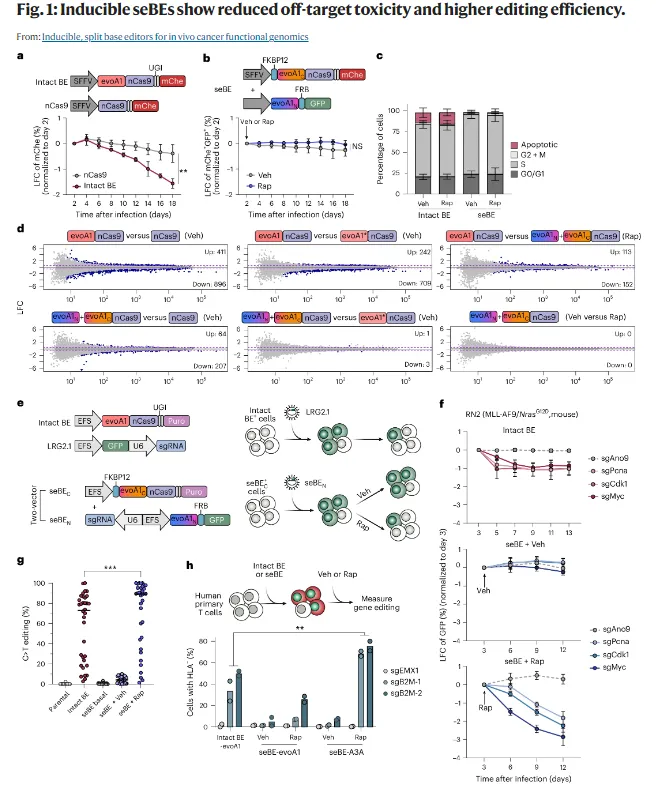
这个设计的好处非常直接:第一,编辑器不再长期“裸奔”,背景毒性明显下降;第二,编辑什么时候开始、持续多久,可以人为控制;第三,这种可控性反过来提升了它在复杂模型,尤其是体内功能基因组学筛选中的可用性。
说得更通俗一点,过去的编辑器像一把一直开着的电钻,握在手里就让人紧张;现在它更像一把带保险开关的工具,不用的时候安静待命,需要时再精准启动。
他们到底做到了什么?
这篇文章不只是“做了一个新工具”,而是真把它用到了高密度筛选里。作者在体外用了大约11,000条sgRNA,在体内用了大约3,700条sgRNA进行筛选,成功找到了癌症治疗相关靶点中已知和此前未知的功能性突变,包括loss-of-function 和 dominant-negative 类型。
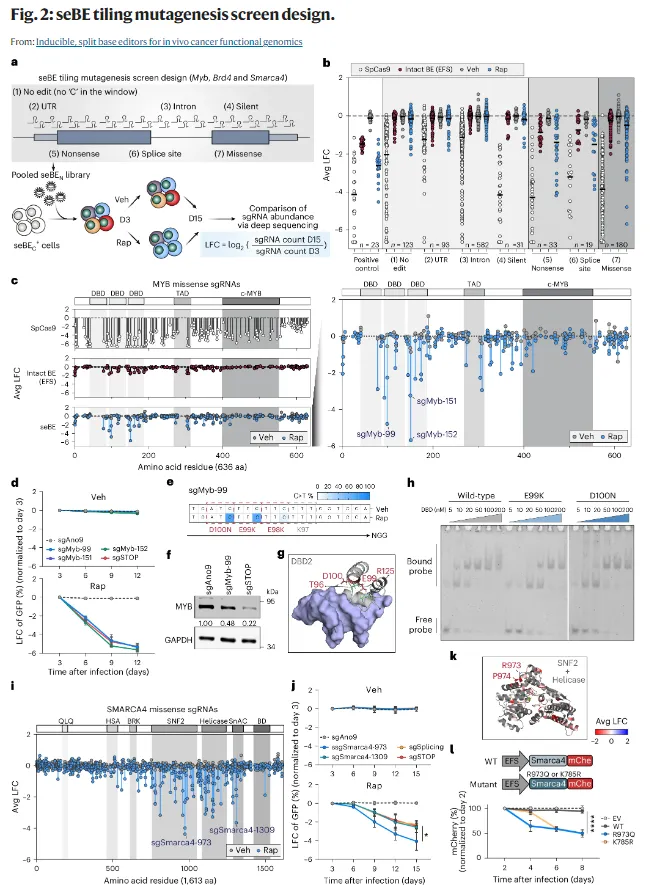
这很关键。因为对于药物研发来说,很多时候最值得知道的,不只是“这个基因重要不重要”,而是“这个蛋白上到底哪几个残基最不能碰”。一旦定位到具体位点,后面的药物设计、机制研究,甚至耐药分析,都会更有抓手。
最有意思的一点:体外没事,体内却很重要
文章里一个很值得多看两眼的靶点是 Adar1。它是癌症免疫治疗领域的一个重要分子。研究团队对Adar1做了更深度的tiling筛选后发现,有些功能域中的关键残基,在体外实验里几乎看不出明显表型,但到了体内,却能明显触发与肿瘤微环境相关的依赖性。
这说明什么?说明肿瘤不是一个“单细胞故事”。很多基因效应,离开了免疫系统、基质细胞、细胞间通讯,根本看不完整。你在培养皿里看到的“没反应”,未必代表它真的不重要;它可能只是把真正的戏份留到了体内。这个发现,也是这篇文章最让我觉得“值钱”的地方之一。
这项工作为什么值得关注?
我觉得它至少回答了三个问题。
第一,碱基编辑能不能更安全、更可控?这篇文章给出的答案是:可以,而且这种“可控”不是锦上添花,而是决定它能不能真正进入体内大规模筛选的关键。
第二,癌症功能基因组学能不能从“基因层面”走向“残基层面”?也可以。过去我们更多是在问某个基因删掉会怎样,现在则可以进一步问:这个蛋白的哪一段、哪个位点,才是癌细胞真正的命门。
第三,体外筛选能不能代表体内真实生物学?未必。作者在Adar1上的结果再次提醒我们,很多癌症相关依赖性,本质上带着强烈的体内环境属性。谁能在体内看得更细,谁就更接近真正有转化价值的答案。
最后说一句
这篇工作最打动人的地方,不只是“把碱基编辑器拆开了”这么简单,而是它把一种原本有些“难驯”的工具,变成了一个可以定时、定量、定场景使用的研究平台。在癌症研究里,这意味着我们未来或许不只是知道“哪个基因重要”,还会越来越清楚:哪个残基最关键,哪个突变最致命,哪个位点最值得做药。
对做基础研究的人来说,这是分辨率的提升。 对做转化的人来说,这是靶点质量的提升。 而对读者来说,记住一句话就够了:编辑器加上“开关”,看到的癌症世界会更真实。
 夜雨聆风
夜雨聆风




