NC |利用CRISPR碱基编辑器筛选,揭示临床menin抑制剂的MEN1突变耐药谱
KMT2A重排和NPM1突变急性白血病依赖于menin-KMT2A蛋白互作维持白血病发生,多款menin抑制剂已进入临床试验并展现出良好活性。然而,接受SNDX-5613治疗的患者中已发现MEN1突变导致获得性耐药,这些突变对不同menin抑制剂的影响程度尚不明确。2026年5月9日,Dana-Farber癌症研究所Scott Armstrong与俄勒冈健康与科学大学Jevon Cutler团队在Nature Communications上发表题为“CRISPR base editor screening identifies spectrum of MEN1 mutations impacting menin inhibitors in clinical trials”的研究论文。该研究利用升级版CRISPR碱基编辑器筛选技术,系统绘制了五种临床menin抑制剂的MEN1突变耐药图谱,鉴定出共享和药物特异性的耐药突变,并通过共晶结构和体内外模型验证了突变产生机制及其临床相关性。

主要研究结果
1. 五种临床menin抑制剂在MEN1野生型细胞系中具有相似的menin结合位点、亲和力及抗白血病活性。
研究比较了五种可逆性menin抑制剂DS-1594、JNJ-6617、KO-539、SNDX-5613和DSP-5336,其中DS-1594和KO-539共享噻吩并嘧啶核心,JNJ-6617、SNDX-5613和DSP-5336共享芳氧基苯甲酰胺核心(图1A)。共晶结构确认各化合物均结合于menin的KMT2A结合口袋,但与口袋内氨基酸残基的距离不同(图1B)。TR-FRET竞争结合实验显示五种抑制剂均以个位数纳摩尔级亲和力置换KMT2A肽段(图1C)。在MOLM13、MV4;11和OCI-AML3细胞系中,所有抑制剂均表现出低纳摩尔半数抑制浓度(图1D)。
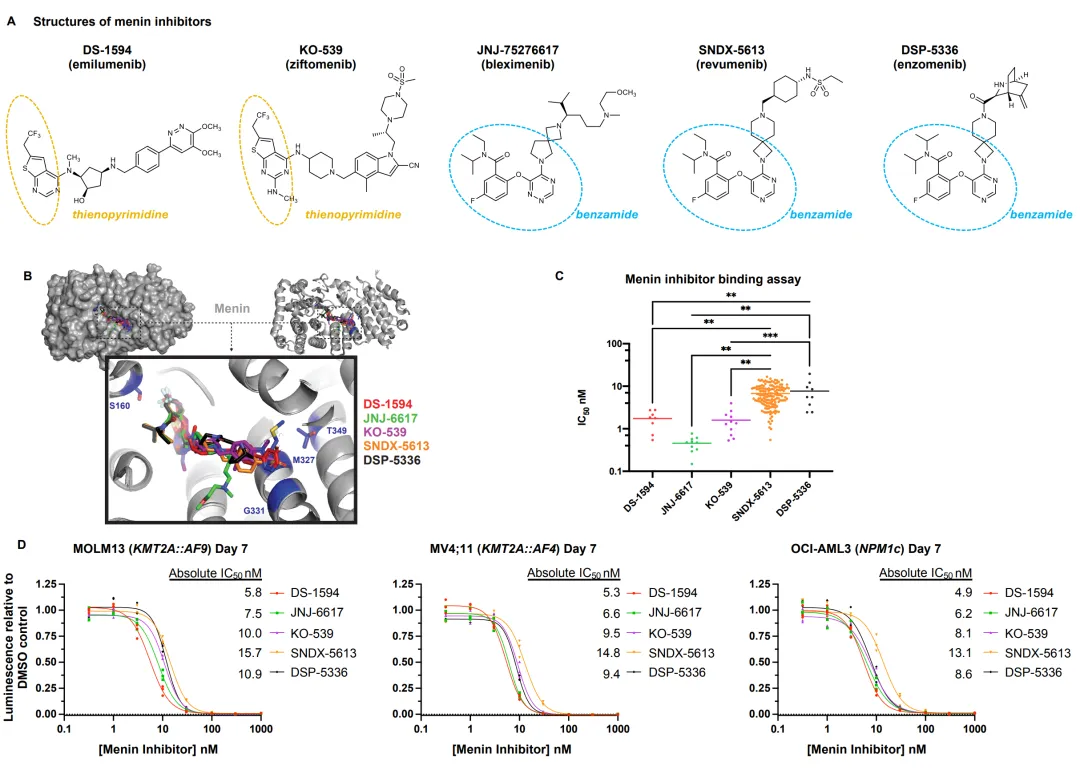
图1 Menin抑制剂在MEN1野生型细胞系中具有相似活性。
2. MEN1聚焦的CRISPR碱基编辑器筛选系统揭示共享和药物特异性耐药突变。
研究建立了MV4;11 A>G和C>T两种碱基编辑器细胞系,设计覆盖MEN1编码外显子的sgRNA文库(图2A)。在21天筛选周期中,使用对每种药物等抑制活性浓度进行处理,细胞在筛选后期出现加速生长(图2B)。sgRNA丰度分析显示,高度富集(Log2FC ≥ 3.75)的sgRNA在少数氨基酸残基处显著聚集,包括已知的SNDX-5613耐药位点(S160、M327、G331、T349)和此前未报道的位点(E368、V372)(图2C)。通过Genomics2Proteins门户预测的氨基酸替换映射到共晶结构上,显示大多数赋予耐药的氨基酸位于KMT2A结合口袋内(图2D)。
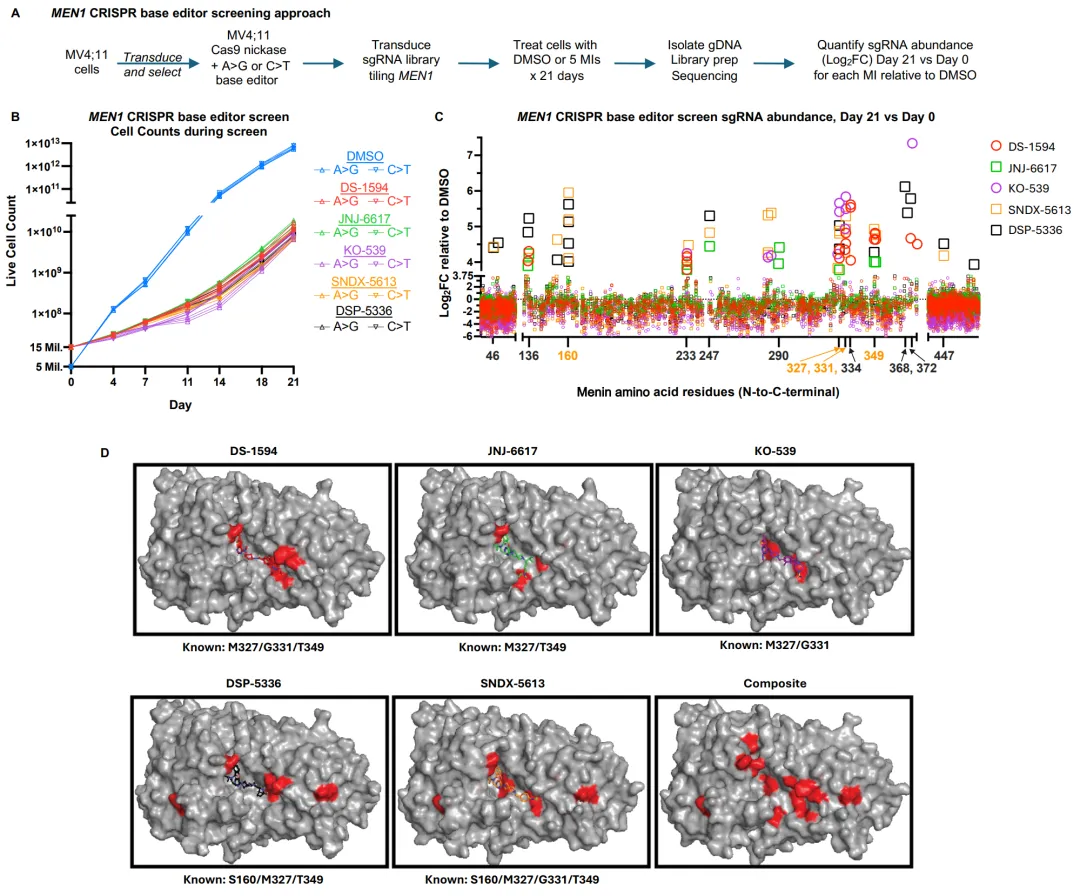
图2 临床menin抑制剂的MEN1碱基编辑器筛选。
3. 单sgRNA验证鉴定出共享和抑制剂特异性MEN1耐药突变。
从筛选结果中选取40个高度富集的sgRNA进行单引导验证。竞争实验显示37个细胞系表现出耐药性。确认性活力测定鉴定出12种MEN1突变细胞系(涵盖M327、G331、T349、A247、D290、C334、E368、V372等8个残基),其绝对IC50较野生型至少偏移10倍(图3A-C)。扩增子测序确认每种细胞系的主要编辑靶向预测的氨基酸残基(图3D)。C334R突变特异性影响DS-1594(>14倍),E368K突变特异性影响DSP-5336(>75倍),V372A突变特异性影响KO-539(>20倍);M327突变具有泛类药物耐药能力,M327T对每种药物偏移至少14倍(图3B-C)。在JNJ-6617处理20天后,D290H和G331D分别被富集,其中D290H主要影响JNJ-6617(>13倍),而G331D赋予泛类耐药性(DS-1594 >177x,SNDX-5613 >72x)(图3E-H)。
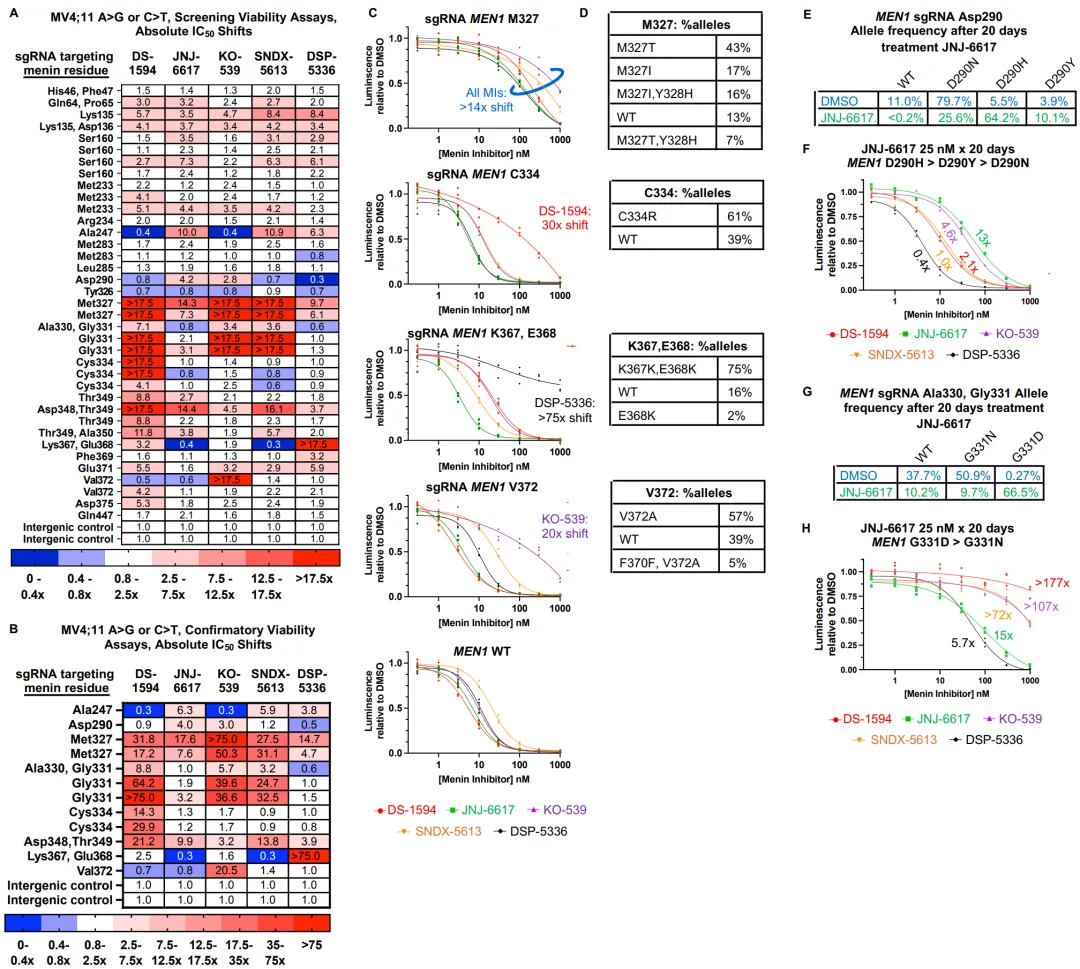
图3 MEN1碱基编辑器筛选的单引导验证。
4. 生化与结构分析揭示MEN1突变耐药机制。
TR-FRET位移实验显示MEN1突变蛋白对menin抑制剂的结合亲和力变化与细胞活力测定中IC50偏移高度相关(图4A-B)。M327I在所有共晶结构中其β-支链甲基取代基直接指向抑制剂,DS-1594、KO-539和SNDX-5613以延伸构象跨过M327位置,遭受更明显的结合姿态扭曲;JNJ-6617和DSP-5336以避开M327的构象结合,位移程度较小(图S10)。A247T突变对芳氧基苯甲酰胺类药物(JNJ-6617、SNDX-5613、DSP-5336)影响更大(图4C-F)。共晶结构揭示E368与DSP-5336形成直接离子对,C334R通过空间冲突影响DS-1594,V372A可能通过削弱KO-539与W346的氢键导致耐药(图4D-F)。将IC50偏移映射到共晶结构上清晰展示了不同药物独特的耐药突变谱(图4G)。
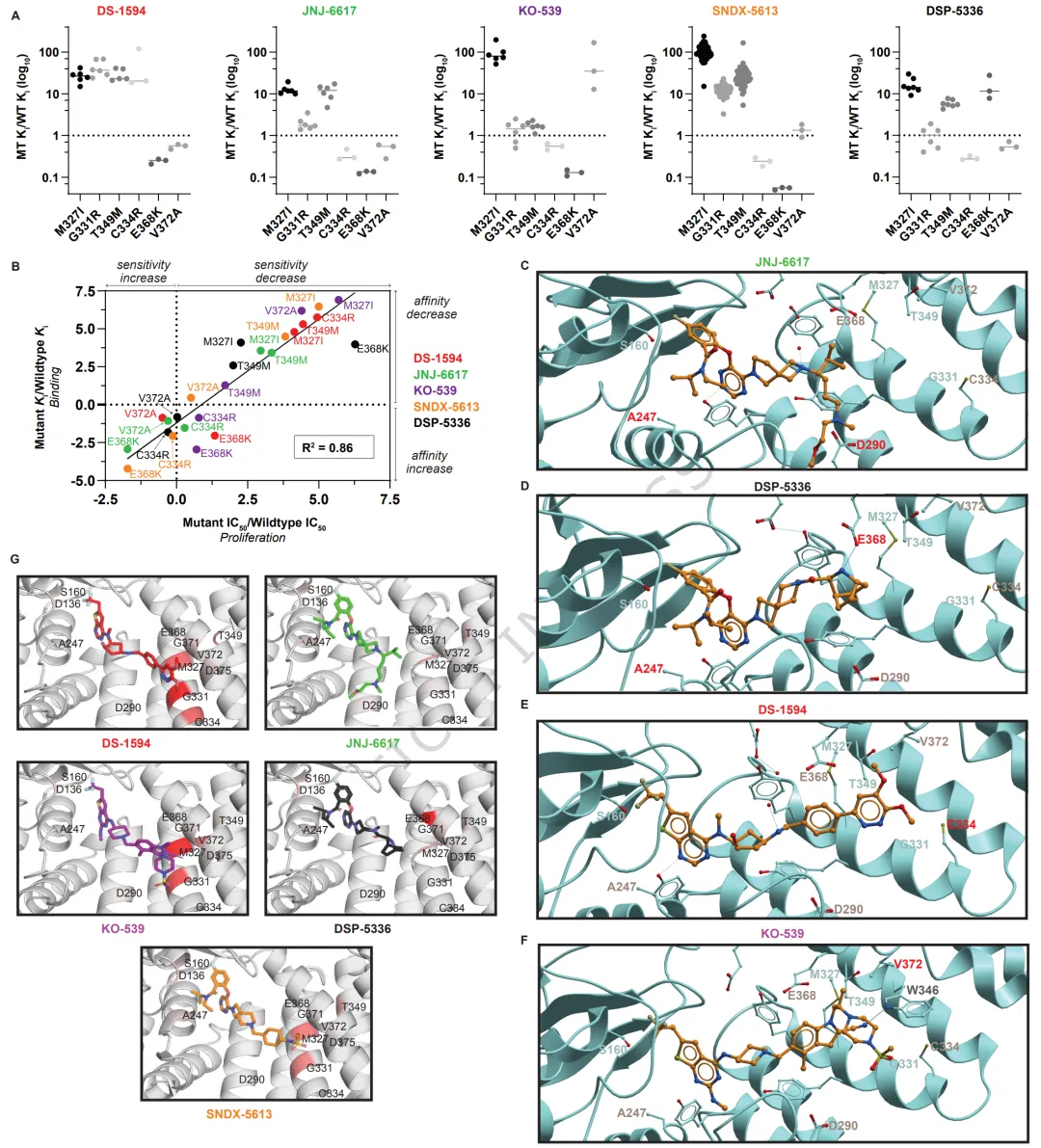
图4 MEN1突变影响的生化与结构洞察。
5. 体外新发MEN1突变生成验证筛选预测。
在22个MOLM13重复培养中以25 nM DSP-5336处理,24天后4个重复出现快速生长,其中2个检测到E368K/V突变(图5A-B)。E368K细胞的活力测定显示仅对DSP-5336显著耐药(>85x),对JNJ-6617和SNDX-5613甚至增敏(图5C)。以JNJ-6617处理发现M327V、T349M和G331D突变(图5D-E),M327V表现出泛耐药性(KO-539最受影响为53x),G331D也使DS-1594、SNDX-5613和KO-539受到最严重影响(图5F)。
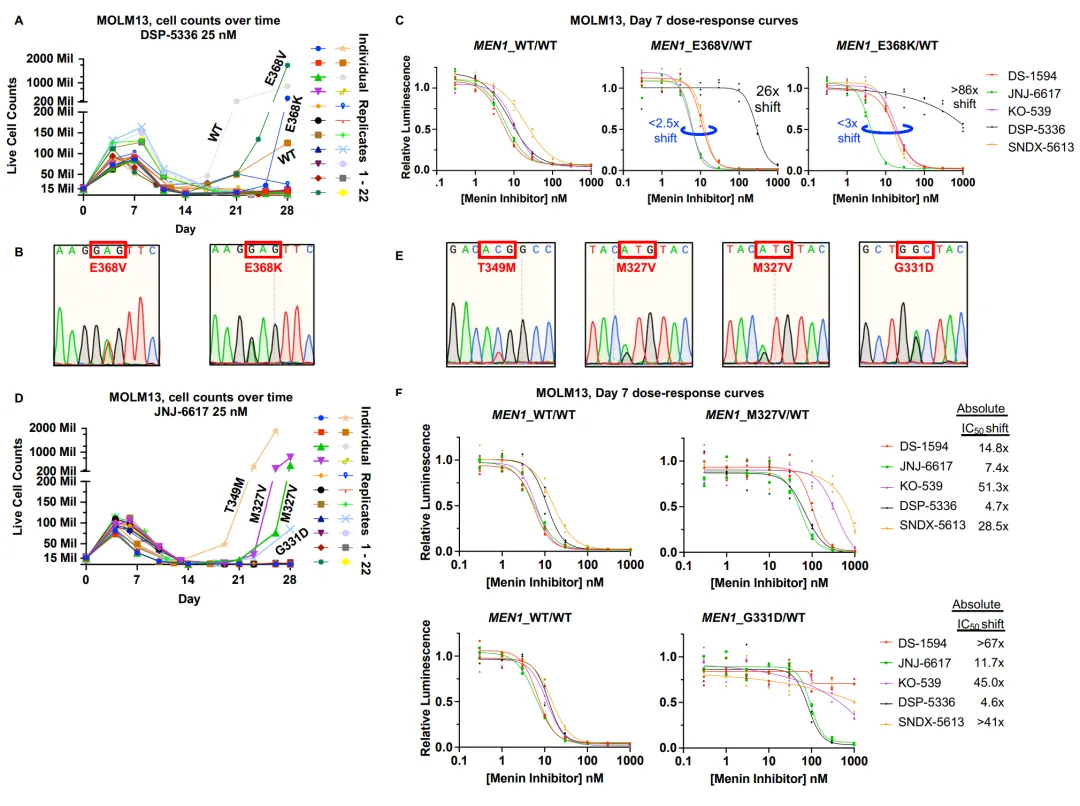
图5 体外新发MEN1突变生成验证筛选结果。
6. 体内PDX模型验证MEN1突变产生并揭示高剂量menin抑制剂可克服耐药。
在CBAM-44728 PDX模型中,SNDX-5613 0.1%饲料剂量下17/20只小鼠在170天内复发并检测到S160T、M327I/V/T、G331R/D和T349M突变;0.3%饲料剂量下仅3/13只小鼠出现MEN1突变,10只小鼠在170天后死亡但未检测到MEN1突变(图6A-C)。JNJ-6617 30 mg/kg/天下4/4只小鼠均出现MEN1突变,而100 mg/kg/天下仅1/4只出现突变(图6B-C)。CPCT-0024 PDX模型中,VTP-50469治疗可清除T349M突变,但M327I成为主导突变;再次移植后含M327I突变的肿瘤对0.033%和0.1% SNDX-5613饲料耐药,但对0.3%饲料可获得治愈(图6D-E)。
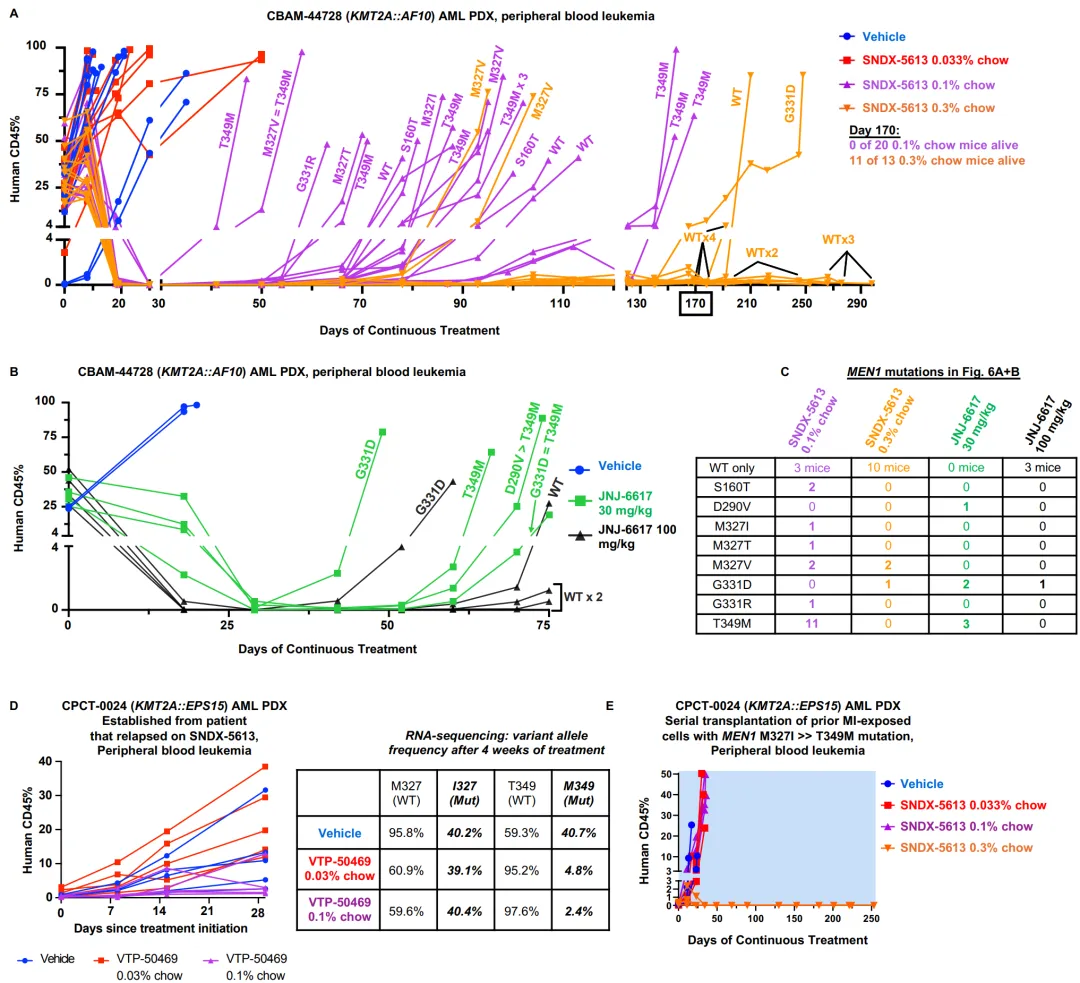
图6 体内新发MEN1突变生成验证筛选结果。
综上所述,该研究利用CRISPR碱基编辑器筛选技术系统绘制了五种临床menin抑制剂的MEN1突变耐药图谱,揭示了共享和药物特异性耐药机制,为临床menin抑制剂耐药监测和序贯治疗提供了依据。然而,碱基编辑器筛选存在固有技术限制,例如G331D在临床上已被发现在SNDX-5613患者中出现,但该筛选主要产生G331N而非G331D;不同MEN1突变之间的比较受到旁观者突变、编辑效率及等位基因突变比例的干扰;仅部分sgRNA达到统计显著性(仅1个通过MAGeCK FDR<0.05),凸显了筛选后进行单引导验证的必要性;尽管提出了基于MEN1突变谱切换menin抑制剂的治疗策略,但低等位基因频率的MEN1突变可能使该策略复杂化,成功治疗较不致命的MEN1突变细胞时,更致命的低丰度突变可能被富集。
参考来源:
Bourgeois, W., Rice, H.E., Wenge, D.V. et al. CRISPR base editor screening identifies spectrum of MEN1 mutations impacting menin inhibitors in clinical trials. Nat Commun (2026). https://doi.org/10.1038/s41467-026-72685-1
免责声明:本文旨在传递基因编辑与治疗最新讯息,不代表平台立场,不构成任何投资意见和建议,以官方/公司公告为准。本文也不是治疗方案推荐,如需获得治疗方案指导,请前往正规医院就诊
 夜雨聆风
夜雨聆风




