STM | 刘如谦团队利用腺嘌呤碱基编辑器直接纠正Dravet综合征小鼠模型Scn1a无义突变,恢复抑制性神经元功能并显著改善癫痫表型和早亡
Dravet综合征(DS)是一种由SCN1A功能丧失变异导致的严重神经发育疾病,表现为耐药性癫痫、发热诱导发作及高猝死率,目前尚无针对病因的治疗。2026年5月13日,博德研究所刘如谦团队联合费城儿童医院Ethan M. Goldberg及杰克逊实验室Cathleen M. Lutz在Science Translational Medicine上发表“In vivo adenine base editing ameliorates Dravet syndrome phenotypes in a mouse model”研究论文。该研究针对DS患者中复发的SCN1AR613X无义突变,筛选优化了腺嘌呤碱基编辑器(ABE),通过双AAV9递送系统在新生及P12 Scn1aR613X/+小鼠中实现高效DNA和RNA纠正(新皮质中分别达59%和97%),恢复小清蛋白阳性抑制性神经元兴奋性和钠电流至野生型水平,消除体温诱导及自发癫痫,并将45天存活率从27%提升至90%。

主要研究结果
1,体外筛选优化ABE策略高效纠正SCN1AR613X。
在工程化SCN1AR613X纯合HEK293T和Neuro-2a细胞中,测试多种ABE变体及Cas9变体(SpCas9、VRQR、NG)的组合。ABE8e-VRQR和ABE8e-NG分别实现72%和92%的A>G纠正效率(图1a-b)。进一步优化sgRNA设计和脱氨酶变体,ABE8e-V106W-VRQR在保持高编辑效率的同时显著降低旁观者突变(图1c-f)。CIRCLE-seq全基因组脱靶分析显示,ABE8e-V106W-VRQR在人细胞中仅检测到极少数潜在脱靶位点,且多数位于中枢神经系统不表达的非编码区(图1g-i)。
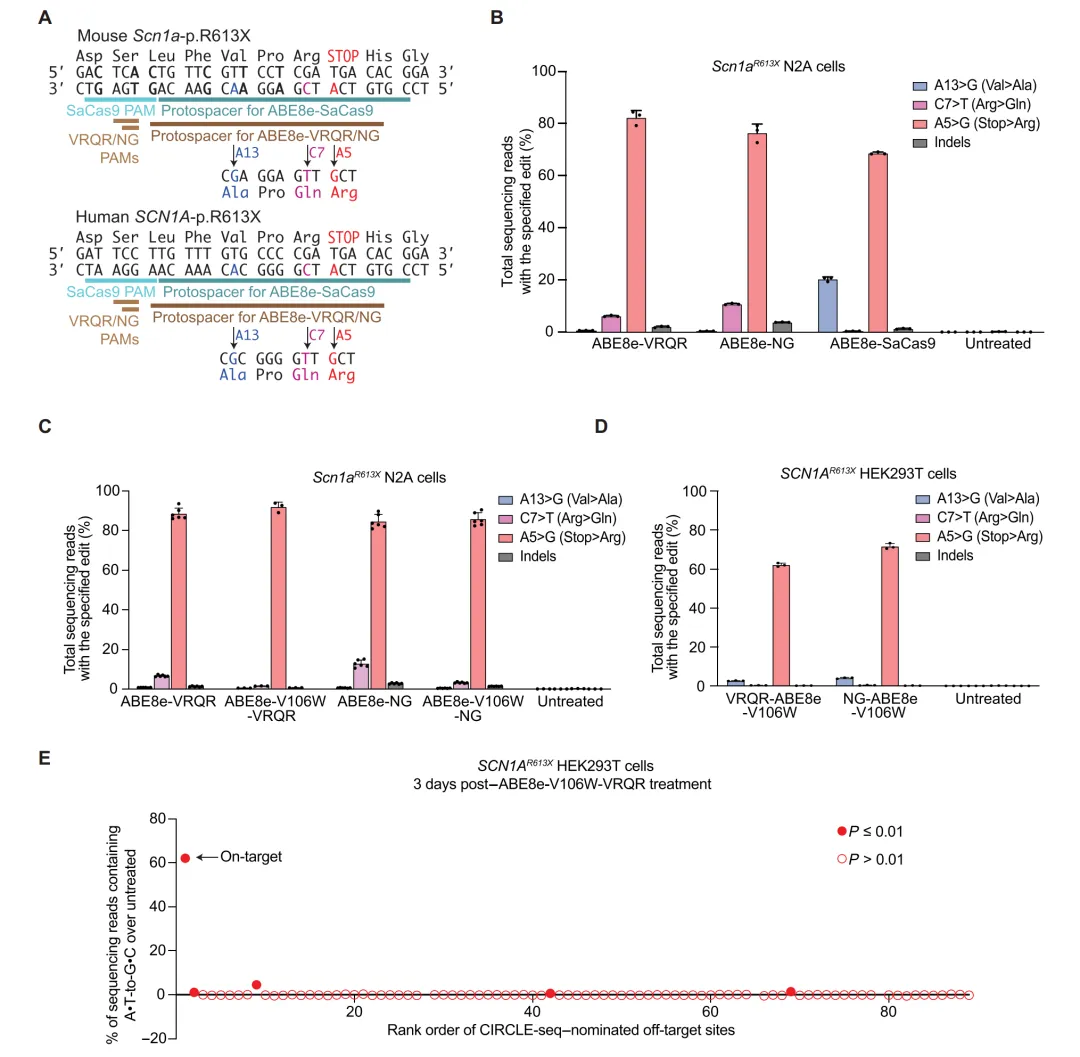
图1 体外筛选高效且特异的ABE策略纠正SCN1AR613X。
2,双AAV9递送ABE在Scn1aR613X/+小鼠脑中实现高效体内编辑。
采用双AAV9载体(Npu DnaE内含肽分割系统)将ABE与Cbh启动子驱动的编辑器以及U6启动子驱动的sgRNA共同递送至新生(P1)小鼠脑室内(图2a)。P21时,ABE8e-VRQR处理组新皮质细胞核基因组中63%的reads包含正常R613密码子,对应致病等位基因纠正率为26%,mRNA水平纠正率达82%(图2b)。ABE8e-V106W-VRQR处理至P45,新皮质和海马体细胞核基因组纠正率分别为59%和52%,而低转导的小脑仅4%(图2c)。cDNA分析显示新皮质和海马体转录本纠正率高达97%和93%,平均indel低于1%(图2d)。ABE处理使Scn1a mRNA水平恢复至野生型的1.8倍(图2e),NaV1.1蛋白表达也恢复至野生型水平(图2f)。
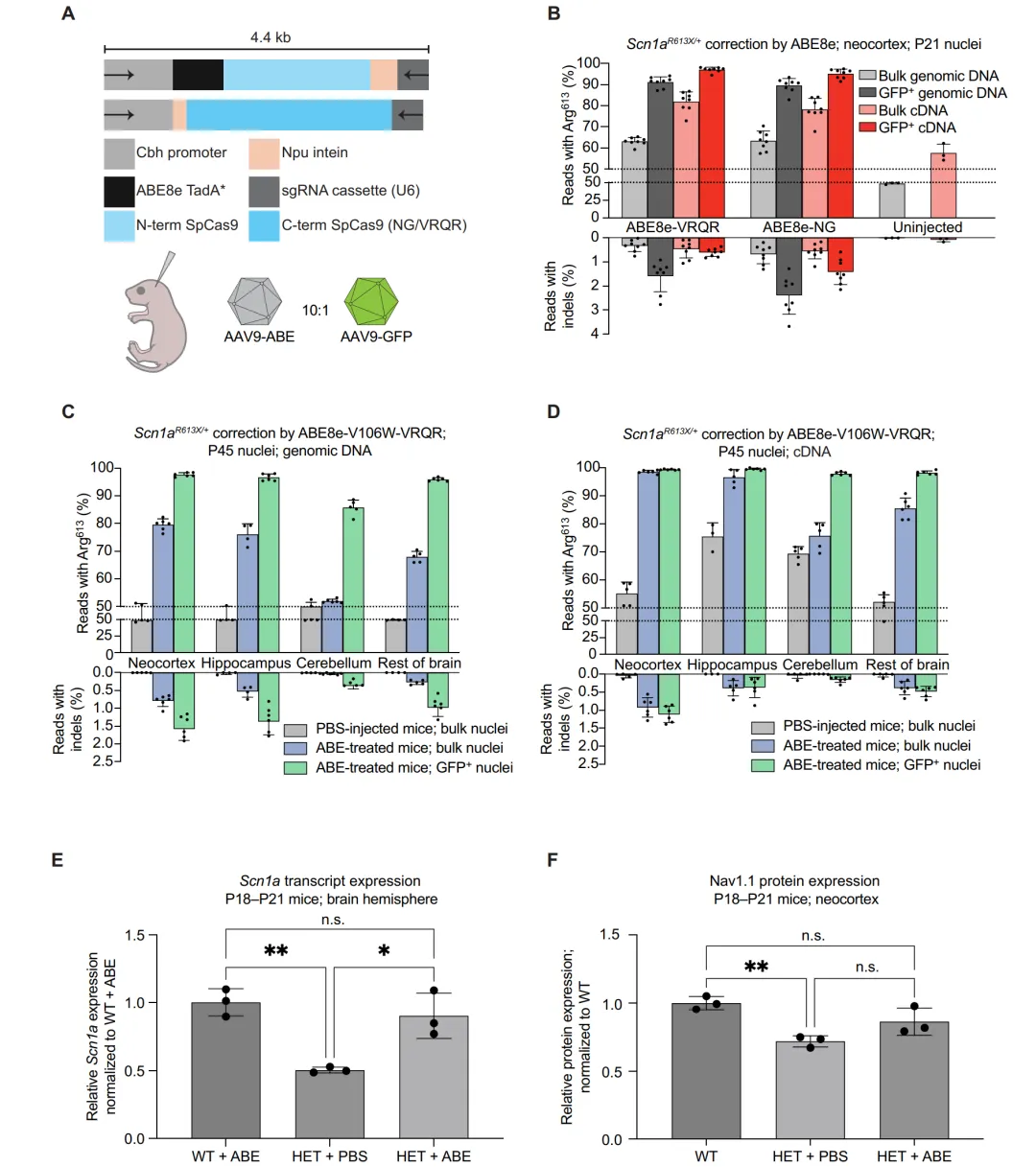
图2 双AAV9递送ABE在Scn1aR613X/+小鼠体内实现高效基因组和转录本纠正。
3,ABE恢复Dravet综合征小鼠抑制性神经元电生理功能。
对P18-P21脑片中小清蛋白阳性抑制性神经元(PVIN)进行全细胞膜片钳记录(图3a-b)。未编辑的Scn1aR613X/+小鼠PVIN兴奋性显著降低,而ABE编辑后的PVIN最大稳态放电频率和最大瞬时放电频率分别恢复1.3倍(图3c-g)。输入阻抗从86±27 MΩ(未编辑)降至72±20 MΩ(编辑),与野生型73±26 MΩ相当(图3h)。最大上升斜率从249±48 mV/ms(未编辑)恢复至306±50 mV/ms(编辑)(图3i),动作电位半宽从0.46±0.11 ms缩窄至0.36±0.04 ms(图3j)。核团巨片钳记录显示,未编辑PVIN钠电流峰值显著低于野生型(-111±43 pA vs -148±82 pA),编辑后恢复至-153±66 pA(图3k-m),激活和失活的电压依赖性无显著变化(图3n)。
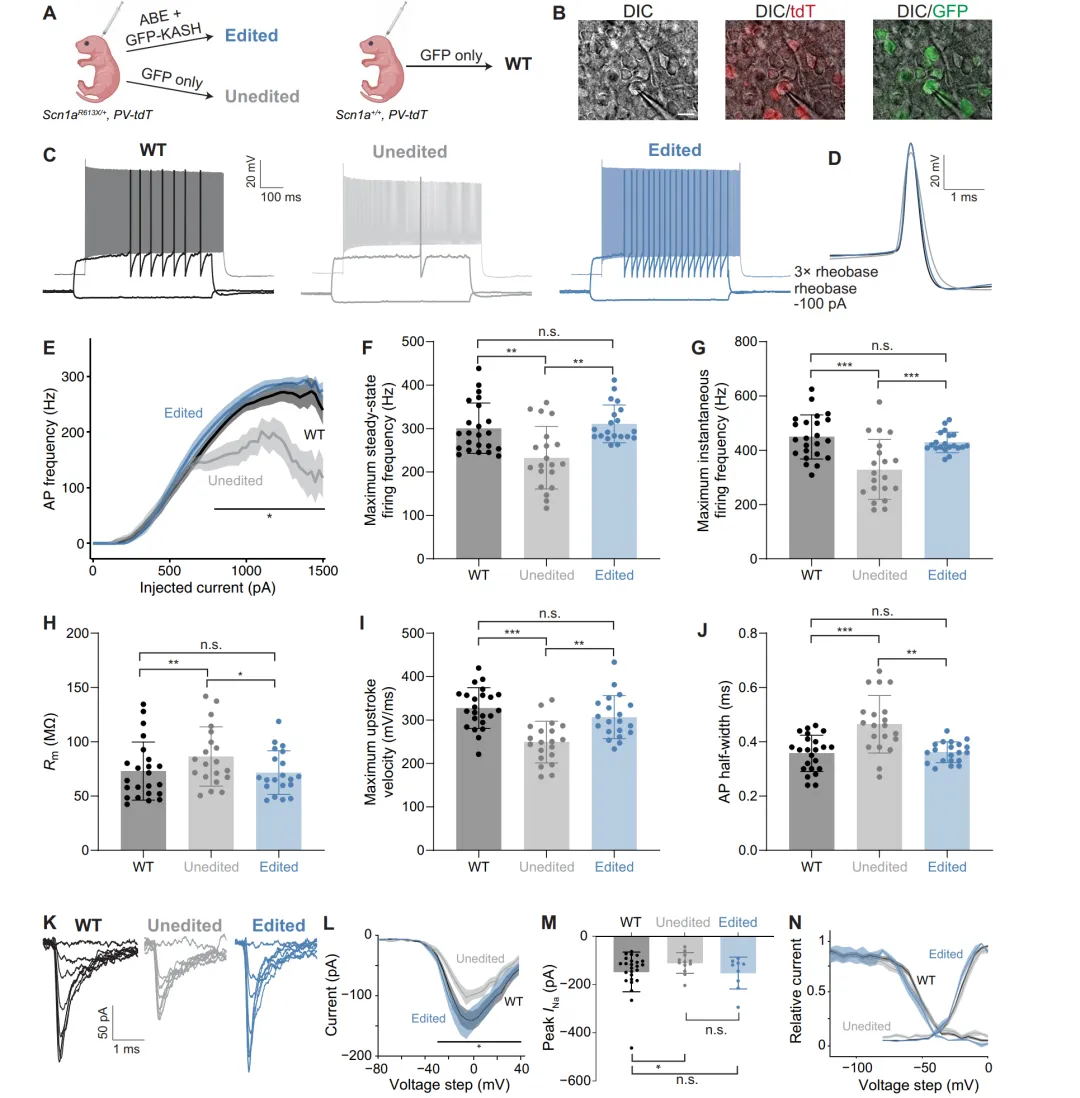
图3 ABE恢复Scn1aR613X/+小鼠PVIN的兴奋性和钠电流。
4,ABE治疗显著改善体温诱导癫痫、自发癫痫和早亡。
P18-P21小鼠体温诱导发作实验中,未编辑组在40±1.4°C时出现癫痫,而所有ABE治疗组小鼠在升至42.5°C时均无癫痫发作(图4b)。P22 24小时视频监测显示,50%雄性和60%雌性未编辑小鼠发生自发癫痫,而ABE治疗组无一发作(图4c)。在45天生存期观察中,未编辑雄性死亡60%(9/15)、雌性死亡87%(13/15),ABE治疗组雄性仅死亡13%(2/15)、雌性仅7%(1/15),七倍降低SUDEP风险(图4d)。在P12(相当于人类3-12月龄)进行ICV注射,至P60时ABE治疗组雌性存活率90%(9/10)、雄性71%(5/7),而对照组雌性0%、雄性50%(图4e)。P22-P26视频监测中,P12治疗小鼠无自发癫痫。
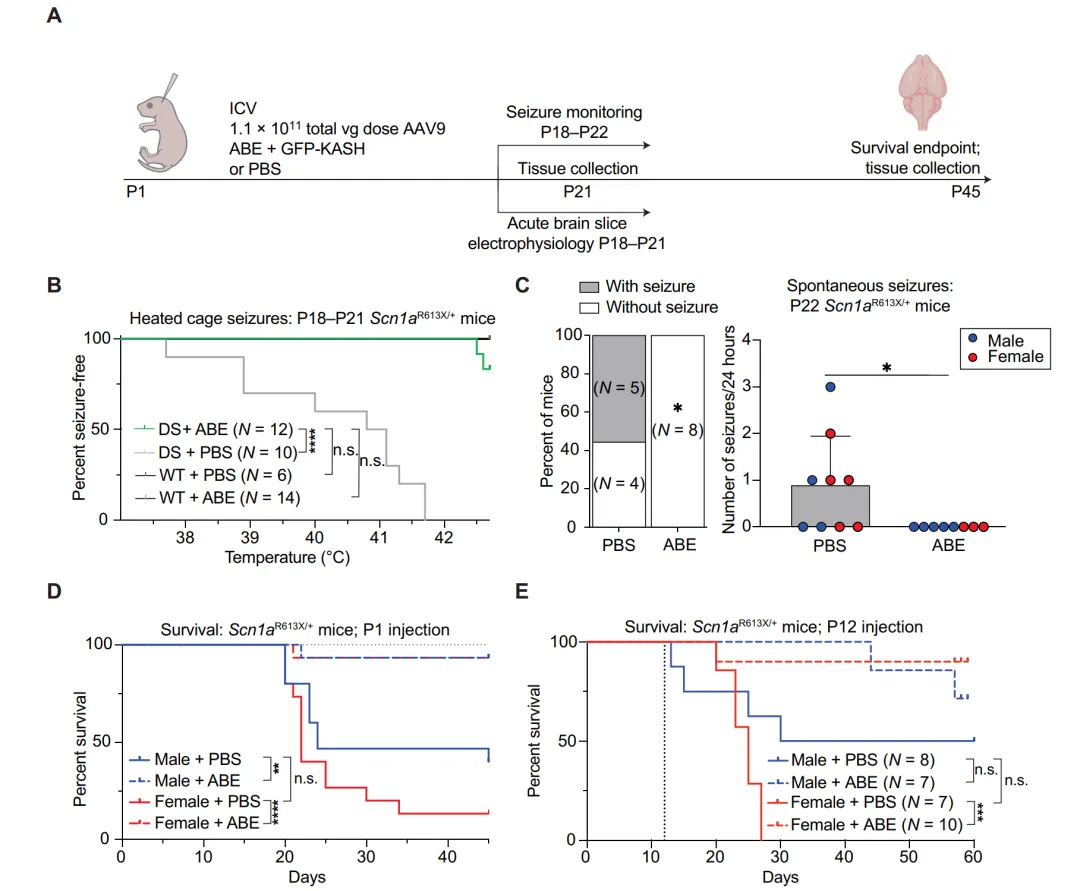
图4 ABE治疗消除体温诱导癫痫、自发癫痫并拯救早亡。
综上所述,本研究首次证明腺嘌呤碱基编辑器可永久纠正Dravet综合征小鼠模型的致病突变,恢复抑制性神经元功能并显著改善癫痫和生存表型,为DS及其他SCN1A相关神经发育疾病提供了潜在的“一劳永逸”基因治疗策略。然而,该研究主要针对R613X这一特定无义突变,而DS患者中SCN1A变异类型多样(错义、移码等),需要针对不同变异分别优化编辑策略;AAV9介导的递送虽高效但存在长期表达和潜在免疫原性问题,且治疗窗口期(P1和P12)在人类中的对应时机尚需谨慎评估;此外,虽然体温诱导癫痫完全消除,但非癫痫行为表型(如多动)是否同样获救尚未明确,长期编辑安全性和脱靶效应仍需更大样本和更长随访验证。
参考来源:
Nelson AT, Hill SF, Simon M, et al. In vivo adenine base editing ameliorates Dravet syndrome phenotypes in a mouse model. Sci Transl Med. 2026;18(849):eadx5999. doi:10.1126/scitranslmed.adx5999
免责声明:本文旨在传递基因编辑与治疗最新讯息,不代表平台立场,不构成任何投资意见和建议,以官方/公司公告为准。本文也不是治疗方案推荐,如需获得治疗方案指导,请前往正规医院就诊
 夜雨聆风
夜雨聆风




