
WLS作为关键的Wnt转运体是癌症治疗的潜在新靶点
Wnt信号通路在胚胎发育和成体稳态中发挥关键作用,其失调与多种癌症密切相关。靶向该通路的策略包括抑制Wnt酰基转移酶PORCN等。然而,作为Wnt蛋白专属转运体的Wntless (WLS/Evi),对于Wnt的分泌至关重要,却因缺乏抑制剂而长期处于“未成药”状态。近期解析的WLS与WNT8A复合物结构显示,其跨膜区存在一个类似GPCR的潜在可成药口袋。基于此,Weijun Xu团队旨在通过超大规模虚拟筛选,寻找首个靶向WLS的小分子抑制剂。
【虚拟筛选靶向膜蛋白】基于结构的跨膜靶点抑制剂发现课题设计
扫码免费获取1V1定制方案设计

一、Highlights
• • 通过超大规模虚拟筛选,首次发现了靶向Wnt转运蛋白Wntless(WLS)的小分子抑制剂ETC-451。
• • 研究证实WLS的跨膜结构域存在类似GPCR的可成药口袋,为靶向该蛋白提供了结构基础。
• • ETC-451能有效阻断WLS与WNT3A的相互作用,并抑制Wnt成瘾性胰腺癌细胞系的增殖。
• • 该研究为针对WLS这一此前“不可成药”靶点的药物发现提供了首个先导化合物骨架。
二、研究方案与思路
(1)靶点结构与口袋分析:基于WLS-WNT8A复合物的冷冻电镜结构,利用Sitemap等工具识别并确认其跨膜区存在一个类似GPCR的可成药口袋。
(2)超大规模虚拟筛选:采用Active Learning/Glide方法,对Enamine REAL 350/3库中近5亿个化合物进行虚拟筛选,通过聚类、多样性选择和膜渗透性过滤,最终选定86个化合物进行定制合成。
(3)细胞水平功能验证:对成功合成的68个化合物进行基于细胞的Wnt报告基因检测等初筛,鉴定出先导化合物ETC-451,并进一步验证其阻断WLS-WNT相互作用、下调靶基因表达及抑制癌细胞增殖的功能。
WLS在Wnt通路中占据上游枢纽位置
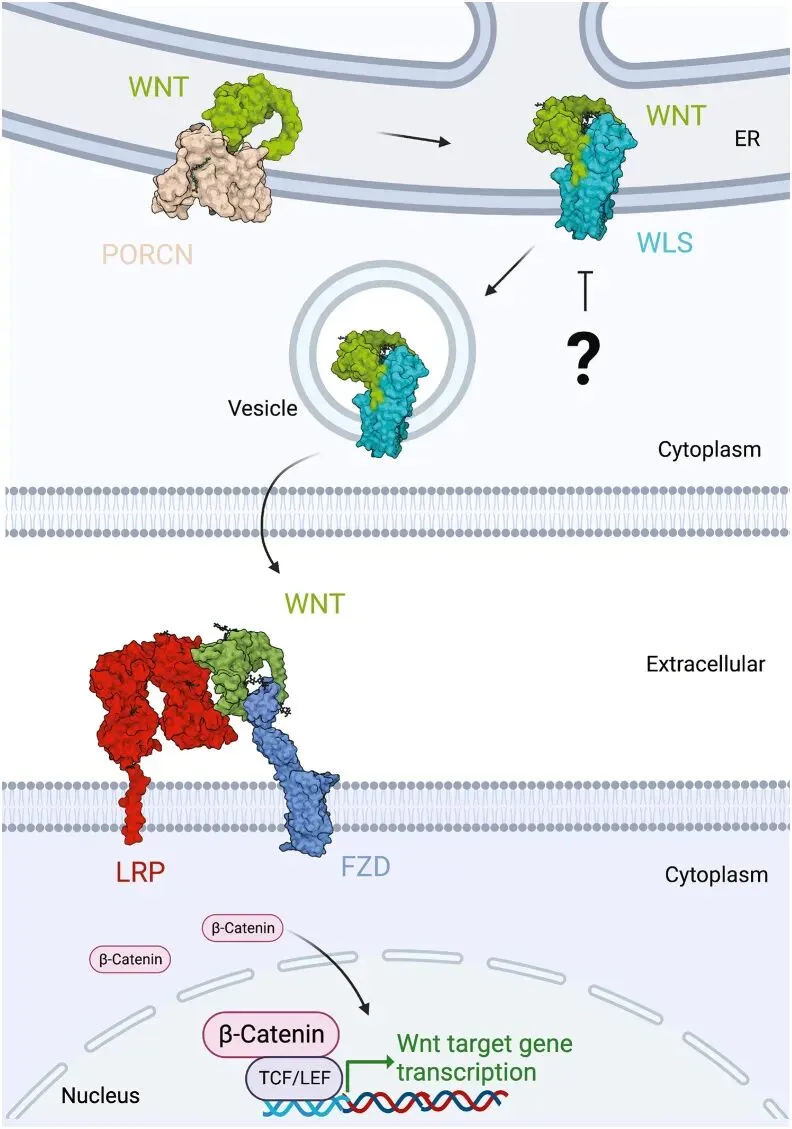
在经典的Wnt/β-catenin信号通路中,Wnt蛋白的分泌是启动下游级联反应的关键第一步。Weijun Xu团队的研究示意图清晰地展示了这一过程。在Wnt产生细胞内,新合成的Wnt蛋白首先需要在内质网中由酰基转移酶PORCN进行棕榈油酰化修饰,这一脂质修饰对于Wnt的后续功能至关重要。随后,经过修饰的Wnt蛋白被其专属转运蛋白Wntless (WLS/Evi) 识别并装载。WLS负责将Wnt从高尔基体转运至细胞膜,并最终将其分泌到细胞外空间。在信号接收细胞一侧,分泌出来的Wnt配体与细胞膜上的Frizzled (FZD) 受体和LRP5/6共受体结合,形成复合物。这一结合事件会抑制细胞内β-catenin的降解复合体,导致β-catenin在细胞质中稳定积累并进入细胞核,进而与TCF/LEF等转录因子结合,启动一系列调控细胞增殖与分化的靶基因表达。由此可见,WLS在通路中扮演着承上启下的枢纽角色,它直接控制着功能性Wnt配体的有效释放。因此,靶向WLS、从源头阻断Wnt的分泌,为干预异常活跃的Wnt信号提供了一种极具潜力的上游策略。
结构分析揭示WLS跨膜域存在可成药口袋
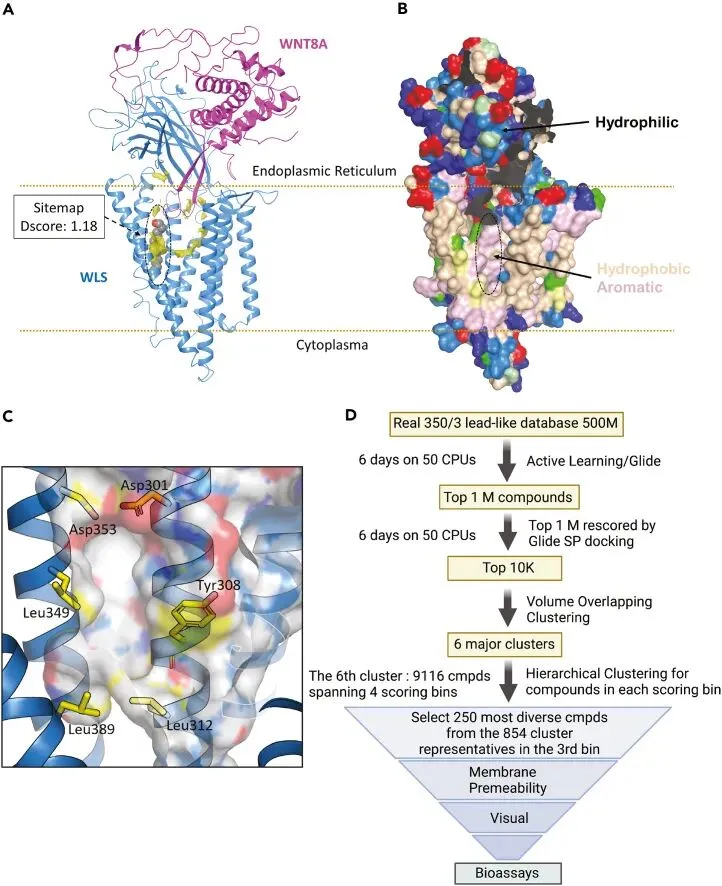
基于解析的WLS-WNT8A复合物冷冻电镜结构,Weijun Xu团队首先利用结合位点检测工具Sitemap对WLS蛋白进行了分析。他们发现,在WLS的七个跨膜螺旋束内部,存在一个与G蛋白偶联受体(GPCR)经典药物结合位点类似的区域,该区域被识别为最具成药潜力的口袋,即Site 1。该口袋的上部由部分极性氨基酸残基构成,而下部主要由疏水性残基构成,形成了一个适合小分子结合的化学环境。
为了从这个口袋中寻找潜在抑制剂,Weijun Xu团队启动了一项超大规模虚拟筛选。他们采用了主动学习与Glide对接相结合的计算策略,对Enamine公司的REAL 350/3 Lead-Like化合物库进行筛选,该库包含了近5亿个符合特定理化性质(分子量270-350,脂水分配系数SlogP≤3等)的类先导化合物。整个筛选流程首先通过随机选取5万个化合物进行Glide SP对接,并利用其得分训练一个深度学习模型,用以预测整个库中化合物的潜在活性。经过多轮主动学习迭代后,模型预测出的前100万个化合物被重新进行Glide SP对接和精确打分。
在后续的命中化合物选择中,Weijun Xu团队依据对接得分聚焦于排名前1万的化合物。他们应用了体积重叠聚类方法,将结合模式相似的化合物归类,并重点考察了其中最大的一个聚类。结合膜渗透性预测进行过滤,并通过视觉检查评估化合物与口袋的拟合度,最终从海量虚拟分子中精选出86个结构多样的化合物,委托Enamine公司进行定制合成,用于后续的实验验证。
化合物ETC-451有效抑制Wnt/β-catenin报告基因活性与WNT3A分泌
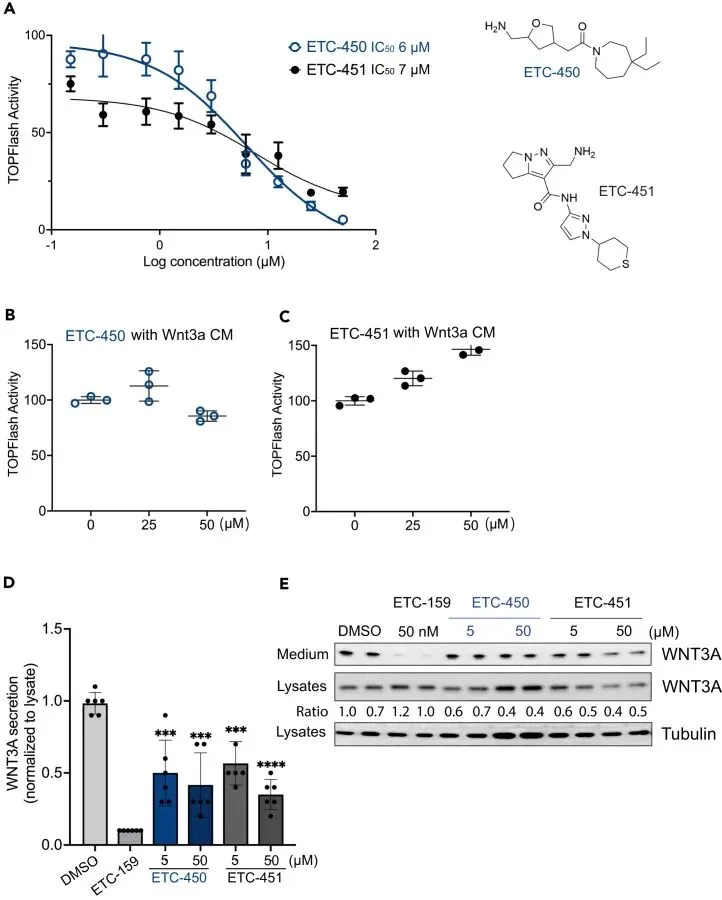
Weijun Xu团队首先对成功合成的68个化合物进行了初步功能筛选。他们使用了稳定表达WNT3A并整合了β-catenin响应性SuperTOPFlash(STF)荧光素酶报告基因的STF3A细胞系。在该细胞中,化合物处理48小时后,通过检测荧光素酶活性来评估其对Wnt/β-catenin信号通路的抑制效果。筛选结果显示,两个化合物ETC-450和ETC-451能够显著抑制STF3A细胞的内源性报告基因活性。进一步的剂量反应实验证实,ETC-450和ETC-451均以剂量依赖的方式发挥作用,其半数抑制浓度(IC50)分别为6.3 μM和7.7 μM。为了验证抑制作用的特异性,Weijun Xu团队在另一组实验中,用WNT3A条件培养基刺激不表达内源性WNT3A的STF报告细胞,发现ETC-450和ETC-451在此条件下均不能有效抑制报告基因活性,这初步提示它们的作用靶点可能位于Wnt配体的产生或分泌环节,而非下游信号接收过程。
随后,Weijun Xu团队直接检测了化合物对Wnt蛋白分泌的影响。他们收集了经ETC-450或ETC-451处理的STF3A细胞的培养上清,并通过免疫印迹分析其中分泌型WNT3A蛋白的水平。实验发现,与阳性对照PORCN抑制剂ETC-159的效果类似,ETC-451处理能剂量依赖性地显著降低培养上清中的WNT3A蛋白含量。与此同时,细胞裂解物中的WNT3A前体蛋白水平并未受到明显影响。这一结果表明ETC-451很可能通过干扰Wnt蛋白的分泌过程来发挥抑制作用,为其作为WLS抑制剂的假说提供了关键的功能性证据。
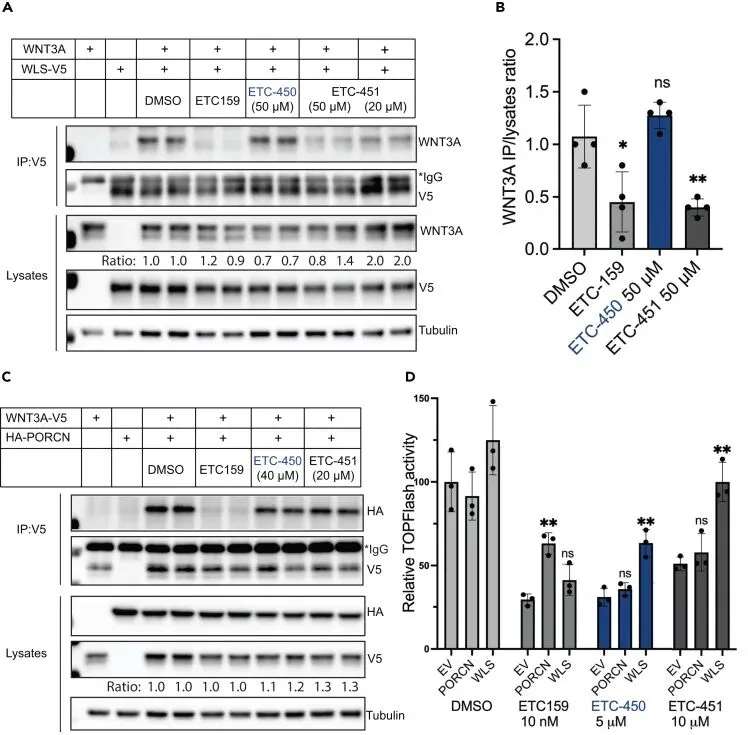
ETC-451通过阻断WNT3A与WLS的相互作用发挥作用
为了阐明ETC-451的作用机制,Weijun Xu团队设计并进行了免疫共沉淀实验。他们在STF细胞中共同表达了WNT3A和带有V5标签的WLS蛋白,随后用不同化合物处理细胞。实验结果显示,与DMSO对照组相比,处理了ETC-451的细胞中,WNT3A与WLS-V5之间的结合被显著削弱。这一结果直接证明,ETC-451能够特异性地干扰WLS与其转运底物WNT3A的相互作用。作为对照,PORCN抑制剂ETC-159则完全阻断了WNT3A与WLS的结合,而化合物ETC-450并未表现出类似的阻断效果。为了进一步确认靶点特异性,Weijun Xu团队还检测了化合物对WNT3A与PORCN结合的影响,发现ETC-451并不干扰这一过程,从而排除了其作为PORCN抑制剂的可能性。这些数据共同表明,ETC-451是通过直接阻断WNT3A与WLS的结合来发挥作用的,这为其作为WLS抑制剂的机制提供了关键证据。
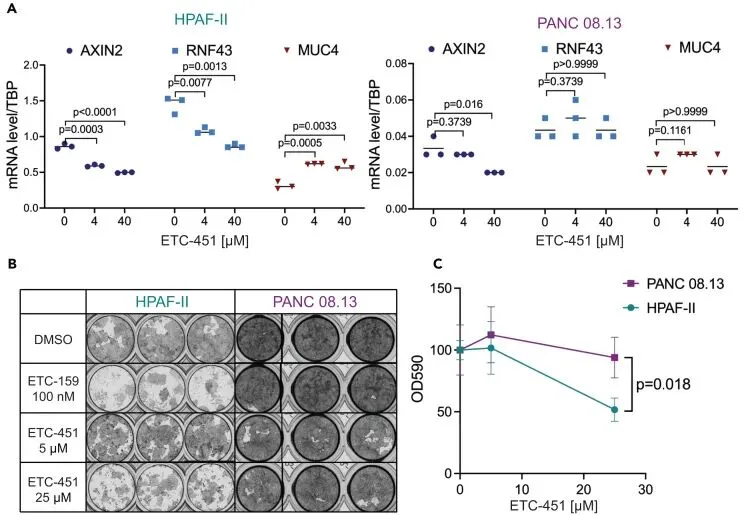
ETC-451选择性抑制Wnt依赖的胰腺癌细胞增殖与基因表达
为了验证ETC-451在更复杂的疾病模型中的特异性和疗效,Weijun Xu团队选择了两种胰腺癌细胞系进行对比研究。他们使用了Wnt信号成瘾的HPAF-II细胞系和Wnt非依赖的PANC 08.13细胞系。首先,团队通过RT-qPCR检测了Wnt通路靶基因的表达变化。结果显示,在HPAF-II细胞中,ETC-451能以剂量依赖的方式显著下调经典Wnt靶基因AXIN2和RNF43的转录水平,同时上调分化标志物MUC4的表达。然而,在PANC 08.13细胞中,相同剂量的ETC-451对这些基因的表达几乎没有影响。这一结果初步表明ETC-451对Wnt通路活性的抑制具有细胞类型选择性。随后,Weijun Xu团队进行了低密度克隆形成实验以评估化合物的长期抗增殖效果。他们发现,ETC-451能够剂量依赖性地抑制HPAF-II细胞的集落形成能力,其效果与阳性对照PORCN抑制剂ETC-159相当。与此形成鲜明对比的是,ETC-451对PANC 08.13细胞的集落生长则没有明显的抑制作用。这些数据共同表明,ETC-451的抗增殖作用严格依赖于细胞对Wnt通路的成瘾性,进一步证实了其作为WLS抑制剂的功能特异性,并提示其在治疗Wnt驱动型癌症中的潜在应用价值。
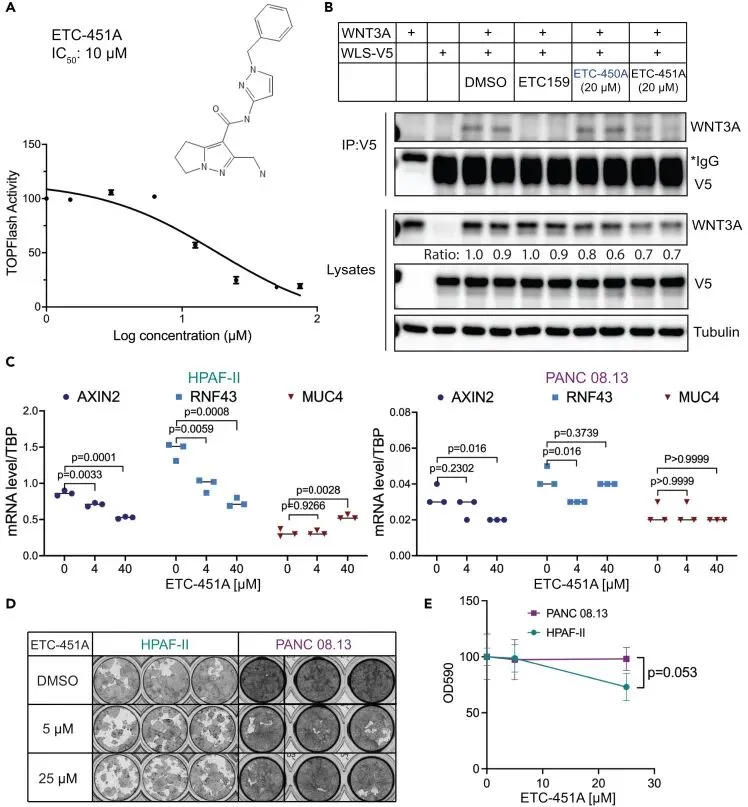
初步构效关系研究为化合物优化提供方向
为了探索ETC-451和ETC-450的化学结构与其抑制活性之间的关系,Weijun Xu团队对这两个先导化合物进行了初步的构效关系研究。他们合成了ETC-451的11个类似物,这些化合物共享相同的二氢吡咯并吡唑核心骨架,并在Wnt/β-catenin报告基因实验中测试了它们的活性。结果显示,分子结构上的细微改变会显著影响其抑制能力。例如,化合物ETC-451A保留了关键的2-氨基甲基基团,但将中央吡唑环上的取代基更换为苄基,其在报告基因实验中表现出的半数抑制浓度与母体化合物ETC-451相似。相反,另外四个缺少2-氨基甲基基团的类似物则完全丧失了抑制活性。这一发现直接表明,2-氨基甲基基团对于维持化合物与WLS的结合及抑制功能至关重要。此外,对ETC-450类似物ETC-450A的测试也显示其未能有效阻断WNT3A与WLS的相互作用。这些初步的构效关系数据清晰地指出,当前发现的ETC-451仅是一个起点,其分子骨架中特定官能团的作用为后续基于结构的药物设计和进一步的化学优化提供了明确且关键的线索。
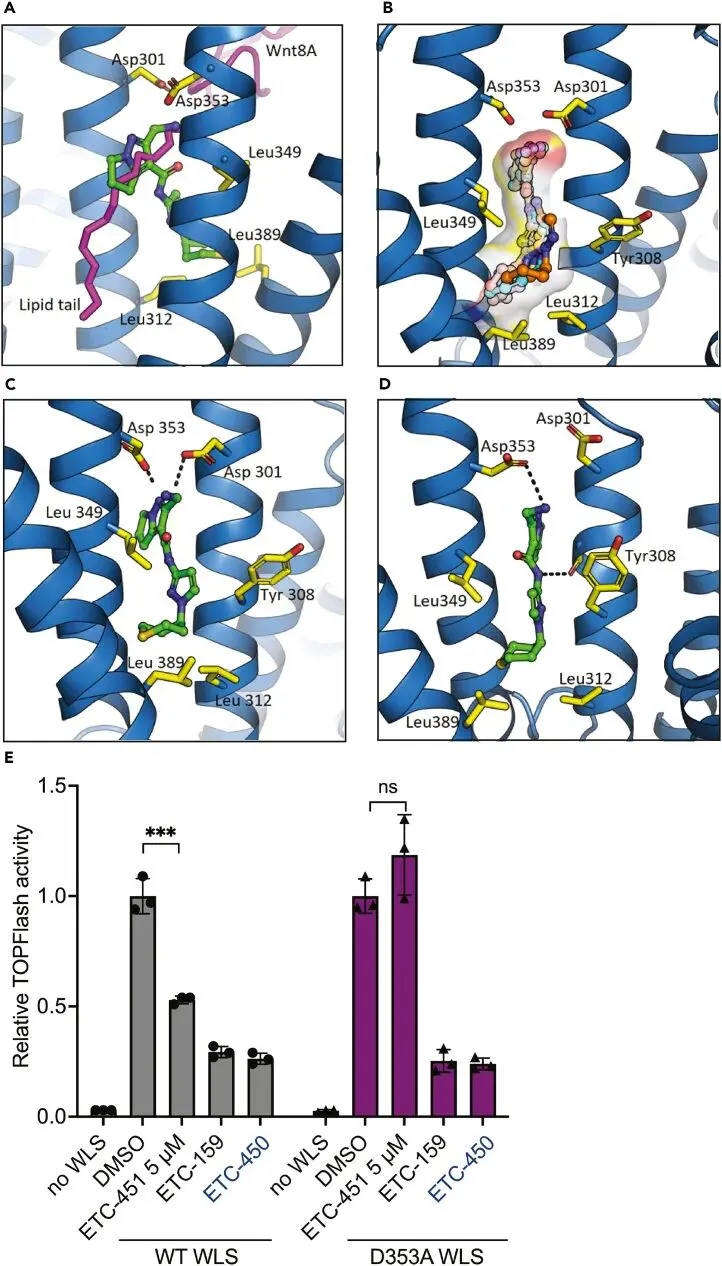
分子对接模型推测ETC-451结合于WLS的跨膜口袋
为了从结构层面理解ETC-451的作用机制,Weijun Xu团队进行了分子对接与动力学模拟分析。他们提出的结合模型显示,ETC-451(绿色棍棒模型)被预测结合在WLS跨膜结构域的可成药口袋中。该分子的空间位置与Wnt配体的棕榈油酸酯修饰尾部(紫色)相邻,部分重叠,这为ETC-451可能通过占据该口袋来竞争性抑制Wnt与WLS的结合提供了结构解释。进一步的分子动力学模拟和点突变功能实验支持了该模型中关键相互作用残基(如Asp353)的重要性。综上所述,这项研究首次通过超大规模虚拟筛选成功鉴定出靶向Wnt转运蛋白WLS的首个小分子抑制剂。ETC-451的发现为开发以Wnt分泌为靶点的新型抗癌疗法提供了首个有价值的化学骨架,具有重要的开创性意义。
【虚拟筛选靶向膜蛋白】基于结构的跨膜靶点抑制剂发现课题设计
扫码免费获取1V1定制方案设计


▍ 了 解 更 多
🌐 光热生物
https://www.grswsci.top/analyze/
🌐 官方网址
https://www.sogentech.com/
🛒订单管理
https://order.sogentech.com/
👆 长按复制网址,在浏览器中打开
关注 索臻矩阵号,获取更多科研干货

© Sogen 索臻科技
一站式科研服务平台
 夜雨聆风
夜雨聆风