本文为个人经验分享,仅供参考,不构成法规解读。
还在复制粘贴?产品综述可不是写说明书。
大家好,我是械语轻言。
产品综述是TCF的第一章,也是NB最先看的部分。
它虽不难,却是NB发补单上的“常客”。很多时候,欠补的不是技术,而是“表达”。
这篇就聊聊:产品综述到底要写什么?怎么让审评一眼看懂?
全文约1600字。
✅本文核心交付:
产品综述12条核心内容的逻辑归类
2个MDR 特色条款拆解
3个亲历的踩坑点+3个落地的写作习惯
✅产品综述写什么?
根据MDR 2017/745 附录II §1.1,产品综述需涵盖 (a) 至 (l) 共12项内容。
内容虽多,但仔细看,大部分都属于常规注册资料的范畴,并不需要从头写起。
我把它们按技术文档的逻辑归纳了一下:
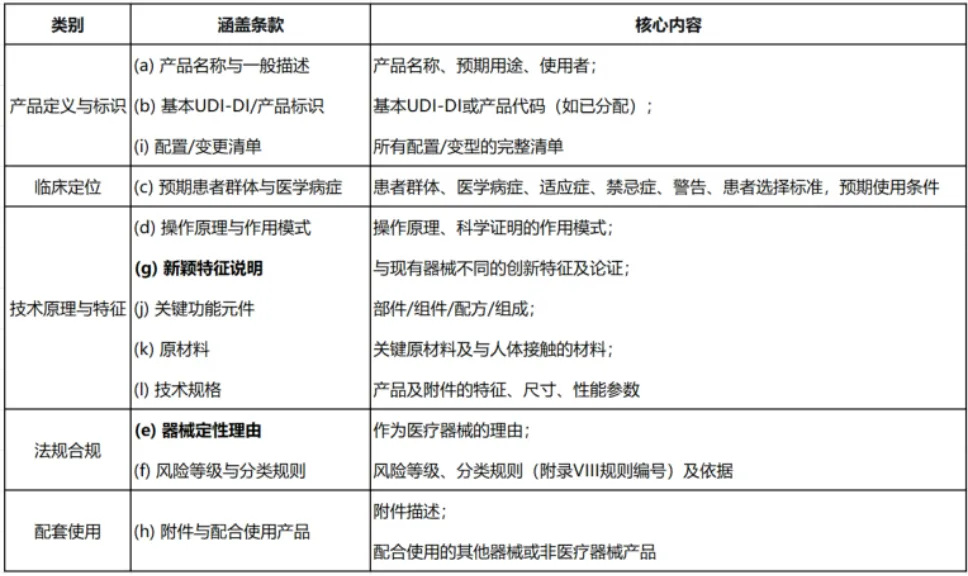
这12条里,(e)和(g)这两条比较有MDR特色,概念性强、但也容易让人理解跑偏。照搬模板可能走不通,得先理解概念后再判断。
下面我们重点展开说说。
✅2个MDR特色条款:身份认定 + 新颖特征
(e)the rationale for the qualification of the product as a device.
这条是产品的“身份证明”。
核心:解释为什么说它是医疗器械(或属于Annex XVI无预期医疗目的器械)。
实操上,应依据MDR Article 2逐条对照,看产品是否符合医疗器械的定义。若产品属于Annex XVI范畴,比如隐形眼镜,也要说明白。
⚠️注意“这里只是定性——判断“是”还是“否”。跟Annex VIII里的分类是两码事。
它可以看作是分类的前置项,先搞定身份认定,再说等级划分。
若存在边界争议(比如可能被误认为是其他产品),别等审核员来挑战,主动把分析过程写清楚,说明你为什么站在医疗器械这一边。
(g)an explanation of any novel features
这条是 § 1.1里比较有MDR特色的。
核心:产品有什么新东西,说清楚,并且拿证据出来。
具体怎么写,我总结了五步:
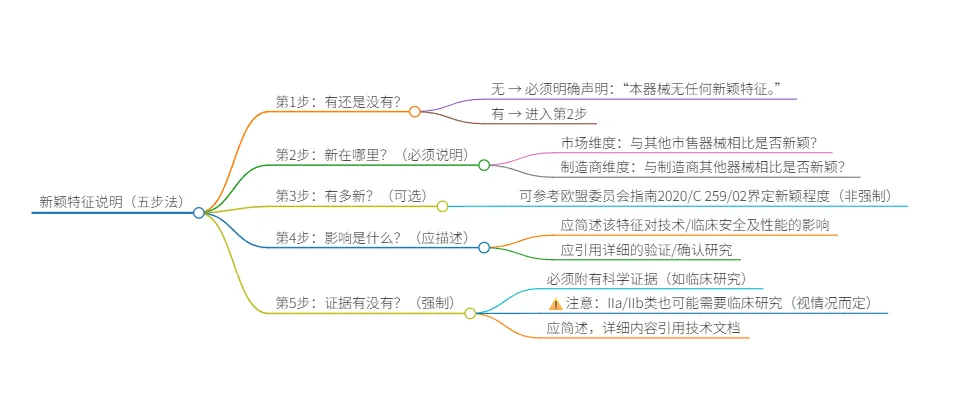
✅3个亲历的踩坑点
除了(e)和(g),下面说说我自己亲历的3个踩坑点:
坑1:预期用途与适应症 混淆
老生常谈,却也是高频雷区——预期用途≠ 适应症。
关于适应症的定义,目前看到最清晰的官方解释来自MDCG 2020-6。
根据定义,所有器械都有预期用途,但不是所有的器械都有适应症——比如以消毒或灭菌为目的的医疗器械。
坑2:组合产品,组件配套使用描述不清
组合产品中需要配套使用的组件(例如适配不同的使用频段/使用模式),写得笼统,审评看不清楚对应关系,自然就会发问。
坑3:工作原理写得太“研发”
写这部分容易陷入一个误区:把技术细节都倒出来——算法、电路、结构设计逻辑写一大堆,审评看完一脸懵。
事实是,审评没有你那么懂这个产品,Ta只需看明白:这个东西到底是靠什么原理起作用的?用通俗易懂的语言把核心逻辑讲清楚就行,而非技术细节的堆砌。
写得太“研发”,审评看不懂,发补就是大概率的事。
✅3个落地的写作习惯
坑讲完了,下面说说我的几个习惯。
1.“分清楚”再动笔
预期用途和适应症别糅在一起,分开写。
预期用途:参考Article 2(1) 医疗器械定义来表述—“用于……的诊断/治疗/监控”。
适应症:参考MDCG 2020-6 Sec 1.2 适应症定义来表述—“适用于……病症/人群”。
没有适应症,就写“无”。
2. “列清楚”配套关系
组合产品里需要配套使用的组件,推荐用表格列出对应关系,别只写一句“可配套使用”。
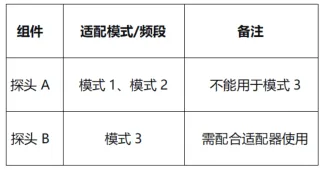
简洁明了,审核员一眼就懂。
不想画表,也至少用“分别对应”这类词把关系点明。
3.少堆术语,讲通逻辑
写工作原理时,不要堆砌技术细节,尤其是专业术语。转换思路,用审评员能看懂的语言写。写完代入审评视角——如果你是第一次看这个产品,能看懂吗?看不懂就重写。技术细节不在这里写,后面的“设计与制造”章节再聊。
✅最后说两句
写产品综述,我把自己当成一个讲故事的人,不是简单的“复制粘贴”,是把产品完整地展示到审评员面前,不求多么生动,能让Ta看懂就行——过关万岁。
如果你写MDR产品综述时,卡在身份认定或新颖特征,或有其他发补问题,欢迎后台私信交流。
👇顺便看看这几篇:
《一个CE产品的6次NB发补实录:从TCF递交到获证,我经历了什么》
PMCF 实操(续):为什么你的 PMCF 计划,总被 NB 发补?
ISO 14971:2019实施指南:医疗器械风险管理的核心要求与落地避坑
下期继续聊。
如果觉得有用,欢迎收藏、分享、关注。
——一个做了多年的医疗器械注册人
 夜雨聆风
夜雨聆风