文档内容
专练 12 钠及其化合物
1.[2022·广东卷]下列关于 Na 的化合物之间转化反应的离子方程式书写正确的是
( )
A.碱转化为酸式盐:OH-+2H++CO===HCO+2HO
2
B.碱转化为两种盐:2OH-+Cl===ClO-+Cl-+HO
2 2
C.过氧化物转化为碱:2O+2HO===4OH-+O↑
2 2
D.盐转化为另一种盐:NaSiO+2H+===H SiO↓+2Na+
2 3 2 3
答案:B
解析:A项题给离子方程式未配平且不是碱转化为酸式盐,A项错误;B项可视为向
NaOH溶液中通入Cl ,离子方程式正确;过氧化物溶于水的离子方程式中,过氧化物应用
2
化学式表示,C项错误;硅酸钠易溶于水,离子方程式中应用SiO表示,D项错误。
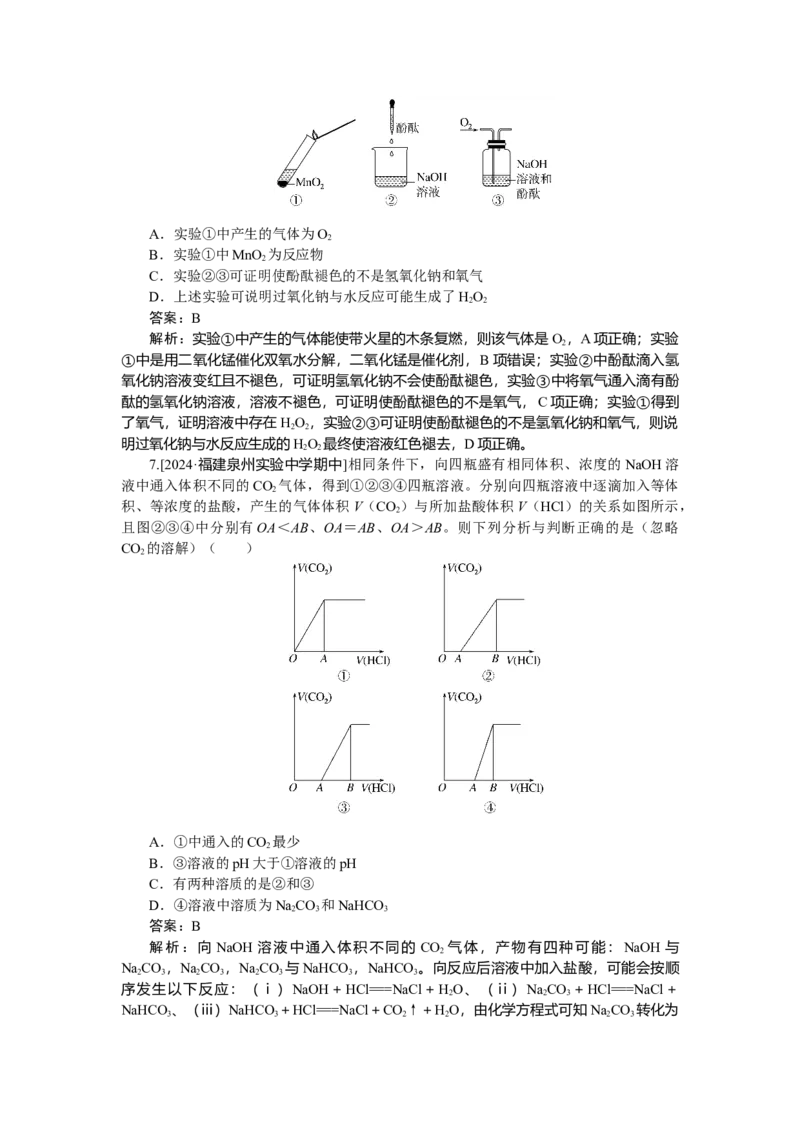
2.[2024·广东模拟]拟在实验室完成一系列实验:①粗盐提纯;②利用提纯后的NaCl模
拟“侯氏制碱法”制备纯碱;③用盐酸标准液滴定纯碱溶液以测定NaCO 含量。在实验过
2 3
程中,下列仪器不可能用到的是( )
答案:D
解析:粗盐提纯中过滤时要用到漏斗;侯氏制碱法中向饱和氨盐水中通入二氧化碳气
体得到NaHCO ;用盐酸标准液滴定纯碱溶液,盐酸盛放在酸式滴定管中,三个实验均没
3
有用到直形冷凝管,故选D。
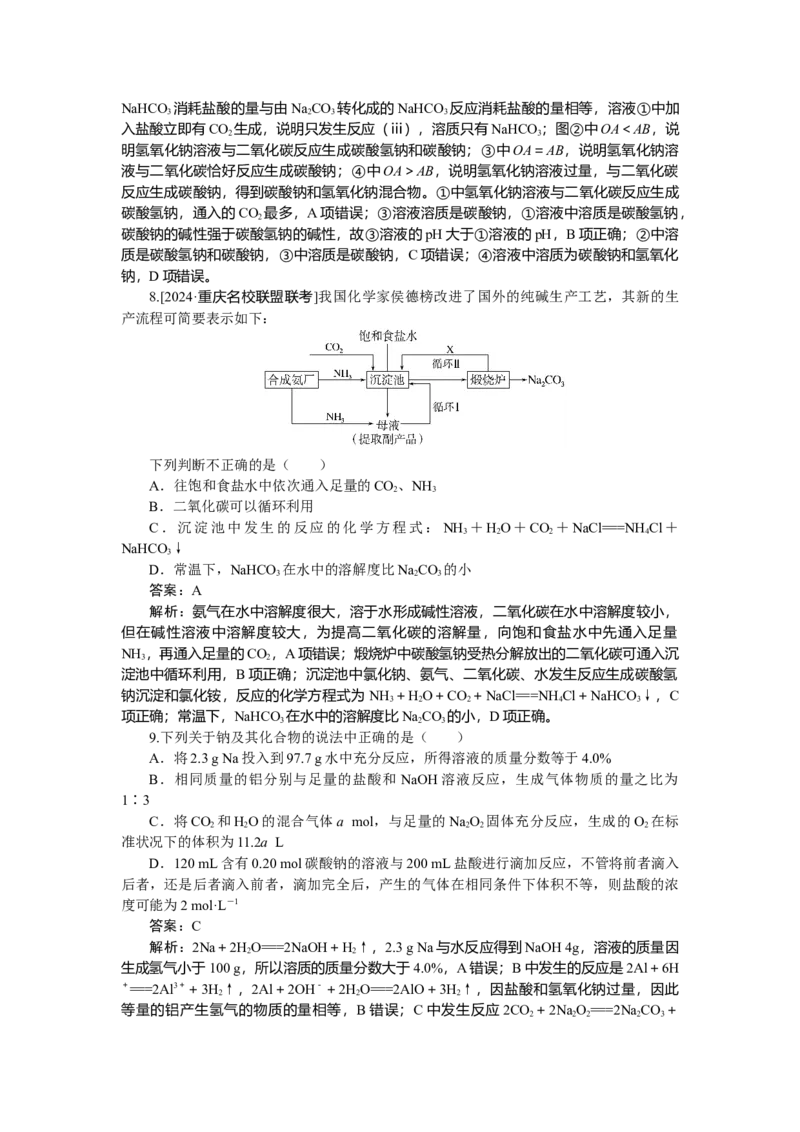
3.[2024·武邑中学高三月考]用如图所示实验装置进行相关实验探究,其中装置不合理
的是( )
A.图1鉴别纯碱与小苏打
B.图2证明NaO 与水反应放热
2 2
C.图3证明Cl 能与烧碱溶液反应
2
D.图4探究钠与Cl 反应
2
答案:A
解析:加热固体,为防止生成的水倒流,试管口应向下倾斜,A错误;观察到脱脂棉燃烧,可说明过氧化钠与水反应放出大量的热,B正确;氯气与NaOH反应,使锥形瓶内
压强减小,气球变大,C正确;钠与氯气加热生成氯化钠,碱液可吸收过量的氯气,D正
确。
4.[2024·北京朝阳期末]以不同类别物质间的转化为线索,认识钠及其化合物。
下列分析不正确的是( )
A.反应③表明CO 具有酸性氧化物的性质
2
B.反应④说明NaHCO 的热稳定性强于NaCO
3 2 3
C.反应⑤、⑥可用于潜水艇中氧气的供给
D.上述转化中发生的反应有分解反应、化合反应、置换反应
答案:B
解析:反应③是2NaOH+CO===Na CO +HO,NaOH为碱,NaCO 为盐,因此CO
2 2 3 2 2 3 2
具有酸性氧化物的性质,A项正确;反应④是2NaHCO =====NaCO+CO↑+HO,说明
3 2 3 2 2
NaCO 比NaHCO 热稳定性强,B项错误;反应⑤、⑥分别是2NaO +2HO===4NaOH+
2 3 3 2 2 2
O↑、2NaO +2CO===2Na CO +O ,因此反应⑤、⑥可用于潜水艇中氧气的供给,C项
2 2 2 2 2 3 2
正确;反应④为分解反应,反应①为化合反应,反应②为置换反应,D项正确。
5.有关NaHCO 和NaCO 的性质,下列叙述中不正确的是( )
3 2 3
A.NaCO 和NaHCO 粉末与同浓度的盐酸反应,NaCO 溶液的碱性强,反应放出气
2 3 3 2 3
体速率快
B.等物质的量的两种盐与足量相同浓度的盐酸反应,NaCO 消耗盐酸的体积是
2 3
NaHCO 的2倍
3
C.向饱和NaCO 溶液中通入过量CO,有NaHCO 晶体析出
2 3 2 3
D.NaCO 和NaHCO 溶液中分别加入BaCl 溶液,产生的现象不同
2 3 3 2
答案:A
解析:与同浓度盐酸反应时,NaHCO 放出气体的速率比NaCO 要快,A错误;1 mol
3 2 3
NaCO 与足量盐酸反应消耗2 mol HCl,1 mol NaHCO 与足量盐酸反应消耗1 mol HCl,故
2 3 3
等物质的量的两种盐与足量的相同浓度的盐酸反应,NaCO 消耗盐酸的体积是NaHCO 的
2 3 3
2 倍,B 正确;向饱和 NaCO 溶液中通入 CO ,发生反应:NaCO +CO +
2 3 2 2 3 2
HO===2NaHCO↓,溶质质量增加,由于反应消耗水,且 NaHCO 的溶解度小于
2 3 3
NaCO ,故有NaHCO 晶体析出,C正确;NaCO 与BaCl 反应生成白色沉淀 BaCO ,
2 3 3 2 3 2 3
NaHCO 与BaCl 不反应,无明显现象,D正确。
3 2
6.[2024·东北师大附中一模]向过氧化钠与水反应后的溶液中滴加酚酞,酚酞先变红后
褪色。某小组欲探究其原因,进行如图所示实验。实验①取反应后溶液加入二氧化锰,立
即产生大量气体,带火星的木条复燃;实验②③中红色均不褪色。下列分析错误的是(
)A.实验①中产生的气体为O
2
B.实验①中MnO 为反应物
2
C.实验②③可证明使酚酞褪色的不是氢氧化钠和氧气
D.上述实验可说明过氧化钠与水反应可能生成了HO
2 2
答案:B
解析:实验①中产生的气体能使带火星的木条复燃,则该气体是O ,A项正确;实验
2
①中是用二氧化锰催化双氧水分解,二氧化锰是催化剂,B项错误;实验②中酚酞滴入氢
氧化钠溶液变红且不褪色,可证明氢氧化钠不会使酚酞褪色,实验③中将氧气通入滴有酚
酞的氢氧化钠溶液,溶液不褪色,可证明使酚酞褪色的不是氧气,C项正确;实验①得到
了氧气,证明溶液中存在HO ,实验②③可证明使酚酞褪色的不是氢氧化钠和氧气,则说
2 2
明过氧化钠与水反应生成的HO 最终使溶液红色褪去,D项正确。
2 2
7.[2024·福建泉州实验中学期中]相同条件下,向四瓶盛有相同体积、浓度的NaOH溶
液中通入体积不同的CO 气体,得到①②③④四瓶溶液。分别向四瓶溶液中逐滴加入等体
2
积、等浓度的盐酸,产生的气体体积V(CO )与所加盐酸体积V(HCl)的关系如图所示,
2
且图②③④中分别有OA<AB、OA=AB、OA>AB。则下列分析与判断正确的是(忽略
CO 的溶解)( )
2
A.①中通入的CO 最少
2
B.③溶液的pH大于①溶液的pH
C.有两种溶质的是②和③
D.④溶液中溶质为NaCO 和NaHCO
2 3 3
答案:B
解析:向 NaOH 溶液中通入体积不同的 CO 气体,产物有四种可能:NaOH 与
2
NaCO ,NaCO ,NaCO 与NaHCO ,NaHCO 。向反应后溶液中加入盐酸,可能会按顺
2 3 2 3 2 3 3 3
序发生以下反应:(ⅰ)NaOH+HCl===NaCl+HO、(ⅱ)NaCO +HCl===NaCl+
2 2 3
NaHCO 、(ⅲ)NaHCO +HCl===NaCl+CO↑+HO,由化学方程式可知NaCO 转化为
3 3 2 2 2 3NaHCO 消耗盐酸的量与由NaCO 转化成的NaHCO 反应消耗盐酸的量相等,溶液①中加
3 2 3 3
入盐酸立即有CO 生成,说明只发生反应(ⅲ),溶质只有NaHCO ;图②中OA<AB,说
2 3
明氢氧化钠溶液与二氧化碳反应生成碳酸氢钠和碳酸钠;③中OA=AB,说明氢氧化钠溶
液与二氧化碳恰好反应生成碳酸钠;④中OA>AB,说明氢氧化钠溶液过量,与二氧化碳
反应生成碳酸钠,得到碳酸钠和氢氧化钠混合物。①中氢氧化钠溶液与二氧化碳反应生成
碳酸氢钠,通入的CO 最多,A项错误;③溶液溶质是碳酸钠,①溶液中溶质是碳酸氢钠,
2
碳酸钠的碱性强于碳酸氢钠的碱性,故③溶液的pH大于①溶液的pH,B项正确;②中溶
质是碳酸氢钠和碳酸钠,③中溶质是碳酸钠,C项错误;④溶液中溶质为碳酸钠和氢氧化
钠,D项错误。
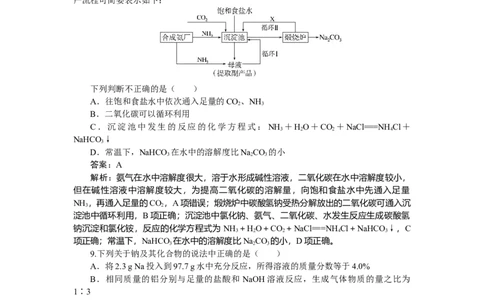
8.[2024·重庆名校联盟联考]我国化学家侯德榜改进了国外的纯碱生产工艺,其新的生
产流程可简要表示如下:
下列判断不正确的是( )
A.往饱和食盐水中依次通入足量的CO、NH
2 3
B.二氧化碳可以循环利用
C.沉淀池中发生的反应的化学方程式:NH +HO+CO +NaCl===NHCl+
3 2 2 4
NaHCO ↓
3
D.常温下,NaHCO 在水中的溶解度比NaCO 的小
3 2 3
答案:A
解析:氨气在水中溶解度很大,溶于水形成碱性溶液,二氧化碳在水中溶解度较小,
但在碱性溶液中溶解度较大,为提高二氧化碳的溶解量,向饱和食盐水中先通入足量
NH ,再通入足量的CO,A项错误;煅烧炉中碳酸氢钠受热分解放出的二氧化碳可通入沉
3 2
淀池中循环利用,B项正确;沉淀池中氯化钠、氨气、二氧化碳、水发生反应生成碳酸氢
钠沉淀和氯化铵,反应的化学方程式为 NH +HO+CO +NaCl===NHCl+NaHCO ↓,C
3 2 2 4 3
项正确;常温下,NaHCO 在水中的溶解度比NaCO 的小,D项正确。
3 2 3
9.下列关于钠及其化合物的说法中正确的是( )
A.将2.3 g Na投入到97.7 g水中充分反应,所得溶液的质量分数等于4.0%
B.相同质量的铝分别与足量的盐酸和 NaOH溶液反应,生成气体物质的量之比为
1∶3
C.将CO 和HO的混合气体a mol,与足量的NaO 固体充分反应,生成的O 在标
2 2 2 2 2
准状况下的体积为11.2a L
D.120 mL含有0.20 mol碳酸钠的溶液与200 mL盐酸进行滴加反应,不管将前者滴入
后者,还是后者滴入前者,滴加完全后,产生的气体在相同条件下体积不等,则盐酸的浓
度可能为2 mol·L-1
答案:C
解析:2Na+2HO===2NaOH+H↑,2.3 g Na与水反应得到NaOH 4g,溶液的质量因
2 2
生成氢气小于100 g,所以溶质的质量分数大于4.0%,A错误;B中发生的反应是2Al+6H
+===2Al3++3H↑,2Al+2OH-+2HO===2AlO+3H↑,因盐酸和氢氧化钠过量,因此
2 2 2
等量的铝产生氢气的物质的量相等,B错误;C中发生反应2CO +2NaO===2Na CO +
2 2 2 2 3O ,2HO+2NaO===4NaOH+O↑,无论是CO 还是HO,消耗2 mol气体,产生1 mol
2 2 2 2 2 2 2
O ,因此a mol混合气体,产生氧气的体积=mol×22.4 L·mol-1=11.2a L,C正确;碳酸
2
钠滴入盐酸中:NaCO +2HCl===2NaCl+HO+CO↑,盐酸滴入到碳酸钠中:HCl+
2 3 2 2
NaCO===NaHCO +NaCl,NaHCO +HCl===NaCl+CO↑+HO,假设无论前者滴入后
2 3 3 3 2 2
者还是后者滴入前者,生成CO 气体体积相等,盐酸的物质的量为2×120×10-3×0.2 mol
2
=0.048 mol,此时盐酸浓度c(HCl)=0.048/200×10-3 mol·L-1=0.24 mol·L-1,因此产生
气体体积不相等时,盐酸浓度应小于0.24 mol·L-1,D错误。
10.NaHCO 和NaO 按2∶1的个数之比混合,在密闭容器中加热使之充分反应,然后
3 2 2
趁热排出气体物质,容器内残留物的成分是( )
A.NaO 和NaHCO
2 2 3
B.NaHCO 和NaCO
3 2 3
C.NaOH和NaCO
2 3
D.只有NaCO
2 3
答案:D
解析:NaHCO 和NaO 按2∶1的个数之比混合,在密闭容器中加热使之充分反应,
3 2 2
发生的反应方程式为2NaHCO =====NaCO +CO↑+HO① 2NaO +2CO===2Na CO
3 2 3 2 2 2 2 2 2 3
+O② 2NaO +2HO===4NaOH+O↑③,CO 和HO同时存在时,遇NaO ,CO 先反
2 2 2 2 2 2 2 2 2 2
应、HO后反应,设NaHCO 和NaO 的物质的量分别是2 mol、1 mol,2 mol NaHCO 完
2 3 2 2 3
全分解生成1 mol Na CO、1 mol CO 、1 mol H O,根据方程式②知,1 mol Na O 完全反应
2 3 2 2 2 2
需要1 mol CO ,所以二氧化碳和过氧化钠恰好完全反应,水蒸气不反应,则最终容器内残
2
留物的成分是NaCO,故选D。
2 3
11.X、Y、Z、W有如图所示的转化关系(反应条件和部分其它反应物省略),则X、
Y、Z可能是 ( )
①Na、NaO 、NaO ② AlCl 、 Al(OH) 、NaAlO ③ Fe、FeCl 、 FeCl
2 2 2 3 3 2 2 3
④NaOH、NaCO、NaHCO
2 3 3
A.①②④ B.②④
C.①②③ D.①②③④
答案:A
解析:①若X为Na、W为O,则Y为NaO,Z为NaO,O 与Na反应在加热的条件
2 2 2 2 2
下生成 NaO ,故①正确;②若 X 为 AlCl ,W 为 NaOH,则 Y 为 Al(OH) ,Z 为
2 2 3 3
NaAlO ,过量NaOH与AlCl 反应生成NaAlO ,故②正确;③若X为Fe,W为Cl ,则Fe
2 3 2 2
与 Cl 只生成 FeCl ,故③错误;④若 X 为 NaOH、W 为 CO ,则 Y 为 NaCO ,Z 为
2 3 2 2 3
NaHCO ,过量CO 与NaOH反应生成NaHCO ,故④正确。所以A选项是正确的。
3 2 3
12.[2024·山东泰安新泰一中期中]如表,对陈述Ⅰ、Ⅱ的正确性及两者间是否具有因果
关系的判断都正确的是( )
选项 陈述Ⅰ 陈述Ⅱ 判断
NaCO 溶液可用于治疗胃酸 Ⅰ对,
A 2 3 NaCO 可与盐酸反应
过多 2 3 Ⅱ对,有
向滴有酚酞的水溶液中加入 Ⅰ对,
B NaO 与水反应生成NaOH
NaO,溶液变红色 2 2 Ⅱ错,无
2 2
高压钠灯能发出透雾性强的 Ⅰ对,
C 金属钠具有强还原性
黄光 Ⅱ对,有NaO 能与CO 或HO反应 Ⅰ对,
D NaO 可为航天员供氧 2 2 2 2
2 2 生成O Ⅱ对,有
2
答案:D
解析:NaCO 能够与盐酸反应,但是NaCO 的碱性较强,具有腐蚀性,不能用于治
2 3 2 3
疗胃酸过多,Ⅰ错误,A错误;NaO 与水反应生成NaOH,NaOH为强碱,水溶液呈碱性,
2 2
能够使酚酞变红,但NaO 具有强氧化性,最终溶液颜色褪去,B错误;钠的焰色为黄色,
2 2
透雾性强,高压钠灯能发出透雾性强的黄光,Ⅰ对,Ⅱ对,但二者无因果关系,C错误;
NaO 能与HO(或CO )反应生成O ,所以可为航天员供氧,Ⅰ、Ⅱ正确,且有因果关
2 2 2 2 2
系,D正确。