文档内容
扬州市 2009 年中考化学试题
相对原子质量:H:1 C:12 N:14 O:16 Na:23 Mg:24 K:39 Ca:40 Br:80
说明:
1.本试卷共6页,包含选择题(第1题~第20题,共40分)、非选择题(第21题~第28题)两
部分。本卷满分100分,考试时间为100分钟。考试结束后,将本卷和答题卡一并交回。
2.答题前,考生务必将本人的姓名、准考证号填写在答题卡相应的位置上,同时务必在试卷
的装订线内江本人的姓名、准考证号、毕业学校填写好,在试卷第一面的右下角填写好座位号。
3.所有试题都必须在专用的“答题卡”上作答,选择题用2B铅笔作答,非选择题在指定位置
用0.5毫米黑水笔作答。在试卷或草稿纸上答题无效。
一、单项选择题(本题包括15小题,每小题2分,共30分,每小题只有一个选项符合题意)
1.“诗画瘦西湖,人文古扬州”是我市的旅游宣传语,清澈的瘦西湖水属于
A.混合物 B.纯净物 C.单质 D.化合物
2.我市是第六个国家级“光谷”,下列过程属于物理变化的是
A.二氧化硅(SiO)与焦炭制粗硅(Si) B.氢气与四氯化硅(SiCl )制纯硅(Si)
2 4
C.太阳能热水器中冷水变热水 D.在催化剂作用下太阳能光解水制氢
3.如图是一幅贴在汽车加油站的宣传广告。下列叙述错误的是
A.由玉米生产的乙醇可添加在汽油中作汽车燃料
B.玉米汁可作汽车燃料
C.推广玉米生产的燃料可在一定程度上缓解当前的能源危机
D.推广乙醇汽油可适度减轻汽车尾气对环境的污染
4.凯氏定氮法中用硼酸(HBO)等试剂进行蛋白质含氮量测定,硼酸中硼元素的化合价是
3 3
A.+1 B.+2 C.+3 D.+6
5.下列说法错误的是
A.月饼盒中放入装有铁粉的小包装,可以防止月饼变质
B.液化气泄漏时,应首先关闭阀门,打开门窗换气
C.车船表面喷涂油漆,可防止生锈
D.石油、天然气、焦炉煤气是三大重要的化石燃料
催化剂
6.科学家探索用CO除去SO ,该研究涉及的一个反应:SO + 2CO ===== 2X + S,则X为
2 2
A.CO B.C C.CS D.COS
2 2
7.现有三种物质:①洁厕灵(含无机酸等)②生理盐水③烧碱溶液,pH大小关系为
A.①>②>③ B.③>②>① C.②<①<③ D.③<①<②
8.人民币防伪技术之一是光学变色油墨。某变色油墨中含有汞的碘化物,汞的元素符号是
A.Ag B.Hg C.Mg D.I
9.下表是今年3月我市环保局在自来水取水口检测的部分结果,有关说法错误的是
扬州市2009年中考化学试题A.溶解氧的“氧”指氧气
取水地点 溶解氧(mg/L) 氨氮(mg/L)
B.氨氮含量高可导致水体富营养化
廖家沟 8.9 0.107
C.取水口附近不能设立排污企业
长江 8.5 0.165
D.生活污水在取水口可以任意排放
10.制作“叶脉书签”需要配制100g12%的NaOH溶液(设水的密度为1g/mL)。下列操作正
确的是
A.称量前调节天平平衡时发现指针向右偏转,可调节游码
B.在左右托盘上垫滤纸称取12.0gNaOH固体
C.将准确称取的NaOH固体直接倒入装有水的量筒中溶解
D.选用100mL量筒量取88.0mL的水
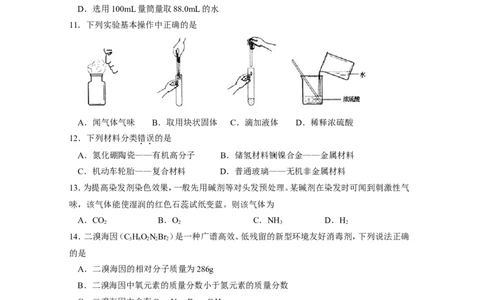
11.下列实验基本操作中正确的是
A.闻气体气味 B.取用块状固体 C.滴加液体 D.稀释浓硫酸
12.下列材料分类错误的是
A.氮化硼陶瓷——有机高分子 B.储氢材料镧镍合金——金属材料
C.机动车轮胎——复合材料 D.普通玻璃——无机非金属材料
13.为提高染发剂染色效果,一般先用碱剂等对头发预处理。某碱剂在染发时可闻到刺激性气
味,该气体能使湿润的红色石蕊试纸变蓝。则该气体为
A.CO B.O C.NH D.H
2 2 3 2
14.二溴海因(C HONBr )是一种广谱高效、低残留的新型环境友好消毒剂,下列说法正确
5 6 2 2 2
的是
A.二溴海因的相对分子质量为286g
B.二溴海因中氧元素的质量分数小于氮元素的质量分数
C.二溴海因中含有O、N、Br 、C H
2 2 2 5 6
D.二溴海因分子中C、H、O、N、Br原子个数比为5∶6∶2∶2∶2
15.如图所示的微观变化与下列反应及反应类型对应正确的是
点燃
A.2CO + O ===== 2CO 化合反应
2 2
B.2HI + Cl ==== 2HCl + I 置换反应
2 2
电解
C.2HO ===== 2H↑ + O↑ 分解反应
2 2 2
D.2HCl + CuO ==== CuCl + HO 复分解反应 反 应前 反应后
2 2
二、不定项选择题(本小题包括5小题,每小题2分,共10分 。每每个小小题球有代一表个一或个两原个子选项符合
扬州市2009年中考化学试题题意。若正确答案只包括一个选项,多选时,该小题为0分;若正确答案包括两个选项,只选一
个且正确的为1分,选两个且都正确的给满分,但只要选错一个该小题就为0分。)
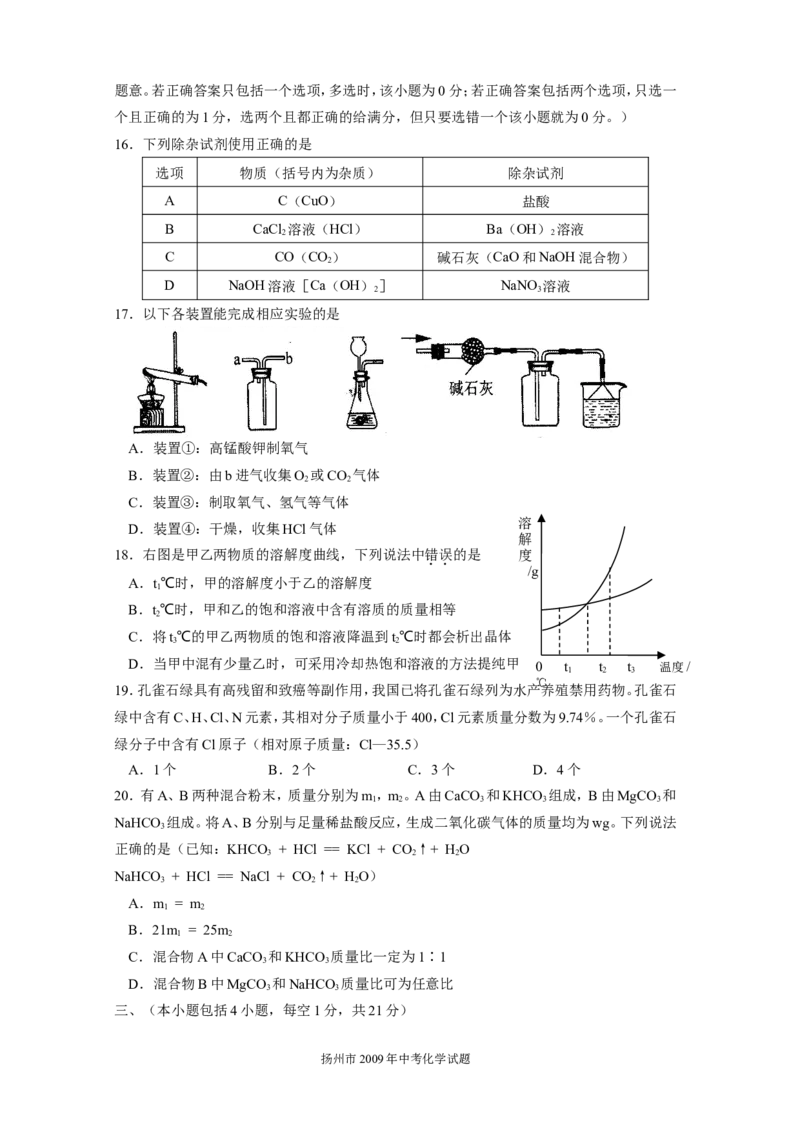
16.下列除杂试剂使用正确的是
选项 物质(括号内为杂质) 除杂试剂
A C(CuO) 盐酸
B CaCl 溶液(HCl) Ba(OH) 溶液
2 2
C CO(CO) 碱石灰(CaO和NaOH混合物)
2
D NaOH溶液[Ca(OH)] NaNO 溶液
2 3
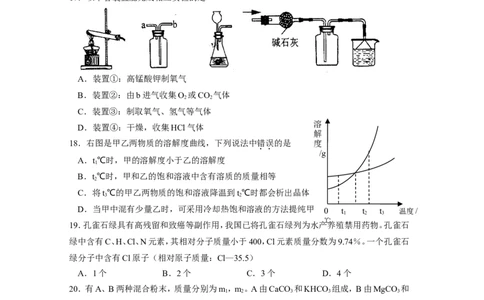
17.以下各装置能完成相应实验的是
A.装置①:高锰酸钾制氧气
B.装置②:由b进气收集O 或CO 气体
2 2
C.装置③:制取氧气、氢气等气体
溶
D.装置④:干燥,收集HCl气体
解
18.右图是甲乙两物质的溶解度曲线,下列说法中错误的是 度
/g
A.t℃时,甲的溶解度小于乙的溶解度
1
B.t℃时,甲和乙的饱和溶液中含有溶质的质量相等
2
C.将t℃的甲乙两物质的饱和溶液降温到t℃时都会析出晶体
3 2
D.当甲中混有少量乙时,可采用冷却热饱和溶液的方法提纯甲 0 t t t 温度/
1 2 3
℃
19.孔雀石绿具有高残留和致癌等副作用,我国已将孔雀石绿列为水产养殖禁用药物。孔雀石
绿中含有C、H、Cl、N元素,其相对分子质量小于400,Cl元素质量分数为9.74%。一个孔雀石
绿分子中含有Cl原子(相对原子质量:Cl—35.5)
A.1个 B.2个 C.3个 D.4个
20.有A、B两种混合粉末,质量分别为m,m。A由CaCO 和KHCO 组成,B由MgCO 和
1 2 3 3 3
NaHCO 组成。将A、B分别与足量稀盐酸反应,生成二氧化碳气体的质量均为wg。下列说法
3
正确的是(已知:KHCO + HCl == KCl + CO↑+ HO
3 2 2
NaHCO + HCl == NaCl + CO↑+ HO)
3 2 2
A.m = m
1 2
B.21m = 25m
1 2
C.混合物A中CaCO 和KHCO 质量比一定为1∶1
3 3
D.混合物B中MgCO 和NaHCO 质量比可为任意比
3 3
三、(本小题包括4小题,每空1分,共21分)
扬州市2009年中考化学试题21.(4分)生活中蕴科学,留心处皆学问。请用下列序号填空。
①NaCO ②CaO ③NH HPO ④C H O
2 3 4 2 4 6 12 6
(1)人体血糖含量的“糖” ▲ ;(2)与水反应放热可以煮鸡蛋 ▲ ;
(3)可作复合肥料 ▲ ;(4)侯氏联合制碱法的主产品 ▲ 。
22.(7分)(1)化学世界绚丽多彩,请选择适当的序号填空。
A.红色 B.绿色 C.黑色 D.白色 E.黄色 F.紫黑色
①高锰酸钾固体 ▲ ②氧化镁 ▲ ③碱式碳酸铜 ▲
(2)化学世界千变万化,请写出下列反应的化学方程式
①硫酸铜溶液和熟石灰配制农药波尔多液 ▲ ②绿色植物进行光合作用 ▲
③用稀硫酸除去铁锈(以Fe O 表示) ▲
2 3
④汽车受到撞击时,30毫秒内安全气囊中NaN 分解为氮气和钠 ▲
3
23.(5分)碘元素对人体健康起着重要的作用,在食盐中加碘科有效预防甲状腺肿大的发生。
如图是某品牌加碘盐的标签,请回答下列问题。(相对原子质量:K—39 I—127 O—16)
(1)写出碘酸钾中阳离子的符号 ▲ ,碘酸钾中K、I、
配料表:氯化钠、碘酸钾(KIO)
O三种元素的质量比为 ▲ 。 3
净含量:500g
(2)下列物质遇到碘(I)显蓝色的是 ▲ 。(填字母序
2
碘含量(以I计):30~60mg/Kg
号)
A.蔗糖水 B.米汤 C.食盐水
(3)高温烹饪会使含碘量降低,说明碘酸钾的化学性质之一是 ▲ 。
(4)根据有关数据估算,每500g该加碘食盐中碘酸钾(KIO )的质量范围是 ▲ 。(填
3
字母序号)
A.15~30mg B.25~51mg C.60~120mg
24.化学实验中常常使用火柴,已知火柴头含有硫、
火柴头
氯 XX牌火柴
酸钾、二氧化锰等,火柴盒侧面含有 红磷、三
火柴梗
硫 火柴盒侧面
化二锑等,试回答以下问题:
(1)锑的元素符号是Sb,则三硫化二锑的化学式为
▲ 。硫在空气中燃烧的化学方程式为 ▲ 。
(2)火柴梗主要成分是纤维素,纤维素属于 ▲ 。(填字母序号)
A.蛋白质 B.糖类 C.油脂
(3)火柴盒侧面使用红磷而不使用白磷,其原因之一是因为红磷的着火点 ▲ (填“高”
或“低”),火柴划燃后时会产生白烟,白烟的主要成分的化学式为 ▲ 。
四、(本小题包括2小题,共15分)
25.(7分)美国化学家西博格说:化学世人类进步的关键。
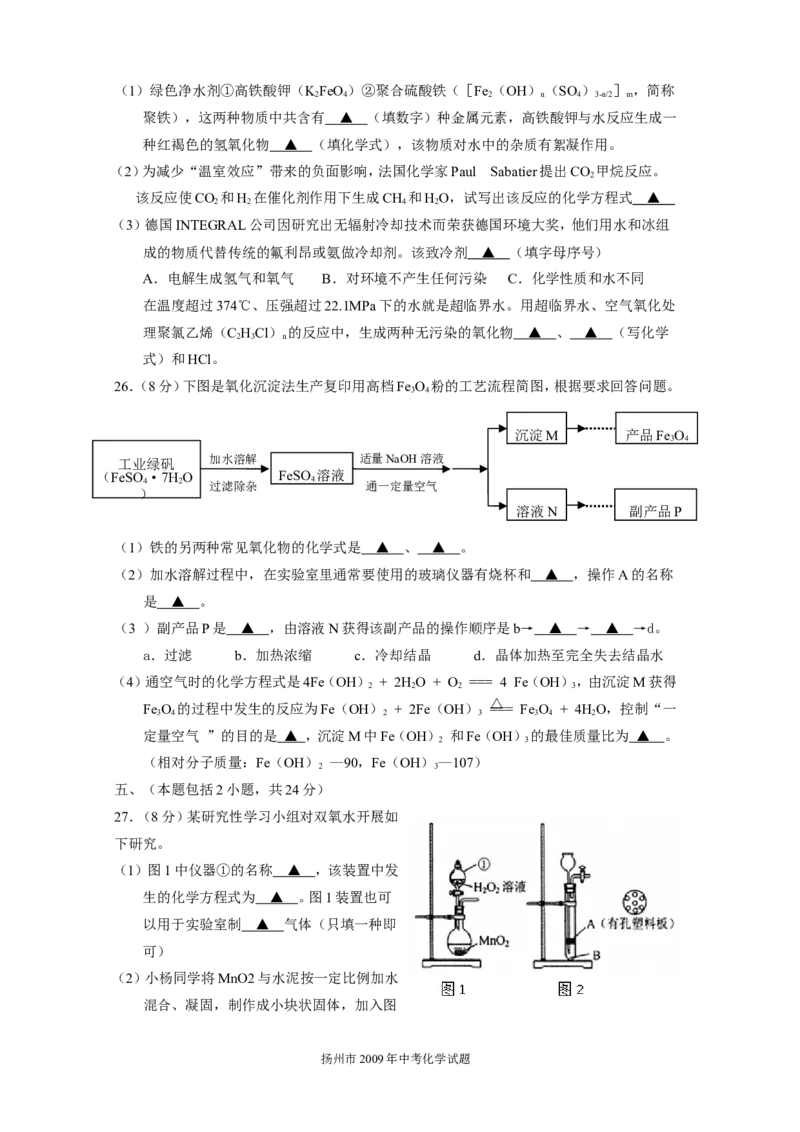
扬州市2009年中考化学试题(1)绿色净水剂①高铁酸钾(KFeO)②聚合硫酸铁([Fe (OH)(SO ) ] ,简称
2 4 2 n 4 3-n/2 m
聚铁),这两种物质中共含有 ▲ (填数字)种金属元素,高铁酸钾与水反应生成一
种红褐色的氢氧化物 ▲ (填化学式),该物质对水中的杂质有絮凝作用。
(2)为减少“温室效应”带来的负面影响,法国化学家Paul Sabatier提出CO 甲烷反应。
2
该反应使CO 和H 在催化剂作用下生成CH 和HO,试写出该反应的化学方程式 ▲
2 2 4 2
(3)德国INTEGRAL公司因研究出无辐射冷却技术而荣获德国环境大奖,他们用水和冰组
成的物质代替传统的氟利昂或氨做冷却剂。该致冷剂 ▲ (填字母序号)
A.电解生成氢气和氧气 B.对环境不产生任何污染 C.化学性质和水不同
在温度超过374℃、压强超过22.1MPa下的水就是超临界水。用超临界水、空气氧化处
理聚氯乙烯(C HCl) 的反应中,生成两种无污染的氧化物 ▲ 、 ▲ (写化学
2 3 n
式)和HCl。
26.(8分)下图是氧化沉淀法生产复印用高档Fe O 粉的工艺流程简图,根据要求回答问题。
3 4
沉淀M 产品Fe O
3 4
工业绿矾 加水溶解 适量NaOH溶液
(FeSO 4 ·7H 2 O 过滤除杂 FeSO 4 溶液 通一定量空气
)
溶液N 副产品P
(1)铁的另两种常见氧化物的化学式是 ▲ 、 ▲ 。
(2)加水溶解过程中,在实验室里通常要使用的玻璃仪器有烧杯和 ▲ ,操作A的名称
是 ▲ 。
(3 )副产品P是 ▲ ,由溶液N获得该副产品的操作顺序是b→ ▲ → ▲ →d。
a.过滤 b.加热浓缩 c.冷却结晶 d.晶体加热至完全失去结晶水
(4)通空气时的化学方程式是4Fe(OH) + 2HO + O === 4 Fe(OH),由沉淀M获得
2 2 2 3
△
Fe O 的过程中发生的反应为Fe(OH) + 2Fe(OH) === Fe O + 4HO,控制“一
3 4 2 3 3 4 2
定量空气 ”的目的是 ▲ ,沉淀M中Fe(OH) 和Fe(OH)的最佳质量比为 ▲ 。
2 3
(相对分子质量:Fe(OH) —90,Fe(OH)—107)
2 3
五、(本题包括2小题,共24分)
27.(8分)某研究性学习小组对双氧水开展如
下研究。
(1)图1中仪器①的名称 ▲ ,该装置中发
生的化学方程式为 ▲ 。图1装置也可
以用于实验室制 ▲ 气体(只填一种即
可)
(2)小杨同学将MnO2与水泥按一定比例加水
混合、凝固,制作成小块状固体,加入图
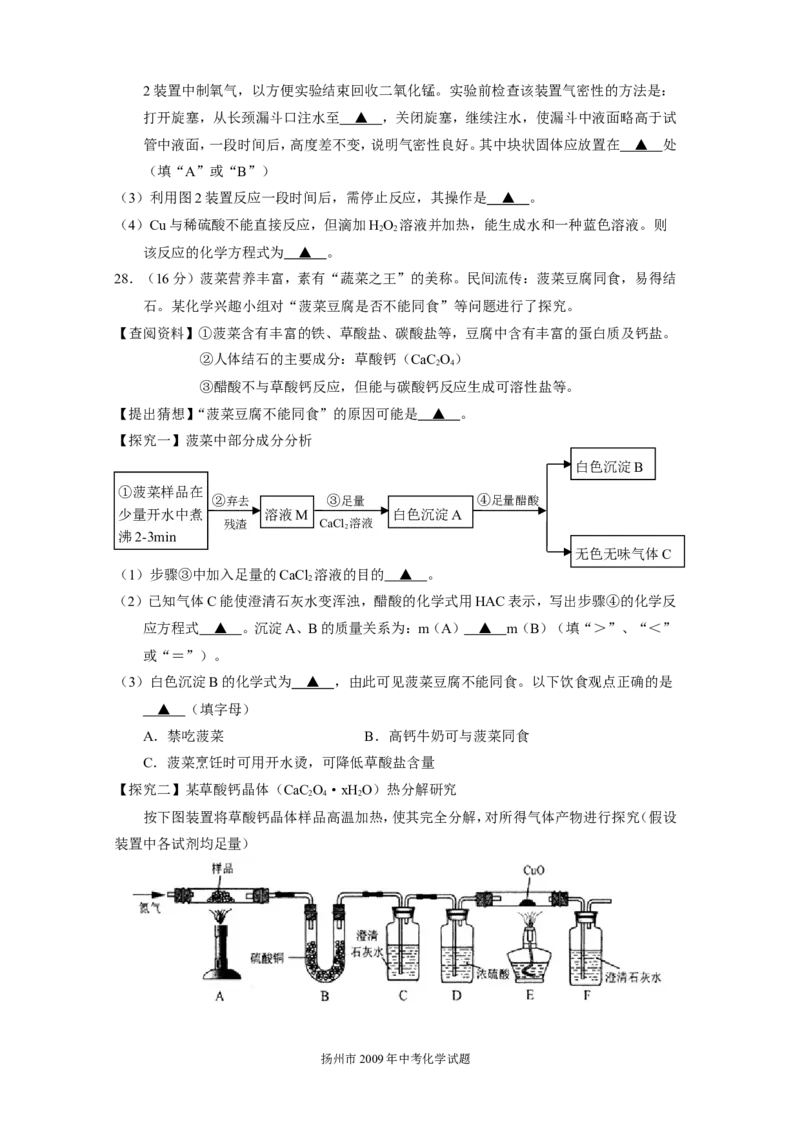
扬州市2009年中考化学试题2装置中制氧气,以方便实验结束回收二氧化锰。实验前检查该装置气密性的方法是:
打开旋塞,从长颈漏斗口注水至 ▲ ,关闭旋塞,继续注水,使漏斗中液面略高于试
管中液面,一段时间后,高度差不变,说明气密性良好。其中块状固体应放置在 ▲ 处
(填“A”或“B”)
(3)利用图2装置反应一段时间后,需停止反应,其操作是 ▲ 。
(4)Cu与稀硫酸不能直接反应,但滴加HO 溶液并加热,能生成水和一种蓝色溶液。则
2 2
该反应的化学方程式为 ▲ 。
28.(16分)菠菜营养丰富,素有“蔬菜之王”的美称。民间流传:菠菜豆腐同食,易得结
石。某化学兴趣小组对“菠菜豆腐是否不能同食”等问题进行了探究。
【查阅资料】①菠菜含有丰富的铁、草酸盐、碳酸盐等,豆腐中含有丰富的蛋白质及钙盐。
②人体结石的主要成分:草酸钙(CaC O)
2 4
③醋酸不与草酸钙反应,但能与碳酸钙反应生成可溶性盐等。
【提出猜想】“菠菜豆腐不能同食”的原因可能是 ▲ 。
【探究一】菠菜中部分成分分析
白色沉淀B
①菠菜样品在
②弃去 ③足量 ④足量醋酸
少量开水中煮 溶液M 白色沉淀A
残渣 CaCl 溶液
2
沸2-3min
无色无味气体C
(1)步骤③中加入足量的CaCl 溶液的目的 ▲ 。
2
(2)已知气体C能使澄清石灰水变浑浊,醋酸的化学式用HAC表示,写出步骤④的化学反
应方程式 ▲ 。沉淀A、B的质量关系为:m(A) ▲ m(B)(填“>”、“<”
或“=”)。
(3)白色沉淀B的化学式为 ▲ ,由此可见菠菜豆腐不能同食。以下饮食观点正确的是
▲ (填字母)
A.禁吃菠菜 B.高钙牛奶可与菠菜同食
C.菠菜烹饪时可用开水烫,可降低草酸盐含量
【探究二】某草酸钙晶体(CaC O·xHO)热分解研究
2 4 2
按下图装置将草酸钙晶体样品高温加热,使其完全分解,对所得气体产物进行探究(假设
装置中各试剂均足量)
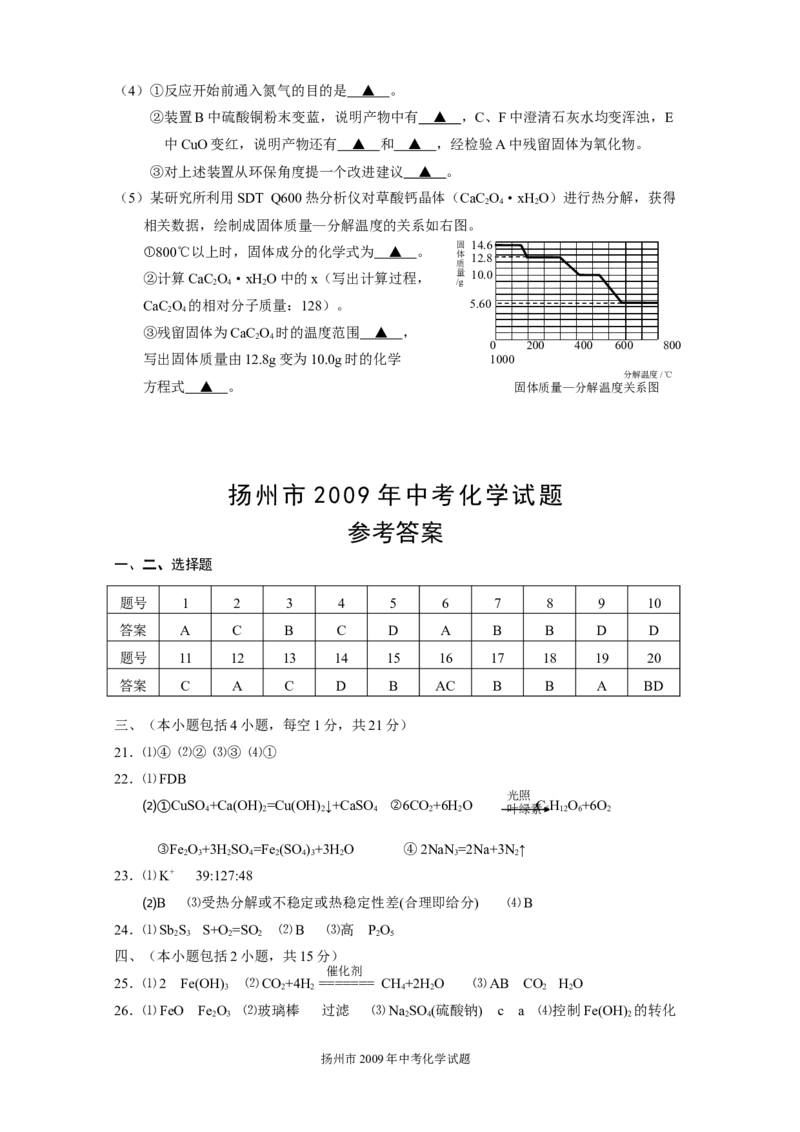
扬州市2009年中考化学试题(4)①反应开始前通入氮气的目的是 ▲ 。
②装置B中硫酸铜粉末变蓝,说明产物中有 ▲ ,C、F中澄清石灰水均变浑浊,E
中CuO变红,说明产物还有 ▲ 和 ▲ ,经检验A中残留固体为氧化物。
③对上述装置从环保角度提一个改进建议 ▲ 。
(5)某研究所利用SDT Q600热分析仪对草酸钙晶体(CaC O·xHO)进行热分解,获得
2 4 2
相关数据,绘制成固体质量—分解温度的关系如右图。
固 14.6
①800℃以上时,固体成分的化学式为 ▲ 。
体 12.8
质
②计算CaC O·xHO中的x(写出计算过程, 量 10.0
2 4 2 /g
CaC O 的相对分子质量:128)。 5.60
2 4
③残留固体为CaC O 时的温度范围 ▲ ,
2 4
0 200 400 600 800
写出固体质量由12.8g变为10.0g时的化学 1000
分解温度/℃
方程式 ▲ 。 固体质量—分解温度关系图
扬州市 2009 年中考化学试题
参考答案
一、二、选择题
题号 1 2 3 4 5 6 7 8 9 10
答案 A C B C D A B B D D
题号 11 12 13 14 15 16 17 18 19 20
答案 C A C D B AC B B A BD
三、(本小题包括4小题,每空1分,共21分)
21.⑴④ ⑵② ⑶③ ⑷①
22.⑴FDB
光照
⑵①CuSO 4 +Ca(OH) 2 =Cu(OH) 2 ↓+CaSO 4 ②6CO 2 +6H 2 O 叶 绿 素C 6 H 12 O 6 +6O 2
③Fe O+3H SO =Fe (SO )+3H O ④2NaN =2Na+3N ↑
2 3 2 4 2 4 3 2 3 2
23.⑴K+ 39:127:48
⑵B ⑶受热分解或不稳定或热稳定性差(合理即给分) ⑷B
24.⑴Sb S S+O=SO ⑵B ⑶高 PO
2 3 2 2 2 5
四、(本小题包括2小题,共15分)
催化剂
25.⑴2 Fe(OH) ⑵CO+4H ======= CH+2H O ⑶AB CO HO
3 2 2 4 2 2 2
26.⑴FeO Fe O ⑵玻璃棒 过滤 ⑶NaSO (硫酸钠) c a ⑷控制Fe(OH) 的转化
2 3 2 4 2
扬州市2009年中考化学试题量(防止Fe(OH) 转化为Fe(OH) 等合理理由均可) 90:214(45:107)
2 3
五、(本题包括2小题,共24分)
MnO
2
27.⑴分液漏斗,2HO====2H O+O↑, CO 或H(合理即给分)
2 2 2 2 2 2
⑵浸没漏斗下端(或形成液封) A
⑶关闭旋塞
△
⑷Cu+H O+H SO =CuSO+2H O
2 2 2 4 4 2
28.
【提出猜想】菠菜中碳酸盐与豆腐中钙盐反应产生草酸钙(易得结石、生成草酸钙等均可给
分)
⑴使溶液M中的草酸盐、碳酸盐完全沉淀
⑵CaCO +2HAc=Ca(Ac) +H O+CO↑,>
3 2 2 2
⑶CaC O, C
2 4
⑷①排尽装置中的空气(防止CO还原CuO时发生爆炸,合理即给分)
②HO、CO 、CO
2 2
③在装置F后增加尾气处理装置(或在装置F后增加点燃CO装置等合理说法均给分)
⑸①CaO
②CaC O·xH O~CaO
2 4 2
128+18x 56
14.6g 5.60g
x=1
高温
③200~400℃,CaC O===CaCO +CO
2 4 3
扬州市2009年中考化学试题