文档内容
开考前秘密 试卷类型:A
二 O 一四年东营市初中学生学业考试
化学试题
(总分 100 分 考试时间 60 分钟)
注意事项:
1.本试题分Ⅰ、Ⅱ两卷。第I卷(选择题 共36分),第Ⅱ卷(非选择题 共64分)。
2.考生答题前务必将自已的姓名、准考证号、座号填写在试卷和答题卡上,考试结束,试卷
和答题卡一并收回。
3.第I卷每题选出答案后,用2B铅笔把答题卡上对应题目的答案标号(ABCD)涂黑,如需
改动,必须用橡皮擦干净后,再选涂其它答案。答第II卷时,用0.5毫米黑色签字笔答在答题卡的
相应位置上。
可能用到的相对原子质量:H 1 C 12 O 16 Cl 35.5 Ca 40 Fe 56 Cu 64
第I卷(选择题 共 36 分)
一、选择题(本题包括9小题,每小题4分,共36分。每小题只有一个选项符合题意)
1.3月29日是本年度的“地球一小时”(Earth Hour)活动日,主题为“蓝天自造”,旨在呼吁
每一位公民从自身开始,采取实际行动,应对当前中国最急迫、最受关注的环境议题——雾
霾。作为一名中学生,下列做法不符合这一主题的是
A.选择自行车和公交车作为出行工具
B.让衣服自然晾干,节约用纸,不使用一次性塑料袋
C.将废纸、汽水瓶等收集起来,一次性焚烧
D.拒绝使用一次性木筷,用电子贺卡代替纸制贺卡
2.下列化学用语表达错误的是
A.复合肥料磷酸二氢铵的化学式:NH HPO
4 2 4
B.碳原子的结构示意图:
C.在人体组织里葡萄糖的转化:C H O+6O 6 CO +6 H O
6 12 6 2 2 2
D.过氧化氢中氢、氧元素的化合价:
3.下列说法不正确的是
A.稀有气体在通常条件下几乎不与任何物质发生反应,化学性质比较稳定
B.铁制品锈蚀主要是铁与空气中的氧气、水蒸气发生化学反应的结果
C.溶液具有均一性和稳定性,是因为溶液中的各种粒子都静止不动
D.元素周期表是学习和研究化学、探索未知世界的重要工具
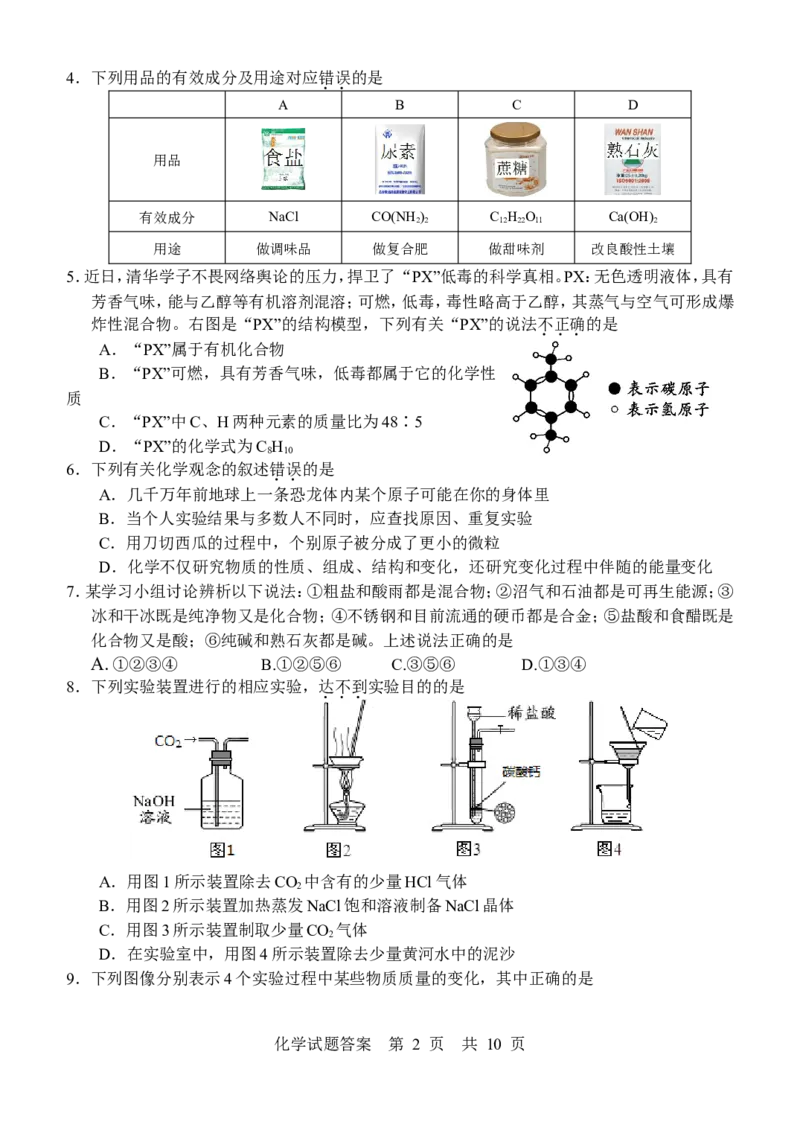
化学试题答案 第 1 页 共 10 页4.下列用品的有效成分及用途对应错误的是
A B C D
用品
有效成分 NaCl CO(NH) C H O Ca(OH)
22 12 22 11 2
用途 做调味品 做复合肥 做甜味剂 改良酸性土壤
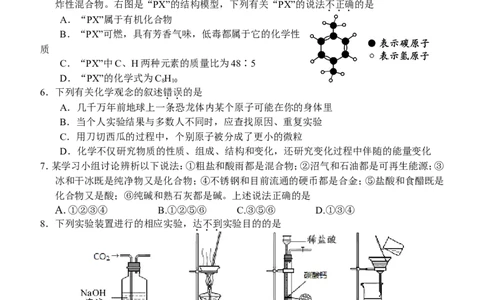
5.近日,清华学子不畏网络舆论的压力,捍卫了“PX”低毒的科学真相。PX:无色透明液体,具有
芳香气味,能与乙醇等有机溶剂混溶;可燃,低毒,毒性略高于乙醇,其蒸气与空气可形成爆
炸性混合物。右图是“PX”的结构模型,下列有关“PX”的说法不正确的是
A.“PX”属于有机化合物
B.“PX”可燃,具有芳香气味,低毒都属于它的化学性
质
C.“PX”中C、H两种元素的质量比为48∶5
D.“PX”的化学式为C H
8 10
6.下列有关化学观念的叙述错误的是
A.几千万年前地球上一条恐龙体内某个原子可能在你的身体里
B.当个人实验结果与多数人不同时,应查找原因、重复实验
C.用刀切西瓜的过程中,个别原子被分成了更小的微粒
D.化学不仅研究物质的性质、组成、结构和变化,还研究变化过程中伴随的能量变化
7.某学习小组讨论辨析以下说法:①粗盐和酸雨都是混合物;②沼气和石油都是可再生能源;③
冰和干冰既是纯净物又是化合物;④不锈钢和目前流通的硬币都是合金;⑤盐酸和食醋既是
化合物又是酸;⑥纯碱和熟石灰都是碱。上述说法正确的是
A. ①②③④ B.①②⑤⑥ C.③⑤⑥ D.①③④
8.下列实验装置进行的相应实验,达不到实验目的的是
A.用图1所示装置除去CO 中含有的少量HCl气体
2
B.用图2所示装置加热蒸发NaCl饱和溶液制备NaCl晶体
C.用图3所示装置制取少量CO 气体
2
D.在实验室中,用图4所示装置除去少量黄河水中的泥沙
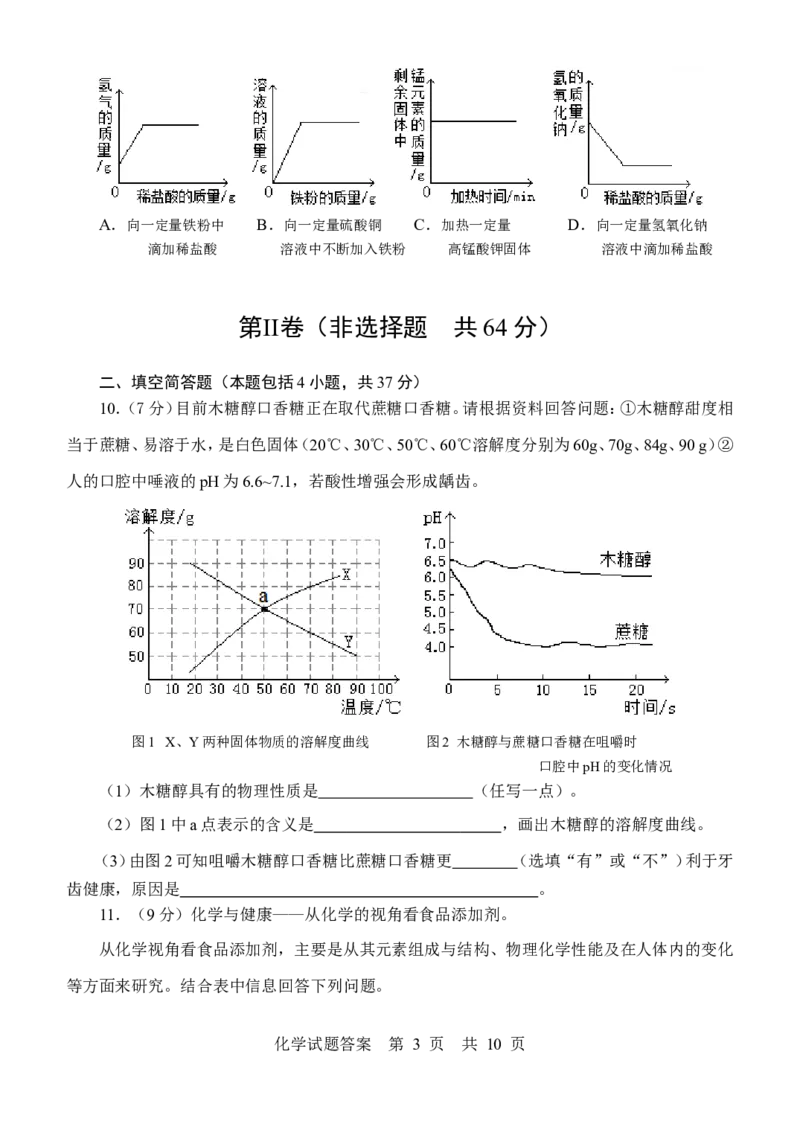
9.下列图像分别表示4个实验过程中某些物质质量的变化,其中正确的是
化学试题答案 第 2 页 共 10 页A.向一定量铁粉中 B.向一定量硫酸铜 C.加热一定量 D.向一定量氢氧化钠
滴加稀盐酸 溶液中不断加入铁粉 高锰酸钾固体 溶液中滴加稀盐酸
第II卷(非选择题 共 64 分)
二、填空简答题(本题包括4小题,共37分)
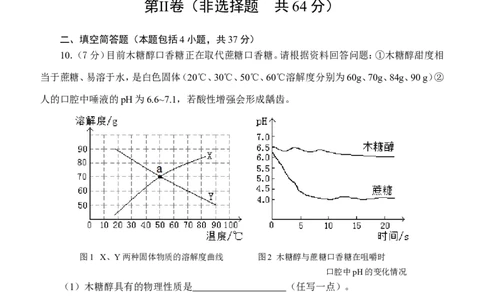
10.(7分)目前木糖醇口香糖正在取代蔗糖口香糖。请根据资料回答问题:①木糖醇甜度相
当于蔗糖、易溶于水,是白色固体(20℃、30℃、50℃、60℃溶解度分别为60g、70g、84g、90 g)②
人的口腔中唾液的pH为6.6~7.1,若酸性增强会形成龋齿。
图1 X、Y两种固体物质的溶解度曲线 图2 木糖醇与蔗糖口香糖在咀嚼时
口腔中pH的变化情况
(1)木糖醇具有的物理性质是 (任写一点)。
(2)图1中a点表示的含义是 ,画出木糖醇的溶解度曲线。
(3)由图2可知咀嚼木糖醇口香糖比蔗糖口香糖更 (选填“有”或“不”)利于牙
齿健康,原因是 。
11.(9分)化学与健康——从化学的视角看食品添加剂。
从化学视角看食品添加剂,主要是从其元素组成与结构、物理化学性能及在人体内的变化
等方面来研究。结合表中信息回答下列问题。
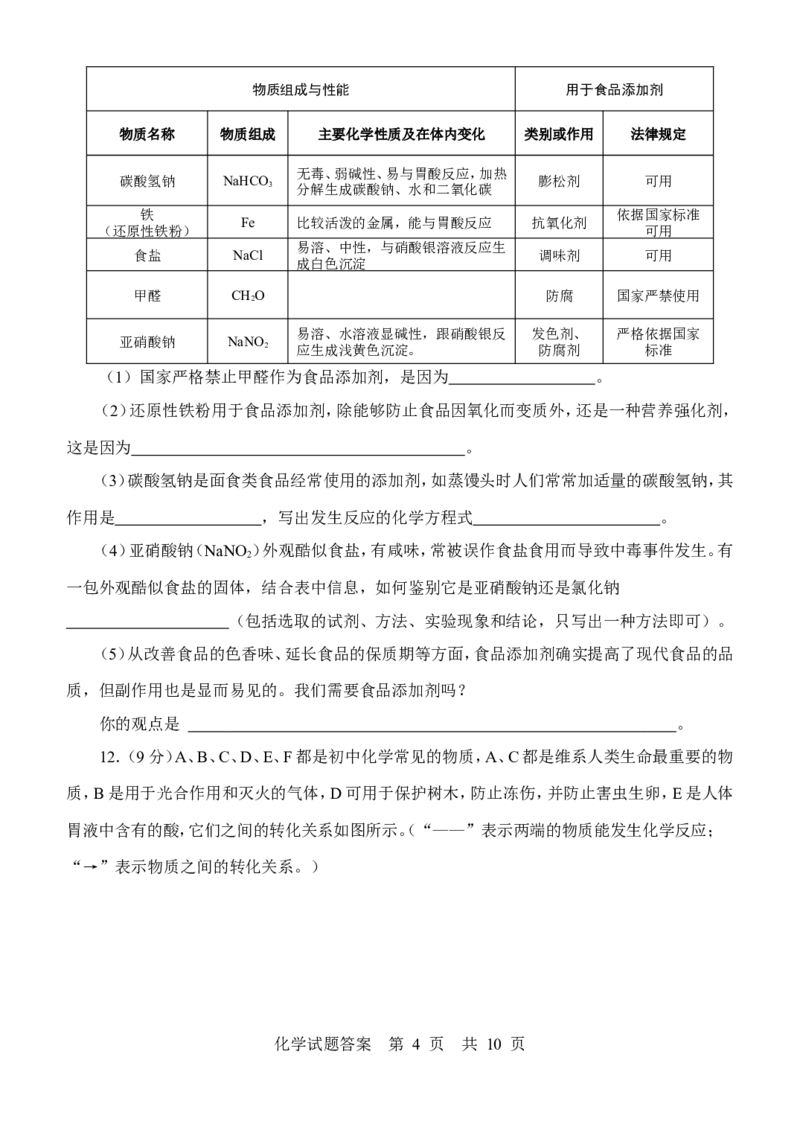
化学试题答案 第 3 页 共 10 页物质组成与性能 用于食品添加剂
物质名称 物质组成 主要化学性质及在体内变化 类别或作用 法律规定
无毒、弱碱性、易与胃酸反应,加热
碳酸氢钠 NaHCO 膨松剂 可用
3 分解生成碳酸钠、水和二氧化碳
铁 依据国家标准
Fe 比较活泼的金属,能与胃酸反应 抗氧化剂
(还原性铁粉) 可用
易溶、中性,与硝酸银溶液反应生
食盐 NaCl 调味剂 可用
成白色沉淀
甲醛 CHO 防腐 国家严禁使用
2
易溶、水溶液显碱性,跟硝酸银反 发色剂、 严格依据国家
亚硝酸钠 NaNO
2 应生成浅黄色沉淀。 防腐剂 标准
(1)国家严格禁止甲醛作为食品添加剂,是因为 。
(2)还原性铁粉用于食品添加剂,除能够防止食品因氧化而变质外,还是一种营养强化剂,
这是因为 。
(3)碳酸氢钠是面食类食品经常使用的添加剂,如蒸馒头时人们常常加适量的碳酸氢钠,其
作用是 ,写出发生反应的化学方程式 。
(4)亚硝酸钠(NaNO )外观酷似食盐,有咸味,常被误作食盐食用而导致中毒事件发生。有
2
一包外观酷似食盐的固体,结合表中信息,如何鉴别它是亚硝酸钠还是氯化钠
(包括选取的试剂、方法、实验现象和结论,只写出一种方法即可)。
(5)从改善食品的色香味、延长食品的保质期等方面,食品添加剂确实提高了现代食品的品
质,但副作用也是显而易见的。我们需要食品添加剂吗?
你的观点是 。
12.(9分)A、B、C、D、E、F都是初中化学常见的物质,A、C都是维系人类生命最重要的物
质,B是用于光合作用和灭火的气体,D可用于保护树木,防止冻伤,并防止害虫生卵,E是人体
胃液中含有的酸,它们之间的转化关系如图所示。(“——”表示两端的物质能发生化学反应;
“→”表示物质之间的转化关系。)
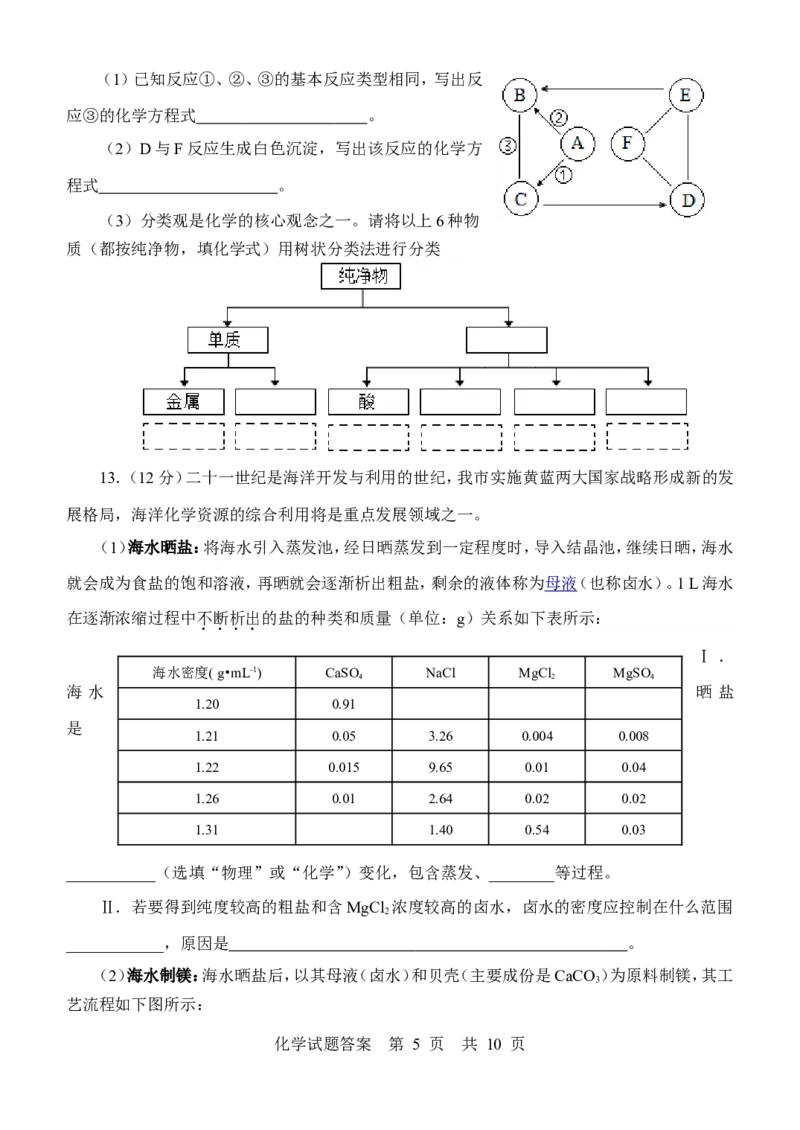
化学试题答案 第 4 页 共 10 页(1)已知反应①、②、③的基本反应类型相同,写出反
应③的化学方程式 。
(2)D与F反应生成白色沉淀,写出该反应的化学方
程式 。
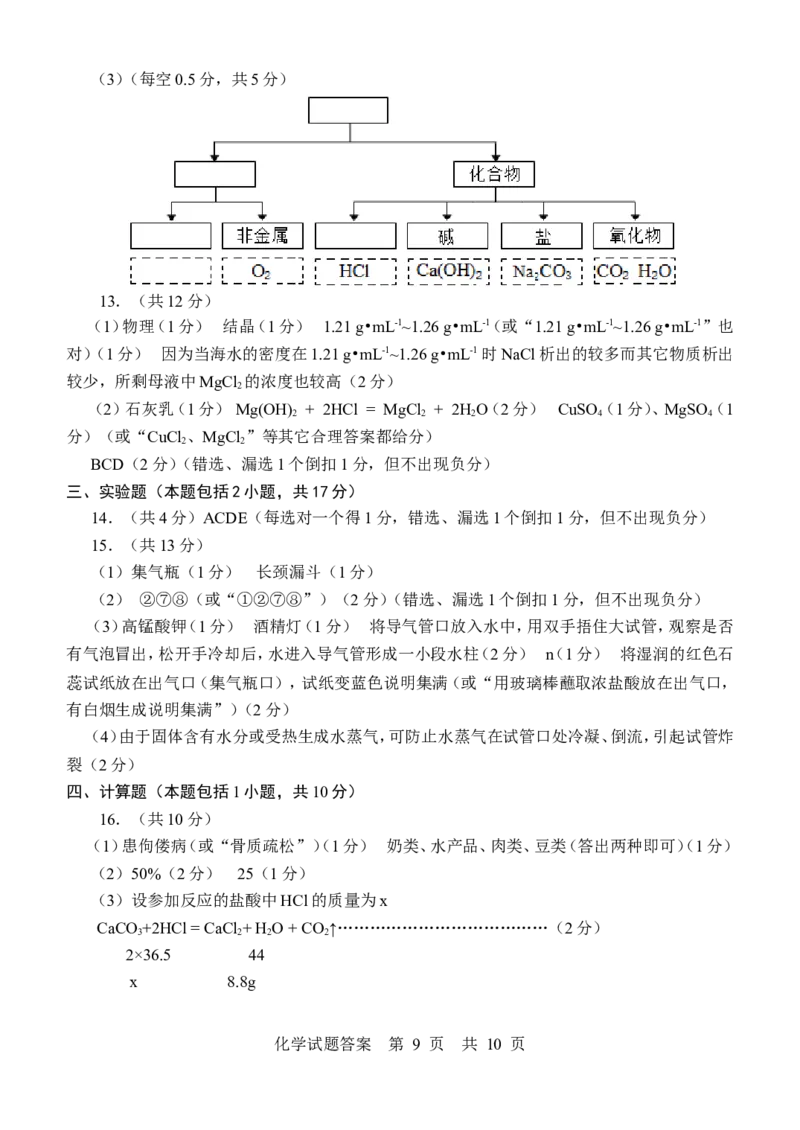
(3)分类观是化学的核心观念之一。请将以上6种物
质(都按纯净物,填化学式)用树状分类法进行分类
13.(12分)二十一世纪是海洋开发与利用的世纪,我市实施黄蓝两大国家战略形成新的发
展格局,海洋化学资源的综合利用将是重点发展领域之一。
(1)海水晒盐:将海水引入蒸发池,经日晒蒸发到一定程度时,导入结晶池,继续日晒,海水
就会成为食盐的饱和溶液,再晒就会逐渐析出粗盐,剩余的液体称为母液(也称卤水)。1 L海水
在逐渐浓缩过程中不断析出的盐的种类和质量(单位:g)关系如下表所示:
Ⅰ .
海水密度( g•mL-1) CaSO NaCl MgCl MgSO
4 2 4
海 水 晒 盐
1.20 0.91
是
1.21 0.05 3.26 0.004 0.008
1.22 0.015 9.65 0.01 0.04
1.26 0.01 2.64 0.02 0.02
1.31 1.40 0.54 0.03
___________(选填“物理”或“化学”)变化,包含蒸发、________等过程。
Ⅱ.若要得到纯度较高的粗盐和含MgCl 浓度较高的卤水,卤水的密度应控制在什么范围
2
____________,原因是 。
(2)海水制镁:海水晒盐后,以其母液(卤水)和贝壳(主要成份是CaCO )为原料制镁,其工
3
艺流程如下图所示:
化学试题答案 第 5 页 共 10 页Ⅰ.步骤①中所加的碱应该是 (选填“氢氧化钠”或“石灰乳”);步骤②反
应的化学方程式是 ;若要验证镁、铁、铜的金属活动性顺序,选择
铁丝后,还要选 、 两种溶液。
Ⅱ.Mg(OH) 加热分解生成MgO和HO,MgO是高熔点的化合物,某些阻燃剂(阻碍燃烧的
2 2
物质)的有效成分是Mg(OH) 。你认为Mg(OH) 能够阻燃的原因可能是 (选填序号)。
2 2
A.Mg(OH) 分解需要吸收大量的热,降低了可燃物的着火点
2
B.生成的氧化镁覆盖在可燃物表面,隔绝了空气
C.生成的蒸气降低了可燃物周围氧气浓度
D.反应因吸热降低了环境温度,使可燃物不易达到着火点
三、实验题(本题包括2小题,共17分)
14.(4分)在实验室中,下列做法正确的是 。
A.在演示实验和分组实验中,要力求利用最少的实验药品,获得最佳的实验效果,最大限
度的减少废弃物
B.稀释浓硫酸时,应沿杯壁向浓硫酸中缓缓加水,并用玻璃棒不断搅拌
C.取用液体药品时,要把瓶塞反放在桌面上,标签朝向手心,放回原处时标签向外
D.做氢气等可燃气体的燃烧实验时,应先检验气体的纯度后再点燃气体,以防爆炸
E.不能用手接触实验室里的药品,不要凑到容器口闻气体的气味,不能尝药品的味道
F.给试管里的液体加热时,不要把拇指按在短柄上,试管口不能对着自己,试管内液体体积
不超过试管容积的一半
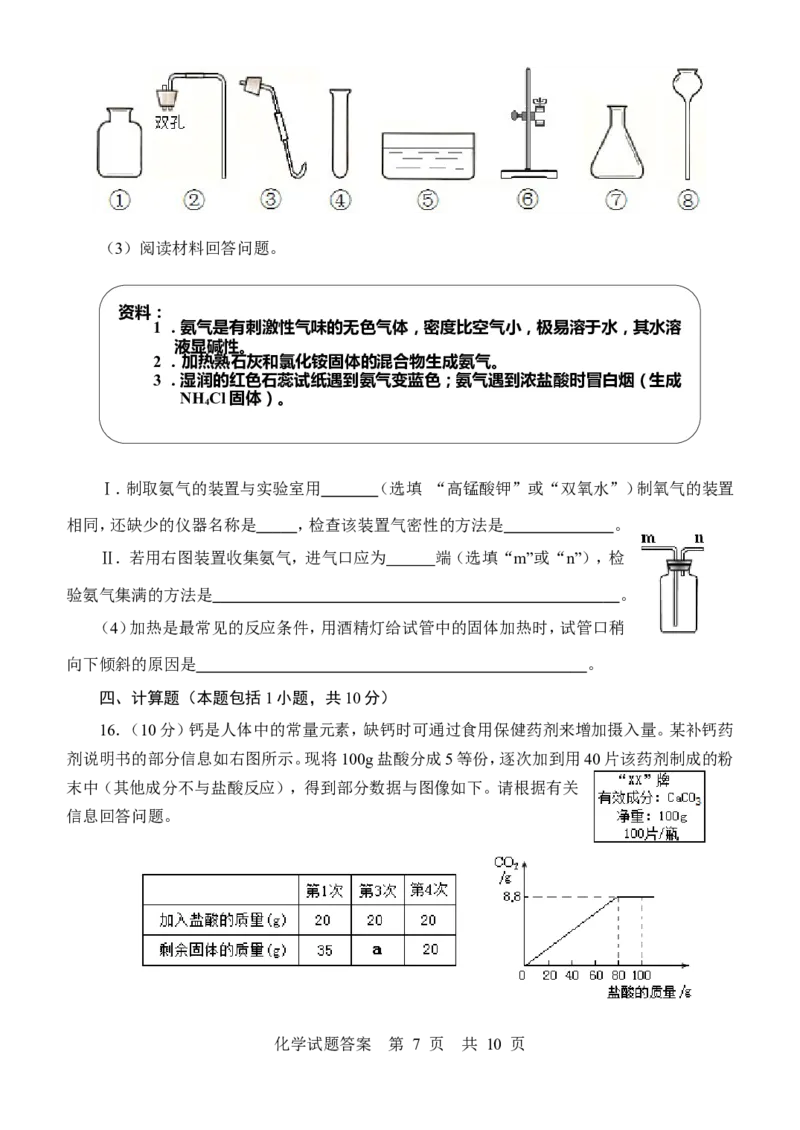
15.(13分)下图是实验室制取氧气或二氧化碳时经常用到的仪器,请回答有关问题。
(1)写出编号仪器名称:① ;⑧ 。
(2)当制取较多量CO 时,制取装置的仪器组合是 (选填序号)。
2
化学试题答案 第 6 页 共 10 页(3)阅读材料回答问题。
资料:
1.氨气是有刺激性气味的无色气体,密度比空气小,极易溶于水,其水溶
液显碱性。
2.加热熟石灰和氯化铵固体的混合物生成氨气。
3.湿润的红色石蕊试纸遇到氨气变蓝色;氨气遇到浓盐酸时冒白烟(生成
NH Cl固体)。
4
Ⅰ.制取氨气的装置与实验室用 (选填 “高锰酸钾”或“双氧水”)制氧气的装置
相同,还缺少的仪器名称是 ,检查该装置气密性的方法是 。
Ⅱ.若用右图装置收集氨气,进气口应为 端(选填“m”或“n”),检
验氨气集满的方法是 。
(4)加热是最常见的反应条件,用酒精灯给试管中的固体加热时,试管口稍
向下倾斜的原因是 。
四、计算题(本题包括1小题,共10分)
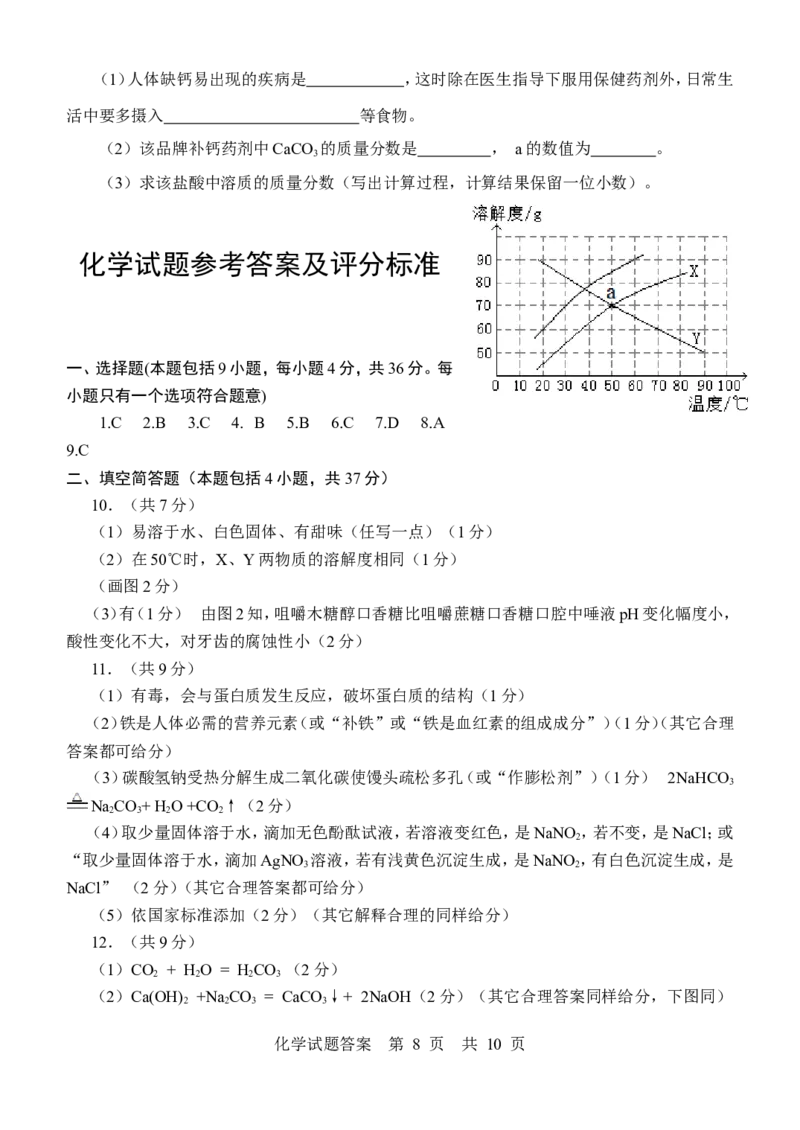
16.(10分)钙是人体中的常量元素,缺钙时可通过食用保健药剂来增加摄入量。某补钙药
剂说明书的部分信息如右图所示。现将100g盐酸分成5等份,逐次加到用40片该药剂制成的粉
末中(其他成分不与盐酸反应),得到部分数据与图像如下。请根据有关
信息回答问题。
化学试题答案 第 7 页 共 10 页(1)人体缺钙易出现的疾病是 ,这时除在医生指导下服用保健药剂外,日常生
活中要多摄入 等食物。
(2)该品牌补钙药剂中CaCO 的质量分数是 , a的数值为 。
3
(3)求该盐酸中溶质的质量分数(写出计算过程,计算结果保留一位小数)。
化学试题参考答案及评分标准
一、选择题(本题包括9小题,每小题4分,共36分。每
小题只有一个选项符合题意)
1.C 2.B 3.C 4. B 5.B 6.C 7.D 8.A
9.C
二、填空简答题(本题包括4小题,共37分)
10.(共7分)
(1)易溶于水、白色固体、有甜味(任写一点)(1分)
(2)在50℃时,X、Y两物质的溶解度相同(1分)
(画图2分)
(3)有(1分) 由图2知,咀嚼木糖醇口香糖比咀嚼蔗糖口香糖口腔中唾液pH变化幅度小,
酸性变化不大,对牙齿的腐蚀性小(2分)
11.(共9分)
(1)有毒,会与蛋白质发生反应,破坏蛋白质的结构(1分)
(2)铁是人体必需的营养元素(或“补铁”或“铁是血红素的组成成分”)(1分)(其它合理
答案都可给分)
(3)碳酸氢钠受热分解生成二氧化碳使馒头疏松多孔(或“作膨松剂”)(1分) 2NaHCO
3
NaCO+ H O +CO ↑(2分)
2 3 2 2
(4)取少量固体溶于水,滴加无色酚酞试液,若溶液变红色,是NaNO ,若不变,是NaCl;或
2
“取少量固体溶于水,滴加AgNO 溶液,若有浅黄色沉淀生成,是NaNO ,有白色沉淀生成,是
3 2
NaCl” (2分)(其它合理答案都可给分)
(5)依国家标准添加(2分)(其它解释合理的同样给分)
12.(共9分)
(1)CO + HO = HCO (2分)
2 2 2 3
(2)Ca(OH) +Na CO = CaCO ↓+ 2NaOH(2分)(其它合理答案同样给分,下图同)
2 2 3 3
化学试题答案 第 8 页 共 10 页(3)(每空0.5分,共5分)
13.(共12分)
(1)物理(1分) 结晶(1分) 1.21 g•mL-1~1.26 g•mL-1(或“1.21 g•mL-1~1.26 g•mL-1”也
对)(1分) 因为当海水的密度在1.21 g•mL-1~1.26 g•mL-1 时NaCl析出的较多而其它物质析出
较少,所剩母液中MgCl 的浓度也较高(2分)
2
(2)石灰乳(1分) Mg(OH) + 2HCl = MgCl + 2HO(2分) CuSO(1分)、MgSO(1
2 2 2 4 4
分)(或“CuCl 、MgCl ”等其它合理答案都给分)
2 2
BCD(2分)(错选、漏选1个倒扣1分,但不出现负分)
三、实验题(本题包括2小题,共17分)
14.(共4分)ACDE(每选对一个得1分,错选、漏选1个倒扣1分,但不出现负分)
15.(共13分)
(1)集气瓶(1分) 长颈漏斗(1分)
(2) ②⑦⑧(或“①②⑦⑧”)(2分)(错选、漏选1个倒扣1分,但不出现负分)
(3)高锰酸钾(1分) 酒精灯(1分) 将导气管口放入水中,用双手捂住大试管,观察是否
有气泡冒出,松开手冷却后,水进入导气管形成一小段水柱(2分) n(1分) 将湿润的红色石
蕊试纸放在出气口(集气瓶口),试纸变蓝色说明集满(或“用玻璃棒蘸取浓盐酸放在出气口,
有白烟生成说明集满”)(2分)
(4)由于固体含有水分或受热生成水蒸气,可防止水蒸气在试管口处冷凝、倒流,引起试管炸
裂(2分)
四、计算题(本题包括1小题,共10分)
16.(共10分)
(1)患佝偻病(或“骨质疏松”)(1分) 奶类、水产品、肉类、豆类(答出两种即可)(1分)
(2)50%(2分) 25(1分)
(3)设参加反应的盐酸中HCl的质量为x
CaCO +2HCl = CaCl + H O + CO↑…………………………………(2分)
3 2 2 2
2×36.5 44
x 8.8g
化学试题答案 第 9 页 共 10 页(1分)
…………………………………………
x = 14.6g…………………………………………(1分)
盐酸中HCl的质量分数为: …………(1分)
答:盐酸中HCl的质量分数为18.3%。
化学试题答案 第 10 页 共 10 页