文档内容
参考答案与试题解析
一、选择题
1. (6分)
答案:D
解析:
乙醚、75%乙醇等消毒剂中,乙醇因分子间氢键与水任意比混溶。
NaClO通过强氧化性破坏病毒结构实现灭活。
过氧乙酸(CH₃COOOH)分子量为12×2+4+16×3=76,计算正确。
氯仿化学名称为三氯甲烷,而非四氯化碳(CCl₄)。
2. (6分)
答案:B
解析:
分子式C₁₄H₁₄O₄符合不饱和度计算(8个不饱和键)。
含碳碳双键及邻位碳氢键的醇羟基,可被酸性重铬酸钾氧化变色。
酯基(—COO—)可发生水解反应。
与—OH相连碳的邻位碳含氢原子,可发生消去反应生成双键。
3. (6分)
答案:A
解析:
SO₂与H₂S均能被酸性高锰酸钾氧化(SO₂→SO₄²⁻,H₂S→S),无法选择性去除
H₂S。
Cl₂(HCl)通过饱和食盐水时,HCl溶解而Cl₂逸出。
N₂(O₂)通过灼热铜网,O₂反应生成CuO而被除去。
NO(NO₂)通过NaOH溶液,NO₂反应生成盐,NO不反应。
4. (6分)
答案:C
解析:
第1页 | 共7页 CH₃COI在反应路径中生成后被消耗,是中间体。
总反应为CH₃OH+CO→CH₃CO₂H,符合质量守恒。
Rh成键数在循环中变化:4→6→5→6→4,并非恒定。
路径中存在CH₃OH+HI→CH₃I+H₂O的取代反应。
5. (6分)
答案:B
解析:
由核反应守恒推知:W=27,Z=13(X为Al),Y质子数15(P)。
Al(X)相对原子质量为27,非26Z。
AlCl₃与PCl₃均可稳定存在。
原子半径:Al>P(同周期递减)。
P含H₃PO₄、HPO₃等多种含氧酸。
6. (6分)
答案:D
解析:
放电负极反应:Zn-2e⁻+4OH⁻→Zn(OH)₄²⁻。
CO₂→HCOOH,碳化合价+4→+2,转移2mol电子。
充电总反应:2Zn(OH)₄²⁻→2Zn+O₂↑+4OH⁻+2H₂O。
充电时正极析氧反应消耗OH⁻,导致OH⁻浓度降低。
7. (6分)
答案:C
解析:
曲线①为δ(HA⁻),曲线②为δ(A²⁻)(终点时A²⁻主导)。
终点消耗NaOH 40.00mL,按2NaOH~H₂A计算,c(H₂A)=0.1000mol·L⁻¹。
HA⁻电离常数:Kₐ=c(H⁺)·c(A²⁻)/c(HA⁻)≈10⁻¹×0.1/0.9=1.0×10⁻²。
终点电荷守恒:c(Na⁺)+c(H⁺)=2c(A²⁻)+c(HA⁻)+c(OH⁻),因碱性环境c(Na⁺)>2c(A²⁻)
+c(HA⁻)。
第2页 | 共7页二、非选择题
(一)必考题
8. (14分)
答案:
(1) 加快酸浸和氧化反应速率
(2) Fe²⁺; VO⁺+2H⁺+MnO₂=VO₂⁺+Mn²⁺+H₂O
(3) K⁺、Mg²⁺、Na⁺、Mn²⁺及部分Al³⁺/Fe³⁺
(4) Fe(OH)₃
(5) NaAlO₂+HCl+H₂O→Al(OH)₃↓+NaCl
(6) 同离子效应促进NH₄VO₃析出
解析:
(1) 升温加速酸溶及MnO₂氧化VO⁺/VO²⁺过程。
(2) Fe²⁺同步被氧化为Fe³⁺;VO⁺氧化离子方程式如答案。
(3) pH=3.0~3.1时,K⁺、Mg²⁺等留在滤液,部分Al³⁺/Fe³⁺未完全沉淀。
(4) 强碱性条件下Fe³⁺转化为Fe(OH)₃滤渣。
(5) 偏铝酸钠与盐酸反应生成Al(OH)₃沉淀。
(6) 过量NH₄⁺降低NH₄VO₃溶解度,提高产率。
9. (15分)
答案:
(1) 烧杯、量筒、托盘天平
(2) KCl
(3) 石墨
(4) 0.09
(5) Fe-2e⁻→Fe²⁺;Fe³⁺+e⁻→Fe²⁺;Fe³⁺;Fe
(6) 取活化液滴加KSCN,不变红即活化完成
解析:
(1) 配制FeSO₄溶液需称量、溶解、定容仪器。
(2) KCl离子迁移率相近且不与体系反应。
(3) 电子由铁流向石墨,阳离子(K⁺)向正极(石墨)迁移。
(4) Fe²⁺增加0.02mol·L⁻¹,石墨区Fe²⁺增加0.04mol·L⁻¹(原0.05mol·L⁻¹)。
第3页 | 共7页 (5) 电极反应及氧化还原性比较如答案。
(6) Fe³⁺被还原后,SCN⁻检验无红色表明活化完成。
10. (14分)
答案:
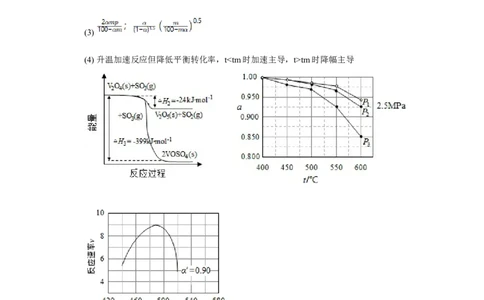
(1) 2V₂O₅(s)+2SO₂(g)=2VOSO₄(s)+V₂O₄(s) ΔH=-351kJ·mol⁻¹
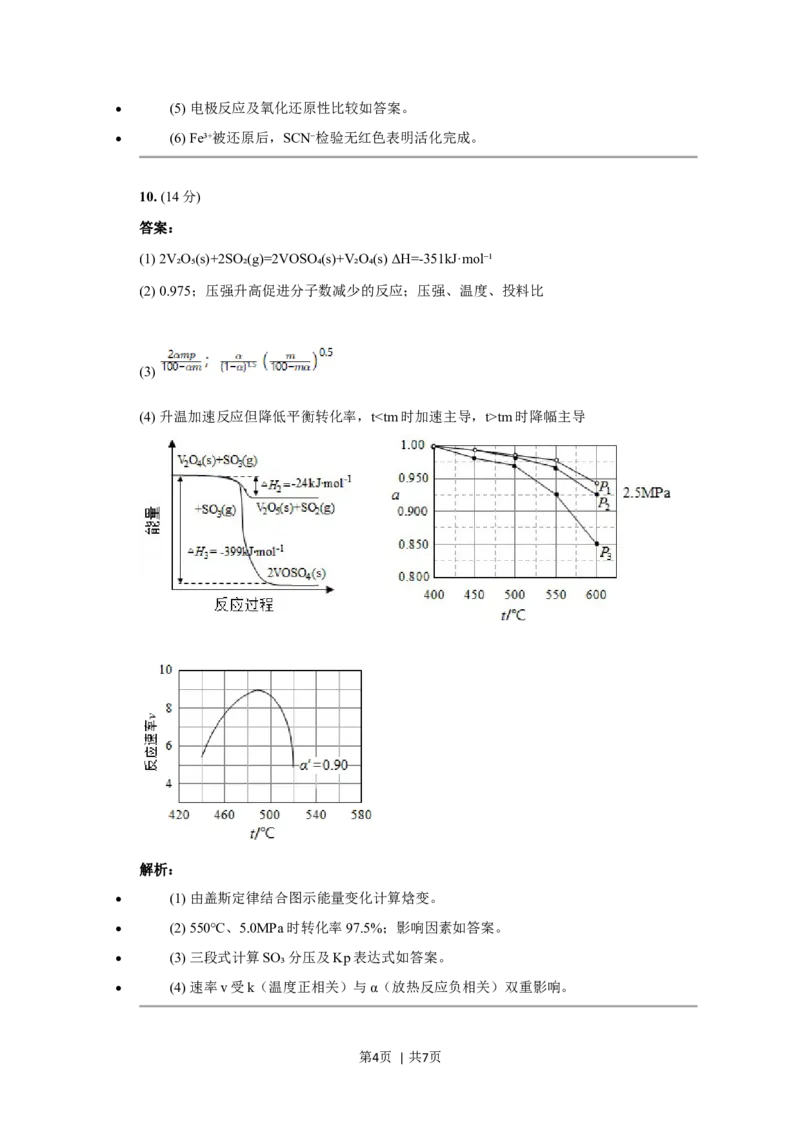
(2) 0.975;压强升高促进分子数减少的反应;压强、温度、投料比
(3)
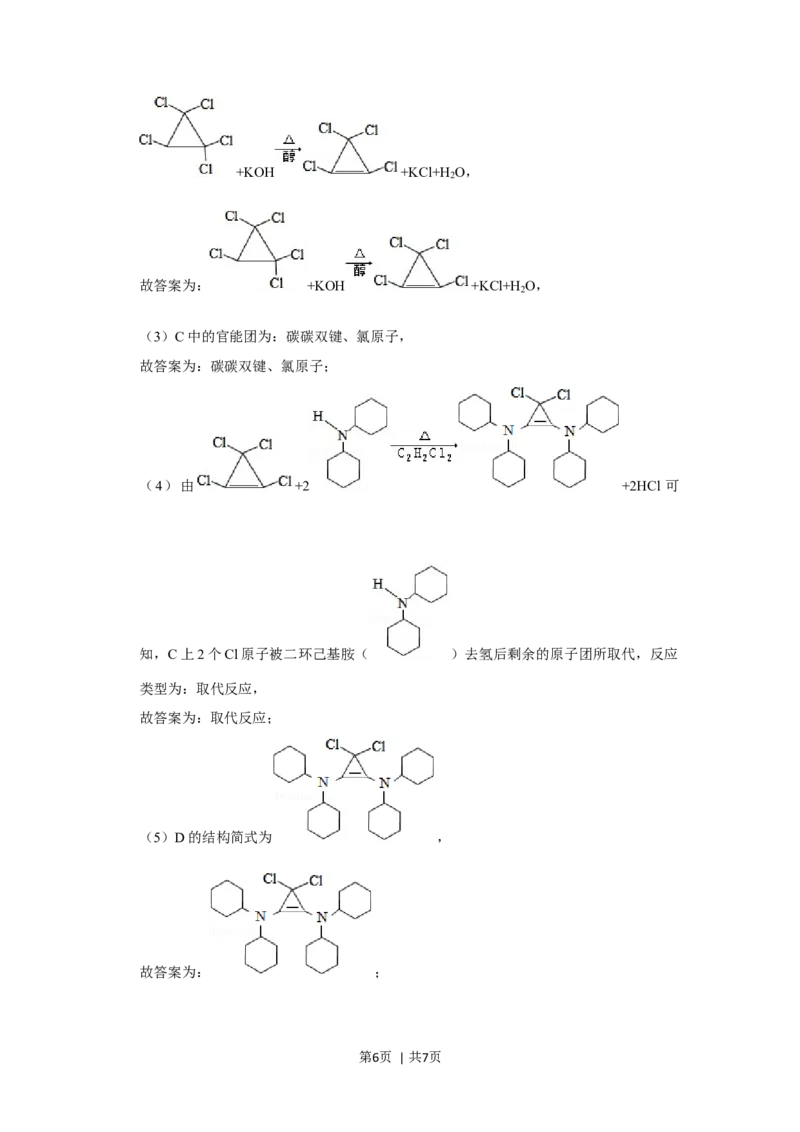
(4) 升温加速反应但降低平衡转化率,ttm时降幅主导
解析:
(1) 由盖斯定律结合图示能量变化计算焓变。
(2) 550℃、5.0MPa时转化率97.5%;影响因素如答案。
(3) 三段式计算SO₃分压及Kp表达式如答案。
(4) 速率v受k(温度正相关)与α(放热反应负相关)双重影响。
第4页 | 共7页(二)选考题
[化学—选修3:物质结构与性质]
11.
解析:
(1) Fe²⁺(d⁶)未成对电子4个,Fe³⁺(d⁵)未成对电子5个。
(2) 同族电离能递变规律及Be全满结构特例。
(3) PO₄³⁻价层电子对4,无孤对电子,正四面体构型。
(4) 晶胞含4个LiFePO₄单元;x=棱心Li⁺(1/4)+面心Li⁺(1/2)的占比;Fe²⁺:Fe³⁺=13:3
由电荷守恒推算。
[化学—选修5:有机化学基础]
12. (15分)
【解答】解:(1)A(C HCl )名称为三氯乙烯,
2 3
故答案为:三氯乙烯;
(2)有分析得出,由B发生消去反应生成C的化学方程式为:
第5页 | 共7页+KOH +KCl+H O,
2
故答案为: +KOH +KCl+H O,
2
(3)C中的官能团为:碳碳双键、氯原子,
故答案为:碳碳双键、氯原子;
(4)由 +2 +2HCl 可
知,C上2个Cl原子被二环己基胺( )去氢后剩余的原子团所取代,反应
类型为:取代反应,
故答案为:取代反应;
(5)D的结构简式为 ,
故答案为: ;
第6页 | 共7页(6)E( )的六元环芳香同分异构体中,与钠反应产生氢气,说明含有羟
基,且核磁共振氢谱有四组峰,峰面积之比为6:2:2:1;说明有两个甲基且对称;又
因苯胺与甲基吡啶互为芳香同分异构体,所以同分异构体的结构简式分别为: ,
, , , , 共6种,其中,芳香环上为二
取代的结构简式为 ,
故答案为:6; 。
【点评】本题考查学生对有机化学基础的理解和掌握,题目难度中等,掌握有机的命名、
反应类型、化学反应原理、同分异构等,明确化学反应及同分异构的书写是解题关键。
同时考查了阅读题目获取新信息的能力,需要学生具备扎实的基础与综合运用知识、信
息分析解决问题能力。
第7页 | 共7页