文档内容
柳州市 2026 届新高三摸底考试
化学
(考试时间 75 分钟 满分 100 分)
注意:1. 请把答案填写在答题卡上,否则答题无效。
2. 答卷前,考生务必将密封线内的项目填写清楚,密封线内不要答题。
3. 选择题,请用 2B 铅笔,把答题卡上对应题目选项的信息点涂黑。非选择
题,请用 0.5mm 黑色字迹签字笔在答题卡指定位置作答。
0.16
一、选择题 (本题共 14 小题, 每小题 3 分, 共 42 分。在每小题给出的四个选项中,
只有一项是 符合题目要求的。)
1. 化学与生活、生产息息相关。下列说法错误的是
A. 铁粉具有还原性, 可用作食品干燥剂
B. 莲藕中富含淀粉, 淀粉可水解为葡萄糖
C. Na CO 溶液呈碱性,可用于去除油污
2 3
D. 清洗铁锅后及时擦干,能减缓铁锅生锈
2. 下列化学用语或图示表示错误的是
A. K+ 的结构示意图: B. NaCl 的电子式: Na:C˙l:
C. 质量数为 16 的氧原子: ❑ 16O D. 乙烯的结构简式: CH =CH
8 2 2
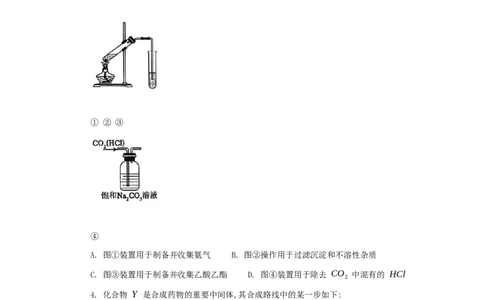
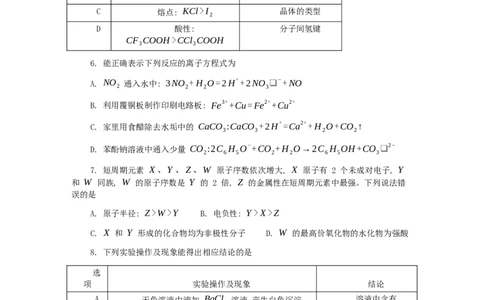
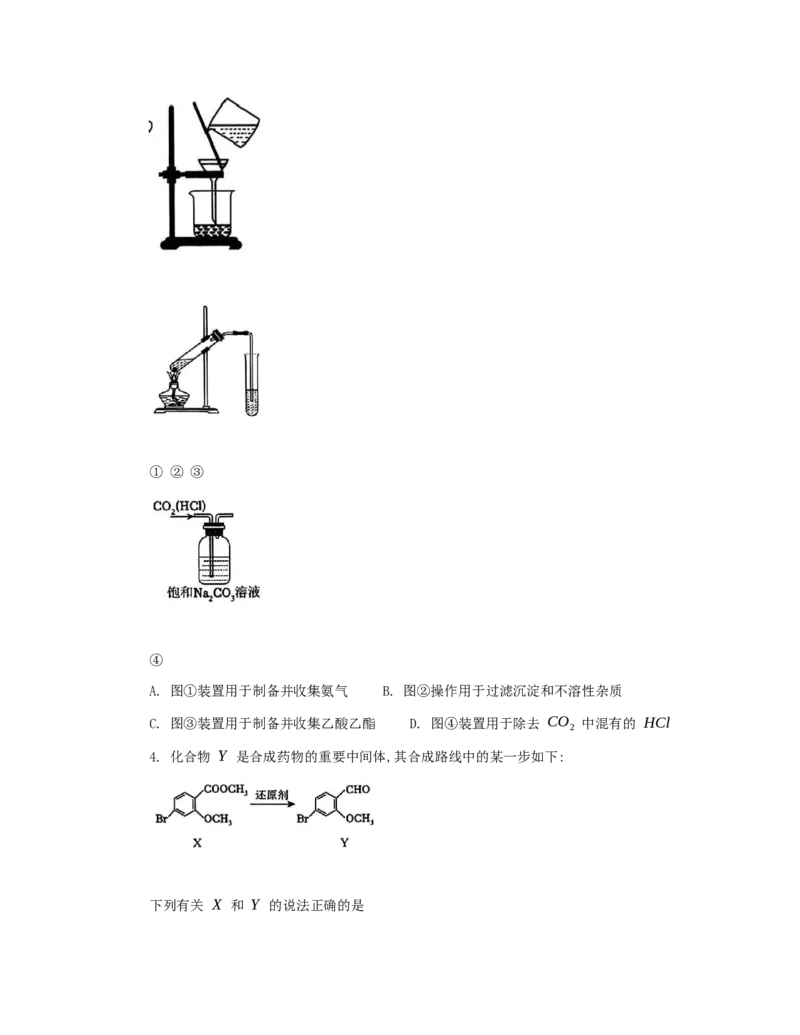
3. 下列实验装置(部分夹持装置已省略)使用或操作正确的是① ② ③
④
A. 图①装置用于制备并收集氨气 B. 图②操作用于过滤沉淀和不溶性杂质
C. 图③装置用于制备并收集乙酸乙酯 D. 图④装置用于除去 CO 中混有的 HCl
2
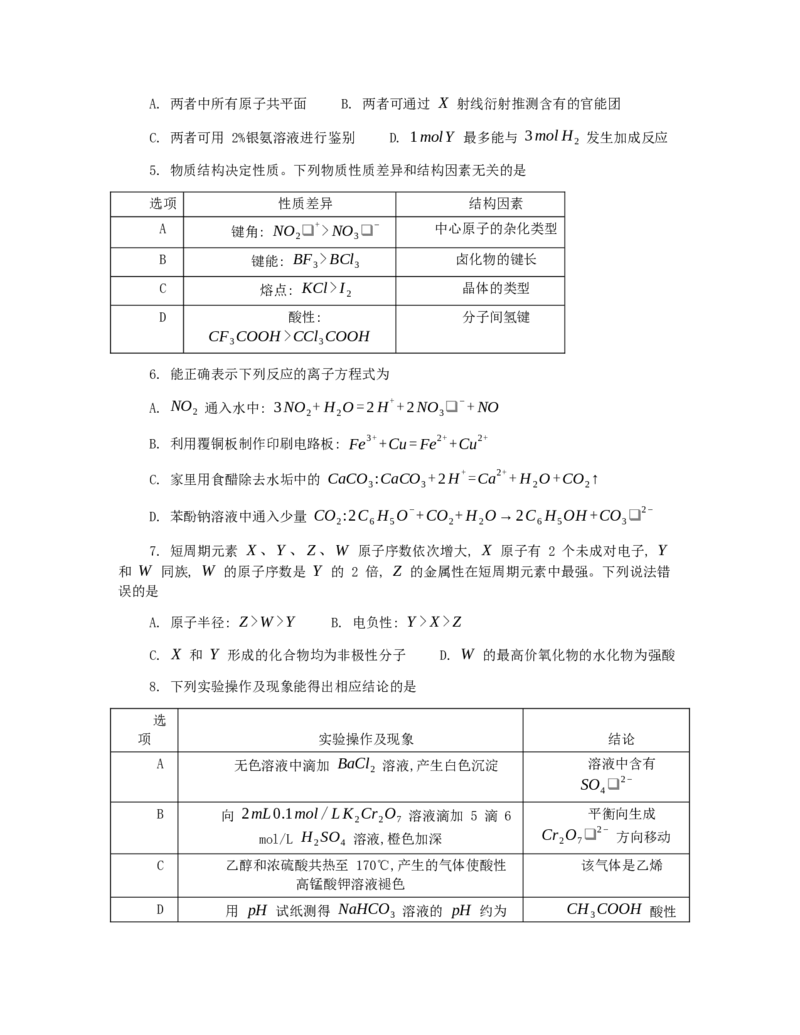
4. 化合物 Y 是合成药物的重要中间体,其合成路线中的某一步如下:
下列有关 X 和 Y 的说法正确的是A. 两者中所有原子共平面 B. 两者可通过 X 射线衍射推测含有的官能团
C. 两者可用 2%银氨溶液进行鉴别 D. 1molY 最多能与 3molH 发生加成反应
2
5. 物质结构决定性质。下列物质性质差异和结构因素无关的是
选项 性质差异 结构因素
A 键角: NO ❑ +>NO ❑ − 中心原子的杂化类型
2 3
B 键能: BF >BCl 卤化物的键长
3 3
C 熔点: KCl>I 晶体的类型
2
D 酸性: 分子间氢键
CF COOH>CCl COOH
3 3
6. 能正确表示下列反应的离子方程式为
A. NO 通入水中: 3NO +H O=2H++2NO ❑ −+NO
2 2 2 3
B. 利用覆铜板制作印刷电路板: Fe3++Cu=Fe2++Cu2+
C. 家里用食醋除去水垢中的 CaCO :CaCO +2H+=Ca2++H O+CO ↑
3 3 2 2
D. 苯酚钠溶液中通入少量 CO :2C H O−+CO +H O→2C H OH+CO ❑ 2−
2 6 5 2 2 6 5 3
7. 短周期元素 X、Y、Z、W 原子序数依次增大, X 原子有 2 个未成对电子, Y
和 W 同族, W 的原子序数是 Y 的 2 倍, Z 的金属性在短周期元素中最强。下列说法错
误的是
A. 原子半径: Z>W>Y B. 电负性: Y>X>Z
C. X 和 Y 形成的化合物均为非极性分子 D. W 的最高价氧化物的水化物为强酸
8. 下列实验操作及现象能得出相应结论的是
选
项 实验操作及现象 结论
A 无色溶液中滴加 BaCl 溶液,产生白色沉淀 溶液中含有
2
SO ❑ 2−
4
B 向 2mL0.1mol/LK Cr O 溶液滴加 5 滴 6 平衡向生成
2 2 7
mol/L H SO 溶液,橙色加深 Cr O ❑ 2− 方向移动
2 4 2 7
C 乙醇和浓硫酸共热至 170℃,产生的气体使酸性 该气体是乙烯
高锰酸钾溶液褪色
D 用 pH 试纸测得 NaHCO 溶液的 pH 约为 CH COOH 酸性
3 39, C H COONa溶液的pH约为 10 强于 H CO
3 2 3
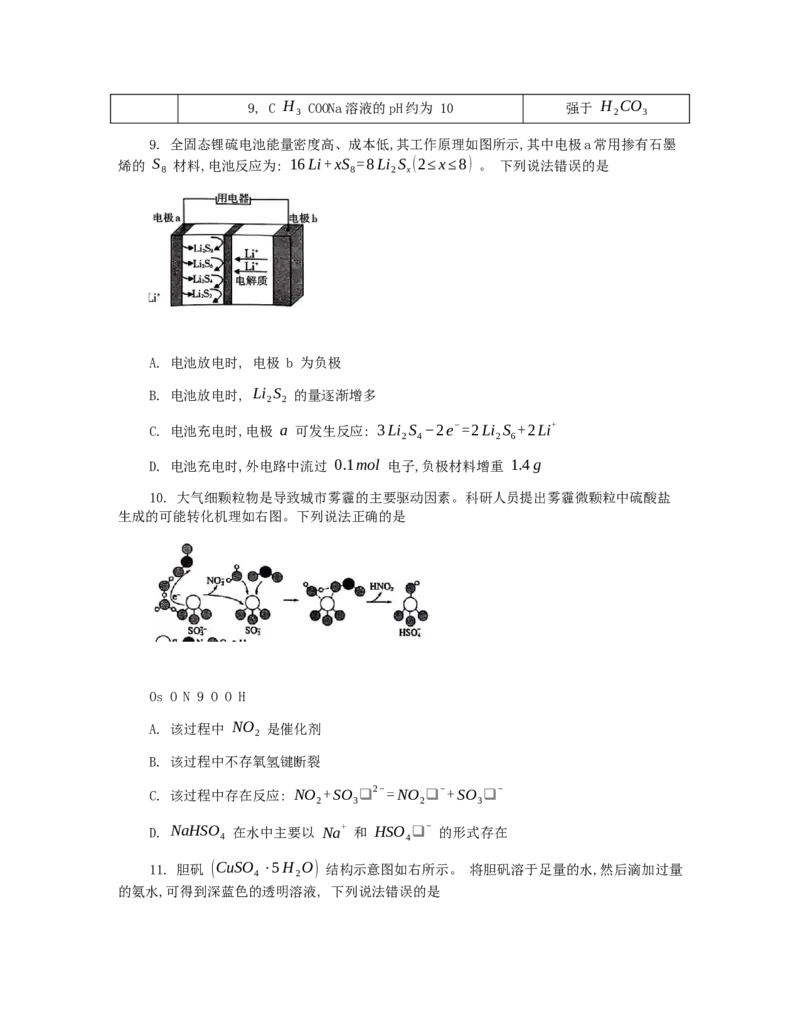
9. 全固态锂硫电池能量密度高、成本低,其工作原理如图所示,其中电极a常用掺有石墨
烯的 S 材料,电池反应为: 16Li+xS =8Li S (2≤x≤8) 。 下列说法错误的是
8 8 2 x
A. 电池放电时, 电极 b 为负极
B. 电池放电时, Li S 的量逐渐增多
2 2
C. 电池充电时,电极 a 可发生反应: 3Li S −2e−=2Li S +2Li+
2 4 2 6
D. 电池充电时,外电路中流过 0.1mol 电子,负极材料增重 1.4g
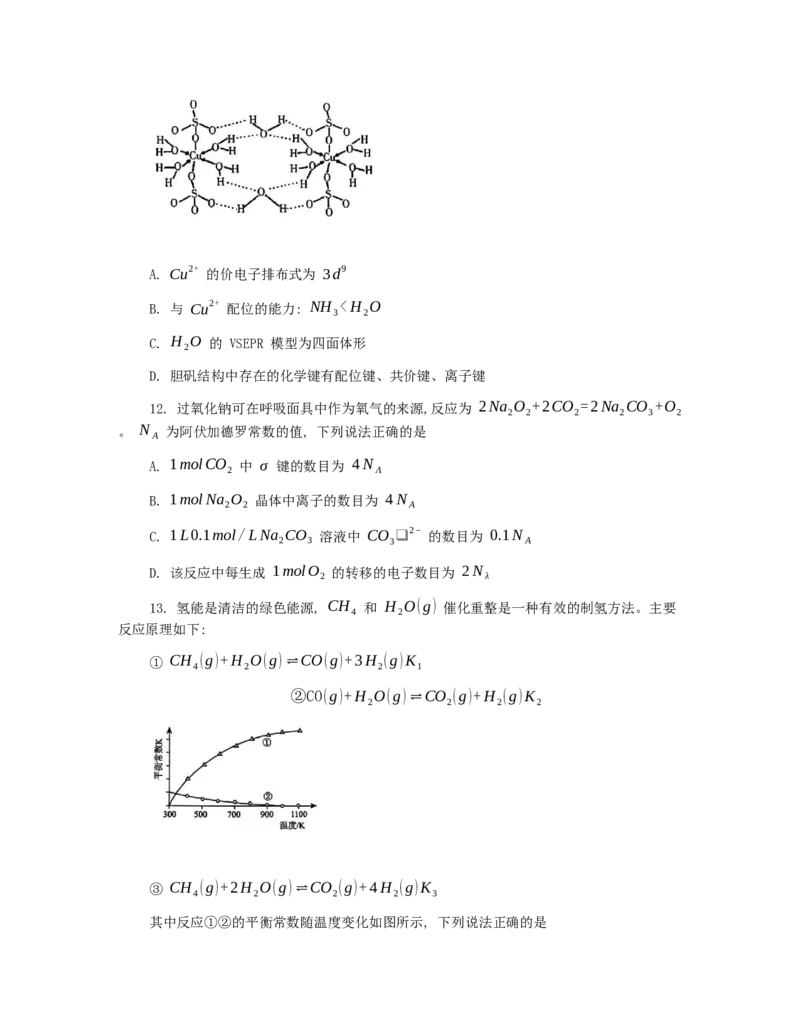
10. 大气细颗粒物是导致城市雾霾的主要驱动因素。科研人员提出雾霾微颗粒中硫酸盐
生成的可能转化机理如右图。下列说法正确的是
Os O N 9 O O H
A. 该过程中 NO 是催化剂
2
B. 该过程中不存氧氢键断裂
C. 该过程中存在反应: NO +SO ❑ 2−=NO ❑ −+SO ❑ −
2 3 2 3
D. NaHSO 在水中主要以 Na+ 和 HSO ❑ − 的形式存在
4 4
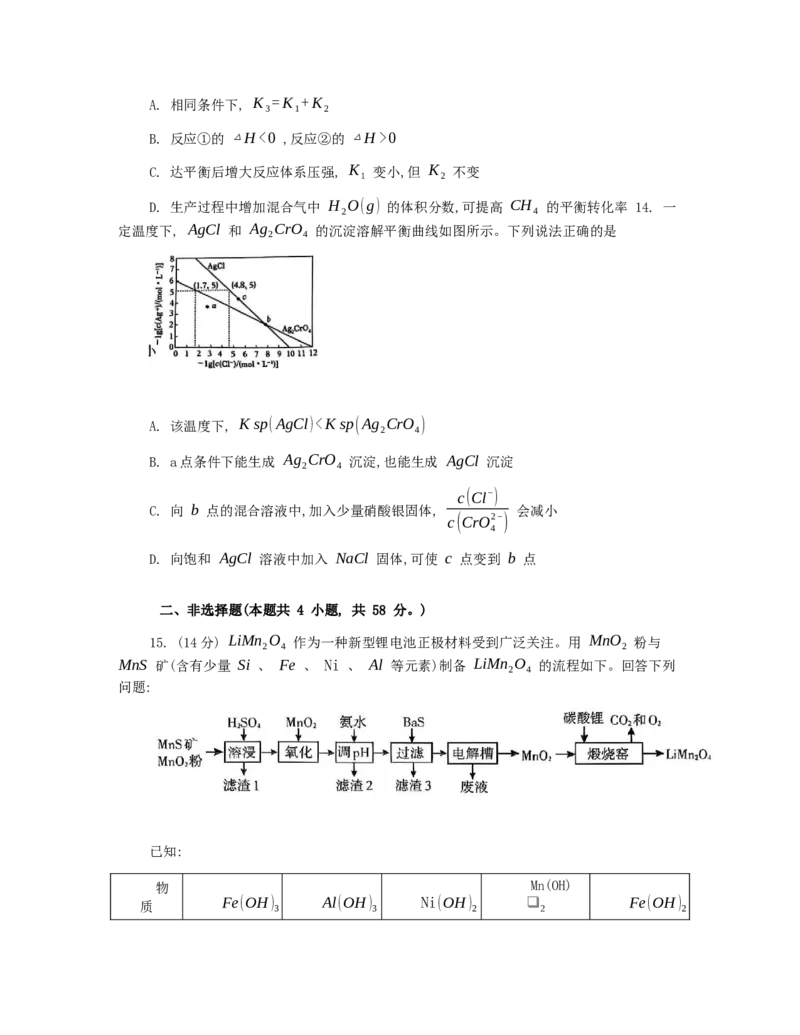
11. 胆矾 (CuSO ⋅5H O) 结构示意图如右所示。 将胆矾溶于足量的水,然后滴加过量
4 2
的氨水,可得到深蓝色的透明溶液, 下列说法错误的是A. Cu2+ 的价电子排布式为 3d9
B. 与 Cu2+ 配位的能力: NH 0
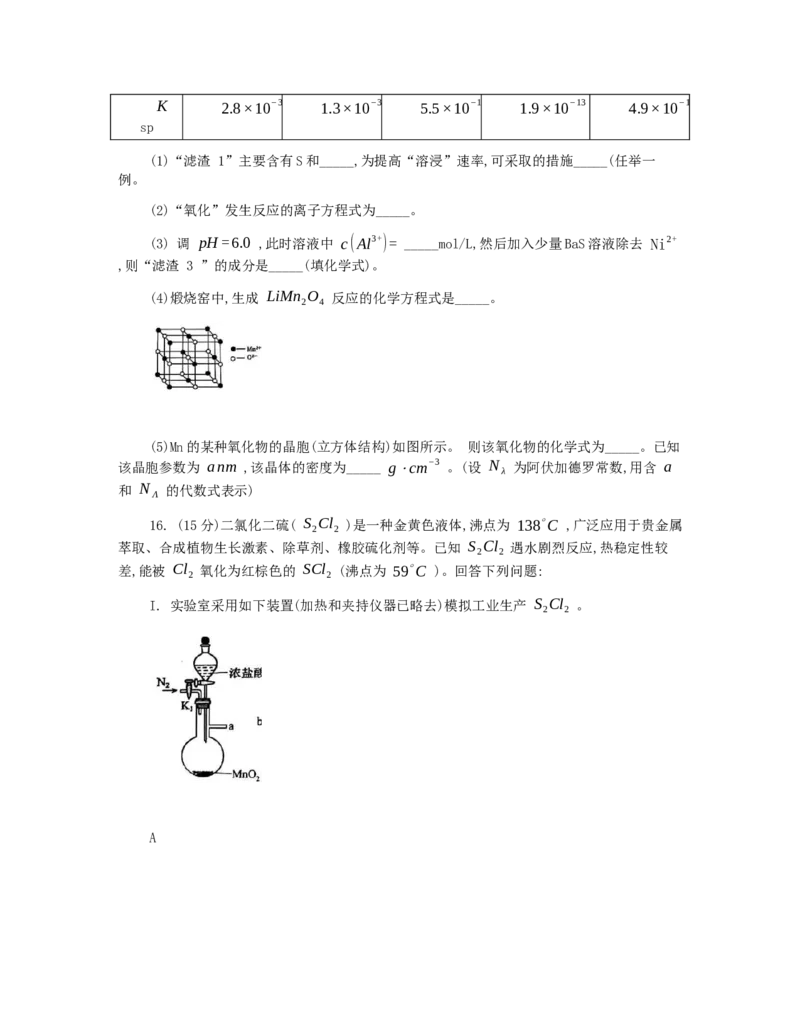
C. 达平衡后增大反应体系压强, K 变小,但 K 不变
1 2
D. 生产过程中增加混合气中 H O(g) 的体积分数,可提高 CH 的平衡转化率 14. 一
2 4
定温度下, AgCl 和 Ag CrO 的沉淀溶解平衡曲线如图所示。下列说法正确的是
2 4
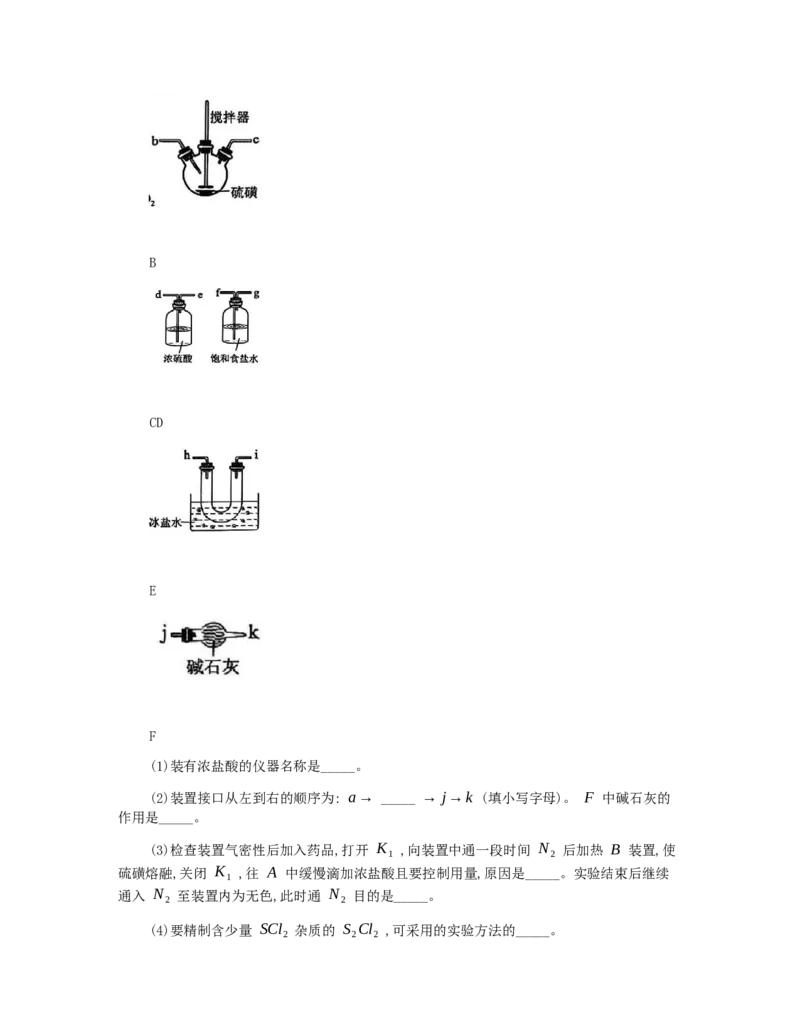
A. 该温度下, Ksp(AgCl)” "<"或"=")。
(正) (逆)
(5)我国科学家以悬浮纳米 Fe O 作催化剂,直接常压电化学合成氨, 工作原理如图所
2 3
示, 阴极的电极反应式为_____。
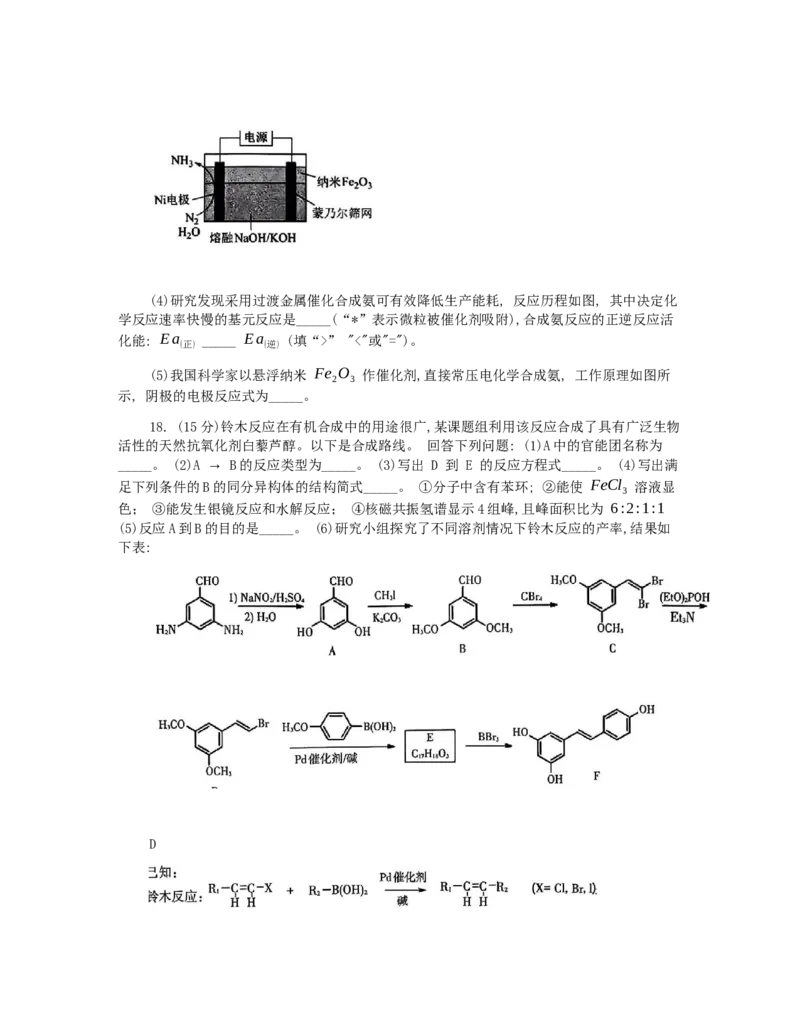
18. (15分)铃木反应在有机合成中的用途很广,某课题组利用该反应合成了具有广泛生物
活性的天然抗氧化剂白藜芦醇。以下是合成路线。 回答下列问题: (1)A中的官能团名称为
_____。 (2)A → B的反应类型为_____。 (3)写出 D 到 E 的反应方程式_____。 (4)写出满
足下列条件的B的同分异构体的结构简式_____。 ①分子中含有苯环; ②能使 FeCl 溶液显
3
色; ③能发生银镜反应和水解反应; ④核磁共振氢谱显示4组峰,且峰面积比为 6:2:1:1
(5)反应A到B的目的是_____。 (6)研究小组探究了不同溶剂情况下铃木反应的产率,结果如
下表:
D溶剂 碱 产率
乙醇/水 KOH 83.9%
NN-二甲基甲酰 KOH 79%
胺/水
水 KOH 15%
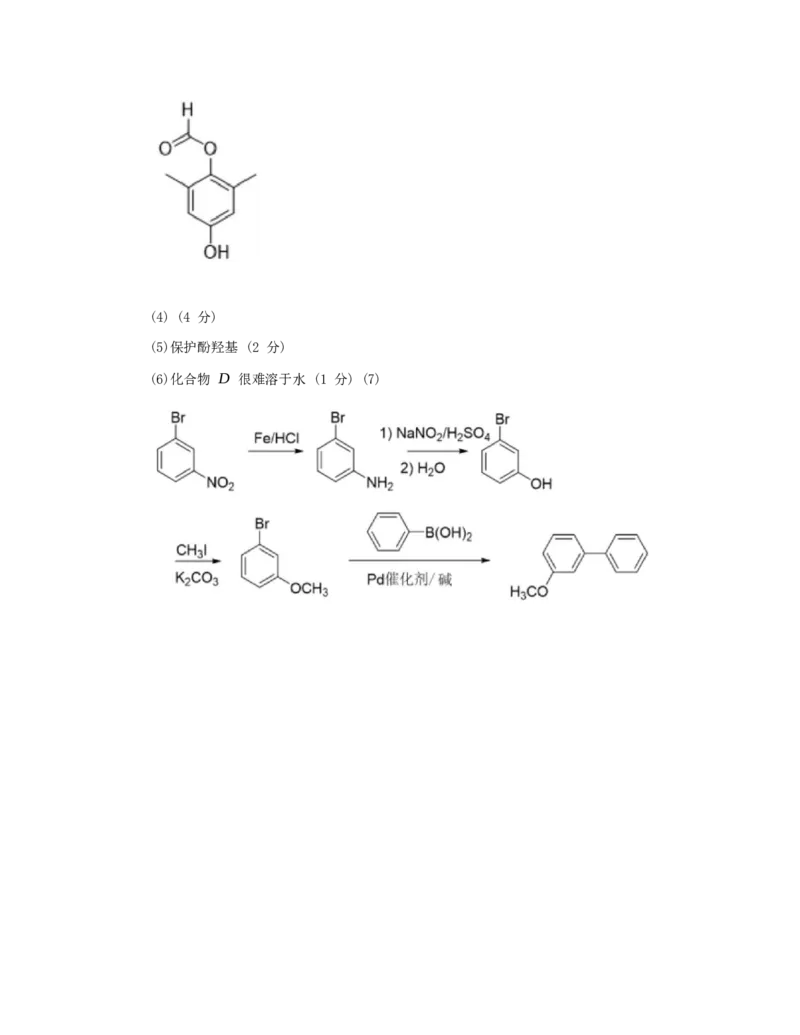
用水做溶剂时产率较低的主要原因是_____。 (7)以 1 - B(OH) 为主要有机原料(无机
2
试剂任选),设计
NO
2
的合成路线。
柳州市 2026 届新高三摸底考试化学参考答案
一、选择题
题号 1 2 3 4 5 6 7
答案 A B A C D A C
题号 8 9 10 11 12 13 14
答案 B D C B D D B
二、非选择题
15.(14分) (1) SiO (或硅酸)(1 分) 粉碎矿石(搅拌、适当升温等符合题意即可得分)
2
(1 分) (2) 2Fe2++MnO +4H+=2Fe3++Mn2++2H O (2 分) (3) 1.3×10−9 (2 分)
2 2
BaSO 、 NiS(2分) (4) 2Li CO +8MnO 震烧 4LiMn O +2CO ↑+O ↑ (2 分) (5)
4 2 3 2 2 4 2 2
284
MnO (2 分) (2 分) 16.(15 分) (1)分液漏斗 (1 分) (2)
N (a×10−7) 3
A
f →g→d→e→b→c→h→i (2 分) 吸收多余的氯气,防止空气中的水蒸气进入装置 (2
分) (3)使 Cl 与 S 充分接触,防止 S Cl 被 Cl 氧化为 SCl (2分) 将装置内的氯气排入
2 2 2 2 2
F 中吸收,将 B 中残留的 S Cl 排入 E 中收集( 2 分)
2 2(4)蒸馏(或分馏) (2 分)
(5) 2S Cl +2H O=4HCl+SO ↑+3S↓ (2 分)
2 2 2 2
270b
(6) ×100% (2 分)
233a
17.(14分)
(1) +90.1 (2 分) (2) BD (2 分)
(3) 4 (2 分)
(1 ) 2
×20
5 1
Kp= =
(1 ) (3 ) 3 432
×20 × ×20
5 5
(2 分)
(4) NH ∗+H∗=NH ∗ (2 分) (2 分)
2 3
(5) N +6e−+6H O=2NH +6OH− (2 分)
2 2 3
18.(15 分)
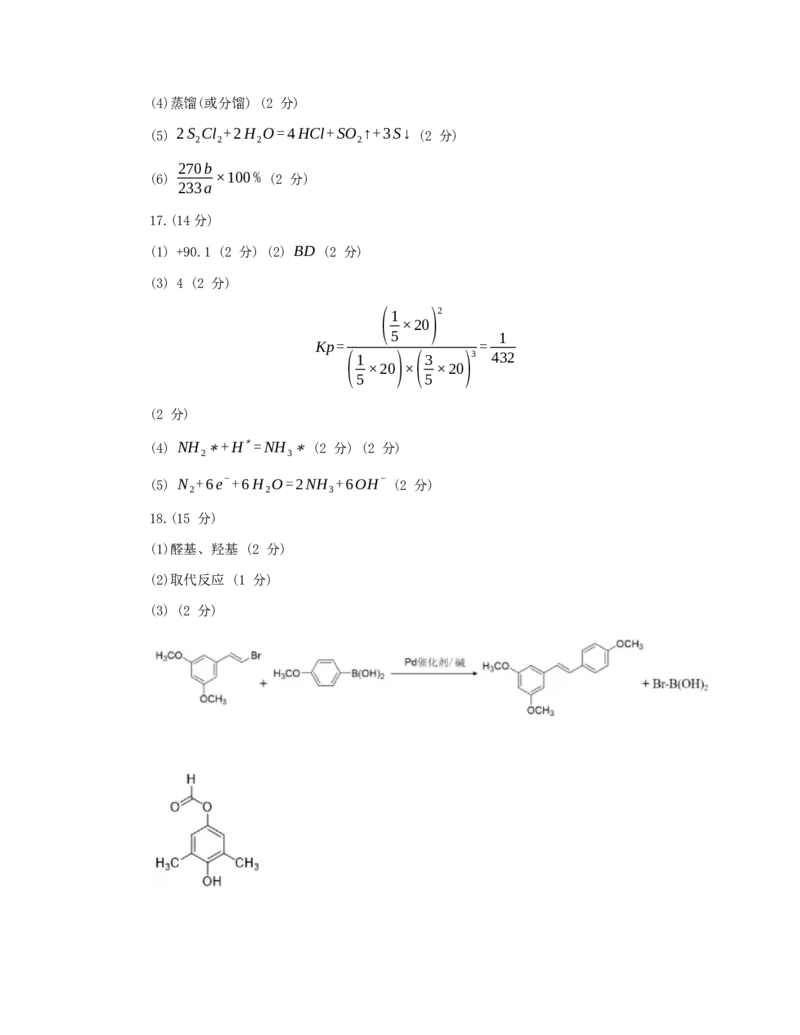
(1)醛基、羟基 (2 分)
(2)取代反应 (1 分)
(3) (2 分)(4) (4 分)
(5)保护酚羟基 (2 分)
(6)化合物 D 很难溶于水 (1 分) (7)