文档内容
A.原子半径:Z>Y>X>W
B.简单氢化物的沸点:Z>Y>X
高三化学试卷(二)
C.第一电离能:Y>X>Z
D.[Cu(W Z)]2+的空间结构为平面正方形,则Cu的杂化方式为sp3
(本试卷满分100分,考试时间75分钟) 2 4
5.下列物质用途和性质均正确且有对应关系的是 ( )
注意事项:1.答题前,考生务必用黑色字迹的签字笔或钢笔将自己的姓名、准考证号分别填写
A.碳酸钡可用作医疗钡餐,体现了碳酸钡的难溶性
在试卷和答题卡规定的位置上。
B.水玻璃可用于木材的防腐和粘合,体现了硅酸钠水溶液的碱性
2.答选择题时,选出每小题答案后,用2B铅笔把答题卡对应题目的答案涂黑,如需
C.浸泡有酸性高锰酸钾溶液的硅藻土可抑制水果早熟,体现了高锰酸钾的氧化性
改动,用橡皮擦干净后,再涂其它答案。非选择题的答案必须用黑色字迹的签字
D.向硫酸铜和硫酸铝的混合溶液中通入氨气可将两种金属元素分离,体现了氢氧化铝的两性
笔或钢笔写在答题卡上相应的区域内,写在本试卷上无效。
6.下列图示实验中操作规范的是 ( )
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Si-28 Br-80
一 、选 择 题 : 本 题 共 15 小 题 ,每 小 题 3分 , 共 4 5分 。 在 每 小 题 给 出 的 四 个选项中,只有一项符
合题目要求。
1.现代社会的发展与进步离不开材料,下列有关材料的说法不正确的是 ( )
A.“辽宁舰”上用于舰载机降落的阻拦索是一种特种钢缆,钢是合金
B.“超轻海绵”使用的石墨烯是新型无机非金属材料 A.将黄铁矿研磨成粉末状
C.某品牌手机使用的麒麟980芯片成分主要是二氧化硅 B.分离乙酸和乙酸乙酯的混合物
D.“中国天眼”FAST用到的碳化硅是一种新型陶瓷材料 C.配制NaCl标准液时,用于加速NaCl溶解
D.用标准浓度的溴水滴定未知浓度的KI溶液
2.下列操作不符合实验安全操作步骤的是 ( )
7.Fe3+在水溶液中易形成络合物,且根据络合能力不同,能相互之间转换。例如向 FeCl溶液
A.氢气还原氧化铜前,需先验纯 3
中加入KCO 溶液会生成黄绿色 K[Fe(CO)],若再加入盐酸,溶液又变为黄色,转换
2 2 4 3 2 4 3
B.进行硫粉燃烧实验中需佩戴护目镜
关系为K[Fe(CO)]+4HCl幑幐K[FeCl]+2KHCO +HCO。设 N 为阿伏加德罗
3 2 4 3 4 2 4 2 2 4 A
C.实验室制备氯气时应在通风橱中完成
常数的值,下列说法正确的是 ( )
D.蒸馏过程中若未加入沸石,应趁热立即加入
A.标准状况下,11.2LHCO 中含有氧原子的数目为2N
2 2 4 A
3.下列离子方程式能正确表示相应描述的是 ( ) B.1molK[FeCl]中含有σ键的数目为4N
4 A
A.工业上制备漂粉精:Cl+2OH-Cl-+ClO-+HO C.1L1mol·L-1KCO 溶液中含有CO2-的数目为N
2 2 2 2 4 2 4 A
B.用醋酸和KI溶液检验加碘盐:IO-+5I-+6H+3I+3HO D.K[Fe(CO)]被氧化时,转移电子的数目为6N
3 2 2 3 2 4 3 A
8.有机物M是一种制备营养神经药物的中间体,其结构简式如图所示。下列关于 M的说法
C.实验室用大理石制备CO:CaCO +2H+Ca2++HO+CO↑
2 3 2 2
错误的是 ( )
D.常温下,铁粉加入浓硝酸中:Fe+6H++3NO-Fe3++3NO↑+3HO
3 2 2
A.分子中所有碳原子可能共平面
4.某种含铜化合物在新能源的开发研究中具有重要的应用,其结构如图所示。W、X、Y、Z为
B.1molM最多能与5molH 发生加成反应
2
原子序数逐渐增大的短周期主族元素,X的基态原子中所有能级的电子数均相等且与 Z同
C.一定条件下可生成高聚物
周期。下列说法正确的是 ( )
D.核磁共振氢谱有7组峰
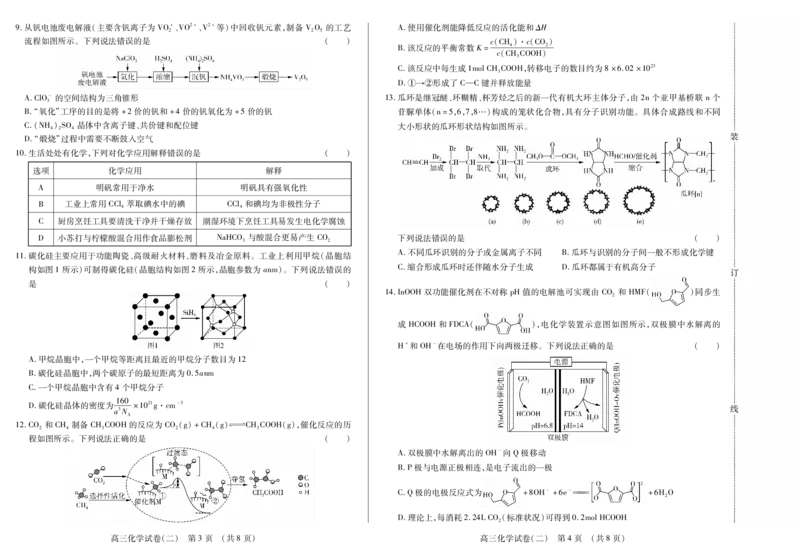
高三化学试卷(二) 第1页 (共8页) 高三化学试卷(二) 第2页 (共8页)9.从钒电池废电解液(主要含钒离子为 VO+、VO2+、V2+等)中回收钒元素,制备 VO 的工艺 A.使用催化剂能降低反应的活化能和ΔH
2 2 5
流程如图所示。下列说法错误的是 ( ) c(CH)·c(CO)
B.该反应的平衡常数K= 4 2
c(CHCOOH)
3
C.该反应中每生成1molCHCOOH,转移电子的数目约为8×6.02×1023
3
D.①→②形成了C—C键并释放能量
A.ClO-的空间结构为三角锥形 13.瓜环是继冠醚、环糊精、杯芳烃之后的新一代有机大环主体分子,由2n个亚甲基桥联 n个
3
B.“氧化”工序的目的是将+2价的钒和+4价的钒氧化为+5价的钒 苷脲单体(n=5,6,7,8…)构成的笼状化合物,具有分子识别功能。具体合成路线和不同
C.(NH)SO 晶体中含离子键、共价键和配位键 大小形状的瓜环形状结构如图所示。
4 2 4
D.“煅烧”过程中需要不断鼓入空气
10.生活处处有化学,下列对化学应用解释错误的是 ( )
选项 化学应用 解释
A 明矾常用于净水 明矾具有强氧化性
B 工业上常用CCl萃取碘水中的碘 CCl和碘均为非极性分子
4 4
C 厨房烹饪工具要清洗干净并干燥存放 潮湿环境下烹饪工具易发生电化学腐蚀
D 小苏打与柠檬酸混合用作食品膨松剂 NaHCO 与酸混合更易产生CO 下列说法错误的是 ( )
3 2
A.不同瓜环识别的分子或金属离子不同 B.瓜环与识别的分子间一般不形成化学键
11.碳化硅主要应用于功能陶瓷、高级耐火材料、磨料及冶金原料。工业上利用甲烷(晶胞结
C.缩合形成瓜环时还伴随水分子生成 D.瓜环都属于有机高分子
构如图1所示)可制得碳化硅(晶胞结构如图2所示,晶胞参数为 anm)。下列说法错误的
是 ( )
14.InOOH双功能催化剂在不对称pH值的电解池可实现由 CO 和 HMF( )同步生
2
成HCOOH和FDCA( ),电化学装置示意图如图所示,双极膜中水解离的
H+和OH-在电场的作用下向两极迁移。下列说法正确的是 ( )
A.甲烷晶胞中,一个甲烷等距离且最近的甲烷分子数目为12
B.碳化硅晶胞中,两个碳原子的最短距离为0.5anm
C.一个甲烷晶胞中含有4个甲烷分子
160
D.碳化硅晶体的密度为 ×1021g·cm-3
a3N
A
12.CO 和CH 制备CHCOOH的反应为CO(g)+CH(g)幑幐CHCOOH(g),催化反应的历
2 4 3 2 4 3
程如图所示。下列说法正确的是 ( )
A.双极膜中水解离出的OH-向Q极移动
B.P极与电源正极相连,是电子流出的一极
C.Q极的电极反应式为 +8OH-+6e- +6HO
2
D.理论上,每消耗2.24LCO(标准状况)可得到0.2molHCOOH
2
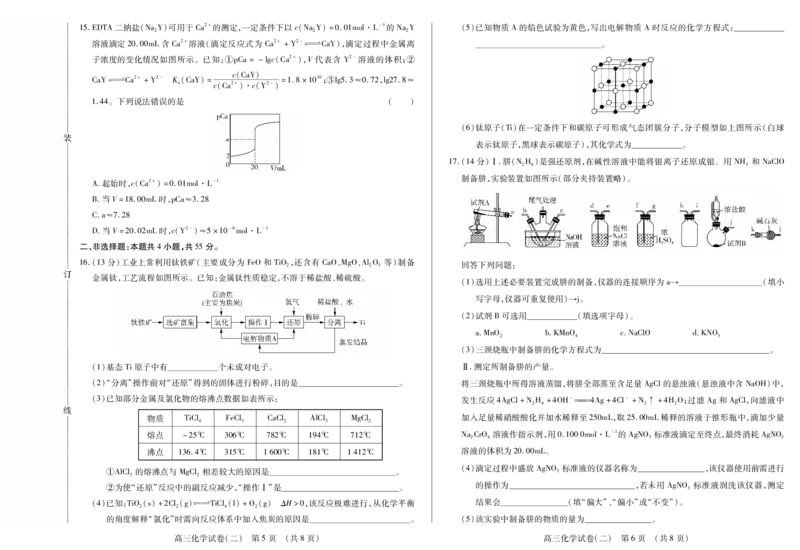
高三化学试卷(二) 第3页 (共8页) 高三化学试卷(二) 第4页 (共8页)15.EDTA二钠盐(NaY)可用于Ca2+的测定,一定条件下以 c(NaY)=0.01mol·L-1的 NaY (5)已知物质A的焰色试验为黄色,写出电解物质 A时反应的化学方程式:
2 2 2
溶液滴定20.00mL含Ca2+溶液(滴定反应式为 Ca2++Y2-幑幐CaY),滴定过程中金属离 。
子浓度的变化情况如图所示。已知:①pCa=-lgc(Ca2+),V代表含 Y2-溶液的体积;②
c(CaY)
CaY幑幐Ca2++Y2- K(CaY)= =1.8×1010;③lg5.3≈0.72,lg27.8≈
a c(Ca2+)·c(Y2-)
1.44。下列说法错误的是 ( )
(6)钛原子(Ti)在一定条件下和碳原子可形成气态团簇分子,分子模型如上图所示(白球
表示钛原子,黑球表示碳原子),其化学式为 。
17.(14分)Ⅰ.肼(NH)是强还原剂,在碱性溶液中能将银离子还原成银。用 NH 和 NaClO
2 4 3
制备肼,实验装置如图所示(部分夹持装置略)。
A.起始时,c(Ca2+)=0.01mol·L-1
B.当V=18.00mL时,pCa≈3.28
C.a≈7.28
D.当V=20.02mL时,c(Y2-)≈5×10-6mol·L-1
二、非选择题:本题共4小题,共55分。
16.(13分)工业上常利用钛铁矿(主要成分为 FeO和 TiO,还含有 CaO、MgO、AlO 等)制备
2 2 3 回答下列问题:
金属钛,工艺流程如图所示。已知:金属钛性质稳定,不溶于稀盐酸、稀硫酸。
(1)选用上述必要装置完成肼的制备,仪器的连接顺序为a→ (填小
写字母,仪器可重复使用)→j。
(2)试剂B可选用 (填选项字母)。
a.MnO b.KMnO c.NaClO d.KNO
2 4 3
(3)三颈烧瓶中制备肼的化学方程式为 。
(1)基态Ti原子中有 个未成对电子。 Ⅱ.测定所制备肼的产量。
(2)“分离”操作前对“还原”得到的固体进行粉碎,目的是 。 将三颈烧瓶中所得溶液蒸馏,将肼全部蒸至含足量AgCl的悬浊液(悬浊液中含 NaOH)中,
(3)已知部分金属及氯化物的熔沸点数据如表所示: 发生反应4AgCl+NH +4OH-4Ag+4Cl-+N↑+4HO;过滤 Ag和 AgCl,向滤液中
2 4 2 2
物质 TiCl FeCl CaCl AlCl MgCl 加入足量稀硝酸酸化并加水稀释至250mL,取25.00mL稀释的溶液于锥形瓶中,滴加少量
4 3 2 3 2
熔点 -25℃ 306℃ 782℃ 194℃ 712℃ NaCrO 溶液作指示剂,用0.1000mol·L-1的AgNO 标准液滴定至终点,最终消耗AgNO
2 4 3 3
沸点 136.4℃ 315℃ 1600℃ 181℃ 1412℃ 溶液的体积为20.00mL。
(4)滴定过程中盛放AgNO 标准液的仪器名称为 ,该仪器使用前需进行
①AlCl的熔沸点与MgCl相差较大的原因是 。 3
3 2
的操作为 ,若未用 AgNO 标准液润洗该仪器,测定
②为使“还原”反应中的副反应减少,“操作Ⅰ”是 。 3
(4)已知:TiO(s)+2Cl(g)幑幐TiCl(l)+O(g) ΔH>0,该反应极难进行,从化学平衡 结果会 (填“偏大”、“偏小”或“不变”)。
2 2 4 2
的角度解释“氯化”时需向反应体系中加入焦炭的原因是 。 (5)该实验中制备肼的物质的量为 。
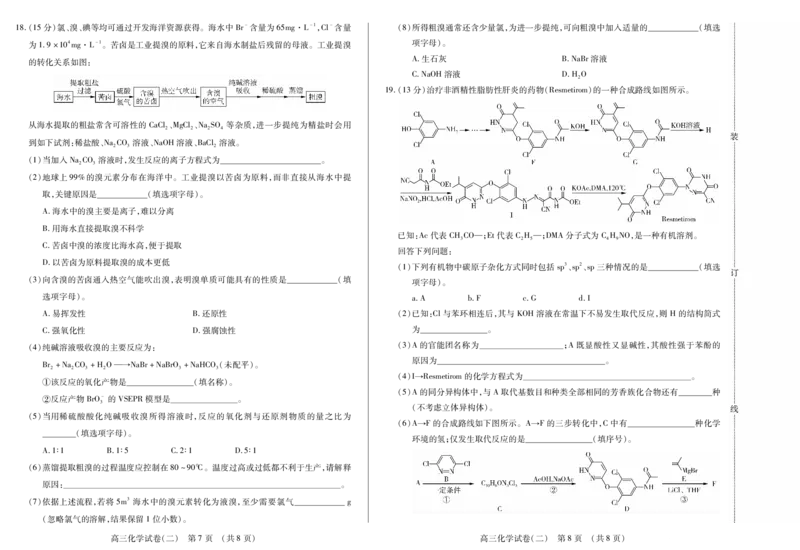
高三化学试卷(二) 第5页 (共8页) 高三化学试卷(二) 第6页 (共8页)18.(15分)氯、溴、碘等均可通过开发海洋资源获得。海水中Br-含量为65mg·L-1,Cl-含量 (8)所得粗溴通常还含少量氯,为进一步提纯,可向粗溴中加入适量的 (填选
为1.9×104mg·L-1。苦卤是工业提溴的原料,它来自海水制盐后残留的母液。工业提溴 项字母)。
A.生石灰 B.NaBr溶液
的转化关系如图:
C.NaOH溶液 D.HO
2
19.(13分)治疗非酒精性脂肪性肝炎的药物(Resmetirom)的一种合成路线如图所示。
从海水提取的粗盐常含可溶性的 CaCl、MgCl、NaSO 等杂质,进一步提纯为精盐时会用
2 2 2 4
到如下试剂:稀盐酸、NaCO 溶液、NaOH溶液、BaCl溶液。
2 3 2
(1)当加入NaCO 溶液时,发生反应的离子方程式为 。
2 3
(2)地球上99%的溴元素分布在海洋中。工业提溴以苦卤为原料,而非直接从海水中提
取,关键原因是 (填选项字母)。
A.海水中的溴主要是离子,难以分离
B.用海水直接提取溴不科学
已知:Ac代表CHCO—;Et代表CH—;DMA分子式为CHNO,是一种有机溶剂。
3 2 5 4 9
C.苦卤中溴的浓度比海水高,便于提取
回答下列问题:
D.以苦卤为原料提取溴的成本更低
(1)下列有机物中碳原子杂化方式同时包括 sp3、sp2、sp三种情况的是 (填选
(3)向含溴的苦卤通入热空气能吹出溴,表明溴单质可能具有的性质是 (填
项字母)。
选项字母)。 a.A b.F c.G d.I
A.易挥发性 B.还原性 (2)已知:Cl与苯环相连后,其与 KOH溶液在常温下不易发生取代反应,则 H的结构简式
C.强氧化性 D.强腐蚀性 为 。
(3)A的官能团名称为 ;A既显酸性又显碱性,其酸性强于苯酚的
(4)纯碱溶液吸收溴的主要反应为:
原因为 。
Br+NaCO +HO→NaBr+NaBrO +NaHCO(未配平)。
2 2 3 2 3 3
(4)I→Resmetirom的化学方程式为 。
①该反应的氧化产物是 (填名称)。
(5)A的同分异构体中,与A取代基数目和种类全部相同的芳香族化合物还有 种
②反应产物BrO-的VSEPR模型是 。
3
(不考虑立体异构体)。
(5)当用稀硫酸酸化纯碱吸收溴所得溶液时,反应的氧化剂与还原剂物质的量之比为
(6)A→F的合成路线如下图所示。A→F的三步转化中,C中有 种化学
(填选项字母)。
环境的氢;仅发生取代反应的是 (填序号)。
A.1∶1 B.1∶5 C.2∶1 D.5∶1
(6)蒸馏提取粗溴的过程温度应控制在80~90℃。温度过高或过低都不利于生产,请解释
原因: 。
(7)依据上述流程,若将5m3海水中的溴元素转化为液溴,至少需要氯气 g
(忽略氯气的溶解,结果保留1位小数)。
高三化学试卷(二) 第7页 (共8页) 高三化学试卷(二) 第8页 (共8页)