文档内容
2024-2025 学年第二学期六校联合体期末考试
高二化学
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Ti 48
一、单项选择题:共 13 小题,每题 3 分,共 39 分。每题只有一个选项最符合
题意。
1. 人形机器人传动关节的材料含有Si、Fe、Cr、Ni等元素,其中不属于第四周期的是
A. Ni B. Fe C. Cr D. Si
2. 反应2H S+SO ===3S+2H O可用于制取硫单质。下列说法正确的是
2 2 2
A. H S的电子式为 B. SO 分子的空间构型为直线形
2 2
C. S 、S 、S 等硫单质互为同素异形体 D. 冰是含极性键的共价晶体
6 8 12
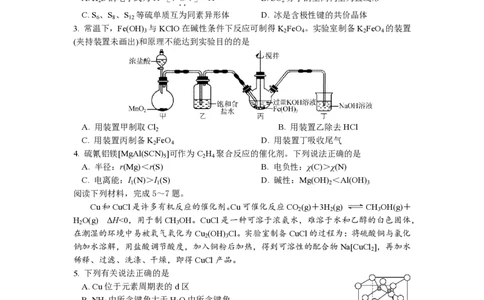
3. 常温下,Fe(OH) 与KClO在碱性条件下反应可制得K FeO 。实验室制备K FeO 的装置
3 2 4 2 4
(夹持装置未画出)和原理不能达到实验目的的是
A. 用装置甲制取Cl B. 用装置乙除去HCl
2
C. 用装置丙制备K FeO D. 用装置丁吸收尾气
2 4
4. 硫氰铝镁[MgAl(SCN) ]可作为C H 聚合反应的催化剂。下列说法正确的是
5 2 4
A. 半径:r(Mg)<r(S) B. 电负性:χ(C)>χ(N)
C. 电离能:I (N)>I (S) D. 碱性:Mg(OH) <Al(OH)
1 1 2 3
阅读下列材料,完成5~7题。
Cu和CuCl是许多有机反应的催化剂。Cu可催化反应CO (g)+3H (g) CH OH(g)+
2 2 3
H O(g) ΔH<0,用于制CH OH。CuCl是一种可溶于浓氨水,难溶于水和乙醇的白色固体,
2 3
在潮湿的环境中易被氧气氧化为Cu (OH) Cl。实验室制备CuCl的过程为:将硫酸铜与氯化
2 3
钠加水溶解,用盐酸调节酸度,加入铜粉后加热,得到可溶性的配合物Na[CuCl ],再加水
2
稀释、过滤、洗涤、干燥,即得CuCl产品。
5. 下列有关说法正确的是
A. Cu位于元素周期表的d区
B. NH 中所含键角大于H O中所含键角
3 2
C. [CuCl ]-中Cu+提供孤电子对与Cl-形成配位键
2
D. CuCl晶胞(如右图所示)中距离每个Cl-最近的Cu+有2个
6. 关于Cu催化CO 制CH OH的反应,下列说法正确的是
2 3
A. 该反应在任意条件下均能自发进行
c(CH OH)
B. 该反应的平衡常数表达式为K= 3
c(CO )·c3(H )
2 2
C. 反应物所含的键能总和小于生成物所含的键能总和
D. 使用Cu作催化剂可以提高CO 的平衡转化率
2
7. 下列化学反应表示正确的是
1点燃
A. Cu在Cl 中燃烧:2Cu+Cl =====2CuCl
2 2
B. Cu与浓硫酸反应:Cu+H SO (浓)===CuSO +SO ↑+H O
2 4 4 2 2
C. CuCl在潮湿的空气中被氧化:4CuCl+O +3H O===2Cu (OH) Cl+Cl
2 2 2 3 2
△
D. CuSO 混合溶液与Cu反应制Na[CuCl ]:Cu2++Cu+4Cl-=====2[CuCl ]-
4 2 2
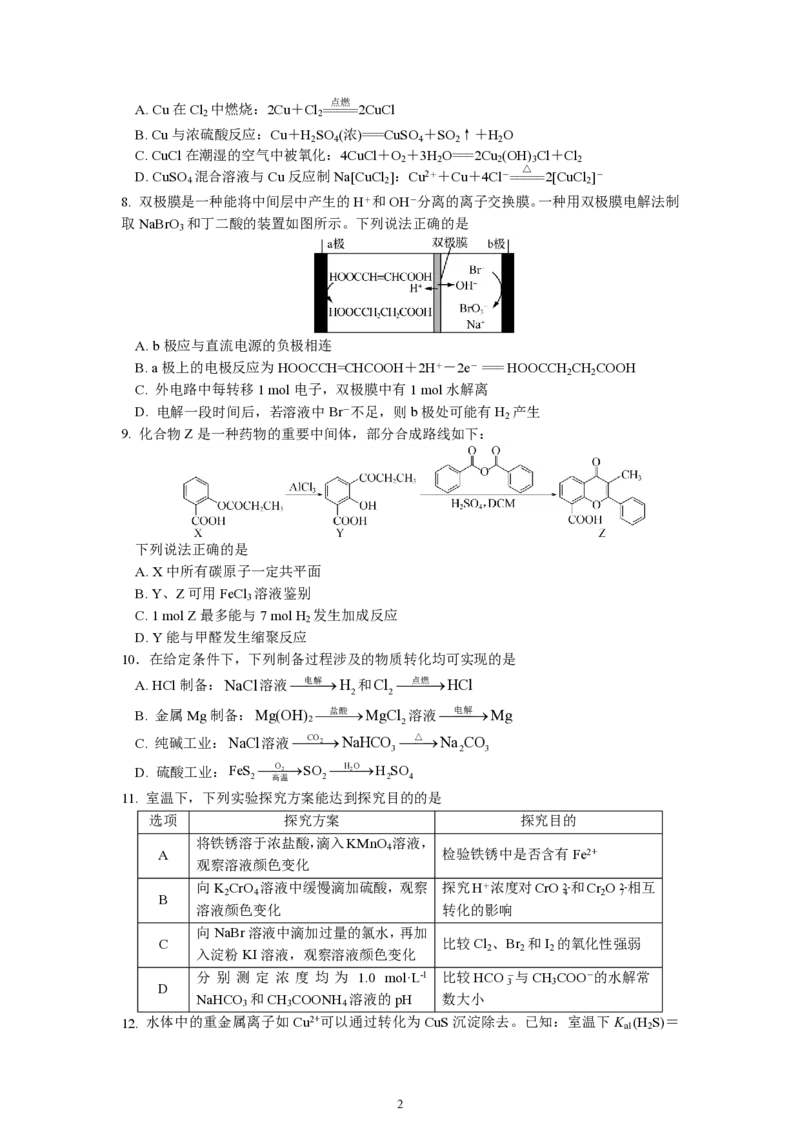
8. 双极膜是一种能将中间层中产生的H+和OH-分离的离子交换膜。一种用双极膜电解法制
取NaBrO 和丁二酸的装置如图所示。下列说法正确的是
3
A. b极应与直流电源的负极相连
B. a极上的电极反应为HOOCCH=CHCOOH+2H+-2e- === HOOCCH CH COOH
2 2
C. 外电路中每转移1 mol电子,双极膜中有1 mol水解离
D. 电解一段时间后,若溶液中Br-不足,则b极处可能有H 产生
2
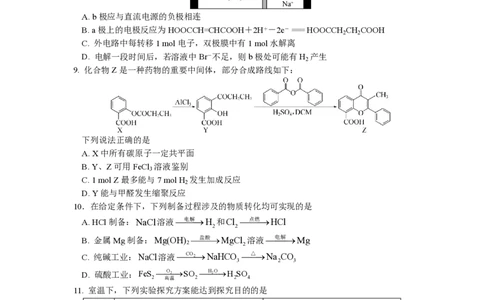
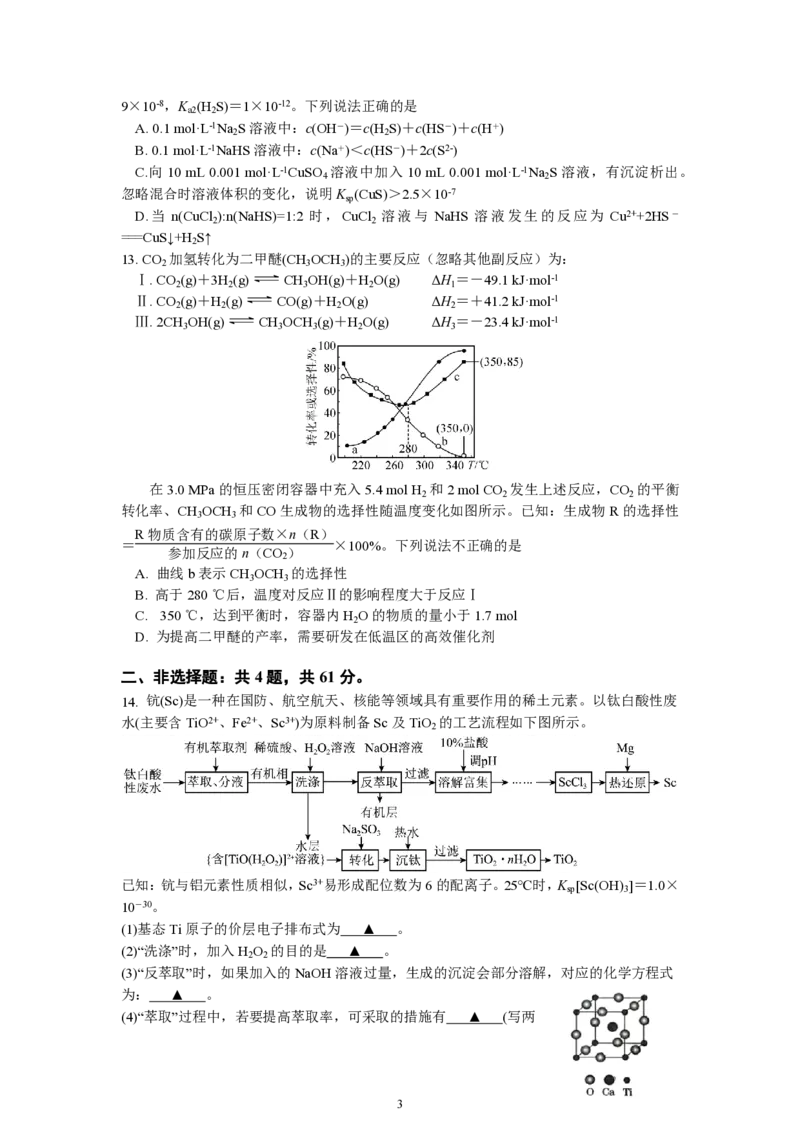
9. 化合物Z是一种药物的重要中间体,部分合成路线如下:
下列说法正确的是
A. X中所有碳原子一定共平面
B. Y、Z可用FeCl 溶液鉴别
3
C. 1 mol Z最多能与7 mol H 发生加成反应
2
D. Y能与甲醛发生缩聚反应
10.在给定条件下,下列制备过程涉及的物质转化均可实现的是
A. HCl制备:NaCl溶液¾电¾解¾®H 和Cl ¾点¾燃¾®HCl
2 2
B. 金属Mg制备:Mg(OH) ¾盐¾¾酸®MgCl 溶液¾电¾¾解®Mg
2 2
C. 纯碱工业:NaCl溶液¾C¾O 2¾®NaHCO ¾△¾®Na CO
3 2 3
D. 硫酸工业:FeS ¾¾O2¾®SO ¾H¾2O¾®H SO
2 高温 2 2 4
11. 室温下,下列实验探究方案能达到探究目的的是
选项 探究方案 探究目的
将铁锈溶于浓盐酸,滴入KMnO 溶液,
4
A 检验铁锈中是否含有Fe2+
观察溶液颜色变化
向K CrO 溶液中缓慢滴加硫酸,观察 探究H+浓度对CrO2-和Cr O2-相互
2 4 4 2 7
B
溶液颜色变化 转化的影响
向NaBr溶液中滴加过量的氯水,再加
C 比较Cl 、Br 和I 的氧化性强弱
2 2 2
入淀粉KI溶液,观察溶液颜色变化
分 别 测 定 浓 度 均 为 1.0 mol·L-1 比较HCO-与CH COO-的水解常
3 3
D
NaHCO 和CH COONH 溶液的pH 数大小
3 3 4
12. 水体中的重金属离子如Cu2+可以通过转化为CuS沉淀除去。已知:室温下K (H S)=
a1 2
29×10-8,K (H S)=1×10-12。下列说法正确的是
a2 2
A. 0.1 mol·L-1Na S溶液中:c(OH-)=c(H S)+c(HS-)+c(H+)
2 2
B. 0.1 mol·L-1NaHS溶液中:c(Na+)<c(HS-)+2c(S2-)
C.向 10 mL 0.001 mol·L-1CuSO 溶液中加入 10 mL 0.001 mol·L-1Na S 溶液,有沉淀析出。
4 2
忽略混合时溶液体积的变化,说明K (CuS)>2.5×10-7
sp
D.当 n(CuCl ):n(NaHS)=1:2 时,CuCl 溶液与 NaHS 溶液发生的反应为 Cu2++2HS-
2 2
===CuS↓+H S↑
2
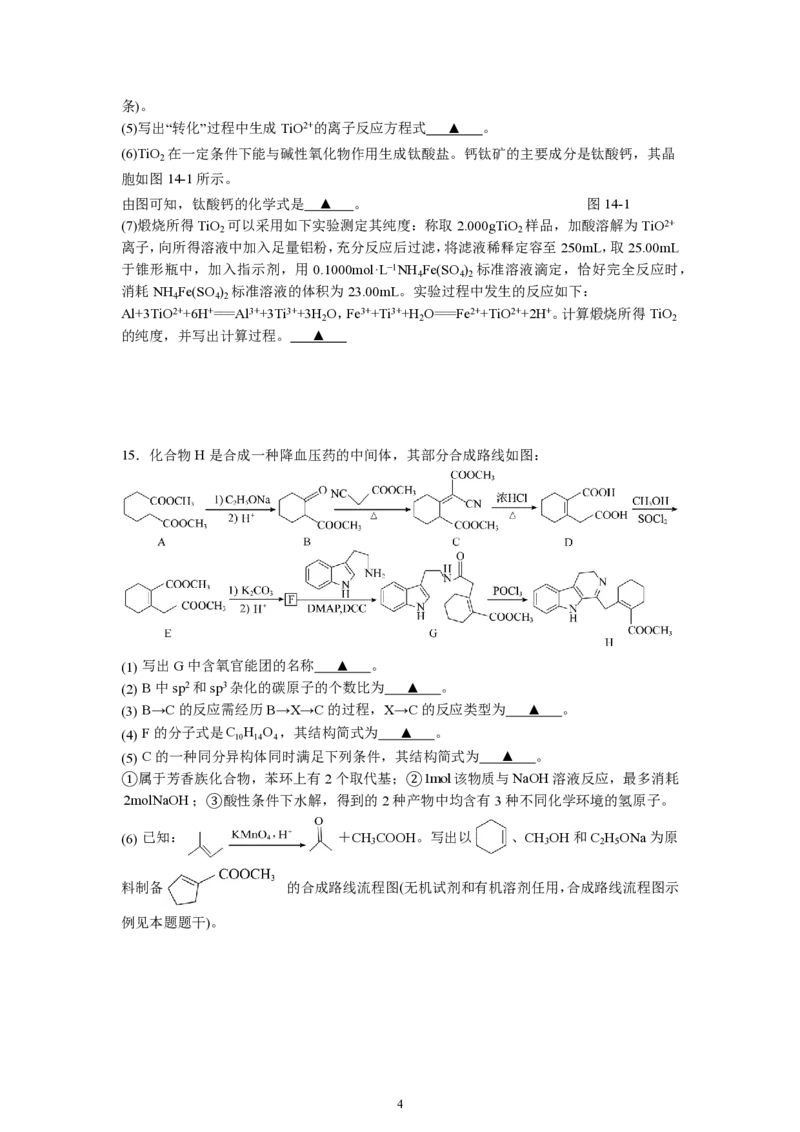
13. CO 加氢转化为二甲醚(CH OCH )的主要反应(忽略其他副反应)为:
2 3 3
Ⅰ. CO (g)+3H (g) CH OH(g)+H O(g) ΔH =-49.1 kJ·mol-1
2 2 3 2 1
Ⅱ. CO (g)+H (g) CO(g)+H O(g) ΔH =+41.2 kJ·mol-1
2 2 2 2
Ⅲ. 2CH OH(g) CH OCH (g)+H O(g) ΔH =-23.4 kJ·mol-1
3 3 3 2 3
在3.0 MPa的恒压密闭容器中充入5.4 mol H 和2 mol CO 发生上述反应,CO 的平衡
2 2 2
转化率、CH OCH 和CO生成物的选择性随温度变化如图所示。已知:生成物R的选择性
3 3
R 物质含有的碳原子数×n(R)
= ×100%。下列说法不正确的是
参加反应的n(CO )
2
A. 曲线b表示CH OCH 的选择性
3 3
B. 高于280 ℃后,温度对反应Ⅱ的影响程度大于反应Ⅰ
C. 350 ℃,达到平衡时,容器内H O的物质的量小于1.7 mol
2
D. 为提高二甲醚的产率,需要研发在低温区的高效催化剂
二、非选择题:共 4题,共 61分。
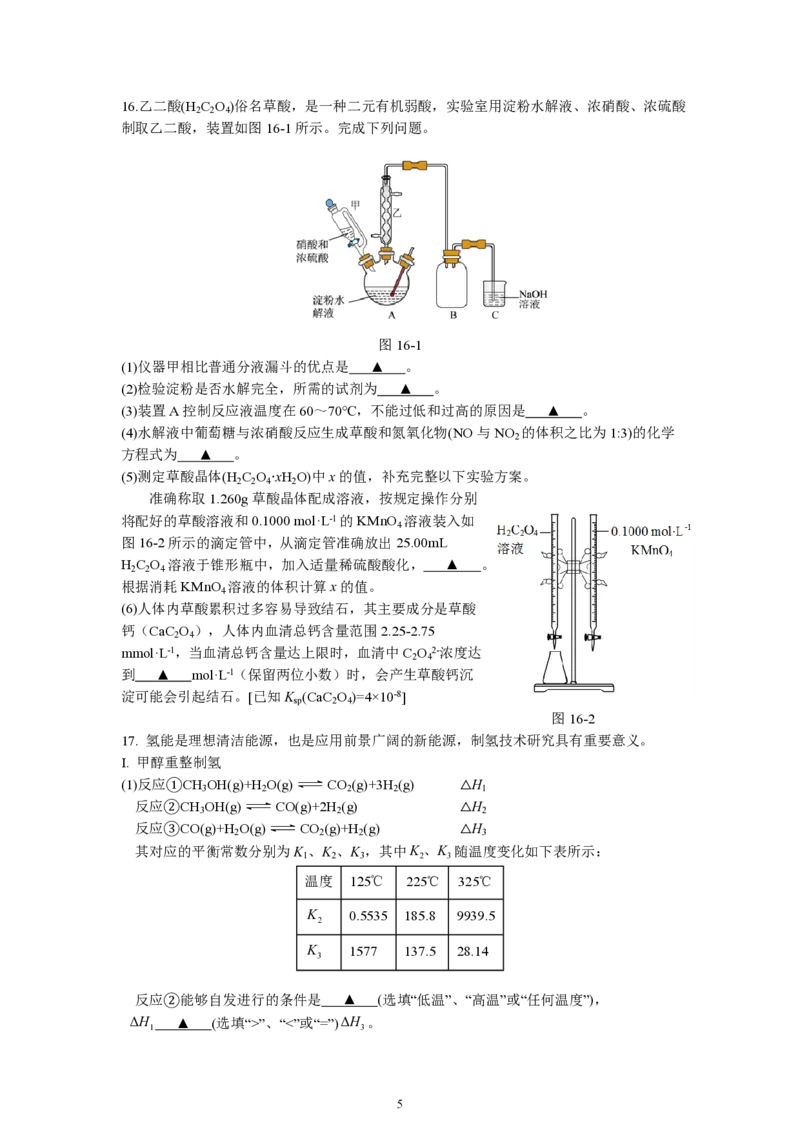
14. 钪(Sc)是一种在国防、航空航天、核能等领域具有重要作用的稀土元素。以钛白酸性废
水(主要含TiO2+、Fe2+、Sc3+)为原料制备Sc及TiO 的工艺流程如下图所示。
2
已知:钪与铝元素性质相似,Sc3+易形成配位数为6的配离子。25℃时,K [Sc(OH) ]=1.0×
sp 3
10-30。
(1)基态Ti原子的价层电子排布式为 ▲ 。
(2)“洗涤”时,加入H O 的目的是 ▲ 。
2 2
(3)“反萃取”时,如果加入的NaOH溶液过量,生成的沉淀会部分溶解,对应的化学方程式
为: ▲ 。
(4)“萃取”过程中,若要提高萃取率,可采取的措施有 ▲ (写两
3条)。
(5)写出“转化”过程中生成TiO2+的离子反应方程式 ▲ 。
(6)TiO 在一定条件下能与碱性氧化物作用生成钛酸盐。钙钛矿的主要成分是钛酸钙,其晶
2
胞如图14-1所示。
由图可知,钛酸钙的化学式是 ▲ 。 图14-1
(7)煅烧所得TiO 可以采用如下实验测定其纯度:称取2.000gTiO 样品,加酸溶解为TiO2+
2 2
离子,向所得溶液中加入足量铝粉,充分反应后过滤,将滤液稀释定容至250mL,取25.00mL
于锥形瓶中,加入指示剂,用0.1000mol·L−1NH Fe(SO ) 标准溶液滴定,恰好完全反应时,
4 4 2
消耗NH Fe(SO ) 标准溶液的体积为23.00mL。实验过程中发生的反应如下:
4 4 2
Al+3TiO2++6H+===Al3++3Ti3++3H O,Fe3++Ti3++H O===Fe2++TiO2++2H+。计算煅烧所得TiO
2 2 2
的纯度,并写出计算过程。 ▲
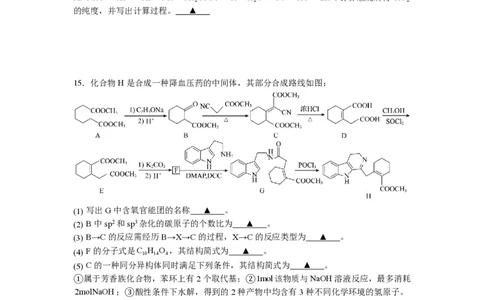
15.化合物H是合成一种降血压药的中间体,其部分合成路线如图:
(1) 写出G中含氧官能团的名称 ▲ 。
(2) B中sp2和sp3杂化的碳原子的个数比为 ▲ 。
(3) B→C的反应需经历B→X→C的过程,X→C的反应类型为 ▲ 。
(4) F的分子式是C H O ,其结构简式为 ▲ 。
10 14 4
(5) C的一种同分异构体同时满足下列条件,其结构简式为 ▲ 。
①属于芳香族化合物,苯环上有2个取代基;②1mol该物质与NaOH溶液反应,最多消耗
2molNaOH;③酸性条件下水解,得到的2种产物中均含有3种不同化学环境的氢原子。
(6) 已知: +CH COOH。写出以 、CH OH和C H ONa为原
3 3 2 5
料制备 的合成路线流程图(无机试剂和有机溶剂任用,合成路线流程图示
例见本题题干)。
416.乙二酸(H C O )俗名草酸,是一种二元有机弱酸,实验室用淀粉水解液、浓硝酸、浓硫酸
2 2 4
制取乙二酸,装置如图16-1所示。完成下列问题。
图16-1
(1)仪器甲相比普通分液漏斗的优点是 ▲ 。
(2)检验淀粉是否水解完全,所需的试剂为 ▲ 。
(3)装置A控制反应液温度在60~70℃,不能过低和过高的原因是 ▲ 。
(4)水解液中葡萄糖与浓硝酸反应生成草酸和氮氧化物(NO与NO 的体积之比为1:3)的化学
2
方程式为 ▲ 。
(5)测定草酸晶体(H C O ·xH O)中x的值,补充完整以下实验方案。
2 2 4 2
准确称取1.260g草酸晶体配成溶液,按规定操作分别
将配好的草酸溶液和0.1000 mol·L-1的KMnO 溶液装入如
4
图16-2所示的滴定管中,从滴定管准确放出25.00mL
H C O 溶液于锥形瓶中,加入适量稀硫酸酸化, ▲ 。
2 2 4
根据消耗KMnO 溶液的体积计算x的值。
4
(6)人体内草酸累积过多容易导致结石,其主要成分是草酸
钙(CaC O ),人体内血清总钙含量范围2.25-2.75
2 4
mmol·L-1,当血清总钙含量达上限时,血清中C O 2-浓度达
2 4
到 ▲ mol·L-1(保留两位小数)时,会产生草酸钙沉
淀可能会引起结石。[已知K (CaC O )=4×10-8]
sp 2 4
图16-2
17. 氢能是理想清洁能源,也是应用前景广阔的新能源,制氢技术研究具有重要意义。
I. 甲醇重整制氢
(1)反应①CH OH(g)+H O(g) CO (g)+3H (g) △H
3 2 2 2 1
反应②CH OH(g) CO(g)+2H (g) △H
3 2 2
反应③CO(g)+H O(g) CO (g)+H (g) △H
2 2 2 3
其对应的平衡常数分别为K 、K 、K ,其中K 、K 随温度变化如下表所示:
1 2 3 2 3
温度 125℃ 225℃ 325℃
K 0.5535 185.8 9939.5
2
K 1577 137.5 28.14
3
反应②能够自发进行的条件是 ▲ (选填“低温”、“高温”或“任何温度”),
ΔH ▲ (选填“>”、“<”或“=”)ΔH 。
1 3
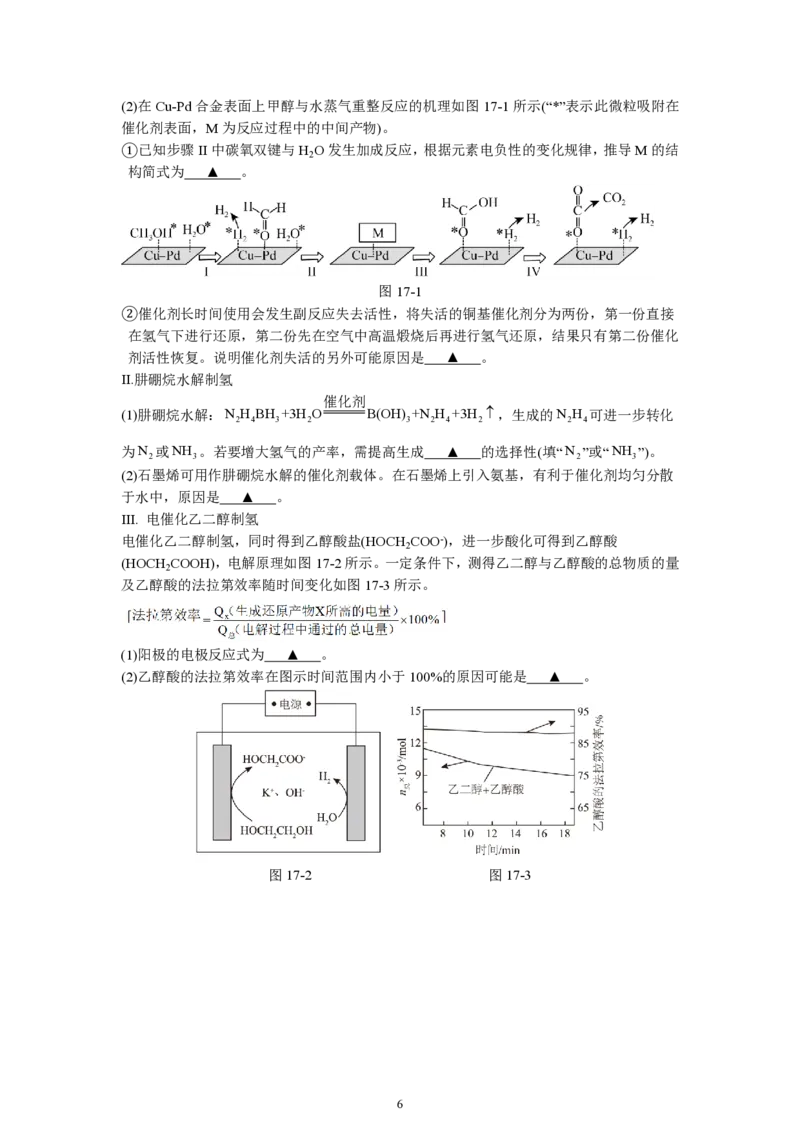
5(2)在Cu-Pd合金表面上甲醇与水蒸气重整反应的机理如图17-1所示(“*”表示此微粒吸附在
催化剂表面,M为反应过程中的中间产物)。
①已知步骤II中碳氧双键与H O发生加成反应,根据元素电负性的变化规律,推导M的结
2
构简式为 ▲ 。
图17-1
②催化剂长时间使用会发生副反应失去活性,将失活的铜基催化剂分为两份,第一份直接
在氢气下进行还原,第二份先在空气中高温煅烧后再进行氢气还原,结果只有第二份催化
剂活性恢复。说明催化剂失活的另外可能原因是 ▲ 。
II.肼硼烷水解制氢
催化剂
(1)肼硼烷水解:N H BH +3H O B(OH) +N H +3H ,生成的N H 可进一步转化
2 4 3 2 3 2 4 2 2 4
为N 或NH 。若要增大氢气的产率,需提高生成 ▲ 的选择性(填“N ”或“NH ”)。
2 3 2 3
(2)石墨烯可用作肼硼烷水解的催化剂载体。在石墨烯上引入氨基,有利于催化剂均匀分散
于水中,原因是 ▲ 。
III. 电催化乙二醇制氢
电催化乙二醇制氢,同时得到乙醇酸盐(HOCH COO-),进一步酸化可得到乙醇酸
2
(HOCH COOH),电解原理如图17-2所示。一定条件下,测得乙二醇与乙醇酸的总物质的量
2
及乙醇酸的法拉第效率随时间变化如图17-3所示。
(1)阳极的电极反应式为 ▲ 。
(2)乙醇酸的法拉第效率在图示时间范围内小于100%的原因可能是 ▲ 。
图17-2 图17-3
62024-2025 学年第二学期六校联合体期末考试
高二化学参考答案
一、单项选择题
1 2 3 4 5 6 7 8 9 10 11 12 13
D C A C B C D C B A B D C
二、非选择题
14.(16分)(1)3d24s2(2分)
(2)将Fe2+氧化为Fe3+;提供配体,生成稳定的配离子[TiO(H O )]2+进入水层,便于分离
2 2
出钛(2分)
(3)Sc(OH) +3NaOH=Na [Sc(OH) ](2分)
3 3 6
(4)反复多次萃取(增加萃取次数)、更换萃取剂或调节pH(2分)
(5)[TiO(H O )]2++SO 2-=TiO2++SO 2-+H O(3分)
2 2 3 4 2
(6)CaTiO (2分)
3
(7)实验过程中发生的反应如下:Al+3TiO2++6H+=Al3++3Ti3++3H O,
2
Fe3++Ti3++H O=Fe2++TiO2++2H+,可得到定量关系:TiO ~TiO2+~Ti3+~Fe3+,则TiO 的物质
2 2 2
250ml
的量n=0.0230L´0.1000mol/L´ =0.0230mol(1分),则煅烧所得的TiO 纯度为
25ml 2
0.0230mol´80g/mol
´100%=92%(2分)。
2.000g
15.(15分)(1)酯基、酰胺基(2分)
(2)1:3(2分)
(3)消去反应(2分)
(4) (2分)
(5) (2分)
(6) ¾K¾Mn¾O4 ,¾H+¾® ¾¾C
S
¾H
OC
3 O
l
H
2
¾¾® ¾¾1¾)
2
C
)
¾2 H
H
5 O
+
¾Na¾¾®
¾¾H¾2 ,¾催化¾剂 ¾® ¾浓¾硫¾酸® (5分)
△
V
16.(15分)(1) 平衡气压,便于液体顺利流下(2分)
(2) 碘水(2分)
(3) 温度过低,化学反应速率过慢;温度过高,硝酸易分解,导致草酸产率下降(2分)
浓H SO
2 4
(4) C H O +12HNO 3H C O +9NO +3NO+9H O(3分)
6 12 6 3 2 2 4 2 2
D
(5) 向锥形瓶中缓慢滴加0.1000mol/LKMnO 溶液,边滴加边振荡锥形瓶,(1分)当滴入最
4
后半滴KMnO 时,溶液恰好由无色突变为粉红色,且半分钟内不褪色(1分),记录滴加
4KMnO 溶液的体积(1分),重复上述操作2~3次(1分)。
4
(6)1.45 ×10-5mol·L-1(2分)
17.(15分) I.(1) 高温 (1分) >(1分)
(2)① (2分) ②催化剂表面有积碳沉积(2分)
II. (1) N (2分)
2
(2) 氨基与水分子之间形成氢键,增大了催化剂的水溶性(2分)
III.(1) HOCH CH OH+5OH--4e-=HOCH COO-+4H O(3分)
2 2 2 2
(2)生成其他含碳副产物(如CO 等)或O (2分)
2 2