文档内容
绝密★启用前
B卷
江苏省 2024~2025 学年高二下学期期末迎考卷
化 学
注意事项:
1. 本试卷100分,考试用时75分钟。
2. 答题前,考生务必将班级、姓名、学号写在密封线内。
可能用到的相对原子质量: H—1 C—12 N—14 O—16 Mn—55 Fe—56
一、 单项选择题:本题包括13小题,每小题3分,共计39分。每小题只有一个选项最符合题意。
1. 美国于2025年4月2号对我国加征34%的关税,但对部分中国产品如:电脑、手机豁免关税。电脑、
手机中含有的芯片中的主要成分为 ( )
A. O B. Si C. SiO D. Fe
2
2. 实验室利用反应2CoCl +10NH +2NH Cl+H O 2[Co(NH ) ]Cl +2H O制备三氯化六氨合钴。
2 3 4 2 2 3 6 3 2
下列有关说法正确的是 ( )
A. Cl-的结构示意图为 B. H O 分子中含离子键
2 2
C. [Co(NH ) ]Cl 中Co元素的化合价为+3 D. NH 的空间结构为平面三角形
3 6 3 3
3. 某化学兴趣小组进行SO 相关实验。下列实验装置和操作能达到实验目的的是 ( )
2
甲 乙 丙 丁
A. 用装置甲制备SO 气体 B. 用装置乙干燥SO 气体
2 2
C. 用装置丙验证SO 是酸性氧化物 D. 用装置丁吸收SO 气体
2 2
4. 硫酸亚铁铵[(NH ) Fe(SO ) ·6H O]又称莫尔盐,可作为基准物质,用于标定高锰酸钾、重铬酸钾等溶
4 2 4 2 2
液的浓度。下列说法正确的是 ( )
A. 半径:r(N3-)>r(O2-) B. 电负性:χ(S)>χ(O)
C. 沸点:H S>H O D. 第一电离能:I (N)0 B. 该反应的平衡常数K=
c2(SO )
3
C. 提高
n(O )
的值,可增大SO 的平衡转化率 D. 使用合适的催化剂可降低反应的焓变
2 2
n(SO )
2
6. 下列化学反应表示正确的是 ( )
A. 单质硫与铁反应:2Fe+3S Fe S
2 3
B. 过量的SO 通入氨水中:SO +NH ·H O N +HS
2 2 3 2 H+ O-
4 3
C. 用FeS除去溶液中的CuSO :Cu2++S2- CuS↓
4
D. 向NaHSO 溶液中滴入稀硫酸:S +2H+ SO ↑+H O
3 O2- 2 2
3
7. 下列说法正确的是 ( )
A. 自然界硫循环中均发生氧化还原反应
B. S 、S 中S原子均为sp2杂化
O2- O2-
4 3
C. H S氧化为S时,H S断裂σ键和π键
2 2
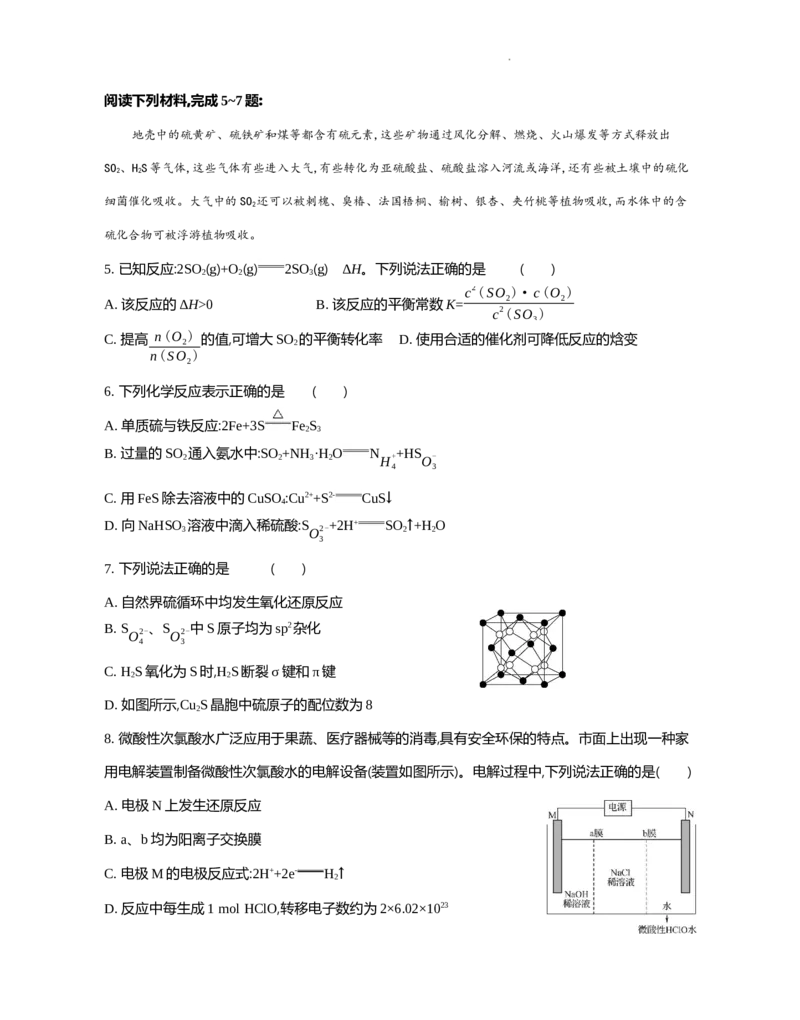
D. 如图所示,Cu S晶胞中硫原子的配位数为8
2
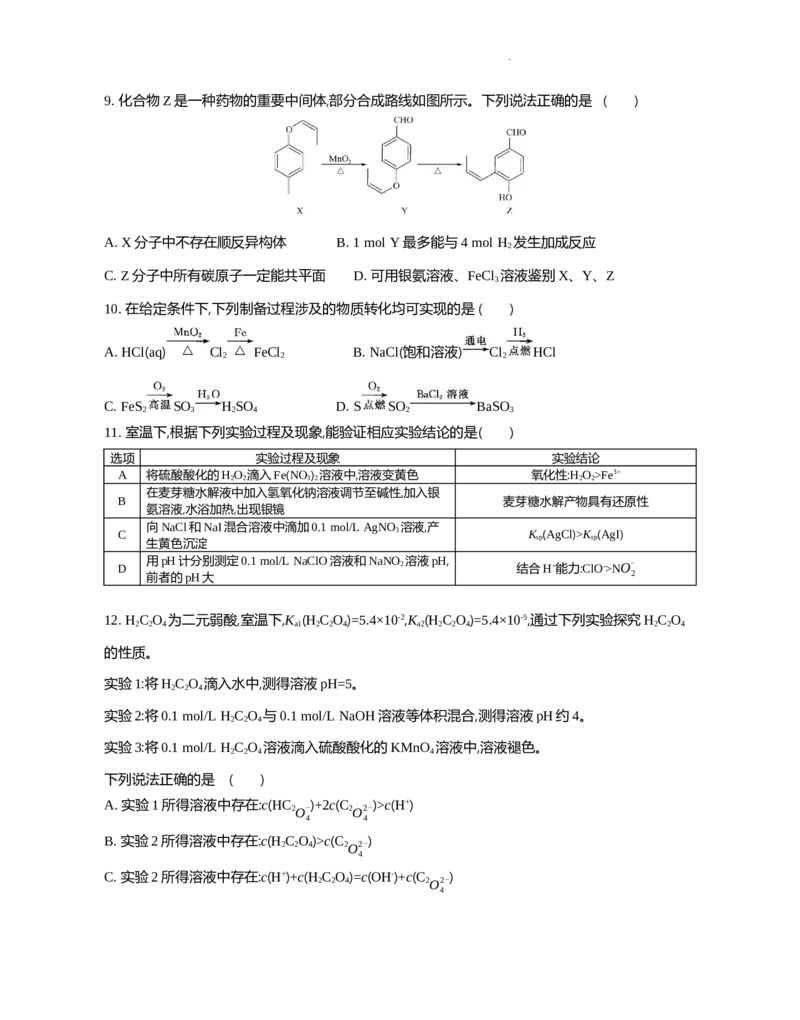
8. 微酸性次氯酸水广泛应用于果蔬、医疗器械等的消毒,具有安全环保的特点。市面上出现一种家
用电解装置制备微酸性次氯酸水的电解设备(装置如图所示)。电解过程中,下列说法正确的是( )
A. 电极N上发生还原反应
B. a、b均为阳离子交换膜
C. 电极M的电极反应式:2H++2e- H ↑
2
D. 反应中每生成1 mol HClO,转移电子数约为2×6.02×1023
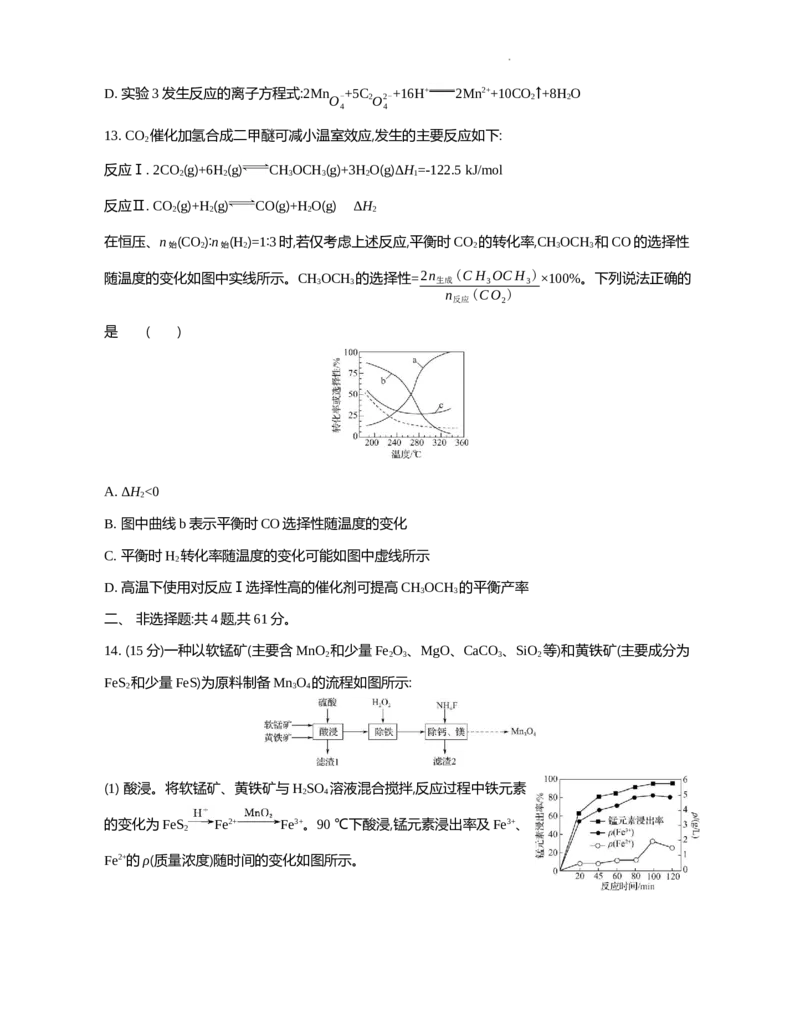
学科网(北京)股份有限公司9. 化合物Z是一种药物的重要中间体,部分合成路线如图所示。下列说法正确的是 ( )
A. X分子中不存在顺反异构体 B. 1 mol Y最多能与4 mol H 发生加成反应
2
C. Z分子中所有碳原子一定能共平面 D. 可用银氨溶液、FeCl 溶液鉴别X、Y、Z
3
10. 在给定条件下,下列制备过程涉及的物质转化均可实现的是( )
A. HCl(aq) Cl FeCl B. NaCl(饱和溶液) Cl HCl
2 2 2
C. FeS SO H SO D. S SO BaSO
2 3 2 4 2 3
11. 室温下,根据下列实验过程及现象,能验证相应实验结论的是( )
选项 实验过程及现象 实验结论
A 将硫酸酸化的HO 滴入Fe(NO ) 溶液中,溶液变黄色 氧化性:HO>Fe3+
2 2 3 2 2 2
在麦芽糖水解液中加入氢氧化钠溶液调节至碱性,加入银
B 麦芽糖水解产物具有还原性
氨溶液,水浴加热,出现银镜
向NaCl和NaI混合溶液中滴加0.1 mol/L AgNO 溶液,产
C 3 K (AgCl)>K (AgI)
sp sp
生黄色沉淀
D
用pH计分别测定0.1 mol/L NaClO溶液和NaNO
2
溶液pH,
结合H+能力:ClO->NO-
前者的pH大 2
12. H C O 为二元弱酸,室温下,K (H C O )=5.4×10-2,K (H C O )=5.4×10-5,通过下列实验探究H C O
2 2 4 a1 2 2 4 a2 2 2 4 2 2 4
的性质。
实验1:将H C O 滴入水中,测得溶液pH=5。
2 2 4
实验2:将0.1 mol/L H C O 与0.1 mol/L NaOH溶液等体积混合,测得溶液pH约4。
2 2 4
实验3:将0.1 mol/L H C O 溶液滴入硫酸酸化的KMnO 溶液中,溶液褪色。
2 2 4 4
下列说法正确的是 ( )
A. 实验1所得溶液中存在:c(HC )+2c(C )>c(H+)
2O- 2O2-
4 4
B. 实验2所得溶液中存在:c(H C O )>c(C )
2 2 4 2O2-
4
C. 实验2所得溶液中存在:c(H+)+c(H C O )=c(OH-)+c(C )
2 2 4 2O2-
4
学科网(北京)股份有限公司D. 实验3发生反应的离子方程式:2Mn +5C +16H+ 2Mn2++10CO ↑+8H O
O- 2O2- 2 2
4 4
13. CO 催化加氢合成二甲醚可减小温室效应,发生的主要反应如下:
2
反应Ⅰ. 2CO (g)+6H (g) CH OCH (g)+3H O(g)ΔH =-122.5 kJ/mol
2 2 3 3 2 1
反应Ⅱ. CO (g)+H (g) CO(g)+H O(g) ΔH
2 2 2 2
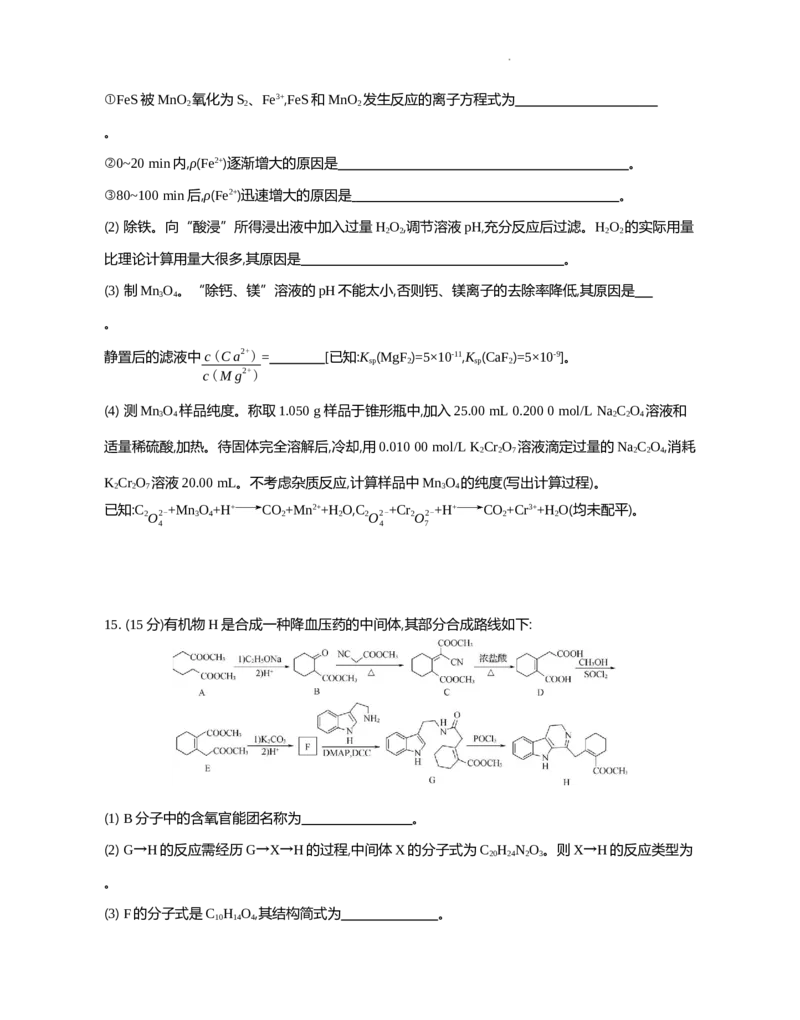
在恒压、n (CO )∶n (H )=1∶3时,若仅考虑上述反应,平衡时CO 的转化率,CH OCH 和CO的选择性
始 2 始 2 2 3 3
随温度的变化如图中实线所示。CH
3
OCH
3
的选择性=2n
生成
(CH
3
OCH
3
) ×100%。下列说法正确的
n (CO )
反应 2
是 ( )
A. ΔH <0
2
B. 图中曲线b表示平衡时CO选择性随温度的变化
C. 平衡时H 转化率随温度的变化可能如图中虚线所示
2
D. 高温下使用对反应Ⅰ选择性高的催化剂可提高CH OCH 的平衡产率
3 3
二、 非选择题:共4题,共61分。
14. (15分)一种以软锰矿(主要含MnO 和少量Fe O 、MgO、CaCO 、SiO 等)和黄铁矿(主要成分为
2 2 3 3 2
FeS 和少量FeS)为原料制备Mn O 的流程如图所示:
2 3 4
(1) 酸浸。将软锰矿、黄铁矿与H SO 溶液混合搅拌,反应过程中铁元素
2 4
的变化为FeS Fe2+ Fe3+。90 ℃下酸浸,锰元素浸出率及Fe3+、
2
Fe2+的ρ(质量浓度)随时间的变化如图所示。
学科网(北京)股份有限公司①FeS被MnO 氧化为S 、Fe3+,FeS和MnO 发生反应的离子方程式为
2 2 2
。
②0~20 min内,ρ(Fe2+)逐渐增大的原因是 。
③80~100 min后,ρ(Fe2+)迅速增大的原因是 。
(2) 除铁。向“酸浸”所得浸出液中加入过量H O ,调节溶液pH,充分反应后过滤。H O 的实际用量
2 2 2 2
比理论计算用量大很多,其原因是 。
(3) 制Mn O 。“除钙、镁”溶液的pH不能太小,否则钙、镁离子的去除率降低,其原因是
3 4
。
静置后的滤液中 c(Ca2+) = [已知:K (MgF )=5×10-11,K (CaF )=5×10-9]。
sp 2 sp 2
c(M g2+)
(4) 测Mn O 样品纯度。称取1.050 g样品于锥形瓶中,加入25.00 mL 0.200 0 mol/L Na C O 溶液和
3 4 2 2 4
适量稀硫酸,加热。待固体完全溶解后,冷却,用0.010 00 mol/L K Cr O 溶液滴定过量的Na C O ,消耗
2 2 7 2 2 4
K Cr O 溶液20.00 mL。不考虑杂质反应,计算样品中Mn O 的纯度(写出计算过程)。
2 2 7 3 4
已知:C +Mn O +H+ CO +Mn2++H O,C +Cr +H+ CO +Cr3++H O(均未配平)。
2O2- 3 4 2 2 2O2- 2O2- 2 2
4 4 7
15. (15分)有机物H是合成一种降血压药的中间体,其部分合成路线如下:
(1) B分子中的含氧官能团名称为 。
(2) G→H的反应需经历G→X→H的过程,中间体X的分子式为C H N O 。则X→H的反应类型为
20 24 2 3
。
(3) F的分子式是C H O ,其结构简式为 。
10 14 4
学科网(北京)股份有限公司(4) C的一种同分异构体同时满足下列条件,其结构简式为 。
碱性条件下水解后酸化,生成X和Y两种有机产物。X分子中有2种不同化学环境的氢原子,能与
NaHCO 反应放出气体;Y分子中含有3种不同化学环境的氢原子,Y能与FeCl 溶液发生显色反应。
3 3
(5) 已知: 。写出以 、CH OH和CH ONa为原料制备
3 3
的合成路线流程图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
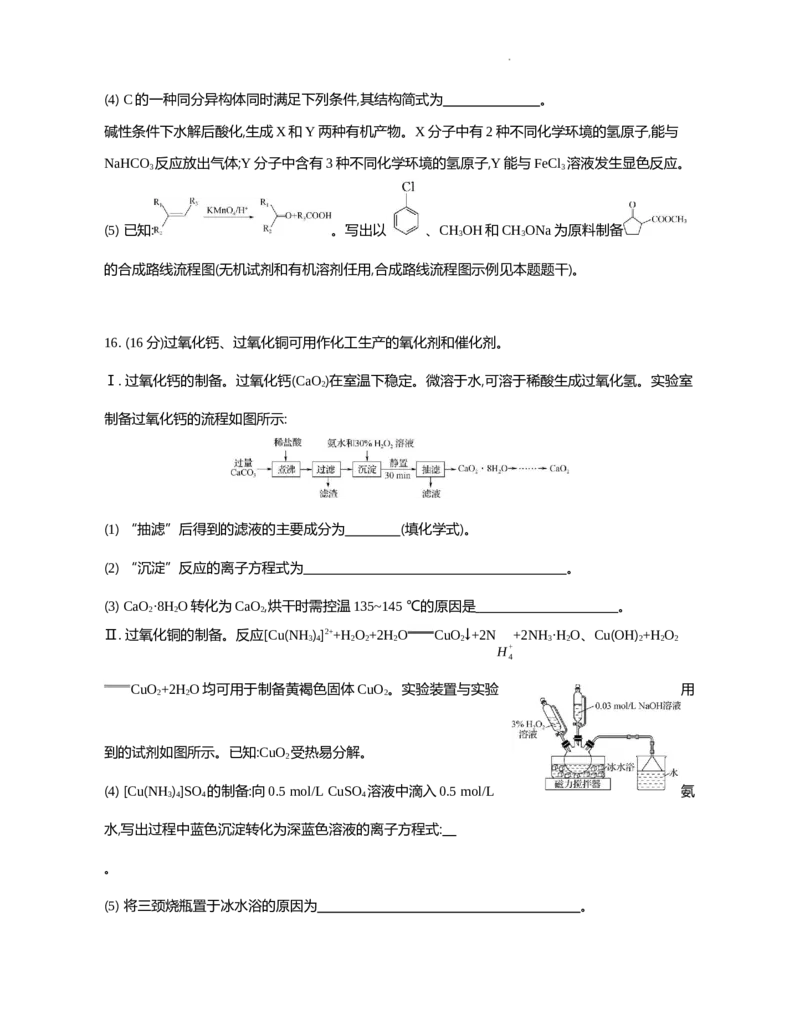
16. (16分)过氧化钙、过氧化铜可用作化工生产的氧化剂和催化剂。
Ⅰ. 过氧化钙的制备。过氧化钙(CaO )在室温下稳定。微溶于水,可溶于稀酸生成过氧化氢。实验室
2
制备过氧化钙的流程如图所示:
(1) “抽滤”后得到的滤液的主要成分为 (填化学式)。
(2) “沉淀”反应的离子方程式为 。
(3) CaO ·8H O转化为CaO ,烘干时需控温135~145 ℃的原因是 。
2 2 2
Ⅱ. 过氧化铜的制备。反应[Cu(NH ) ]2++H O +2H O CuO ↓+2N +2NH ·H O、Cu(OH) +H O
3 4 2 2 2 2 3 2 2 2 2
H+
4
CuO +2H O均可用于制备黄褐色固体CuO 。实验装置与实验 用
2 2 2
到的试剂如图所示。已知:CuO 受热易分解。
2
(4) [Cu(NH ) ]SO 的制备:向0.5 mol/L CuSO 溶液中滴入0.5 mol/L 氨
3 4 4 4
水,写出过程中蓝色沉淀转化为深蓝色溶液的离子方程式:
。
(5) 将三颈烧瓶置于冰水浴的原因为 。
学科网(北京)股份有限公司(6) 补充完整由CuCl 制备过氧化铜的实验步骤:5 mL含PVP(稳定剂)的0.01 mmol/L CuCl 水溶液中,
2 2
,过滤、洗涤、
晾干、称重(须选试剂:0.03 mol/L NaOH溶液、3% H O 溶液)。
2 2
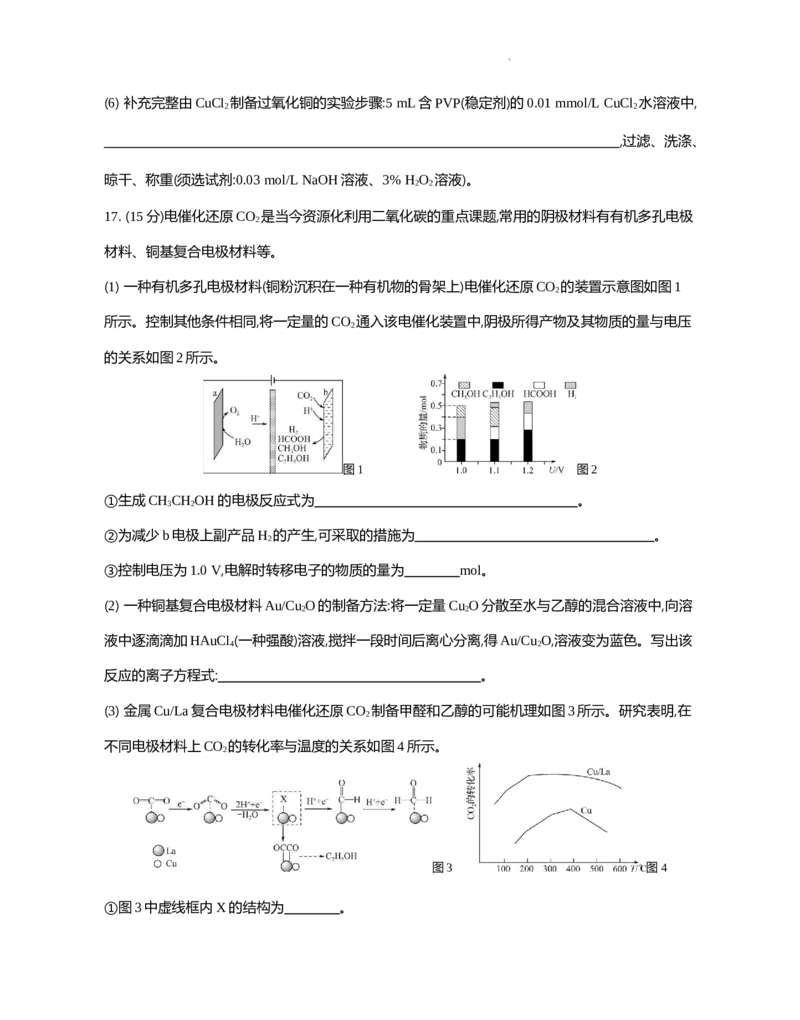
17. (15分)电催化还原CO 是当今资源化利用二氧化碳的重点课题,常用的阴极材料有有机多孔电极
2
材料、铜基复合电极材料等。
(1) 一种有机多孔电极材料(铜粉沉积在一种有机物的骨架上)电催化还原CO 的装置示意图如图1
2
所示。控制其他条件相同,将一定量的CO 通入该电催化装置中,阴极所得产物及其物质的量与电压
2
的关系如图2所示。
图1 图2
①生成CH CH OH的电极反应式为 。
3 2
②为减少b电极上副产品H 的产生,可采取的措施为 。
2
③控制电压为1.0 V,电解时转移电子的物质的量为 mol。
(2) 一种铜基复合电极材料Au/Cu O的制备方法:将一定量Cu O分散至水与乙醇的混合溶液中,向溶
2 2
液中逐滴滴加HAuCl (一种强酸)溶液,搅拌一段时间后离心分离,得Au/Cu O,溶液变为蓝色。写出该
4 2
反应的离子方程式: 。
(3) 金属Cu/La复合电极材料电催化还原CO 制备甲醛和乙醇的可能机理如图3所示。研究表明,在
2
不同电极材料上CO 的转化率与温度的关系如图4所示。
2
图3 图4
①图3中虚线框内X的结构为 。
学科网(北京)股份有限公司②与单纯的Cu电极相比,利用Cu/La复合电极材料电催化还原CO 的优点是 。
2
学科网(北京)股份有限公司