文档内容
2010年四川省高考理综试题
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Mg 24 Al 27 S 32 Cl 35.5 Ca 40 Mn
55 Fe 56 Co 59 Cu 64 Br 80 Ba 137
1.(2010四川高考)节能减排对发展经济、保护环境有重要意义。下列措施不能减少二氧
化碳排放的是
A.利用太阳能制氢 B.关停小火电企业
C.举行“地球一小时”熄灯活动 D.推广使用煤液化技术
2.(2010四川高考)N表示阿伏伽德罗常数的值,下列说法正确的是
A
A.标准状况下,22.4L二氯甲烷的分子数约为N个
A
B.盛有SO的密闭容器中含有N个氧原子,则SO的物质的量为0.5mol
2 A 2
C.17.6g丙烷中所含的极性共价键为4N个
A
D.电解精炼铜时,若阴极得到电子数为2N个,则阳极质量减少 64g
A
3.(2010四川高考)下列说法正确的是
A.原子最外层电子数为2的元素一定处于周期表第ⅡA族
B.主族元素X、Y能形成XY型化合物,则X与Y的原子序数之差可能为2或5
2
C.氯化氢的沸点比氟化氢的沸点高
D.同主族元素形成的氧化物的晶体类型均相同
4.(2010四川高考)下列离子方程式书写正确的是
A.向明矾溶液中加入过量的氢氧化钡溶液:
Al3+ + 2SO2-+2Ba2+ + 4OH-= 2BaSO↓+ AlO-+ 2HO
4 4 2 2
B.向氢氧化亚铁中加入足量的稀硝酸:Fe(OH) + 2H+ = Fe2+ + 2HO
2 2
C.向磷酸二氢铵溶液中加入足量的氢氧化钠溶液:NH+ + OH-= NH∙HO
4 3 2
D.向CHBrCOOH中加入足量的
2
氢氧化钠溶液并加热:
CHBrCOOH + OH-CHBrCOO-+ HO
2 2 2
5.(2010四川高考)有关①100mL0.1mol/LNaHCO、②100mL0.1mol/LNaCO两种溶液的叙
3 2 3
述不正确的是
A.溶液中水电离出的H+个数:②>① B.溶液中阴离子的物质的量浓度之和:②>①
C.①溶液中:c(CO2-)>c(HCO) D.②溶液中:c(HCO-)>c(HCO)
3 2 3 3 2 3
6.(2010四川高考)中药狼把草的成分之一M具有消炎杀菌作用,M的结构如图所示:
下列叙述正确的是
A.M的相对分子质量是180
B.1molM最多能与2molBr发生反应
2
C.M与足量的NaOH溶液发生反应时,所得有机产物的化学式为CHONa
9 4 5 4
D.1molM与足量NaHCO反应能生成2molCO
3 2
第1页 | 共4页7.(2010四川高考)标准状况下V
L氨气溶解在1L水中(水的密度近似为1g/mL),所得溶液的密度为ρg/mL,质量分数为ω
,物质的量浓度为c mol/L,则下列关系中不正确的是
A.ρ = (17V + 22400) / (22.4 + 22.4V) B.ω = 17c / (1000ρ)
C.ω = 17V / (17V + 22400) D.c = 1000Vρ /(17V + 22400)
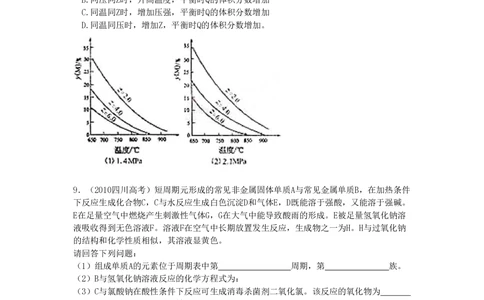
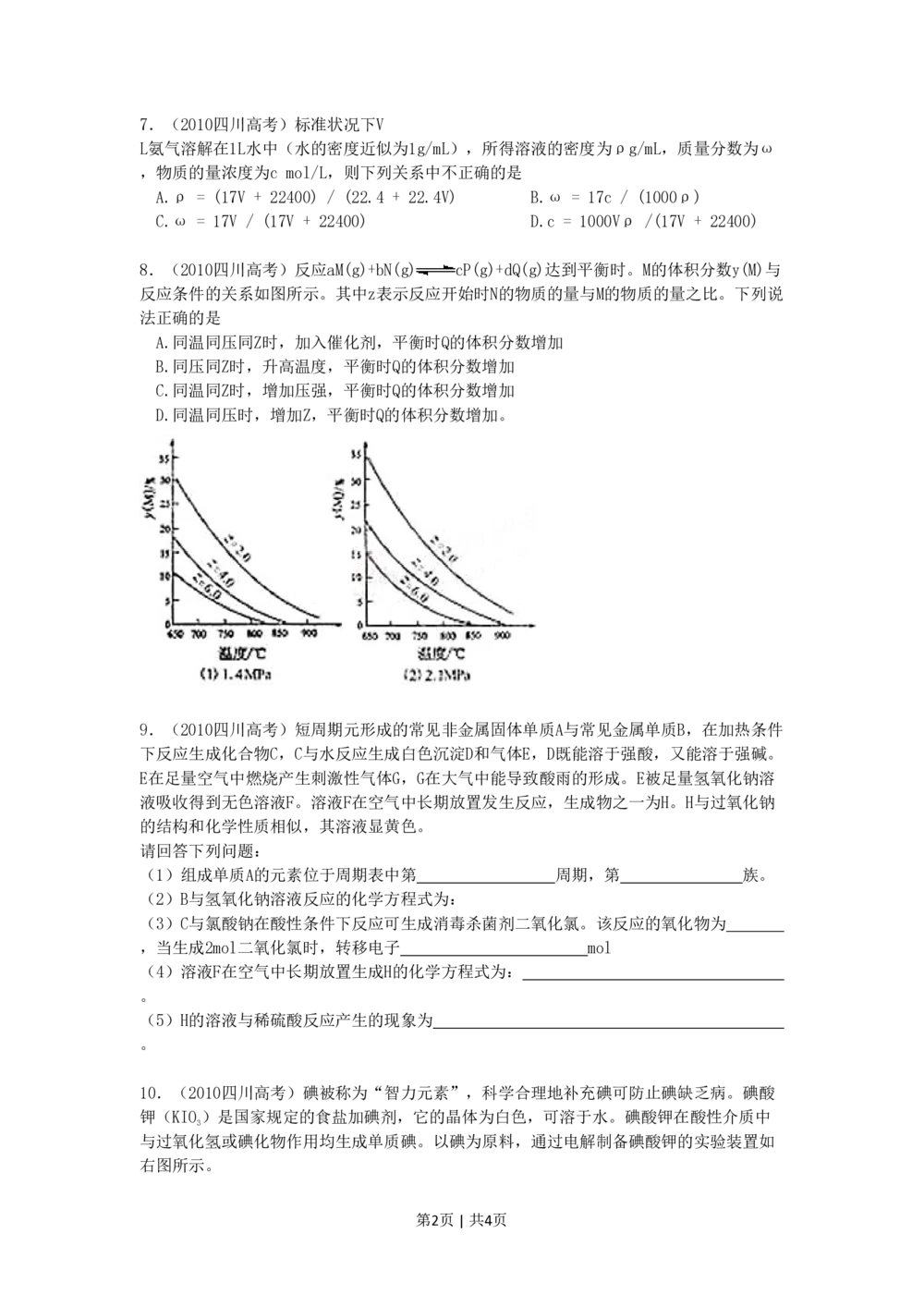
8.(2010四川高考)反应aM(g)+bN(g) cP(g)+dQ(g)达到平衡时。M的体积分数y(M)与
反应条件的关系如图所示。其中z表示反应开始时N的物质的量与M的物质的量之比。下列说
法正确的是
A.同温同压同Z时,加入催化剂,平衡时Q的体积分数增加
B.同压同Z时,升高温度,平衡时Q的体积分数增加
C.同温同Z时,增加压强,平衡时Q的体积分数增加
D.同温同压时,增加Z,平衡时Q的体积分数增加。
9.(2010四川高考)短周期元形成的常见非金属固体单质A与常见金属单质B,在加热条件
下反应生成化合物C,C与水反应生成白色沉淀D和气体E,D既能溶于强酸,又能溶于强碱。
E在足量空气中燃烧产生刺激性气体G,G在大气中能导致酸雨的形成。E被足量氢氧化钠溶
液吸收得到无色溶液F。溶液F在空气中长期放置发生反应,生成物之一为H。H与过氧化钠
的结构和化学性质相似,其溶液显黄色。
请回答下列问题:
(1)组成单质A的元素位于周期表中第 周期,第 族。
(2)B与氢氧化钠溶液反应的化学方程式为:
(3)C与氯酸钠在酸性条件下反应可生成消毒杀菌剂二氧化氯。该反应的氧化物为
,当生成2mol二氧化氯时,转移电子 mol
(4)溶液F在空气中长期放置生成H的化学方程式为:
。
(5)H的溶液与稀硫酸反应产生的现象为
。
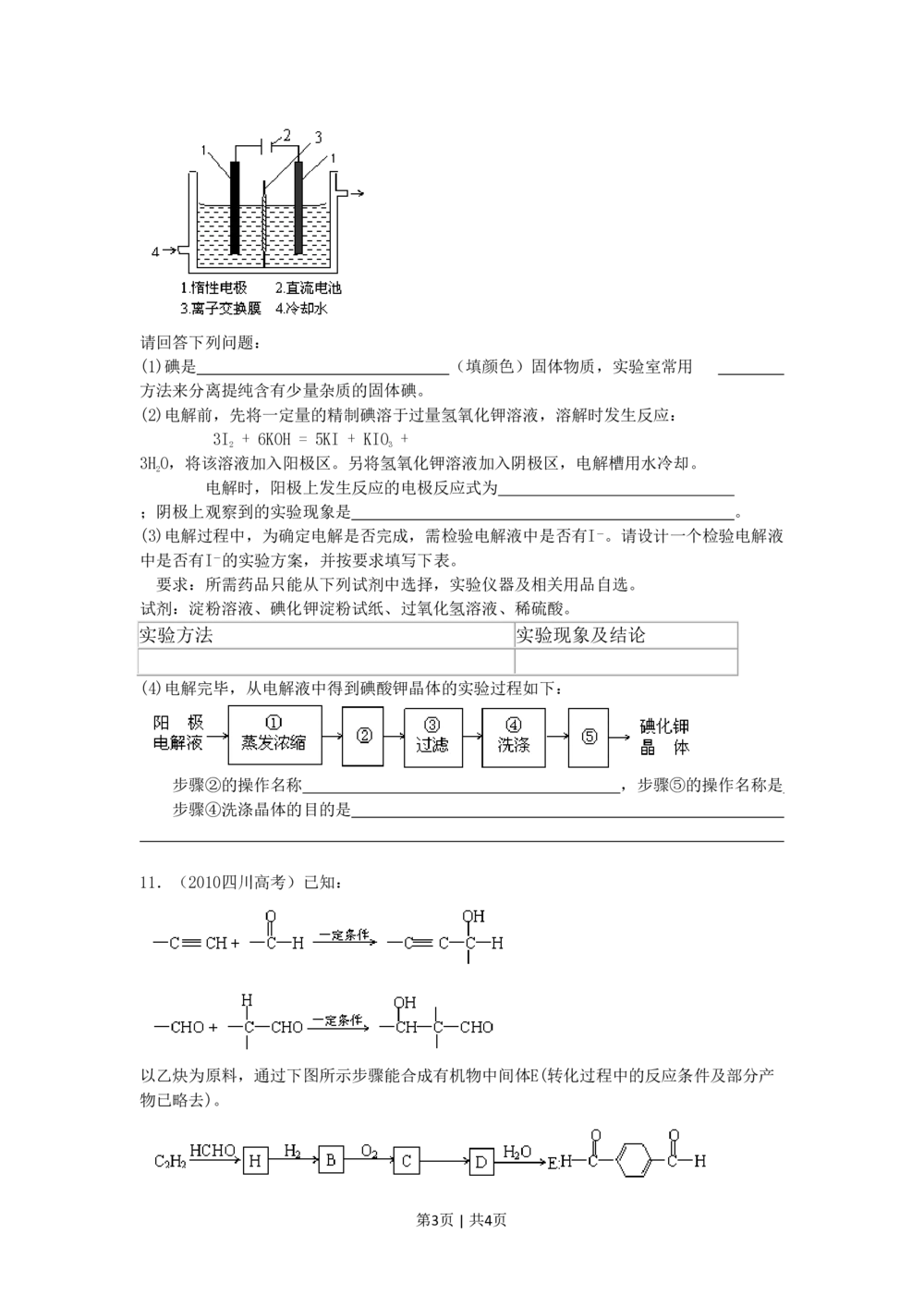
10.(2010四川高考)碘被称为“智力元素”,科学合理地补充碘可防止碘缺乏病。碘酸
钾(KIO)是国家规定的食盐加碘剂,它的晶体为白色,可溶于水。碘酸钾在酸性介质中
3
与过氧化氢或碘化物作用均生成单质碘。以碘为原料,通过电解制备碘酸钾的实验装置如
右图所示。
第2页 | 共4页请回答下列问题:
(1)碘是 (填颜色)固体物质,实验室常用
方法来分离提纯含有少量杂质的固体碘。
(2)电解前,先将一定量的精制碘溶于过量氢氧化钾溶液,溶解时发生反应:
3I + 6KOH = 5KI + KIO +
2 3
3HO,将该溶液加入阳极区。另将氢氧化钾溶液加入阴极区,电解槽用水冷却。
2
电解时,阳极上发生反应的电极反应式为
;阴极上观察到的实验现象是 。
(3)电解过程中,为确定电解是否完成,需检验电解液中是否有I-。请设计一个检验电解液
中是否有I-的实验方案,并按要求填写下表。
要求:所需药品只能从下列试剂中选择,实验仪器及相关用品自选。
试剂:淀粉溶液、碘化钾淀粉试纸、过氧化氢溶液、稀硫酸。
实验方法 实验现象及结论
(4)电解完毕,从电解液中得到碘酸钾晶体的实验过程如下:
步骤②的操作名称 ,步骤⑤的操作名称是
步骤④洗涤晶体的目的是
11.(2010四川高考)已知:
以乙炔为原料,通过下图所示步骤能合成有机物中间体E(转化过程中的反应条件及部分产
物已略去)。
第3页 | 共4页其中,A、B、C、D分别代表一种有机物;B的化学式为CH O,分子中无甲基。
4 10 2
请回答下列问题:
(1)A生成B的化学反应类型是 。
(2)写出生成A的化学方程式: 。
(3)B在浓硫酸催化下加热,可生成多种有机产物。写出两种相对分子质量比A小的有机产物
的结构简式:
、
。
(4)写出C生成D的化学反应方程式: 。
(5)含有苯环,且与E互为同分异构体的酯有
种,写出其中一种同分异构体的结构简式:
。
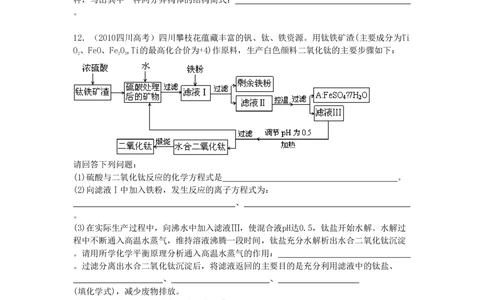
12.(2010四川高考)四川攀枝花蕴藏丰富的钒、钛、铁资源。用钛铁矿渣(主要成分为Ti
O、FeO、FeO,Ti的最高化合价为+4)作原料,生产白色颜料二氧化钛的主要步骤如下:
2 2 3
请回答下列问题:
(1)硫酸与二氧化钛反应的化学方程式是 。
(2)向滤液Ⅰ中加入铁粉,发生反应的离子方程式为:
、
。
(3)在实际生产过程中,向沸水中加入滤液Ⅲ,使混合液pH达0.5,钛盐开始水解。水解过
程中不断通入高温水蒸气,维持溶液沸腾一段时间,钛盐充分水解析出水合二氧化钛沉淀
。请用所学化学平衡原理分析通入高温水蒸气的作用:
。过滤分离出水合二氧化钛沉淀后,将滤液返回的主要目的是充分利用滤液中的钛盐、
、 、
(填化学式),减少废物排放。
(4)A可用于生产红色颜料(FeO),其方法是:将556a kg
2 3
A(摩尔质量为278g/mol)溶于水中,加入过量氢氧化钠溶液恰好完全反应,鼓入足量空气搅
拌,产生红褐色胶体,再向红褐色胶体中加入3336b kg A和112c
kg铁粉,鼓入足量空气搅拌,反应完全后,有大量FeO附着在胶体粒子上以沉淀形式析出
2 3
;过滤后,沉淀经高温灼烧得红色颜料,若所得滤液中溶质只有硫酸钠和硫酸铁,则理论
上可生产红色颜料 kg。
第4页 | 共4页