文档内容
微信公众号:文采学社
2 0 2 5 年 上 教 师 资 格 · 化 学 学 科 笔 试
社
学
采
道
文
渠
:
新
号
更
众
一
公
唯
信
微
主讲老师 岳筱涵
粉笔教师教育 粉笔教师微信公众号:文采学社
硫及其化合物
社
学
采
道
文
渠
:
新
号
更
众
一
公
唯
信
微微信公众号:文采学社
P73
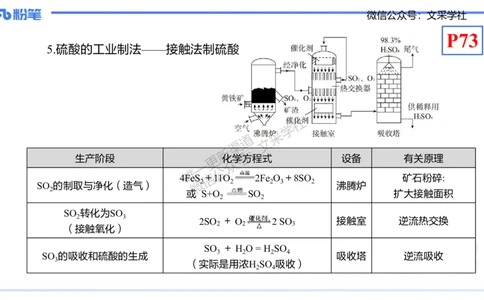
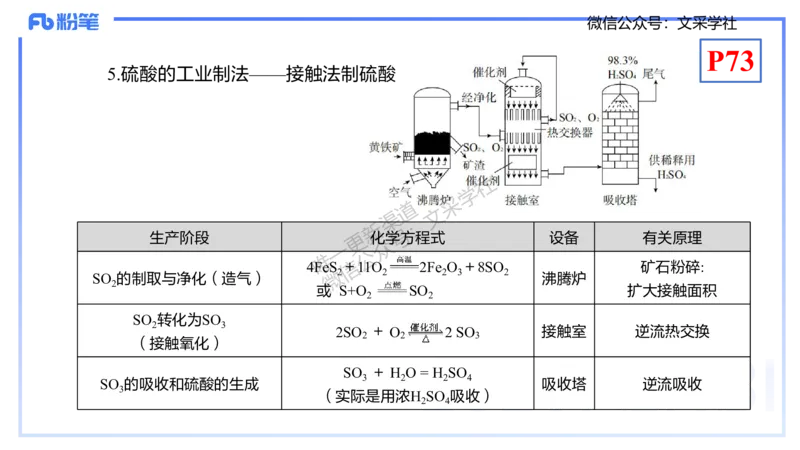
5.硫酸的工业制法——接触法制硫酸
社
学
采
道
文
渠
:
新
号
生产阶段 更化学方程式 设备 有关原理
众
一
公
唯
4FeS 信+11O 2Fe O +8SO 矿石粉碎:
微2 2 2 3 2
SO 的制取与净化(造气) 沸腾炉
2
或 S+O SO 扩大接触面积
2 2
SO 转化为SO
2 3
2SO + O 2 SO 接触室 逆流热交换
2 2 3
(接触氧化)
SO + H O = H SO
3 2 2 4
SO 的吸收和硫酸的生成 吸收塔 逆流吸收
3
(实际是用浓H SO 吸收)
2 4微信公众号:文采学社
吸收 SO 用 98.3% 的浓硫酸的原因:水和 SO 反应放出大量热,产生 P73
3 3
的酸雾悬浮在吸收塔中无法短时间内沉降下去,不利于反应正向进行,
从而降低吸收效率。而用98.3% 的浓硫酸吸收时放热很少,SO 作为溶质
3
溶解在 H SO 中,得到含 SO 的硫酸溶液,又叫发烟硫酸,以液体的形
2 4 3 社
学
采
式离开反应体系,平衡正向移动。 道
文
渠
:
新
号
更
众
一
公
唯
信
微微信公众号:文采学社
6.硫酸的用途:
P74
生产化肥、染料、精炼石油、炸药、农药等。
社
学
采
道
文
渠
:
新
号
更
众
一
公
唯
信
微微信公众号:文采学社
【粉笔提示】 P74
检验SO 2-时要排除Ag+、CO 2-的干扰,常用检测试剂是BaCl 溶液和
4 3 2
稀盐酸。
正确操作:
社
学
采
被检液加足量盐酸酸化,取清液滴加道氯化钡溶液,观察,若有沉淀,
文
渠
:
新
号
更
则有SO 2-;若无沉淀,则无SO 2-。
众
4 4一
公
唯
信
微微信公众号:文采学社
氮及其化合物
社
学
采
道
文
渠
:
新
号
更
众
一
公
唯
信
微微信公众号:文采学社
一、氮气的性质及用途 P75
(一)氮元素在自然界的存在
氮在自然界中既有游离态,又有化合态。N 是空气的主要成分,氮是生
2
命物质中的重要组成元素,是构成蛋白质和核酸不社可缺少的元素,是农作物生
学
采
道
长所必需的元素。 文
渠
:
新
号
更
众
一
公
唯
信
微微信公众号:文采学社
(二)化学性质 P75
常温下,N 的化学性质很不活泼,可代替稀有气体作保护气,但
2
在高温、放电、点燃等条件下,N 能与H 、O 、Mg、Ca等发生化学
2 2 2
反应。
社
学
采
1.N +3H 2NH 是工业上道合成氨的反应原理。
文
2 2 3 渠
:
新
号
更
2.与O 反应:N +O 2N众O
2 2 2 一
公
唯
信
3.与Mg反应:N +3Mg 微 Mg N
2 3 2
Mg N +6H O 3Mg(OH) +2NH ↑
3 2 2 2 3微信公众号:文采学社
(三)氮气的用途 P75
合成氨;制硝酸;作保护气,保护农副产品;液氮可作冷冻剂。
(四)氮气的工业制法 社
学
采
道
文
利用液态氮的沸点比液态氧的沸点渠低,从液态空气中将其分离而
:
新
号
更
众
制得氮气。 一
公
唯
信
微微信公众号:文采学社
P75
(五)氮的固定
将空气中游离的氮气转变为氮的化合物的方法,统称为氮的固定。氮的
固定有三种途径:
(1)生物固氮:豆科作物根瘤菌将N 转化为化合态氮。
社
2
学
采
(2)自然固氮:天空中打雷闪电时,道 N 转化为NO。
文
渠 2
:
新
号
更
(3)工业固氮:在一定条件下,由N 和H 合成氨。(也叫人工固氮)
众
一 2 2
公
唯
信
微微信公众号:文采学社
P76
二、氮的化合物
(一)氮的氧化物
氮氧化合物的种类
氮有+1、+2、+3、+4、+5五种正化合价,社可形成N O、NO、
学 2
采
道
N O 、NO 、N O 、N O 六种氧化物, 渠 其中N文O 和N O 分别是HNO 和
2 3 2 2 4 2 5 :2 3 2 5 2
新
号
更
众
HNO 的酸酐。 一
3 公
唯
信
微微信公众号:文采学社
1.一氧化氮(NO)
P76
(1)物理性质:无色、无味气体,有毒,难溶于水,密度与空
气接近,只能用排水法收集。
(2)化学性质:
社
学
采
2NO+O 2NO (常温下很容易道化合)
2 2 文
渠
:
新
号
4NO+3O +2H O 4HNO更
众
2 2 一3
公
唯
信
微微信公众号:文采学社
(3)实验室制备:
P76
3Cu+8HNO (稀) 3Cu(NO ) +2NO↑+4H O
3 3 2 2
(4)工业制备:
4NH +5O 4NO+6H O
3 2 2 社
学
采
N +O 2NO 道
2 2 文
渠
:
新
号
更
众
一
公
唯
信
微微信公众号:文采学社
2.二氧化氮(NO )
P76
2
(1)物理性质:红棕色气体,有刺激性气味,有毒,易液化,
易溶于水,只能用向上排空气法收集。
(2)化学性质:
社
学
采
3NO +H O 2HNO +NO(工业道上利用这一原理生产硝酸)
2 2 3 文
渠
:
新
号
4NO +O +2H O 4HNO更
众
2 2 2 一3
公
唯
信
NO +SO SO +NO(NO 具有强氧化性)
微
2 2 3 2微信公众号:文采学社
P76
2NO +2NaOH NaNO +NaNO +H O(自身的氧化还原反应)
2 3 2 2
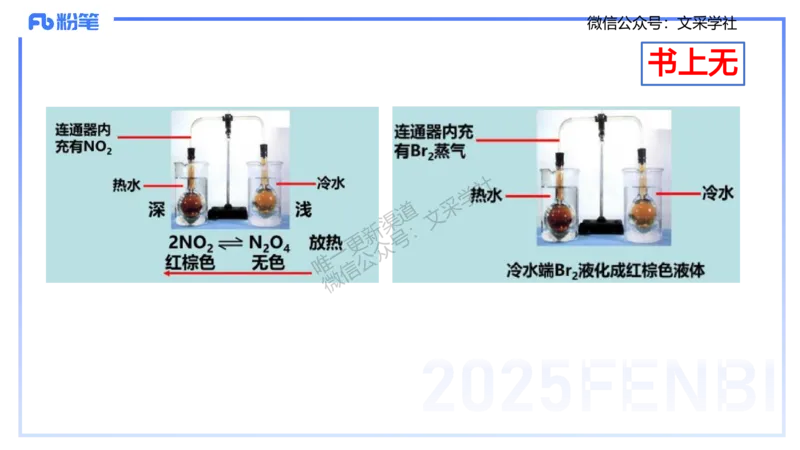
2NO N O (利用颜色变化判断平衡)
2 2 4
2NO 2NO+O (加热时分解)
2 2
社
学
采
(3)实验室制备: 道
文
渠
:
新
号
Cu+4HNO (浓) Cu(NO )更+2NO ↑+2H O
众
3 一3 2 2 2
公
唯
信
微微信公众号:文采学社
P76
【粉笔提示】
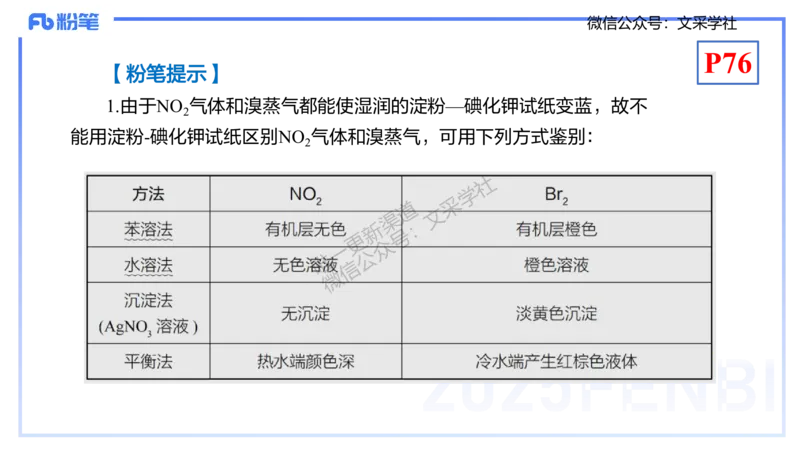
1.由于NO 气体和溴蒸气都能使湿润的淀粉—碘化钾试纸变蓝,故不
2
能用淀粉-碘化钾试纸区别NO 气体和溴蒸气,可用下列方式鉴别:
2
社
学
采
道
文
渠
:
新
号
更
众
一
公
唯
信
微微信公众号:文采学社
书上无
社
学
采
道
文
渠
:
新
号
更
众
一
公
唯
信
微微信公众号:文采学社
【粉笔提示】 P77
2.NO 是造成光化学烟雾的主要因素。NO 在紫外线照射下,会发生
2 2
一系列光化学反应,生成一种有毒的烟雾——光化学烟雾。光化学烟雾
刺激呼吸器官,危害人体的健康。
社
学
采
道
文
渠
:
新
号
更
众
一
公
唯
信
微微信公众号:文采学社
(二)氨的性质及用途
P77
NH 是无色、有刺激性气味的气体,极易溶于水且溶解得很快;
3
常温时,1体积水大约可以溶解700体积的氨。
1.与水反应
社
学
采
氨的水溶液叫作氨水。氨溶于水时,道大部分氨与水结合成一水合
文
渠
:
新
号
氨(NH ·H O),NH ·H O易挥发,更受热会分解为NH 和H O。
众
3 2 3 2 一 3 2
公
唯
信
NH +H O NH ·H O
微
3 2 3 2
NH ·H O NH ↑+H O
3 2 3 2微信公众号:文采学社
常温下,一水合氨中有一小部分电离成NH +和OH-,所以氨水
P77
4
有弱碱性,能使酚酞变红、使紫色石蕊试纸变蓝。
氨在水中的反应可以表示如下:
社
学
采
NH +H O NH ·H O NH +道+OH-
3 2 3 2 4 文
渠
:
新
号
也可以简单表示如下: 更
众
一
公
唯
信
NH +H O NH ++OH-
微
3 2 4
NH 是中学阶段唯一能使湿润的红色石蕊试纸变蓝的气体。
3微信公众号:文采学社
P77
2.与酸反应
NH 与HCl、H SO 反应的离子方程式:
3 2 4
NH +H+ NH +。
3 4
社
学
采
NH 与HNO 反应: 道
3 3 文
渠
:
新
号
NH +HNO NH NO (不更能发生氧化还原反应)。
众
3 3 4 3 一
公
唯
信
微微信公众号:文采学社
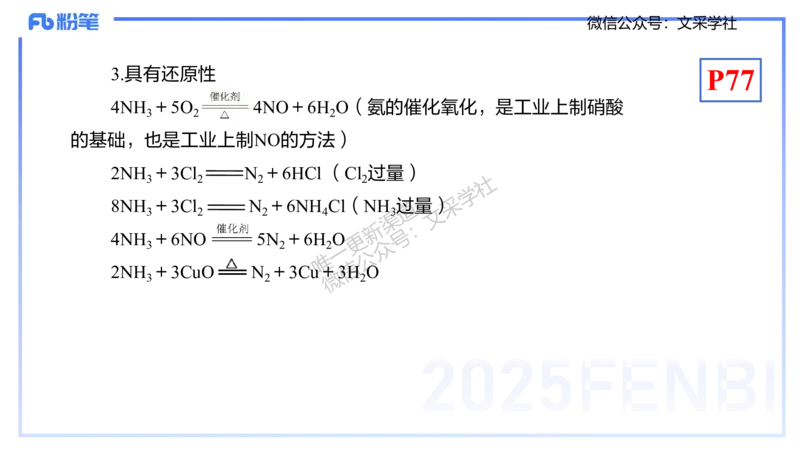
3.具有还原性
P77
4NH +5O 4NO+6H O(氨的催化氧化,是工业上制硝酸
3 2 2
的基础,也是工业上制NO的方法)
2NH +3Cl N +6HCl (Cl 过量)
3 2 2 2 社
学
采
8NH +3Cl N +6NH Cl(NH 道过量)
3 2 2 4 3 文
渠
:
新
号
4NH +6NO 5N +6H O更
众
3 2 2一
公
唯
信
2NH +3CuO N +3Cu+3H O
微
3 2 2微信公众号:文采学社
4.氨的用途
P78
(1)氨是氮肥工业及制造硝酸、铵盐、纯碱等的重要原料。
(2)氨也是有机合成工业的常用原料(如制尿素、合成纤维、
染料等)。
社
学
采
(3)氨还可用作制冷剂。 道
文
渠
:
新
号
更
众
一
公
唯
信
微微信公众号:文采学社
【粉笔提示】 P78
实验一:氨气的实验室制法
1.原理:铵盐与碱共热,产生氨气。
2NH Cl+Ca(OH) CaCl +2NH ↑+2H O社
4 2 2 3 2
学
采
道
2.装置:固-固反应加热装置,发生装置文与制取O 的相似。
渠
2
:
新
号
更
3.收集:由于NH 易溶于水,密度众比空气小,所以只能用向下排空气法。
一
3 公
唯
信
4.检验:①用湿润的红色石微蕊试纸(变蓝);
②蘸有浓盐酸的玻璃棒靠近瓶口(产生白烟)。微信公众号:文采学社
5.注意:
P78
①消石灰不能用固体KOH或固体NaOH代替,因后两者易吸湿结
块,不利于产生NH ,且高温下会腐蚀试管。
3
②不能用P O 或浓H SO 干燥氨气,也不能用无水CaCl
2 5 2 4 社 2
学
采
(8NH +CaCl CaCl ·8NH ),通道常用碱石灰干燥氨气。
3 2 2 3 文
渠
:
新
号
6.其他制法: 更
众
一
公
唯
信
浓氨水或浓铵盐溶液滴到生石灰或烧碱中制氨气,直接加热浓氨
微
水也可制氨气。微信公众号:文采学社
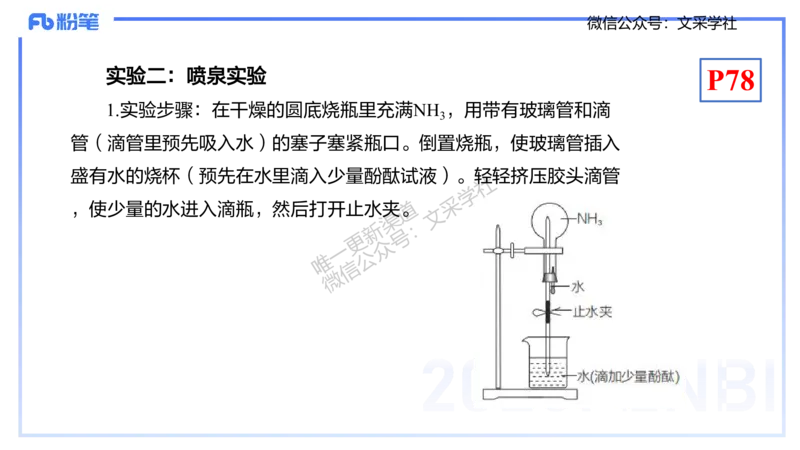
实验二:喷泉实验 P78
1.实验步骤:在干燥的圆底烧瓶里充满NH ,用带有玻璃管和滴
3
管(滴管里预先吸入水)的塞子塞紧瓶口。倒置烧瓶,使玻璃管插入
盛有水的烧杯(预先在水里滴入少量酚酞试液)。轻轻挤压胶头滴管
社
学
采
,使少量的水进入滴瓶,然后打开止水夹道。
文
渠
:
新
号
更
众
一
公
唯
信
微微信公众号:文采学社
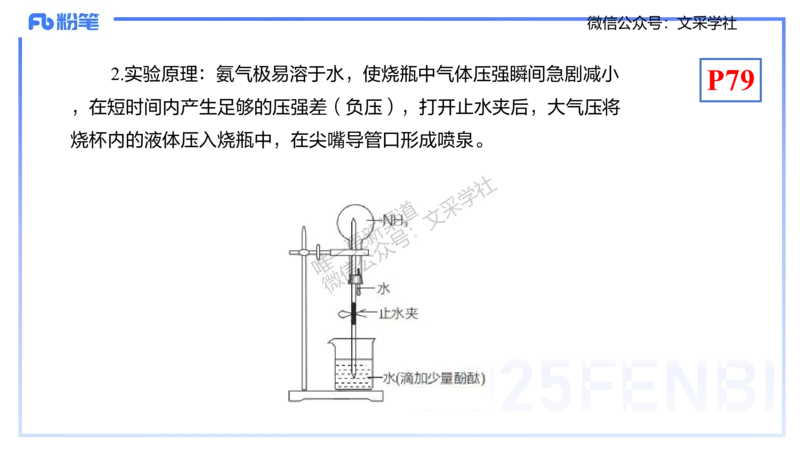
2.实验原理:氨气极易溶于水,使烧瓶中气体压强瞬间急剧减小
P79
,在短时间内产生足够的压强差(负压),打开止水夹后,大气压将
烧杯内的液体压入烧瓶中,在尖嘴导管口形成喷泉。
社
学
采
道
文
渠
:
新
号
更
众
一
公
唯
信
微微信公众号:文采学社
3.实验成功关键:
P79
①盛气体的烧瓶必须干燥;
②气体充满烧瓶;
③烧瓶不能漏气(实验前应先检查装置的气密性);
社
学
采
④所用气体能大量溶于所用液体或气道体与液体快速反应。
文
渠
:
新
号
CO 、H S、Cl 等与水不能形成更喷泉,但与NaOH溶液可形成喷泉。
众
2 2 2 一
公
唯
信
微微信公众号:文采学社
(三)铵盐的性质 P79
1.物理性质
铵盐是由铵根离子和酸根离子构成的化合物,铵盐一般都是白色
或无色晶体,都易溶于水。
社
学
采
道
文
渠
:
新
号
更
众
一
公
唯
信
微微信公众号:文采学社
2.化学性质
P79
(1)受热分解(热解)
NH Cl NH ↑+HCl↑
4 3
NH HCO NH ↑+H O+CO ↑
4 3 3 2 2 社
学
采
(2)与强碱反应(碱解——铵盐的共道性)
文
渠
:
新
号
NH NO +NaOH NaNO +更NH ↑+H O
众
4 3 一3 3 2
公
唯
信
(3)水解反应
微
NH ++H O NH ·H O+H+(强酸的铵盐溶液呈酸性)
4 2 3 2微信公众号:文采学社
3.NH +的检验
P79
4
取少许样品(固体或溶液),与强碱(固体或溶液)共热,用湿
润的红色石蕊试纸检验生成的气体,试纸变蓝。
社
学
采
4.用途 道
文
渠
:
新
号
作氮肥、制炸药、制焊药等。更
众
一
公
唯
信
微微信公众号:文采学社
(四)硝酸
P80
1.物理性质
(1)纯硝酸为无色、有刺激性气味的液体。
(2)硝酸易挥发,在空气中遇水蒸气呈白雾状。
社
(3)质量分数为69%以上的硝酸称为浓硝酸。
学
采
道
文
渠
:
新
号
更
2.化学性质 众
一
公
唯
信
(1)强酸性
微
能与碱、CuO等碱性氧化物、BaCO 等盐反应,稀硝酸能使紫色
3
石蕊试液变红。微信公众号:文采学社
(2)不稳定性
P80
硝酸不稳定,见光或受热易分解,其反应方程式为:
4HNO 2H O+4NO ↑+O ↑
3 2 2 2
存放:HNO 应盛放在棕色试剂瓶里,并存放在黑暗阴凉处。
3 社
学
采
浓硝酸常呈黄色是因为HNO 分解产道生的NO 溶解于浓硝酸,去
3 文 2
渠
:
新
号
掉浓硝酸中黄色的方法是通入少量更O ,发生的反应为:
众
一 2
公
唯
信
4NO +O +2H O 4HNO
微
2 2 2 3微信公众号:文采学社
(3)强氧化性
P80
①浓硝酸使紫色石蕊溶液先变红(H+作用),加热后褪色(强氧化
性,即漂白作用)。用此可以证明浓硝酸的氧化性比稀硝酸强。
②与金属单质的反应(大部分金属能与硝酸反应)
社
学
采
Cu+4HNO (浓) Cu(NO ) +2N道O ↑+2H O
3 3 2 2 文 2
渠
:
新
号
3Cu+8HNO (稀) 3Cu(NO更) +2NO↑+4H O
众
3 一3 2 2
公
唯
信
③常温下,铁、铝遇冷的浓HNO 发生钝化,原因是浓HNO 使Fe、
微
3 3
Al表面生成一层致密的氧化物薄膜,阻止了酸与内层金属的进一步反应,
故常温下可用铁、铝容器盛装冷的浓HNO 。
3微信公众号:文采学社
④与非金属单质(木炭)的反应
P80
C+4HNO (浓) CO ↑+4NO ↑+2H O
3 2 2 2
⑤与其他还原剂反应
3Fe2++4H++NO - 3Fe3++NO↑+2H O
3 2 社
学
采
6I-+8H++2NO - 3I +2NO↑+道4H O
3 2 文2
渠
:
新
号
⑥浓硝酸和浓盐酸按体积比1:更3混合即为王水,王水的氧化性更强,
众
一
公
唯
信
能溶解Pt、Au等金属。
微
3.用途:制炸药、染料、塑料、硝酸盐等。微信公众号:文采学社
4.制备实验——氨催化氧化法制硝酸
P81
(1)实验原理
4NH +5O 4NO+6H O
3 2 2
社
2NO+O 2NO 学
2 2 采
道
文
渠
:
新
号
3NO +2H O 2HNO +N更O
2 2 3 众
一
公
唯
信
微微信公众号:文采学社
P81
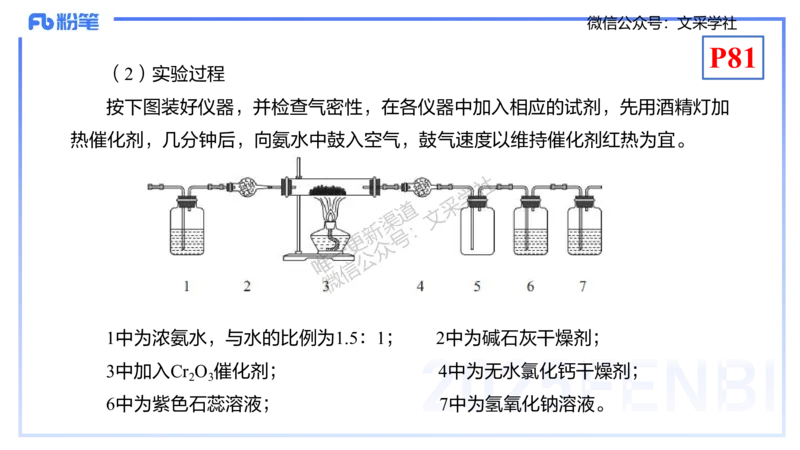
(2)实验过程
按下图装好仪器,并检查气密性,在各仪器中加入相应的试剂,先用酒精灯加
热催化剂,几分钟后,向氨水中鼓入空气,鼓气速度以维持催化剂红热为宜。
社
学
采
道
文
渠
:
新
号
更
众
一
公
唯
信
微
1中为浓氨水,与水的比例为1.5:1; 2中为碱石灰干燥剂;
3中加入Cr O 催化剂; 4中为无水氯化钙干燥剂;
2 3
6中为紫色石蕊溶液; 7中为氢氧化钠溶液。微信公众号:文采学社
P81
【粉笔提示】 三种强酸的比较
盐酸 硫酸 硝酸
①无色、有刺激性气味、易挥发
①无色、易挥发的液体
物理 ①无色、粘稠、油状液体 的液体
②浓盐酸在空气中易形 社
性质 ②沸点高因而难挥发学 ②在空气中形成白雾,质量分数
成白雾 道 采
文
渠 在98%以上时有“发烟”现象
:
新
号
更
①稀盐酸侧重于强酸性, 众
一
①强酸唯性:稀公 H SO 具有酸的通性 ①强酸性:具有酸的通性
信 2 4
具有酸的通性
微
化学 ②浓H SO 具有吸水性、脱水性、 ②强氧化性:
2 4
②浓盐酸侧重于还原性:
性质 强氧化性: Cu+4HNO (浓)
3
MnO +4HCl(浓)
2
Cu+2H SO (浓) CuSO +SO ↑+2H O Cu(NO ) +2NO ↑+2H O
2 4 4 2 2 3 2 2 2
MnCl +Cl ↑+2H O
2 2 2
工业
H 在Cl 中燃烧 接触法 氨催化氧化法
2 2
制法微信公众号:文采学社
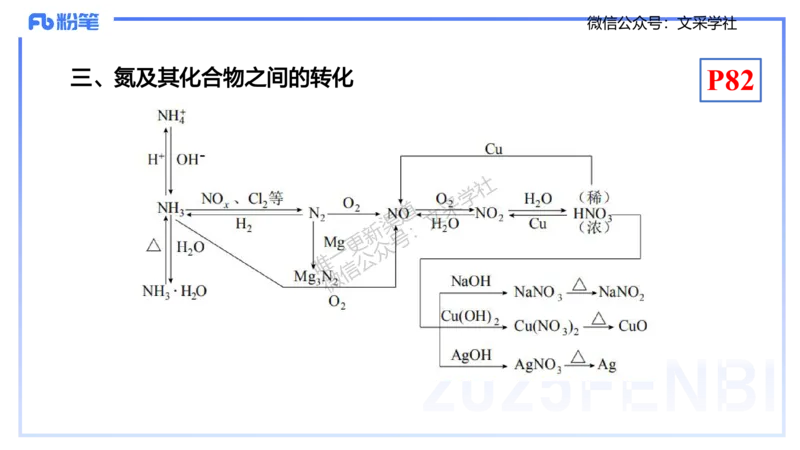
三、氮及其化合物之间的转化 P82
社
学
采
道
文
渠
:
新
号
更
众
一
公
唯
信
微微信公众号:文采学社
P82
1. 某些气体分子的微观示意图如下表所示:
社
学
采
道
文
渠
:
一定条件下,3.4g 甲物质和 4.8g 氧气恰好完全新反应,生成 5.4g 乙物质和另一物质 X。下列判断不
号
更
众
一
正确的是( )。 唯 公
信
微
A. 物质甲的化学式是 NH
3
B. 物质 X 的质量为 2.8g
C. 物质 X 含两种元素
D. 该反应的化学方程式中物质 X 与 O 的化学计量数之比为 2 ∶ 3
2微信公众号:文采学社
P83
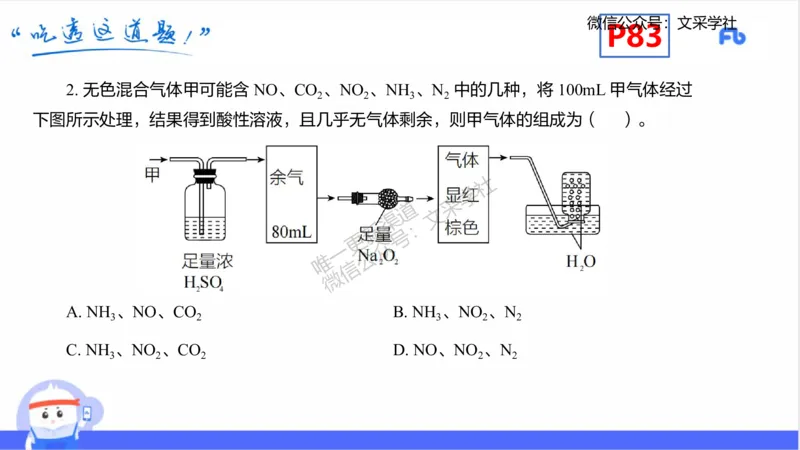
2. 无色混合气体甲可能含 NO、CO 、NO 、NH 、N 中的几种,将 100mL 甲气体经过
2 2 3 2
下图所示处理,结果得到酸性溶液,且几乎无气体剩余,则甲气体的组成为( )。
社
学
采
道
文
渠
:
新
号
更
众
一
公
唯
信
微
A. NH 、NO、CO B. NH 、NO 、N
3 2 3 2 2
C. NH 、NO 、CO D. NO、NO 、N
3 2 2 2 2微信公众号:文采学社
社
学
采
道
文
渠
:
新
号
更
众
一
公
唯
信
微
粉笔教师教育 粉笔教师