文档内容
2 0 2 5 年 上 教 师 资 格 · 化 学 学 科 笔 试
主讲老师 王双奕
粉笔教师教育 粉笔教师目
录
content
1 化学反应与能量
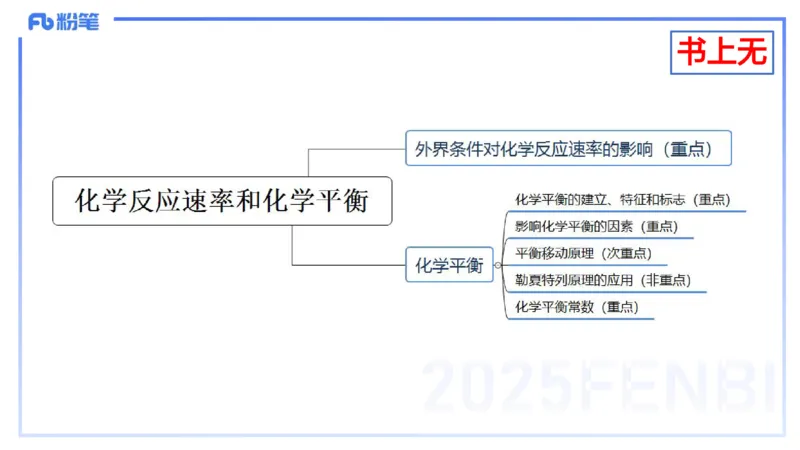
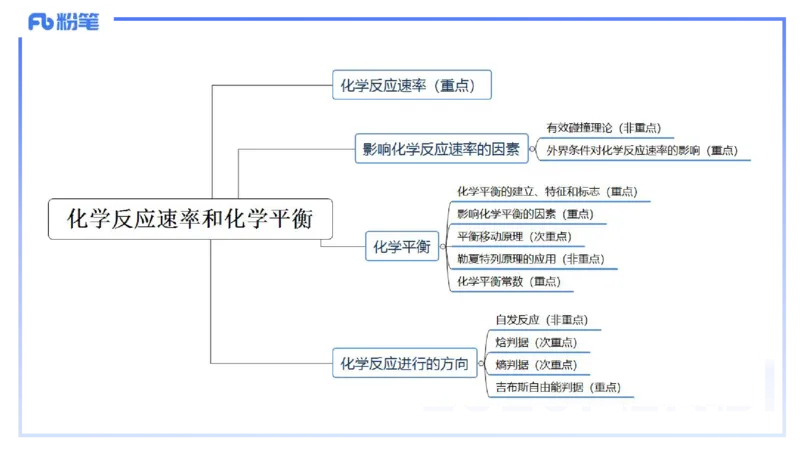
2 化学反应速率和化学平衡
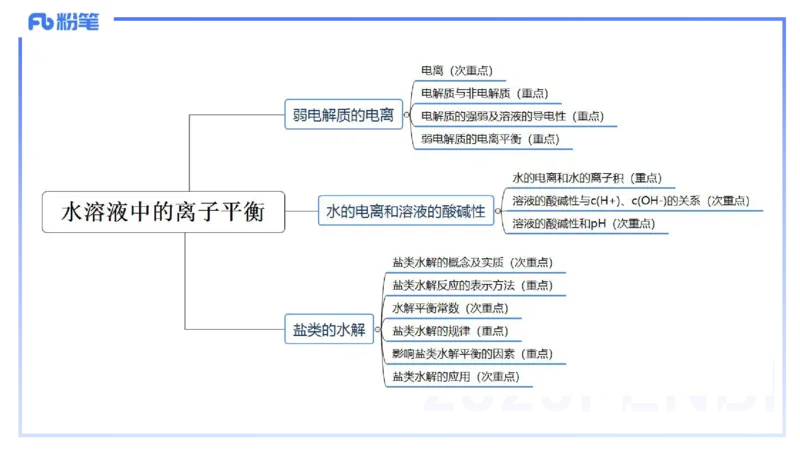
3 水溶液中的离子平衡
4 电化学基础化学反应速率和化学平衡P138
2.化学平衡常数的应用
(1)K 值越大,说明平衡体系中生成物所占的比例越大,它的正向反应
进行的程度越大,即该反应进行得越完全,反应物转化率越大;反之,反应
进行得就越不完全,反应物转化率就越小。
(2)若用任意状态的浓度幂之积的比值(称为浓度商,用 Q 表示)与K
c
比较,可判断可逆反应是否达到平衡状态和反应进行的方向。P138
对于一般的可逆反应 aA(g) + bB(g) cC(g) + dD(g) :
Q < K,反应向正反应方向进行;
c
Q = K,反应达到平衡状态;
c
Q > K,反应向逆反应方向进行。
cP141P139
(3)利用 K 可判断反应的热效应。
若升高温度,K 值增大,则反应正向进行,正反应为吸热反应;
若升高温度,K 值减小,则反应逆向进行,正反应为放热反应。
(4)计算转化率
依据起始浓度(或平衡浓度)和平衡常数可以计算平衡浓度(或起始浓
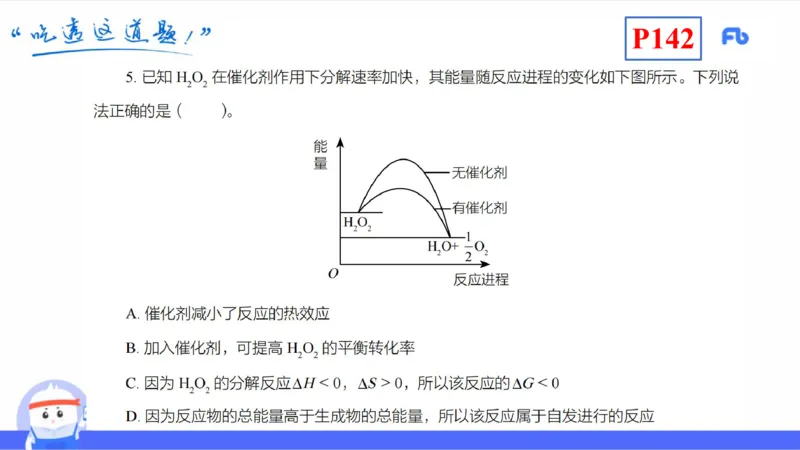
度),从而计算反应物的转化率。(结合三段式法)P142书上无P139
四、化学反应进行的方向
(一)自发反应
在一定条件下,无需外界帮助就能自发进行的反应称为自发反应。
例如:镁条燃烧,酸碱中和,铁器暴露在潮湿空气中会生锈,甲烷或氢
气与氧气的混合气体遇明火就爆炸,锌与硫酸铜溶液会自动反应生成铜和硫
酸锌等。P139
(二)焓判据
自发过程的体系总是趋向于从高能量状态转变为低能量状态,这时
体系会对外做功,释放能量,表现为焓变 ∆H<0, 这一判断方式的主要
依据是焓变,也称为焓判据。P139
焓判据 放热反应过程中体系能量降低,具有自发性进行的倾向
多数放热反应 (∆H<0)能自发进行,
例如酸碱中和反应、钠与水的反应、生石灰与水的反应
自发反应与焓变
部分吸热反应 (∆H>0)也能自发进行,例如盐类的水解
的关系
有一些吸热反应 (∆H>0) 常温下不能自发进行,但在较高温度下则能
自发进行,例如碳酸钙受热分解
多数自发进行的化学反应是放热反应,但也有很多吸热反应能自发进
结论
行。因此,只根据焓变判断反应进行的方向是不全面的P139
(三)熵判据
1.熵与熵变
熵:衡量一个体系混乱度的物理量,符号为 S。熵值越大,体系的
混乱度越大。
熵变:发生化学反应时物质熵的变化,符号为 ∆S。P140
【粉笔提示】
影响物质熵值大小的因素:
(1)同一条件下,不同的物质熵值不同。
(2)同一物质的熵,气态时熵值最大,液态时次之,固态时最小,即 S > S > S 。
g l s
(3)同一物质在相同的聚集状态时,其熵值随温度的升高而增大,即 S > S 。
高温 低温
(4)同一条件下,同一物质物质的量越大,分子数越多,熵值越大。
(5)混合物或溶液的熵值往往比相应的纯物质的熵值大,即 S > S 。
混合物 纯物质P140
2.熵增原理
(1)熵增原理
自发过程的体系趋向于有序转变为无序,导致体系的熵增加,叫作熵增原
理,也是反应方向判断的熵判据。
(2)常见的熵增过程
固体的溶解过程、气体的扩散过程、水的汽化过程及墨水的扩散过程都是
体系混乱度增大的过程,即熵增的过程。P140
(3)常见的熵增反应
产生气体的反应以及气体物质的量增大的反应,熵变通常都是正值,为
熵增加的反应。
例如:碳酸钙受热分解,碳与 H O(g) 反应生成 CO 与 H ,NH HCO 固
2 2 4 3
体溶解于醋酸溶液中。P140
3.反应的熵变与反应方向
(1)熵增加的反应大多能在常温常压下自发进行,例如过氧化氢的分
解反应。
(2)有些熵增加的反应在常温常压下不能自发进行,但在较高温度下
可自发进行,例如碳酸钙受热分解、碳与 H O(g) 反应生成 CO 与 H 。
2 2
(3)有些熵减小的反应(∆S<0)在一定条件下也可以自发进行,例
如铝热反应。
熵变是判断反应能否进行的又一个因素,但不是唯一因素,只根据熵
变来判断反应进行的方向也是不全面的。P140
(四)吉布斯自由能判据
正确判断一个化学反应是否能自发进行,必须综合考虑反应的焓变(ΔH)
和熵变(ΔS)。为了同时考虑能量和混乱度两方面的因素,化学家 Gibbs 提
出了一个新的热力学函数——吉布斯自由能 G 。
反应自发性的判断依据如下:
ΔG=ΔH-TΔS<0,反应能自发进行;
ΔG=ΔH-TΔS=0,反应达到平衡状态;
ΔG=ΔH-TΔS>0,反应不能自发进行。书上无
ΔH ΔS ΔG = ΔH-TΔS 自发性
<0 >0 永远<0 任何温度下,正反应自发
>0 <0 永远>0 任何温度下,正反应非自发
>0 >0 T高时为负值 在高温下,正反应自发
<0 <0 T低时为正值 在低温下,正反应自发P141P142水溶液中的离子平衡P144
一、弱电解质的电离
(一)电离
概念:电解质在水溶液里或熔融状态下产生能够自由移动的离子的过程。
电离的条件:熔融状态(离子化合物)或水溶液里(离子化合物和共价化合
物)。
电解质溶液导电的原因:电解质在溶液中发生电离,产生了能够自由移动的
离子。P145
( 二 ) 电 解 质 与 非 电 解 质
类别 定义 相同点 不同点 实例
在水溶液里或熔融状态 一定条件下能够电离, NaCl、
电解质
下能够导电的化合物 产生的离子能导电 H SO 、NaOH
都是 2 4
化合物
在水溶液里和熔融状态
非电解质 不能电离,不能导电 蔗糖、酒精
下都不导电的化合物P145
【粉笔提示】
1.必须是化合物自身在水溶液里或熔融状态下电离出离子,该化合物才是电解质。
一种物质溶于水形成的溶液能导电,原物质不一定是电解质,如 SO 、SO 、NH 等都
2 3 3
是非电解质。
2.单质和混合物既不是电解质也不是非电解质。
3.用实验区分离子化合物与共价化合物的常用方法:看熔融状态时是否导电。
4.常见的酸都是共价化合物(液态醋酸、硫酸等均不导电)。(三)电解质的强弱及溶液的导电性 P145
1.强、弱电解质的比较
强电解质 弱电解质
相同点 都是电解质,在水溶液中都能电离,都能导电
电离程度 完全电离 部分电离
电离过程 不可逆过程 可逆过程,存在电离平衡
不
表示方法 用等号 用可逆符号
同
电解质在溶液
点
离子 分子、离子
中的存在形式
电离方程式 HI = H++I- NH ·H O NH ++OH-
3 2 4
强酸:HCl、H SO 、HNO 、HBr 等;弱酸:CH COOH、 H CO 、HCN 等;
2 4 3 3 2 3
举例 强碱:KOH、NaOH、Ba(OH) 等; 弱碱: NH ·H O、Cu(OH) 等;
2 3 2 2
绝大部分盐:BaSO 、BaCl 等 H O及小部分盐:(CH COO) Pb 等
4 2 2 3 2P146
2.电解质溶液的导电性
溶液的导电性,主要取决于溶液中离子浓度的大小。
对于相同条件(相同温度、相同浓度)下的强、弱电解质来说,强电解
质溶液的导电性比弱电解质溶液的导电性强,这主要是因为强电解质在水溶
液中能完全电离,而弱电解质在水溶液中只有少部分电离,大部分以分子形
式存在于溶液中。P146
(四)弱电解质的电离平衡
1.电离平衡的建立
在一定条件(如温度、浓度)下,当电解质分子电离成离子的速率和离子结合
成分子的速率相等时,电离过程就达到了平衡状态。平衡建立过程的 ν-t 图像如
下图所示。P146
2.电离平衡的特征
(1)等:ν(电离)=ν(结合)。
(2)动:ν(电离)=ν(结合)≠ 0的动态平衡,反应仍在不断进行。
(3)定:达到平衡后,分子和离子浓度一定。
(4)变:条件改变,平衡破坏,发生移动。P146
3.电离平衡的移动
电离平衡受温度、浓度等因素的影响,加入与电解质含相同离子的盐
或能与电解质发生反应的物质也能使电离平衡发生移动。
(1)温度:升高温度,平衡正移,电离程度增大。(因为水解和电离
都是吸热的)P146
(2)浓度:以弱电解质 HB 的电离平衡 HB H++B- 为例。
①增大弱电解质的浓度,平衡正移,但电离程度减弱。
②减小弱电解质的浓度(稀释),平衡正移,但电离程度增加。
所以,溶液越稀越电离。P147
(3)同离子效应:加入与电解质含相同离子的盐,平衡逆向移动,电
离程度减弱。
(4)加入能与电解质离子发生反应的物质使电离平衡正向移动,电离
程度增加。P147
4.电离平衡常数
(1)概念
在一定条件下,弱电解质的电离达到平衡时,溶液中电离所生成的各种
离子浓度幂的乘积跟溶液中未电离的分子浓度幂的比是一个常数,这个常数
叫作电离平衡常数,简称电离常数,用 K 表示(酸用 K 表示,碱用 K 表
a b
示)。P147
(2)表示方法
对于可逆反应AB A+ + B-,有:
c(A )c(B )
K
c(AB)
对于多元弱酸(弱碱),其电离是分步进行的,每步电离都有电离常数,
通常用 K 、K 、K 等分别表示,且有 K >>K >>K 。
1 2 3 1 2 3P147
(3)影响因素
温度: K (或 K )只随温度的变化而变化,不随浓度的变化而变化。
a b
(4)意义
反映弱酸、弱碱酸碱性的相对强弱。
在一定温度下, K 越大(多元弱酸以 K 为依据),弱酸的电离程度就越
a a1
大,溶液浓度相同时 c(H+) 也越大,弱酸的酸性越强。
K 越小,对应强碱弱酸盐的水解程度越大。
aP147
二、水的电离和溶液的酸碱性
(一)水的电离和水的离子积
1.水的电离
水是一种极弱的电解质,它能微弱地电离:
H O H++OH-
2
实验测得:25 ℃ 时,1 L 纯水中只有 1×10-7 mol 的水分子发生电离,
故 25 ℃ 时的纯水中 c(H+) = c(OH-) = 10-7 mol/L。P148
2.水的离子积
一定温度下,c(H+) 与 c(OH-) 的乘积是一个常数,称为水的离子积常数,
简称水的离子积,用符号 K 表示,即 K = c(H+)·c(OH-) 。
w w
(1)在一定温度下,水的离子积是一个常数,在 25 ℃ 时 K =1×10-14。
w
(2) K 随温度的变化而变化,温度升高, K 增大。
w w
(3)在酸性或碱性的稀溶液中,由水电离出的 c(H+) 和 c(OH-) 总是相等
的,即 c(H+) = c(OH-) 。
水 水P148
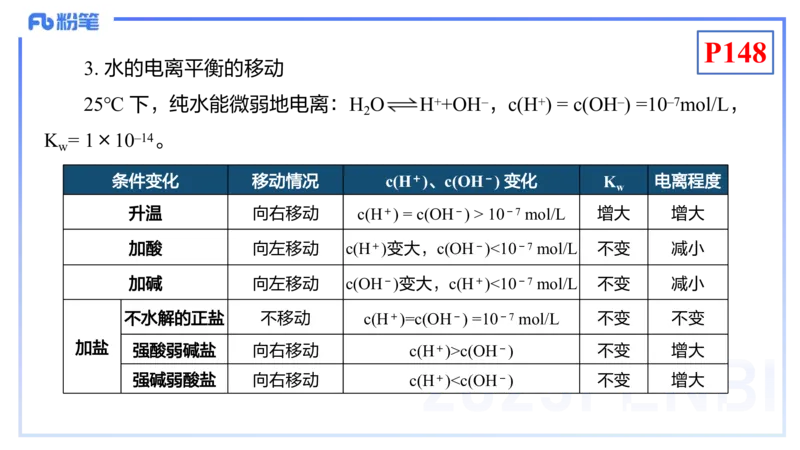
3. 水的电离平衡的移动
25℃ 下,纯水能微弱地电离:H O H++OH–,c(H+) = c(OH–) =10–7mol/L,
2
K = 1×10–14。
w
条件变化 移动情况 c(H+)、c(OH-) 变化 K 电离程度
w
升温 向右移动 c(H+) = c(OH-) > 10-7 mol/L 增大 增大
加酸 向左移动 c(H+)变大,c(OH-)<10-7 mol/L 不变 减小
加碱 向左移动 c(OH-)变大,c(H+)<10-7 mol/L 不变 减小
不水解的正盐 不移动 c(H+)=c(OH-) =10-7 mol/L 不变 不变
加盐
强酸弱碱盐 向右移动 c(H+)>c(OH-) 不变 增大
强碱弱酸盐 向右移动 c(H+) c(OH-) 的溶液为酸性溶液;
c(H+) < c(OH-) 的溶液为碱性溶液。
由于在 25 ℃ 的温度下,K =1×10-14,所以,在 25 ℃ 时:
w
中性溶液:c(H+) = c(OH-) = 10-7 mol/L;
酸性溶液:c(H+) > c(OH-),c(H+) > 1×10-7 mol/L;
碱性溶液:c(H+) < c(OH-),c(H+) <1×10-7 mol/L。P148
(三)溶液的酸碱性和pH
1.pH
水溶液里 H+浓度的负对数叫作 pH,即 pH=-lg c(H+) 。
常温条件下:
pH = 7,则为中性溶液;
pH < 7,则为酸性溶液;
pH > 7,则为碱性溶液。
pH 越小,c(H+) 越大,溶液的酸性越强;
pH 越大,c(OH-) 越大,溶液的碱性越强。P149
用 c(H+) > 1×10-7 mol/L 或 pH < 7 判断溶液呈酸性的前提条件是溶液
温度为 25 ℃。
c(H+) > c(OH-) 或 c(H+) < c(OH-) 是溶液呈酸性或碱性的充分必要条
件。P149
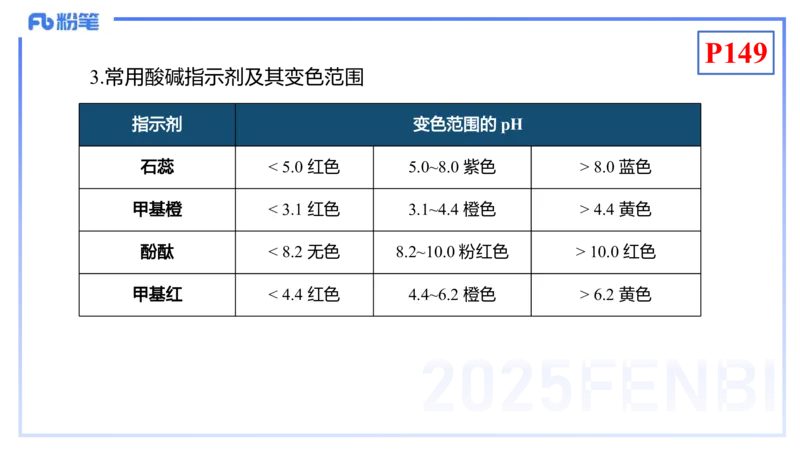
2.pH 的测定方法
(1)pH 试纸;
(2)酸碱指示剂;
(3)pH 计。
用 pH 试纸测定溶液 pH 的实验操作是:用洁净的玻璃棒蘸取待测溶液点
在 pH 试纸的中部,与标准比色卡对照,读出溶液的 pH 。P149
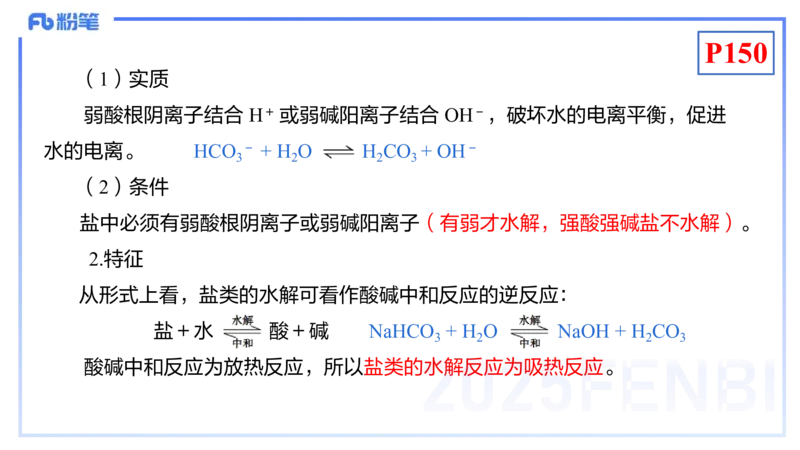
3.常用酸碱指示剂及其变色范围
指示剂 变色范围的 pH
石蕊 < 5.0 红色 5.0~8.0 紫色 > 8.0 蓝色
甲基橙 < 3.1 红色 3.1~4.4 橙色 > 4.4 黄色
酚酞 < 8.2 无色 8.2~10.0 粉红色 > 10.0 红色
甲基红 < 4.4 红色 4.4~6.2 橙色 > 6.2 黄色P161P149
三、盐类的水解
(一)盐类水解的概念及实质
1.定义
在溶液中由盐电离出来的离子跟水电离产生的 H+ 或 OH- 结合生成弱
电解质的反应,叫作盐类的水解。
以 NaHCO 溶液为例:NaHCO === Na+ + HCO -
3 3 3
H O OH-+H+
2
HCO -+H+ H CO
3 2 3
HCO - + H O H CO + OH-
3 2 2 3P150
(1)实质
弱酸根阴离子结合 H+ 或弱碱阳离子结合 OH-,破坏水的电离平衡,促进
水的电离。 HCO - + H O H CO + OH-
3 2 2 3
(2)条件
盐中必须有弱酸根阴离子或弱碱阳离子(有弱才水解,强酸强碱盐不水解)。
2.特征
从形式上看,盐类的水解可看作酸碱中和反应的逆反应:
盐+水 酸+碱 NaHCO + H O NaOH + H CO
3 2 2 3
酸碱中和反应为放热反应,所以盐类的水解反应为吸热反应。P150
(二)盐类水解反应的表示方法
1.一般模式
(1)用化学方程式表示:盐+水 酸+碱
(2)用离子方程式表示:盐的离子+水 弱酸(或弱碱)+OH-(或H+)
NaHCO + H O NaOH + H CO
3 2 2 3
HCO - + H O H CO + OH-
3 2 2 3P150
2.水解类型
(1)一元弱酸强碱盐和一元弱碱强酸盐
CH COO-+H O CH COOH+OH-
3 2 3
NH ++H O NH ·H O+H+
4 2 3 2
(2)多元弱酸强碱盐(正盐)
由于多元弱酸的电离是分步进行的,所以多元弱酸的酸根离子的水解也是分步进
行的,必须分步书写。多元弱酸根离子的第一步水解程度远大于第二步,溶液的碱性
主要由第一步水解决定。
CO 2-+H O HCO - + OH-
3 2 3
HCO -+H O H CO + OH-
3 2 2 3P150
(3)多元弱碱强酸盐
不要求分步表示多元弱碱的金属阳离子的水解,而是“一步到位”。
(4)弱酸的铵盐
如(NH ) CO 、NH HCO 、CH COONH 等弱酸的铵盐,弱酸根离子与 NH +
4 2 3 4 3 3 4 4
的水解互相促进而使水解程度增大,但其水解程度仍然很小,离子间可以大量共
存,水解方程式仍用可逆符号表示,不标示“↑”和“↓”,不稳定产物也忽略其分解。
此类水解称为不完全双水解。P151
(5)完全双水解
某些盐溶液在混合时,一种盐的阳离子和另一种盐的阴离子,相互促进
对方的水解,使两种离子的水解趋于完全,这样的水解称为完全双水解。此
类反应的离子方程式用 “ ” 而不用 “ ” 表示,并标示 “↑” 和 “↓” 。
写离子方程式时,一般要根据水解的特征、水解生成的酸和碱的特点确
定反应物和生成物,以离子的电荷守恒和质量守恒相结合的方法进行配平。P151
(三)水解平衡常数
水解反应的平衡常数叫作水解平衡常数或水解常数,用 K 表示。
h
以NH ++H O NH ·H O+H+ 为例,NH +水解的水解平衡常数表
4 2 3 2 4
达式为:
K 数值越大,水解趋势越大。
hP151
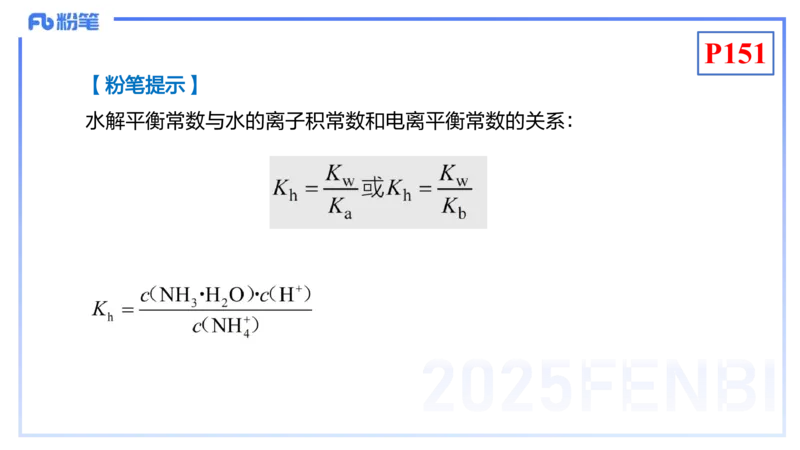
【粉笔提示】
水解平衡常数与水的离子积常数和电离平衡常数的关系: