文档内容
运城市 2025-2026学年第一学期期中调研测试
高三化学试题
202511
本试题满分100分,考试时间75分钟。答案一律写在答题卡上。
注意事项:
1答题前,考生务必先将自己的姓名、准考证号填写在答题卡上,认真核对条形码上的姓
名、准考证号,并将条形码粘贴在答题卡的指定位置上。
2答题时使用05毫米的黑色中性(签字)笔或碳素笔书写,字体工整、笔迹清楚。
3请按照题号在各题的答题区域(黑色线框)内作答,超出答题区域书写的答案无效。
4保持卡面清洁,不折叠,不破损。
可能用到的相对原子质量:H—1 Li—7 N—14 Al—27
一、选择题(本题共14小题,每小题3分,共42分。在每小题列出的四个选项中,只有一项是
符合题目要求的)
1.“中国名片”、“中国制造”在众多领域受到世界瞩目。下列说法错误的是
A.“望宇”登月服用的聚酰亚胺隔热层属于有机高分子材料
B.中国天眼用到的SiC属于新型无机非金属材料
C.革新了海水原位电解制氢工艺,其关键材料多孔聚四氟乙烯有很强的耐腐蚀性
D.“福建舰”航空母舰防腐涂料中使用的石墨烯是乙烯的同系物
2.下列化学用语或图式表述中正确的是
A.SiO 的电子式: B.顺-2-丁烯分子结构模型:
2
C.聚丙烯的链节:—CH—CH—CH— D.NaCl晶胞:
2 2 2
3.下列有关物质性质与用途对应关系错误的是
A.硅的导电性介于导体和绝缘体之间,可用于制造光导纤维
B.氯化铁溶液能与铜反应,可用于刻蚀铜板
C.氧化钙能与二氧化硫反应,可作为工业废气处理时的脱硫剂
D.离子液体具有导电性,可作为原电池电解质
高三化学试题 第 1页(共8页)
书书书4.实验室安全至关重要。下列做法不符合实验安全要求的是
A.少量白磷保存时用乙醇液封
B.苯酚溅到皮肤上,应立即用酒精冲洗,再用清水冲洗
C.进行化学实验时需要佩戴护目镜
D.溴易挥发且有毒,取用液溴时,应注意防护和通风
5.常温下,下列各组离子在给定溶液中能大量共存的是
A.葡萄糖溶液中:MnO-、K+、H+、SO2-
4 4
B.加入铁粉会放出氢气的溶液中:Cl-、SO2-、SO2-、K+
2 3 4
C.0.1mol/LFe(SO)溶液:Cu2+、NH+、NO-、SO2-
2 4 3 4 3 4
D.pH=1的溶液中:K+、CO2-、[Al(OH)]-
3 4
6.NaO 可用作潜水或宇航装置的CO 吸收剂和供氧剂。N 为阿伏加德罗常数的值。下列
2 2 2 A
说法错误的是
A.1molNaO 晶体中阳离子数目为2N
2 2 A
B.1L1mol/LNaCO 溶液含有的氧原子数目为3N
2 3 A
C.44gCO 中σ键的数目为2N
2 A
D.反应生成标准状况2.24LO 时转移的电子数目为0.2N
2 A
7.下列有关反应方程式正确的是
A.用红色Fe(SCN)溶液溶解铁粉:2Fe3++Fe=3Fe2+
3
B.钢铁发生吸氧腐蚀的正极反应:O +4e-+2HO=4OH-
2 2
C.铅酸蓄电池充电:Pb+PbO +2HSO =2PbSO +2HO
2 2 4 4 2
高温
D.铁在加热条件下与水蒸气反应产生气体:2Fe+3HO(g)FeO +3H
2 2 3 2
8.氢能是一种重要的清洁能源,由 HCOOH可以制得 H。在催化剂作用下,单个 HCOOH释
2
氢的反应机理和相对能量的变化情况分别如图1和图2所示。研究发现,其他条件不变
时,以HCOOK水溶液代替HCOOH释氢的效果更佳。下列叙述正确的是
A.HCOOH催化释放氢的过程中有极性键和非极性键的的断裂
B.其他条件不变时,以HCOOK水溶液代替HCOOH可以提高释放氢气的纯度
高三化学试题 第 2页(共8页)C.键长:C-H>O-H,在催化剂表面解离C-H键比解离O-H键更容易
D.HCOOH催化释氢的热化学方程式为HCOOH(g)=CO(g)+H(g) ΔH=-0.45eV
2 2
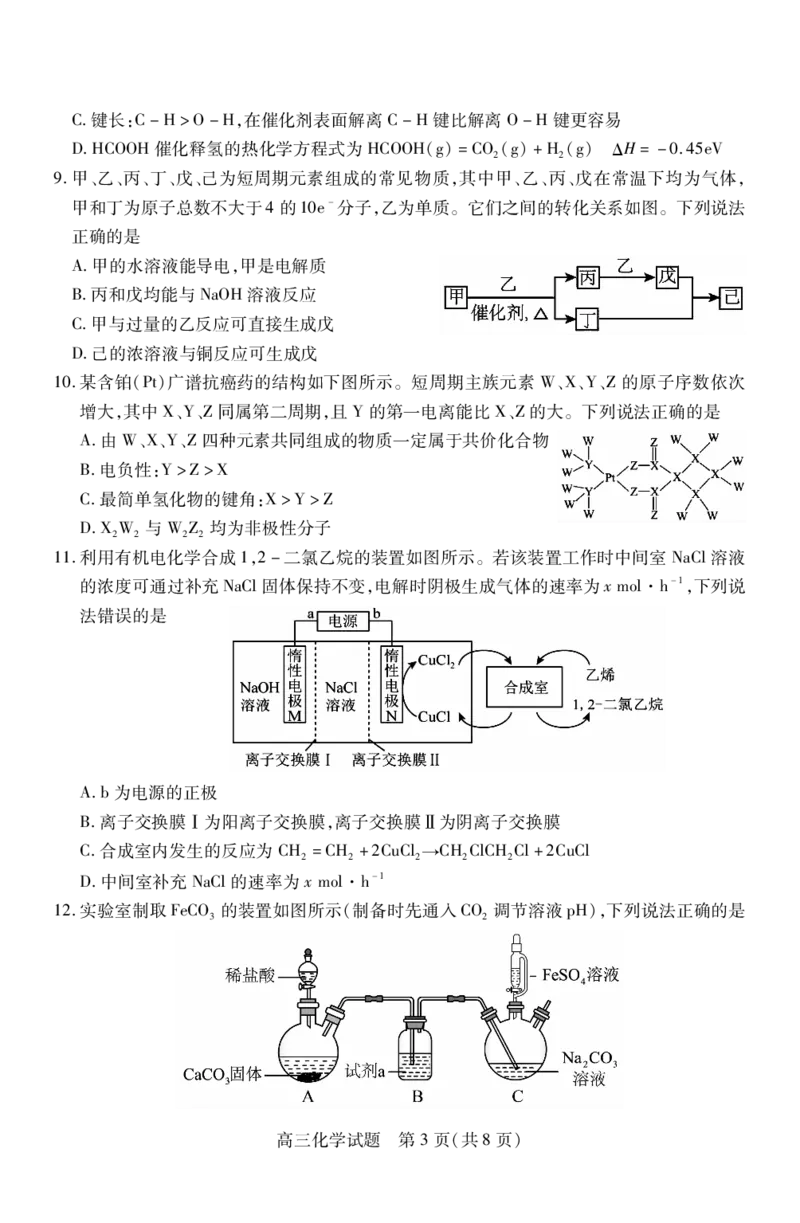
9.甲、乙、丙、丁、戊、己为短周期元素组成的常见物质,其中甲、乙、丙、戊在常温下均为气体,
甲和丁为原子总数不大于4的10e-分子,乙为单质。它们之间的转化关系如图。下列说法
正确的是
A.甲的水溶液能导电,甲是电解质
B.丙和戊均能与NaOH溶液反应
C.甲与过量的乙反应可直接生成戊
D.己的浓溶液与铜反应可生成戊
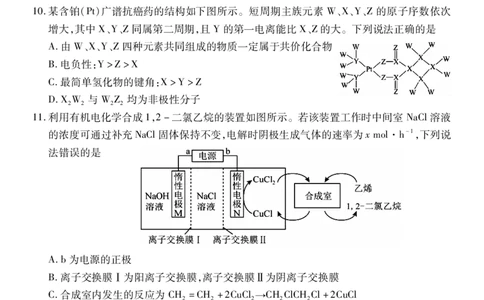
10.某含铂(Pt)广谱抗癌药的结构如下图所示。短周期主族元素 W、X、Y、Z的原子序数依次
增大,其中X、Y、Z同属第二周期,且Y的第一电离能比X、Z的大。下列说法正确的是
A.由W、X、Y、Z四种元素共同组成的物质一定属于共价化合物
B.电负性:Y>Z>X
C.最简单氢化物的键角:X>Y>Z
D.XW 与W Z均为非极性分子
2 2 2 2
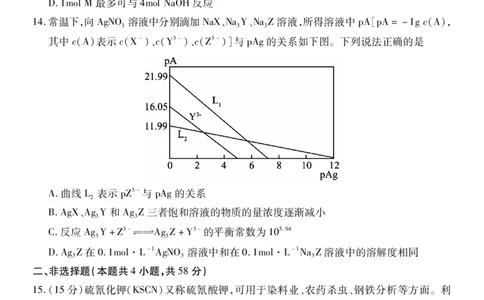
11.利用有机电化学合成1,2-二氯乙烷的装置如图所示。若该装置工作时中间室 NaCl溶液
的浓度可通过补充NaCl固体保持不变,电解时阴极生成气体的速率为xmol·h-1,下列说
法错误的是
A.b为电源的正极
B.离子交换膜Ⅰ为阳离子交换膜,离子交换膜Ⅱ为阴离子交换膜
C.合成室内发生的反应为CH =CH +2CuCl→CHClCHCl+2CuCl
2 2 2 2 2
D.中间室补充NaCl的速率为xmol·h-1
12.实验室制取FeCO 的装置如图所示(制备时先通入CO 调节溶液pH),下列说法正确的是
3 2
高三化学试题 第 3页(共8页)A.A中稀盐酸可换成稀硫酸
B.试剂a是饱和NaCO 溶液
2 3
C.调节pH的目的是防止生成铁的氢氧化物
D.配制FeSO 溶液时,加入稀盐酸抑制Fe2+的水解
4
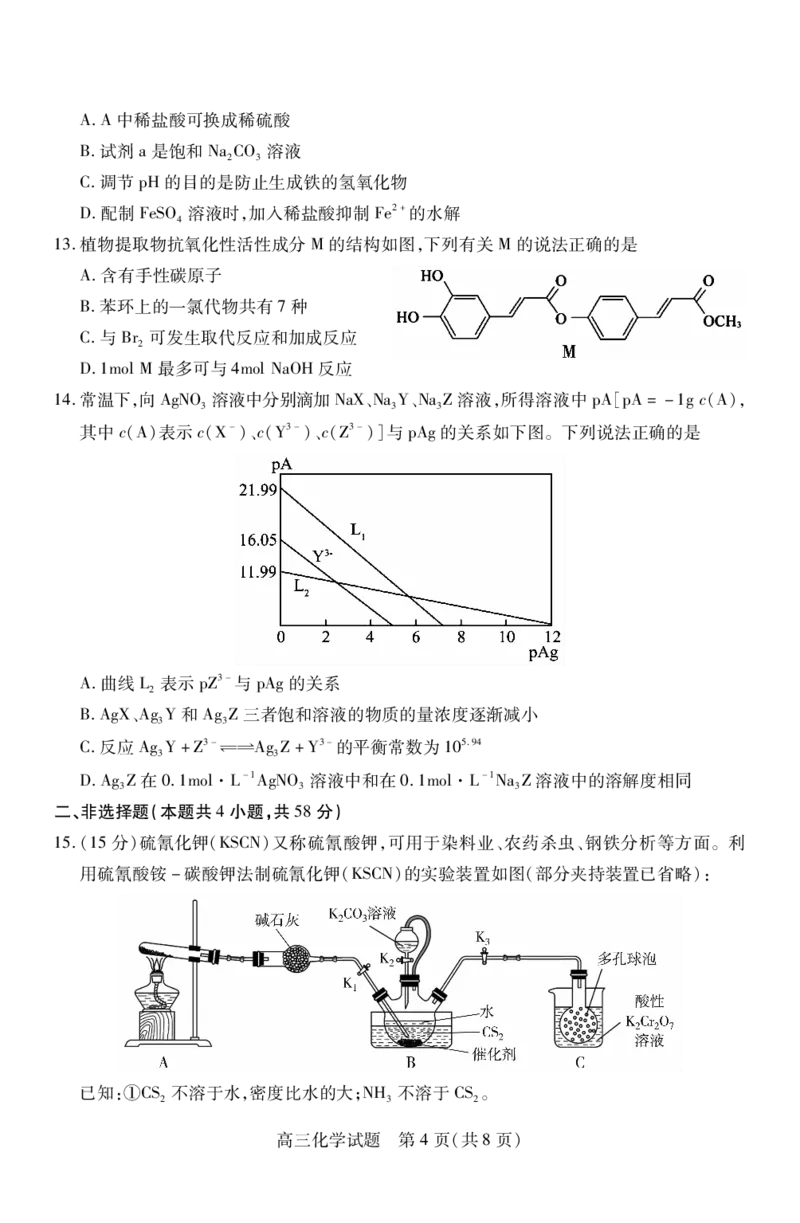
13.植物提取物抗氧化性活性成分M的结构如图,下列有关M的说法正确的是
A.含有手性碳原子
B.苯环上的一氯代物共有7种
C.与Br可发生取代反应和加成反应
2
D.1molM最多可与4molNaOH反应
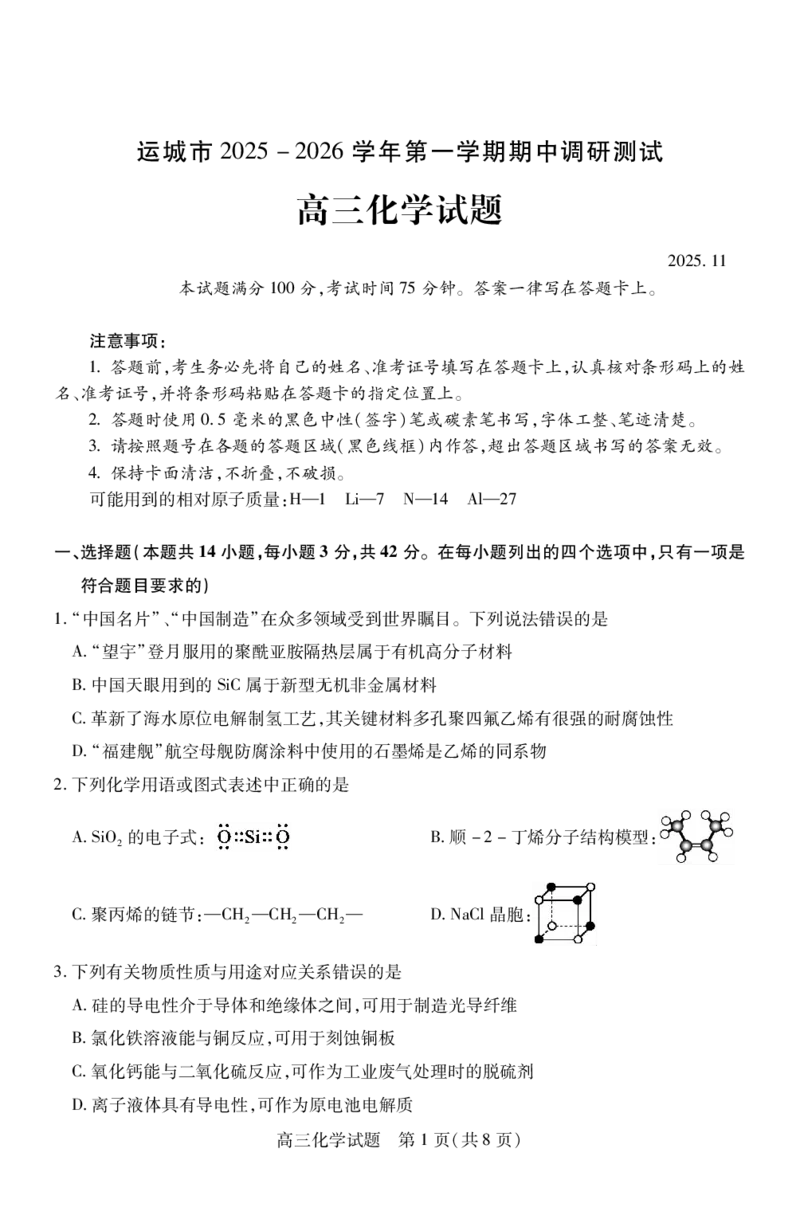
14.常温下,向AgNO 溶液中分别滴加NaX、NaY、NaZ溶液,所得溶液中pA[pA=-1gc(A),
3 3 3
其中c(A)表示c(X-)、c(Y3-)、c(Z3-)]与pAg的关系如下图。下列说法正确的是
A.曲线L表示pZ3-与pAg的关系
2
B.AgX、AgY和AgZ三者饱和溶液的物质的量浓度逐渐减小
3 3
C.反应AgY+Z3-幑幐AgZ+Y3-的平衡常数为105.94
3 3
D.AgZ在0.1mol·L-1AgNO 溶液中和在0.1mol·L-1NaZ溶液中的溶解度相同
3 3 3
二、非选择题(本题共4小题,共58分)
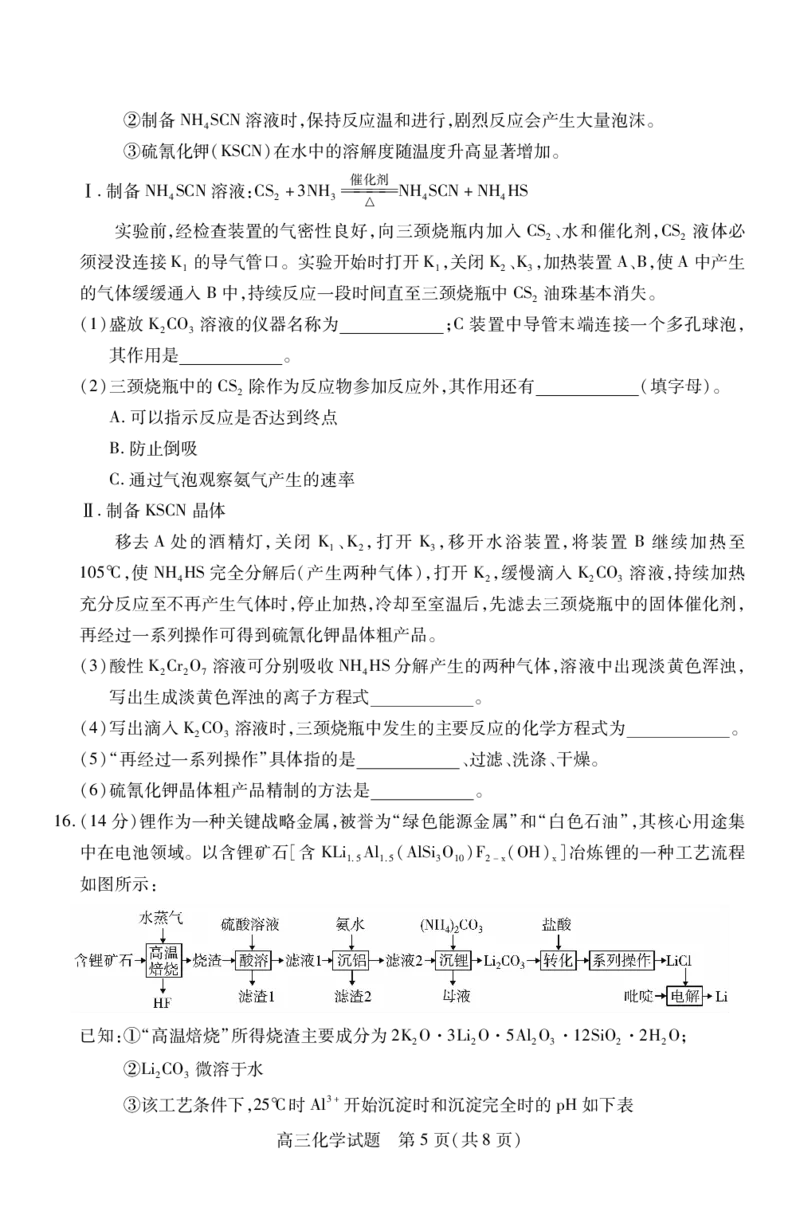
15.(15分)硫氰化钾(KSCN)又称硫氰酸钾,可用于染料业、农药杀虫、钢铁分析等方面。利
用硫氰酸铵-碳酸钾法制硫氰化钾(KSCN)的实验装置如图(部分夹持装置已省略):
已知:①CS不溶于水,密度比水的大;NH 不溶于CS。
2 3 2
高三化学试题 第 4页(共8页)②制备NHSCN溶液时,保持反应温和进行,剧烈反应会产生大量泡沫。
4
③硫氰化钾(KSCN)在水中的溶解度随温度升高显著增加。
催化剂
Ⅰ.制备NHSCN溶液:CS+3NH NHSCN+NHHS
4 2 3 △ 4 4
实验前,经检查装置的气密性良好,向三颈烧瓶内加入 CS、水和催化剂,CS液体必
2 2
须浸没连接K 的导气管口。实验开始时打开K,关闭K、K,加热装置A、B,使A中产生
1 1 2 3
的气体缓缓通入B中,持续反应一段时间直至三颈烧瓶中CS油珠基本消失。
2
(1)盛放KCO 溶液的仪器名称为 ;C装置中导管末端连接一个多孔球泡,
2 3
其作用是 。
(2)三颈烧瓶中的CS除作为反应物参加反应外,其作用还有 (填字母)。
2
A.可以指示反应是否达到终点
B.防止倒吸
C.通过气泡观察氨气产生的速率
Ⅱ.制备KSCN晶体
移去A处的酒精灯,关闭 K、K,打开 K,移开水浴装置,将装置 B继续加热至
1 2 3
105℃,使NHHS完全分解后(产生两种气体),打开 K,缓慢滴入 KCO 溶液,持续加热
4 2 2 3
充分反应至不再产生气体时,停止加热,冷却至室温后,先滤去三颈烧瓶中的固体催化剂,
再经过一系列操作可得到硫氰化钾晶体粗产品。
(3)酸性KCrO 溶液可分别吸收NHHS分解产生的两种气体,溶液中出现淡黄色浑浊,
2 2 7 4
写出生成淡黄色浑浊的离子方程式 。
(4)写出滴入KCO 溶液时,三颈烧瓶中发生的主要反应的化学方程式为 。
2 3
(5)“再经过一系列操作”具体指的是 、过滤、洗涤、干燥。
(6)硫氰化钾晶体粗产品精制的方法是 。
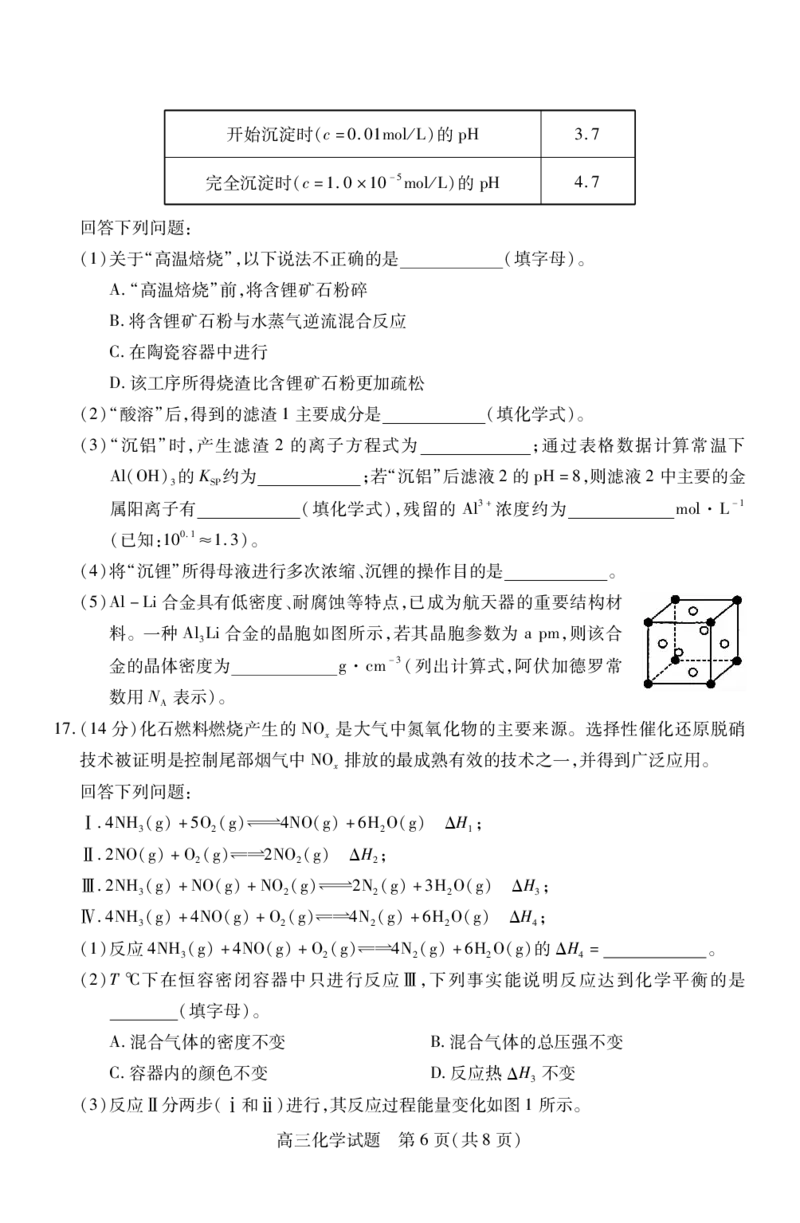
16.(14分)锂作为一种关键战略金属,被誉为“绿色能源金属”和“白色石油”,其核心用途集
中在电池领域。以含锂矿石[含KLiAl(AlSiO )F (OH)]冶炼锂的一种工艺流程
1.5 1.5 3 10 2-x x
如图所示:
已知:①“高温焙烧”所得烧渣主要成分为2KO·3LiO·5AlO·12SiO·2HO;
2 2 2 3 2 2
②LiCO 微溶于水
2 3
③该工艺条件下,25℃时Al3+开始沉淀时和沉淀完全时的pH如下表
高三化学试题 第 5页(共8页)开始沉淀时(c=0.01mol/L)的pH 3.7
完全沉淀时(c=1.0×10-5mol/L)的pH 4.7
回答下列问题:
(1)关于“高温焙烧”,以下说法不正确的是 (填字母)。
A.“高温焙烧”前,将含锂矿石粉碎
B.将含锂矿石粉与水蒸气逆流混合反应
C.在陶瓷容器中进行
D.该工序所得烧渣比含锂矿石粉更加疏松
(2)“酸溶”后,得到的滤渣1主要成分是 (填化学式)。
(3)“沉铝”时,产生滤渣 2的离子方程式为 ;通过表格数据计算常温下
Al(OH)的K 约为 ;若“沉铝”后滤液2的pH=8,则滤液2中主要的金
3 SP
属阳离子有 (填化学式),残留的 Al3+浓度约为 mol·L-1
(已知:100.1≈1.3)。
(4)将“沉锂”所得母液进行多次浓缩、沉锂的操作目的是 。
(5)Al-Li合金具有低密度、耐腐蚀等特点,已成为航天器的重要结构材
料。一种AlLi合金的晶胞如图所示,若其晶胞参数为 apm,则该合
3
金的晶体密度为 g·cm-3(列出计算式,阿伏加德罗常
数用N 表示)。
A
17.(14分)化石燃料燃烧产生的 NO 是大气中氮氧化物的主要来源。选择性催化还原脱硝
x
技术被证明是控制尾部烟气中NO 排放的最成熟有效的技术之一,并得到广泛应用。
x
回答下列问题:
Ⅰ.4NH(g)+5O(g)幑幐4NO(g)+6HO(g) ΔH;
3 2 2 1
Ⅱ.2NO(g)+O(g)幑幐2NO(g) ΔH;
2 2 2
Ⅲ.2NH(g)+NO(g)+NO(g)幑幐2N(g)+3HO(g) ΔH;
3 2 2 2 3
Ⅳ.4NH(g)+4NO(g)+O(g)幑幐4N(g)+6HO(g) ΔH;
3 2 2 2 4
(1)反应4NH(g)+4NO(g)+O(g)幑幐4N(g)+6HO(g)的ΔH = 。
3 2 2 2 4
(2)T℃下在恒容密闭容器中只进行反应Ⅲ,下列事实能说明反应达到化学平衡的是
(填字母)。
A.混合气体的密度不变 B.混合气体的总压强不变
C.容器内的颜色不变 D.反应热ΔH 不变
3
(3)反应Ⅱ分两步(ⅰ和ⅱ)进行,其反应过程能量变化如图1所示。
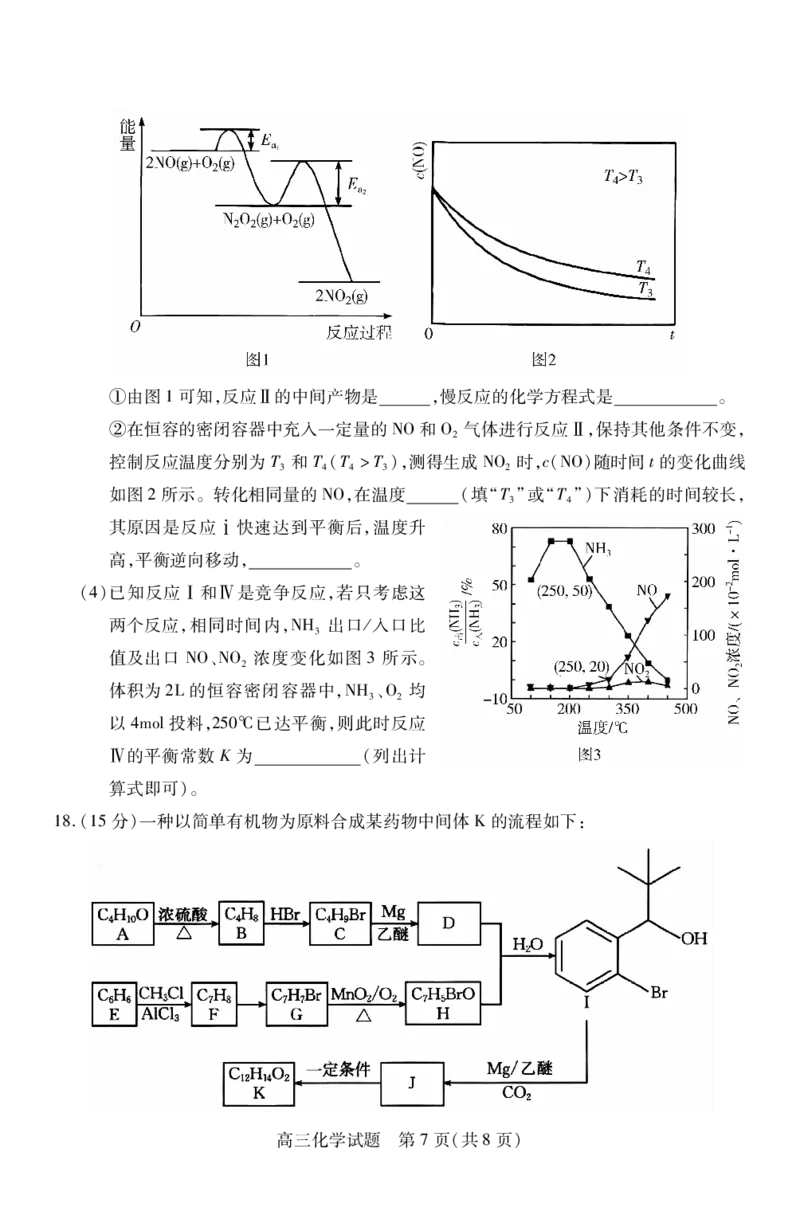
高三化学试题 第 6页(共8页)①由图1可知,反应Ⅱ的中间产物是 ,慢反应的化学方程式是 。
②在恒容的密闭容器中充入一定量的NO和O 气体进行反应Ⅱ,保持其他条件不变,
2
控制反应温度分别为T和T(T>T),测得生成NO 时,c(NO)随时间t的变化曲线
3 4 4 3 2
如图2所示。转化相同量的NO,在温度 (填“T”或“T”)下消耗的时间较长,
3 4
其原因是反应ⅰ快速达到平衡后,温度升
高,平衡逆向移动, 。
(4)已知反应Ⅰ和Ⅳ是竞争反应,若只考虑这
两个反应,相同时间内,NH 出口/入口比
3
值及出口 NO、NO 浓度变化如图 3所示。
2
体积为2L的恒容密闭容器中,NH、O 均
3 2
以4mol投料,250℃已达平衡,则此时反应
Ⅳ的平衡常数 K为 (列出计
算式即可)。
18.(15分)一种以简单有机物为原料合成某药物中间体K的流程如下:
高三化学试题 第 7页(共8页)已知:
回答下列问题:
(1)A转化为B的反应类型为 。
(2)C的名称为 (用系统命名法命名)。
(3)F转化为G的化学方程式为 。
(4)H中含氧官能团的名称是 。
(5)已知K是环酯,下列关于J的说法正确的是 (填字母)。
A.J中含有2个手性碳原子
B.J中可能存在分子内氢键
C.J能发生银镜反应
D.1molJ与足量金属钠反应,可以产生1molH
2
(6)在I的芳香族同分异构体中,同时满足下列条件的结构有 种(不考虑立
体异构)。
①苯环上只含有2个取代基;②能与FeCl溶液发生显色反应;③含3个甲基。
3
其中,在核磁共振氢谱上有5组峰且峰面积比为1∶1∶2∶2∶9的结构简式是 。
(7)结合合成K的相关信息,以2-丁醇为原料合成2-甲基丁酸的合成路线(其他无机试
剂及溶剂任选)。
高三化学试题 第 8页(共8页)