文档内容
娄底市新高考模拟预测卷(一)
化 学(解析版)
本试题卷分为选择题和非选择题两部分,共 页。时量75分钟,满分 100分。
可能用到的相对原子质量:H-1 C-12 O-16 N-14 Na-23 S-32
一、选择题(本题共 14小题,每小题 3分,共42分。在每小题给出的四个选项中,只有一项
是符合题目要求的。)
1.化学与生活密切相关,下列不涉及化学变化的是( )
A.冬月灶中所烧薪柴之灰,混合铵态氮肥施用会减弱肥效
B.液氮用于治疗皮表的血管瘤
C.炖排骨汤时加点醋味道更鲜
D.漂白粉去除衣服上的污渍时需要在水中浸泡一段时间
答案:B
解析:A. 草木灰的主要成分为碳酸钾,与铵态氮肥混合施用会减弱肥效,其原理是碳酸根离子与铵根离
子会发生双水解而使肥效减弱,涉及化学变化,故A错误;
B.液氮在常温下汽化吸热,可以使患处温度降低,迅速将活体组织冻结便于切除,属于物理变化,故B正
确;
2. 下列有关化学用语表示正确的是( )
A. BF 的空间结构: (三角锥形)
3
B.CaO 的电子式:
2
C.H S分子的比例模型::
2
D.乙烯分子可以写为:(CH )
2 2
答案:B
3−3
解析:A. BF 的中心原子B原子孤电子对数= =0,价层电子对数=3,空间构型为平面三角形,空间结构
3
2
模型为: ,故A错误;
B. CaO 为离子化合物,由Ca2+和O22-构成,并且过氧根离子内的氧原子之间共用一对电子,其电子式:
2
,故B正确;
C. H S分子是“V”形结构,因此该图不是H S分子的比例模型,故C错误;
2 2
D.乙烯分子不可以写为 (CH ) ,D错误;
2 2
学科网(北京)股份有限公司
{#{QQABSQAEggCoAAJAAQgCUwEKCkAQkAEAAIoOABAAoAAASRFABAA=}#}3.SCR(选择性催化还原)技术可有效降低柴油发动机在空气过量条件下的NOx排放,其工作原理如
图:
下列有关说法不正确的是( )
A、尿素[CO(NH ) ]水溶液热分解为NH 和CO ,该反应的化学方程式:
2 2 3 2
CO(NH
2
)
2
+H
2
O=C O
2
↑+2NH
3
↑
B、反应器中每生成1molN2转移12N 个电子
A
C、利用SCR(选择性催化还原)技术还可以处理空气中含硫化合物的排放
D、反应器中氧化剂和还原剂的个数比为3:4
答案:B。
解析:根据分析可以知道A正确;每生成1molN 转移7/12N 个电子,B错误;根据电子守恒可以知
2 A
道,反应器中氧化剂和还原剂的个数比为3:4,C正确;利用SCR(选择性催化还原)技术还可以处理空
气中含硫化合物的排放,D正确。
4.下列有关离子方程式错误的是
A、碱性锌锰电池的正极反应:MnO +H O+e-=MnO(OH)+OH-
2 2
B、Ca(OH) 溶液中加入少量的Mg(HCO ) 溶液:
2 3 2
Ca2++2OH-+Mg2++2HCO -=CaCO ↓+2H O+MgCO ↓
3 3 2 3
C、K [Fe(CN) ]溶液滴入FeCl 溶液中:K++Fe2++[Fe(CN)6]3- =KFe[Fe(CN) ]↓
3 6 2 6
D、、TiCl 加入水中:TiCl +(x+2)H O=TiO ·xH O↓+4H++4Cl-
4 4 2 2 2
答案:B。
解析:碱性锌锰电池的正极反应:MnO +H O+e-=MnO(OH)+OH-,A 正确;Ca(OH) 溶液中加入少量的
2 2 2
Mg(HCO ) 溶液,应该先沉淀 Mg(OH) ,所以 B 错误;K [Fe(CN) ]溶液滴入 FeCl 溶液中:
3 2 2 3 6 2
K++Fe2++[Fe(CN)6]3-=KFe[Fe(CN) ]↓,C 正确;TiCl 加入水中:TiCl +(x+2)H O=TiO ·xH O↓+4H++4Cl-,
6 4 4 2 2 2
D正确。
5.下列说法正确的是( )
A B C D
学科网(北京)股份有限公司
{#{QQABSQAEggCoAAJAAQgCUwEKCkAQkAEAAIoOABAAoAAASRFABAA=}#}饱和NaHSO 溶液
3
排出盛有KMnO 溶液
4
分离乙醇和乙酸 除去SO 中混有的少量HCl 实验室制备氯气
2
滴定管尖嘴内的气泡
答案:C
解析:A.高锰酸钾溶液具有强氧化性,会腐蚀橡胶管,所以高锰酸钾溶液应盛放在酸式滴定管在,不能
盛放在碱式滴定管中,故A错误;
B.乙醇和乙酸是互溶的,不能采用分液的方式分离,应采用蒸馏来分离,B错误
C.用饱和NaHSO 溶液除去SO 中混有的少量HCl,C正确
3 2
MnO 固体加热条件下将HCl氧化为Cl ,缺少加热装置,因此D项错误。
2 2
6.1875年,法国人布瓦博德朗发现了Ga,并测定了它的一系列物理化学性质。门捷列夫认为Ga正是他
在1869年所预言的“类铝”元素,并重新测定了Ga的密度。Ga的发现证实了元素周期律的重要性和正确
性。已知X、Ga、Y周期数依次递增,且主族数相同。以下说法不正确的是( )
A、X、Ga、Y与水反应越来越剧烈
B、已知Ga(OH) 常温下能与氨水反应,则酸性:Ga(OH) >Al(OH)
3 3 3
C、NaGaO 能与CO 反应,说明镓的金属性强于铝
2 2
D、X、Ga、Y分别形成氯化物的化学键构成不同
答案:C。
解析:本题考察的是元素周期律的递变性,同主族元素随着原子序数的递增,金属性增强,A 正确。
Al(OH) 常温下不与氨水反应,Ga(OH) 也具有两性,体现酸性比Al(OH) 强。B正确。金属性的比较主要
3 3 3
从金属与酸的反应剧烈程度以及与水的反应,最高价氧化物对应水化物的碱性强弱,C不能作为比较依据。
AlCl 与GaCl 共价键成分较多,属于共价化合物。lnCl 则属于离子化合物。
3 3 3
7.约翰等化学家在锂电池研发中做出的突出贡献,获得 2019 年诺贝尔化学奖;锂电池是新能源汽车的动
力电池之一,主要以磷酸亚铁锂(LiFePO )为原料。以下是在锂电池废料中回收锂和正极金属,流程如
4
下,下列叙述正确的是( )
学科网(北京)股份有限公司
{#{QQABSQAEggCoAAJAAQgCUwEKCkAQkAEAAIoOABAAoAAASRFABAA=}#}A、上述流程中可用NaNO 代替Na CO
3 2 3
B、废旧电池属于湿垃圾,可通过掩埋土壤中进行处理
C、从“正极片”中可回收的金属元素有Al、Fe、Li
D、“沉淀”反应的金属离子为Fe2+
答案:C。
解析:正极片碱溶时铝转化为偏铝酸钠,滤渣中含有磷酸亚铁锂,加入硫酸和硝酸酸溶,过滤后滤渣是
炭黑,得到含Li、P、Fe的滤液,加入碱液生成氢氧化铁沉淀,滤液中加入碳酸钠生成含锂的沉淀,硝酸
锂能溶于水,因此上述流程中不能用硝酸钠代替碳酸钠,A错误。废旧电池中含有重金属,随意排放容易
污染环境,B错误;根据流程的转化可知从正极片中可回收的金属元素有Al、Fe、Li,C正确;加入碱液
生成氢氧化铁沉淀,因此“沉淀”反应的金属离子是Fe3+,D错误。
8..下列方案设计、现象和结论都正确的是( )
目的 方案设计 现象和结论
取少量待测样品溶于蒸馏水,加
探究Na SO 固体样品 若有白色沉淀产生,则样品已经
2 3
A 入足量稀硝酸,再加入足量
是否变质 变质
BaCl 溶液
2
取2 mL卤代烃样品于试管中,
判断某卤代烃中的卤 加入5 mL 20% KOH水溶液混 若产生的沉淀为白色,则该卤代
B
素 合后加热,冷却后加入稀硝酸酸 烃中含有氯元素
化,再滴加AgNO 溶液
3
取1mL 0.1 mol·L-1KI溶液于试
探究KI与FeCl 反应 管中,加入5 mL 0.1 mol·L-1 若溶液变血红色,则KI与FeCl
3 3
C
的限度 FeCl 溶液,充分反应后滴入5 的反应有一定限度
3
滴15% KSCN溶液
取4mL乙醇,加入12mL浓硫
探究乙醇消去反应的 酸、少量沸石,迅速升温至 若溴水褪色,则乙醇消去反应的
D
产物 140℃,将产生的气体通入2mL 产物为乙烯
溴水中
答案:B
学科网(北京)股份有限公司
{#{QQABSQAEggCoAAJAAQgCUwEKCkAQkAEAAIoOABAAoAAASRFABAA=}#}解析:A.加入硝酸,会将亚硫酸根离子氧化为硫酸根离子,因此无法判断是否变质,A选项不符合题意;
B. 溶液中加入KOH后体系中剩余大量的OH-,加硝酸中和氢氧化钾,再加入硝酸银,生产白色沉淀即为
AgCl,B正确;C. 向KI溶液中滴加FeCl ,因为FeCl 过量,因此即使有剩余也不能说明该反应是有限
3 3
度的,C错误;D. 乙醇在140℃,浓硫酸的作用下,会发生分子间脱水,而不发生消去反应,D项不符合
题意;
9.近日,在《science》顶刊上出现了一种基于计算机技术的药物设计方法—CADD。利用计算机模拟药物
与生物大分子的相互作用,加快了药物靶向的速度和准确性,对人类攻克肿瘤难题具有具有重要意义。
CADD最开始以以下物质为靶向物进行初实验,关于该物质下列说法不正确的是( )
A、该物质可以使酸性高锰酸钾溶液褪色
B、1mol该物质最多可以和4molH 发生加成反应
2
C、该物质的分子式为C H N O
6 6 4
D、所有C原子均采用SP2杂化
答案:B
解析:该选项考查的是对有机物基本反应的考查。 该物质含有碳碳双键,可以使酸性高锰酸钾溶液
褪色,A正确。含有3个不饱和键,最多可以和3molH 发生加成反应,B错误。
2
该物质中所有碳原子均有不饱和双键,因此均采用SP2杂化。
10.铜基多向催化剂性能优异,耐受高温,广泛应用于一系列的重要化工反应中。三甲胺[(CH )
3
NCHO]用于调节动物肝脏对体内脂肪的代谢和促生长。单个三甲胺在Cu表面的催化作用反应历程如图
2
所示,下列说法不正确的是( )
A、该反应历程中最大能量值为1.19ev
B、该反应为放热反应
C、涉及极性键的断裂与形成
D、升高温度增大单位体积内活化分子百分数,从而增大化学反应速率
学科网(北京)股份有限公司
{#{QQABSQAEggCoAAJAAQgCUwEKCkAQkAEAAIoOABAAoAAASRFABAA=}#}答案:A。
解析:该反应历程中最大能量值为2.16ev,A错误。该反应反应物的总能量大于生成物的总能量,为放热
反应。反应涉及到碳氢键的形成以及氢氧键的断裂,C正确。
11.Mg Si是Mg-Si二元体系的唯一稳定化合物,具有高熔点、高硬度、高弹性模量的特性,是一种半导
2
体材料,在光电子器件、激光、半导体制造等领域具有重要应用前景,其立方晶胞的晶胞参数为apm,
且在xy、xz、yz的平面投影如图所示,以下说法正确的是( )
A.基态原子的第一电离能:Mg>Si
B.离Mg原子最近的Si原子个数为8
C.Si原子和Mg原子的最短距离为√3
a pm
4
4×76
D.该晶胞密度为: g/cm3
NA×a3×10−36
答案:C
解析:根据Mg Si其立方晶胞在xy、xz、yz的平面投影及组成,可以画出其晶胞结构,如图所示:
2
A.根据 基态原子的第一电离能:Si>Mg,A错误;
B.根据所画出的晶胞结构分析可得:离 Mg原子最近的 Si原子位置如图所示, 因此
最近的Si原子个数为4,B错误;
1 √3
C.Si原子和Mg原子之间的最短距离是体对角线的 ,为 a pm,C正确;
4 4
4×(28+24×2) 4×76
D.由晶胞的质量公式可得该晶胞密度为: = g/cm3,D错误。
𝑁𝐴×𝑎3×10−30 𝑁𝐴×𝑎3×10−30
学科网(北京)股份有限公司
{#{QQABSQAEggCoAAJAAQgCUwEKCkAQkAEAAIoOABAAoAAASRFABAA=}#}12.硼酸(H BO )可以通过电解NaB(OH) 溶液的方法制备,工作原理如图所示。
3 3 4
下列有关表述正确的是( )
A.M室的石墨为电解池的阴极
B.N室的电极反应式为OH--4e-===O ↑+4H+
2
C.b 膜为阴离子交换膜,产品室发生反应为 H++[B(OH) ]-
4
===H BO +H O
3 3 2
D.理论上每生成1 mol H BO ,阳极室可生成11.2 L(标准状况) 气体
3 3
答案:C。
解析:由题意知,通过电解 NaB(OH) 溶液的方法制备硼酸(H BO ),所以原料室里的[B(OH) ]-移向左边
4 3 3 4
产品室,所以左边为阳极室,右边为阴极室。所以 A 不符合题意。N 室发生还原反应 H O+2e-
2
==H ↑+2OH- 所以B不符合题意。阳极上水电离产生的 OH-放电,同时产生H+,所以 a膜为阳离子交换
2
膜、b膜为阴离子交换膜,产品室发生反应为H++[B(OH) ]-===H BO +H O;所以 C符合题意。理论上
4 3 3 2
每生成1 mol H BO ,装置中每转移1mol电子,阳极室可生成5.6 L(标准状况)气体.所以D错误
3 3
13..McMorris测定和计算了在136~180℃范围内下列反应的平衡常数K 。
p
1 1
得到lgK ~ 和lgK ~ 均为线性关系,如下图所示,下列说法正确的是:( )
p1 T p2 T
A、NOCl分解为NO和Cl 的逆反应的ΔH大于0
2
B、反应2ICl(g)Cl (g)I (g)的K=K /K
2 2 p1 p2
C、反应2ICl(g)Cl (g)I (g)的的ΔH大于0
2 2
D、K 的单位为kpa
p1
答案: C
1 1
解析:A、结合图可知,lgKp 越随着 的增大而逐渐减小。温度越高, 越小,lgKp 越大,即Kp 越
2 2 2
T T
大,说明升高温度平衡2NOCl(g) 2NO(g)+Cl (g)正向移动,则NOCl分解为NO和Cl 反应的ΔH大
2 2
于0,则其逆反应的ΔH小于0;
B、Ⅰ.
学科网(北京)股份有限公司
{#{QQABSQAEggCoAAJAAQgCUwEKCkAQkAEAAIoOABAAoAAASRFABAA=}#}Ⅱ.
Ⅰ+Ⅱ得2ICl(g)Cl (g)I (g),则2ICl(g)Cl (g)I (g)的K=K K ;
2 2 2 2 p1 p2
C该反应2ICl(g)Cl (g)I (g)的ΔH大于0;
2 2
1 1
设T T,即 < ,由图可知:lgK (T')lgK (T)> lgK (T')lgK (T) lgK (T)lgK (T')
T′ T p2 p2 p1 p1 p1 p1
则:lgK (T')K (T')lgK (T)K (T),即k(T')>k(T),因此该反应正反应为吸热反应,即ΔH
p2 p1 p2 p1
大于0;
D、K 的单位为kpa-1
p1
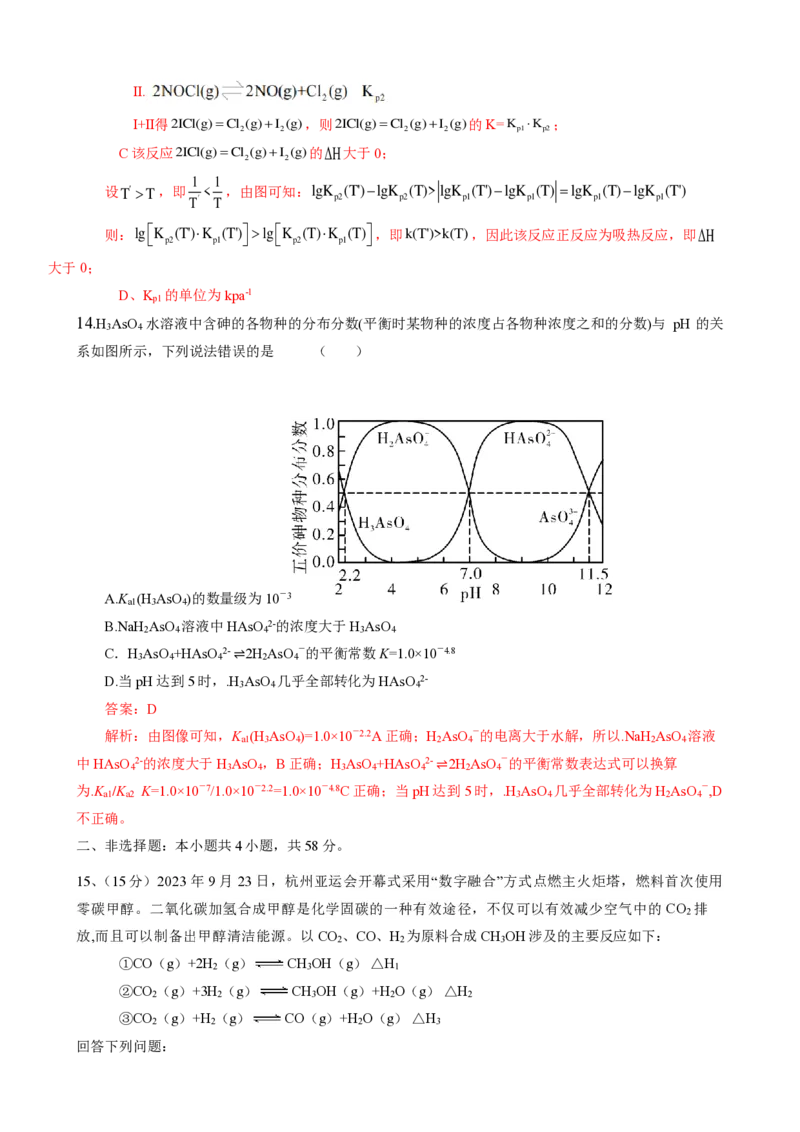
14.H AsO 水溶液中含砷的各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与 pH 的关
3 4
系如图所示,下列说法错误的是 ( )
A.K (H AsO )的数量级为10-3
a1 3 4
B.NaH AsO 溶液中HAsO 2-的浓度大于H AsO
2 4 4 3 4
C.H AsO +HAsO 2- ⇌2H AsO -的平衡常数K=1.0×10-4.8
3 4 4 2 4
D.当pH达到5时,.H AsO 几乎全部转化为HAsO 2-
3 4 4
答案:D
解析:由图像可知,K (H AsO )=1.0×10-2.2A正确;H AsO -的电离大于水解,所以.NaH AsO 溶液
a1 3 4 2 4 2 4
中HAsO 2-的浓度大于H AsO ,B正确;H AsO +HAsO 2- ⇌2H AsO -的平衡常数表达式可以换算
4 3 4 3 4 4 2 4
为.K /K K=1.0×10-7/1.0×10-2.2=1.0×10-4.8C正确;当pH达到5时,.H AsO 几乎全部转化为H AsO -,D
a1 a2 3 4 2 4
不正确。
二、非选择题:本小题共4小题,共58分。
15、(15分)2023年9月23日,杭州亚运会开幕式采用“数字融合”方式点燃主火炬塔,燃料首次使用
零碳甲醇。二氧化碳加氢合成甲醇是化学固碳的一种有效途径,不仅可以有效减少空气中的 CO 排
2
放,而且可以制备出甲醇清洁能源。以CO 、CO、H 为原料合成CH OH涉及的主要反应如下:
2 2 3
①CO(g)+2H (g) CH OH(g) △H
2 3 1
②CO (g)+3H (g) CH OH(g)+H O(g) △H
2 2 3 2 2
③CO (g)+H (g) CO(g)+H O(g) △H
2 2 2 3
回答下列问题:
学科网(北京)股份有限公司
{#{QQABSQAEggCoAAJAAQgCUwEKCkAQkAEAAIoOABAAoAAASRFABAA=}#}(1)已知反应①中的相关的化学键键能数据如下:
由此计算△H = kJ·mol-1,已知△H =-58kJ·mol-1,则△H = kJ·mol-1。
1 2 3
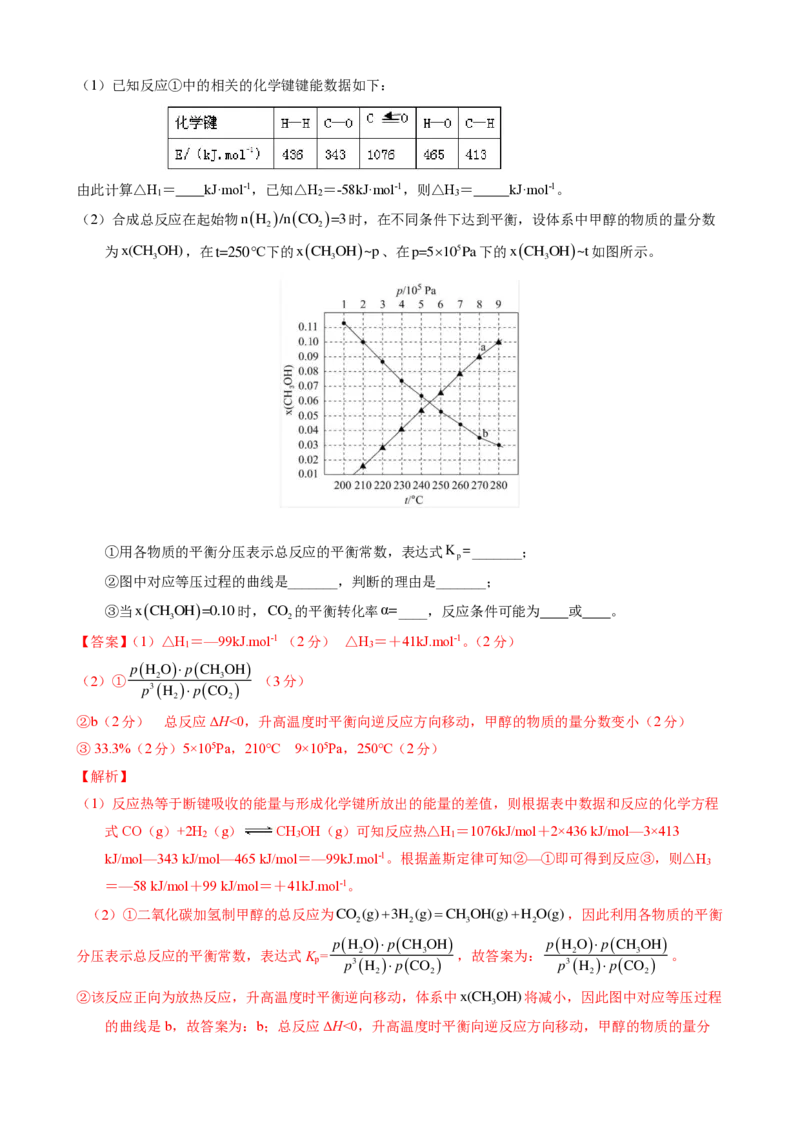
(2)合成总反应在起始物nH /nCO =3时,在不同条件下达到平衡,设体系中甲醇的物质的量分数
2 2
为x(CH OH),在t=250℃下的xCH OH~p、在p=5105Pa下的xCH OH~t如图所示。
3 3 3
①用各物质的平衡分压表示总反应的平衡常数,表达式K =_______;
p
②图中对应等压过程的曲线是_______,判断的理由是_______;
③当xCHOH=0.10时,CO 的平衡转化率α=____,反应条件可能为 或 。
3 2
【答案】(1)△H =—99kJ.mol-1 (2分) △H =+41kJ.mol-1。(2分)
1 3
pH OpCH OH
(2)① 2 3 (3分)
p3H pCO
2 2
②b(2分) 总反应ΔH<0,升高温度时平衡向逆反应方向移动,甲醇的物质的量分数变小(2分)
③ 33.3%(2分)5×105Pa,210℃ 9×105Pa,250℃(2分)
【解析】
(1)反应热等于断键吸收的能量与形成化学键所放出的能量的差值,则根据表中数据和反应的化学方程
式CO(g)+2H (g) CH OH(g)可知反应热△H =1076kJ/mol+2×436 kJ/mol—3×413
2 3 1
kJ/mol—343 kJ/mol—465 kJ/mol=—99kJ.mol-1。根据盖斯定律可知②—①即可得到反应③,则△H
3
=—58 kJ/mol+99 kJ/mol=+41kJ.mol-1。
(2)①二氧化碳加氢制甲醇的总反应为CO (g)3H (g)CH OH(g)H O(g),因此利用各物质的平衡
2 2 3 2
pH OpCH OH pH OpCH OH
分压表示总反应的平衡常数,表达式K = 2 3 ,故答案为: 2 3 。
p p3H pCO p3H pCO
2 2 2 2
②该反应正向为放热反应,升高温度时平衡逆向移动,体系中x(CH OH)将减小,因此图中对应等压过程
3
的曲线是b,故答案为:b;总反应ΔH<0,升高温度时平衡向逆反应方向移动,甲醇的物质的量分
学科网(北京)股份有限公司
{#{QQABSQAEggCoAAJAAQgCUwEKCkAQkAEAAIoOABAAoAAASRFABAA=}#}数变小。
3H g+CO g CH OHg+H Og
2 2 3 2
起始mol
3 1 0 0
③设起始n(CO )=1mol,n(H )=3mol,则 ,当平衡时
2 2 转化mol
3x x x x
平衡mol
3-3x 1-x x x
1
x 1 mol
xCH
3
OH=0.10时,
3-3x+1-x+x+x
=0.1,解得x=
3
mol,平衡时CO
2
的转化率α=3
100%
1mol
=33.3%;
由图可知,满足平衡时xCHOH=0.10的条件有:5×105Pa,210℃或9×105Pa,250℃,故答案为:
3
33.3%;5×105Pa,210℃;9×105Pa,250℃。
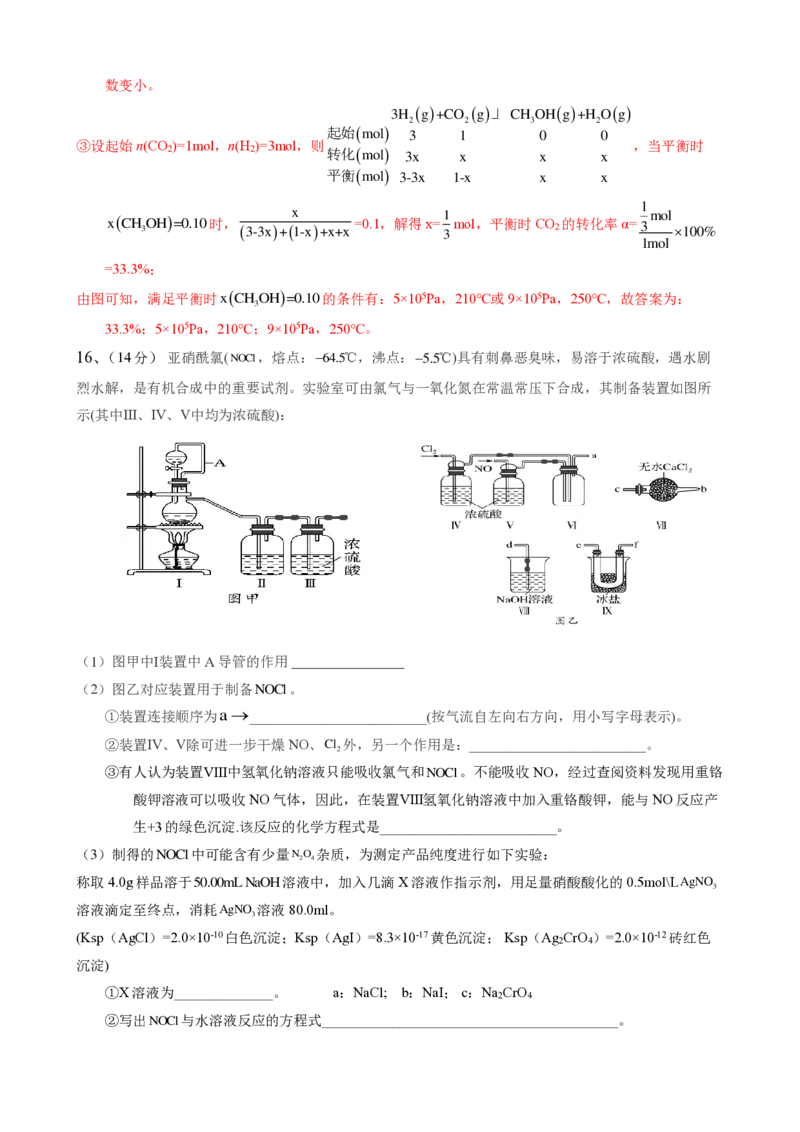
16、(14分) 亚硝酰氯(NOCl,熔点:64.5℃,沸点:5.5℃)具有刺鼻恶臭味,易溶于浓硫酸,遇水剧
烈水解,是有机合成中的重要试剂。实验室可由氯气与一氧化氮在常温常压下合成,其制备装置如图所
示(其中Ⅲ、Ⅳ、Ⅴ中均为浓硫酸):
(1)图甲中Ⅰ装置中A导管的作用
(2)图乙对应装置用于制备NOCl。
①装置连接顺序为a_________________________(按气流自左向右方向,用小写字母表示)。
②装置Ⅳ、Ⅴ除可进一步干燥NO、Cl 外,另一个作用是:_________________________。
2
③有人认为装置Ⅷ中氢氧化钠溶液只能吸收氯气和NOCl。不能吸收NO,经过查阅资料发现用重铬
酸钾溶液可以吸收NO气体,因此,在装置Ⅷ氢氧化钠溶液中加入重铬酸钾,能与NO反应产
生+3的绿色沉淀.该反应的化学方程式是_________________________。
(3)制得的NOCl中可能含有少量NO 杂质,为测定产品纯度进行如下实验:
2 4
称取4.0g样品溶于50.00mL NaOH溶液中,加入几滴X溶液作指示剂,用足量硝酸酸化的0.5mol\LAgNO
3
溶液滴定至终点,消耗AgNO 溶液80.0ml。
3
(Ksp(AgCl)=2.0×10-10白色沉淀;Ksp(AgI)=8.3×10-17黄色沉淀; Ksp(Ag CrO )=2.0×10-12砖红色
2 4
沉淀)
①X溶液为______________。 a:NaCl; b:NaI; c:Na CrO
2 4
②写出NOCl与水溶液反应的方程式__________________________________________。
学科网(北京)股份有限公司
{#{QQABSQAEggCoAAJAAQgCUwEKCkAQkAEAAIoOABAAoAAASRFABAA=}#}③样品的纯度(质量分数)为_______%(计算结果保留1位小数)。
答案:(1)保持分液漏斗上下压强相等,液体由于重力能顺利流下(2分)
(2)①e→f→c→b→d(2分) ②观察气泡的速率,调节气体的流速(2分)
③K Cr O +2NO+3H O=2KNO +2Cr(OH) ↓(2分)
2 2 7 2 3 3
(3)①根据AgCl,AgI和Ag CrO 三种物质的Ksp,在三种离子的混合溶液中:逐滴滴加AgNO 溶
2 4 3
液时,三种离子沉淀的先后顺序I->Cl->CrO 2-。为了指示反应的终点,应让Cl-先沉淀。所以选用Na CrO
4 2 4
作指示剂(2分)
②NOCl+H O=HCl+HNO (2分)
2 2
③n AgNO 3 =0.08L×0.5mol\L=0.04mol 由 关 系 式 得 : NOCl —NaCl—AgNO 3 n NOCl
=0.08L×0.5mol\L=0.04mol 则样品的纯度为(0.04mol×65.5g\mol)\4.0g×100%=65.5%(2分)
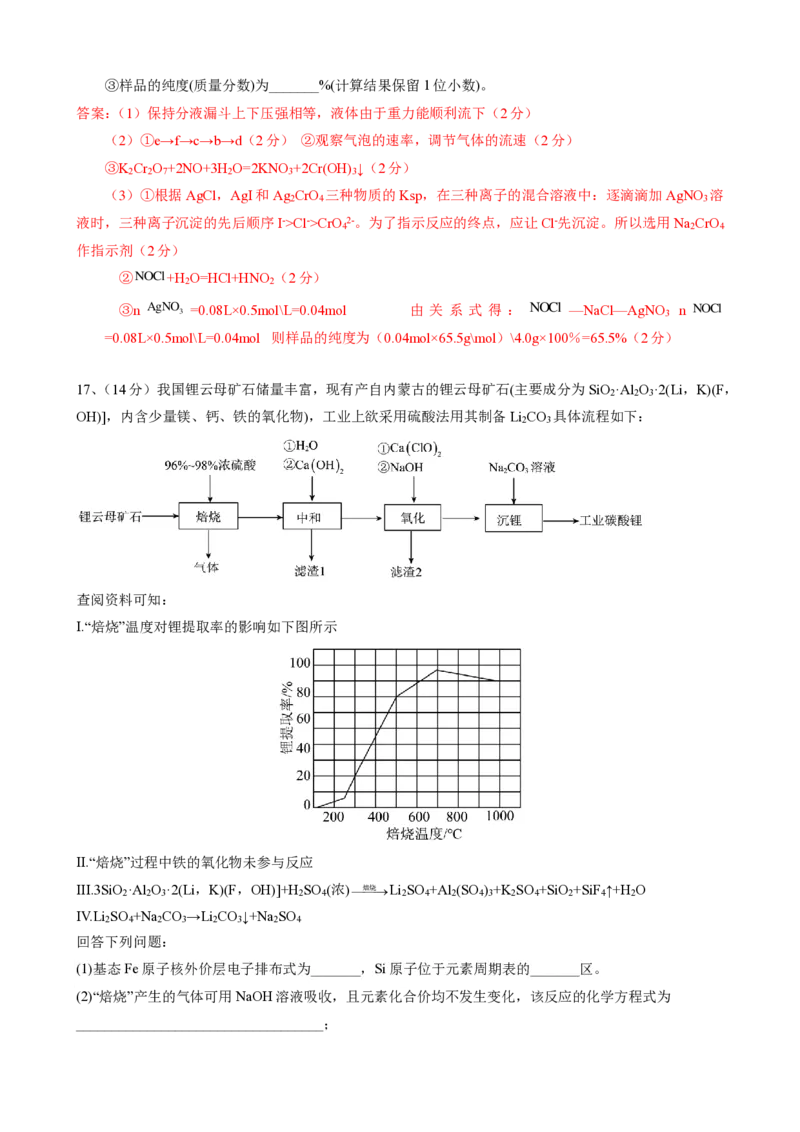
17、(14分)我国锂云母矿石储量丰富,现有产自内蒙古的锂云母矿石(主要成分为SiO ·Al O ·2(Li,K)(F,
2 2 3
OH)],内含少量镁、钙、铁的氧化物),工业上欲采用硫酸法用其制备Li CO 具体流程如下:
2 3
查阅资料可知:
I.“焙烧”温度对锂提取率的影响如下图所示
II.“焙烧”过程中铁的氧化物未参与反应
III.3SiO
2
·Al
2
O
3
·2(Li,K)(F,OH)]+H
2
SO
4
(浓)焙烧Li
2
SO
4
+Al
2
(SO
4
)
3
+K
2
SO
4
+SiO
2
+SiF
4
↑+H
2
O
IV.Li SO +Na CO →Li CO ↓+Na SO
2 4 2 3 2 3 2 4
回答下列问题:
(1)基态Fe原子核外价层电子排布式为_______,Si原子位于元素周期表的_______区。
(2)“焙烧”产生的气体可用NaOH溶液吸收,且元素化合价均不发生变化,该反应的化学方程式为
___________________________________;
学科网(北京)股份有限公司
{#{QQABSQAEggCoAAJAAQgCUwEKCkAQkAEAAIoOABAAoAAASRFABAA=}#}(3)在“中和”过程中,为使Fe3+和Al3+完全沉淀,pH值至少调整为_______;部分金属氢氧化物的
pK (pK =-lgK )如图所示:
sp sp sp
(4) “氧化”过程中发生氧化还原反应的离子方程式为________________________________;
(5)石墨可用作锂离子电池的负极材料,充电时可由Li C 形成Li+计按如图所示均匀分布的锂碳化合
1-x 6
物,该物质中存在的化学键有_______,充电时该电极的电极反应式为
_____________________________________________。
答案:(1)3d64s2(2分) p(2分)
(2)“焙烧”生成SiF 气体,Si为+4价,F为-1价;用NaOH溶液吸收,且元素化合价均不发生变化,所
4
以方程式为SiF +6NaOH=Na SiO +4NaF+3H O;故答案为SiF +6NaOH=Na SiO +4NaF+3H O。(2分)
4 2 3 2 4 2 3 2
(3)为使Fe3+和Al3+完全沉淀,且溶液中离子浓度为110-5mol/L视为完全沉淀,由图可知,Al3+完全沉
11032
淀pH值高,此时溶液中c(OH-)=3 1109mol/L,此时pH=5,所以pH值至少调整为5。(2分)
1105
(4)“氧化”过程主要是氧化亚铁离子,并调pH使其沉淀,所以离子方程式为ClO-+2Fe2++H O+4OH-
2
=2Fe(OH) ↓+Cl-。(2分)
3
(5)离子键,非极性共价键(2分)
Li C -(1/4-X)e-=(1/4-X)Li++Li C (2分)
1-x 6 3/4 6
18.(15 分)多环氨基甲酰基吡啶酮类似物 F,可以作为药物原料或中间体合成新型抗流感病
毒药物。
已知:
学科网(北京)股份有限公司
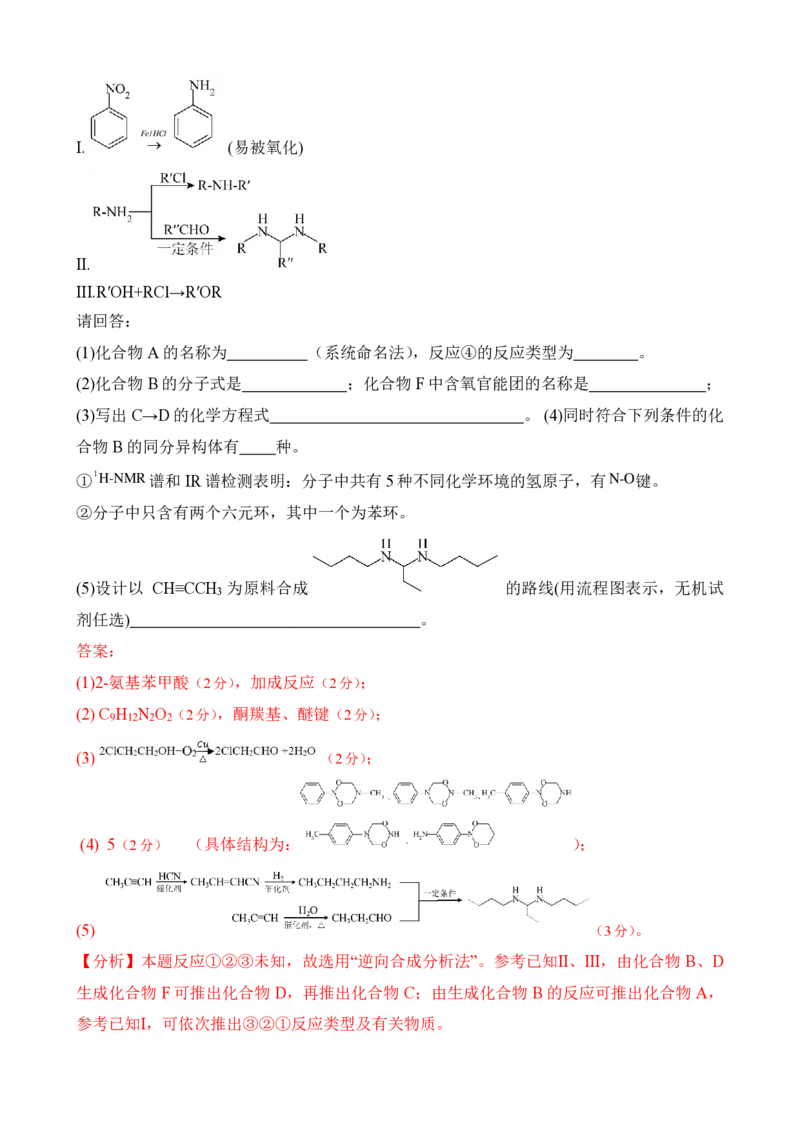
{#{QQABSQAEggCoAAJAAQgCUwEKCkAQkAEAAIoOABAAoAAASRFABAA=}#}Fe/HCl
I. (易被氧化)
II.
III.R′OH+RCl→R′OR
请回答:
(1)化合物A的名称为 (系统命名法),反应④的反应类型为 。
(2)化合物B的分子式是 ;化合物F中含氧官能团的名称是 ;
(3)写出C→D的化学方程式 。 (4)同时符合下列条件的化
合物 B的同分异构体有 种。
①1H-NMR谱和IR谱检测表明:分子中共有 5种不同化学环境的氢原子,有N-O键。
②分子中只含有两个六元环,其中一个为苯环。
(5)设计以 CH≡CCH 为原料合成 的路线(用流程图表示,无机试
3
剂任选) 。
答案:
(1)2-氨基苯甲酸(2分),加成反应(2分);
(2) C
9
H
12
N
2
O
2
(2分),酮羰基、醚键(2分);
(3) (2分);
(4) 5(2分) (具体结构为: );
(5) (3分)。
【分析】本题反应①②③未知,故选用“逆向合成分析法”。参考已知Ⅱ、Ⅲ,由化合物 B、D
生成化合物 F可推出化合物 D,再推出化合物 C;由生成化合物 B的反应可推出化合物 A,
参考已知Ⅰ,可依次推出③②①反应类型及有关物质。
学科网(北京)股份有限公司
{#{QQABSQAEggCoAAJAAQgCUwEKCkAQkAEAAIoOABAAoAAASRFABAA=}#}【详解】(1)生成化合物 B 的反应为羧基与氨基间的成肽反应,故化合物 A 含有官能团-
COOH,则A的结构简式为 ,系统命名为2-氨基苯甲酸;对比反应物C H 与产物
2 4
C分子组成,可以确定反应④为加成反应。
(2)根据化合物B的结构简式确定其分子式为C H N O ;根据化合物F的结构简式确定其
9 12 2 2
含氧官能团名称为:,酮羰基、醚键。
(3)根据化合物 C生成化合物 D的条件确定该反应为醇催化氧化为醛,故化合物 C的结构
CH ClCHO
简式为:CH 2 ClCH 2 OH,化合物 D 的结构简式为: 2 ,该反应的化学方程式为:
;
(4)化合物 B 除苯环外,还有一个 C=O,其同分异构体要求除苯环外,还有一个六元环,
因此第二个六元环各原子间全是单键;分子中有 5 种不同化学环境的氢,要求分子结构具有
较强的对称性,如果两个环形成稠环结构,无法产生强对称性,故两个环是分开的,当第二
个六元环由 2 个 N、2 个 O、2 个 C 组成时,有四种结构,当第二个六元环由 1 个 N,2 个
O,3个C组成时,有一种结构。故共有五种同分异构体:
(5)参考已知反应Ⅱ,该产品可由 2分子的 CH CH CH CH NH 与 1分子的 CH CH CHO合
3 2 2 2 2 3 2
成,CH C≡CH 与水反应可制备 CH CH CHO,碳链增加一个 C原子需要使用 HCN,故制备
3 3 2
CH CH CH CH NH 的流程为: ,最终产品合成路线
3 2 2 2 2
为:
学科网(北京)股份有限公司
{#{QQABSQAEggCoAAJAAQgCUwEKCkAQkAEAAIoOABAAoAAASRFABAA=}#}