文档内容
稳昇高教育高2026届12月联合质量检测
化学参考答案及解析
一、选择题
1 2 3 4 5 6 7 8 9 10 11 12 13 14
C C B B C A B D A A D D C D
1.C【解析】液氧是臭氧的同素异形体
2.C【解析】生铁发生吸氧腐蚀时的负极反应式应为:Fe-2e—=Fe2+
3.B【解析】A项,CO 的空间结构模型应为直线形;
2
C项,氯化铵的电子式应为
D项,NaHCO 的电离方程式应为NaHCO = Na++ HCO -
3 3 3
4.B【解析】A项,HF 标况下不是气体;
C 项,SO 与O 的反应是可逆反应;
2 2
D 项,Fe(OH) 胶体属于粒子集合体,1 mol K FeO 在水中完全反应生成的
3 2 4
Fe(OH) 胶体粒子数目小于N
3 A
5.C【解析】A项,SO 2-不能大量共存;
3
B 项,Fe3+不能大量共存;
D项,AlO -与HCO -不共存
2 3
6.A【解析】钾离子的焰色需通过蓝色钴玻璃观察
7.B【解析】A项,Li 在过量O 中燃烧只得到Li O
2 2
C 项,铝热反应可以冶炼活泼性弱于 Al 的金属
D项,工业上通过电解熔融 NaCl 生成Na
8.D【解析】A项,X为HCl
B 项,N分子的核磁共振氢谱有4组峰
C 项,1mol M 最多可与 5mol H 加成,注意-CN 可与 H 加成
2 2
9.A【解析】B 项,操作顺序应为“向某溶液中滴加 KSCN溶液,无明显现象,再通入氯气”;
C 项,悬浊液红色先褪去,振荡后又变为红色,体现溶解平衡的移动
D项,甲苯也能使酸性高锰酸钾褪色,不能说明2-甲基苯甲醛中含有醛基
10.A【解析】左1不是NaCl 的晶胞
111.D【解析】阳极室发生反应 2H O-4e-=O ↑+4H+,产生的 H+通过 A 膜迁出,即电解过
2 2
程阳极室 n(H O)减少,故 pH 应减小
2
12.D【解析】W、X、Y、Z分别为H、O、N、S,该物质为(NH ) S O ,含有过氧键,具有
4 2 2 8
较强氧化性。
13.C【解析】V→VI反应随温度升高,正反应速率和逆反应速率均增大,其中后者增大
幅度更大
14.D【解析】A项,图中线上的点代表H 或CO还原铁氧化物的平衡状态。由图可知,随温
2
度升高,Fe 与FeO、Fe 与Fe O 的分界线均呈下降趋势,即平衡时H 的体积分
3 4 2
数减小,说明H 还原铁氧化物的反应均为吸热反应;
2
B 项,600℃时将Fe O 与FeO 的分界线,CO的占比小于H 的,说明平衡时反
3 4 2
应进行的程度更大;
C 项,H (g)+FeO(s)=H O(g)+Fe(s),反应的K = PH2O = 1−0.668 =0.497;
2 2 p
PH2 0.668
D项,由图可知,一定条件下 Fe O 可直接被还原为Fe。
3 4
二、非选择题
15.(14分,无特殊标注,每空2分)
(1)6(1分) VIIB(1分)
(2)X射线衍射法(1分)
(3)将Re氧化为 Re O ,除去催化剂表面的积碳和有机物
2 7
(4)Re O +2NaOH 2NaReO +H O
2 7 4 2
(5)①Al(OH) +3H+=Al3++3H O
3 2
②Cl
2
(6)+4 (1分) 2KReO +7H 2Re+2KOH+6H O
4 2 2
16.(15分,无特殊标注,每空2分)
(1)MnO +4HCl(浓) MnCl +2H O+Cl ↑
2 2 2 2
(2)饱和食盐水 (1分)
吸收多余的Cl 防污染,防止空气中水蒸气进入使AlCl 水解
2 3
(3)作溶剂(1分)
2(4)反应液中不再有气泡产生
(5)分液漏斗 洗去氯化钠和碳酸钠
(6)蒸馏(1分)
(7)58.6%
17.(14分,每空2分)
(1)-385 kJ⋅ mol-1
(2)AD
(3)①2H* +O* →H O
2
②H O 为该反应的催化剂,适量H O 可加快反应速率,提高乙醇酸一定时间内的产率
2 2
(4)3.41
(5)HOOCCOOH+ 4e- +4H+ =HOCH COOH+H O
2 2
(6)62.5%
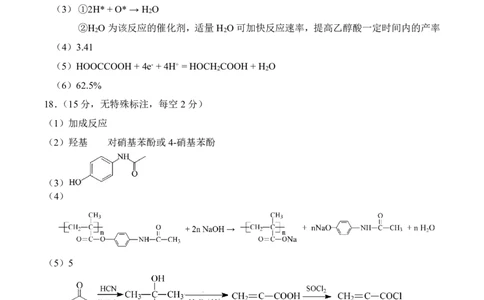
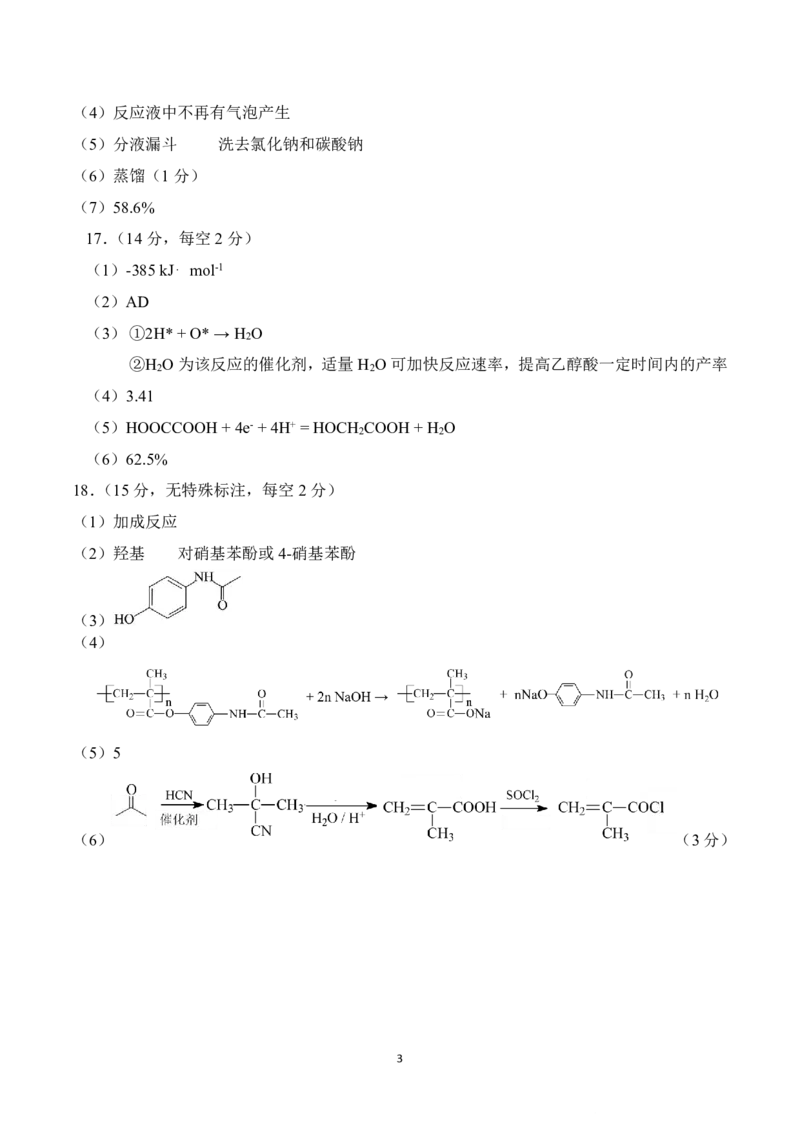
18.(15分,无特殊标注,每空2分)
(1)加成反应
(2)羟基 对硝基苯酚或4-硝基苯酚
(3)
(4)
(5)5
(6) (3分)
3