文档内容
2023~2024 学年度第一学期教学质量检查
高三化学
注意事项:
1.本试卷分选择题和非选择题两部分。
2.试卷满分100分,考试时间75分钟。
可能用到的相对原子质量:
一、选择题:本题包括 16小题,共44分。第1~10小题,每小题2分;第11~16小题,每小
题4分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1.线条来去,纹彩风流,文物上的纹样记录了五千年的华夏之美。下列纹样载体主要由合金材料制成的是(
)。
纹样载体
选项 A.清夔龙纹磁笔洗 B.西周吴虎鼎 C.战国燕饕餮纹瓦当 D.汉卷云纹玉壁
2.科技是第一生产力,近年我国科学家在诸多领域做出了卓越成就。下列说法正确的是( )。
A.核地研院发现月壤中“嫦娥石”富含稀有元素钇, 和 互为同素异形体
B.“天舟四号”配置砷化镓太阳能电池,其能量转化形式为太阳能转化为电能
C.中科院化学所研制纳米四氧化三铁晶体材料,该晶体为金属晶体
D.杭州亚运会主火炬塔使用废碳再生的“绿色零碳甲醇”燃料,该燃料不含碳元素
3.化学用语是化学的特殊语言。下列选项正确的是( )。
A.羟基的电子式:
B. 中存在:p-p 键和s-s 键
C.基态Cr原子的价层电子轨道表示式:
D. 价层电子对互斥模型:
4.建设粤港澳大湾区,共筑新时代新梦想,时时处处有化学。下列说法正确的是( )。
A.湾区制造聚焦新材料,电池级针状焦石墨属于金属材料
B.“岭南通”服务大湾区智慧出行,卡基材料聚氯乙烯易降解
C.湾区化妆品产值国内居首,纳米 反射紫外线防晒利用的是化学变化
学科网(北京)股份有限公司D.氢能产业助力湾区高质量发展, 在燃料电池中被氧化
5.劳则有思,动则有得。下列劳动项目与所述的化学知识没有关联的是( )。
选项 劳动项目 化学知识
A 用糯米和麦芽制作传统麦芽糖 淀粉可发生酶促水解反应
B 用煤油擦拭自行车上的沥青 有机物结构相似能互溶
C 用紫外灯给环境消毒 紫外线使蛋白质变性
D 用含铁的红色涂料粉刷房屋外墙 氧化铁为碱性氧化物
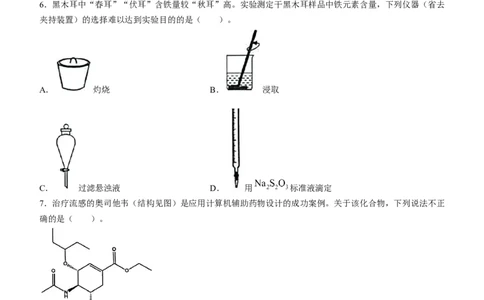
6.黑木耳中“春耳”“伏耳”含铁量较“秋耳”高。实验测定干黑木耳样品中铁元素含量,下列仪器(省去
夹持装置)的选择难以达到实验目的的是( )。
A. 灼烧 B. 浸取
C. 过滤悬浊液 D. 用 标准液滴定
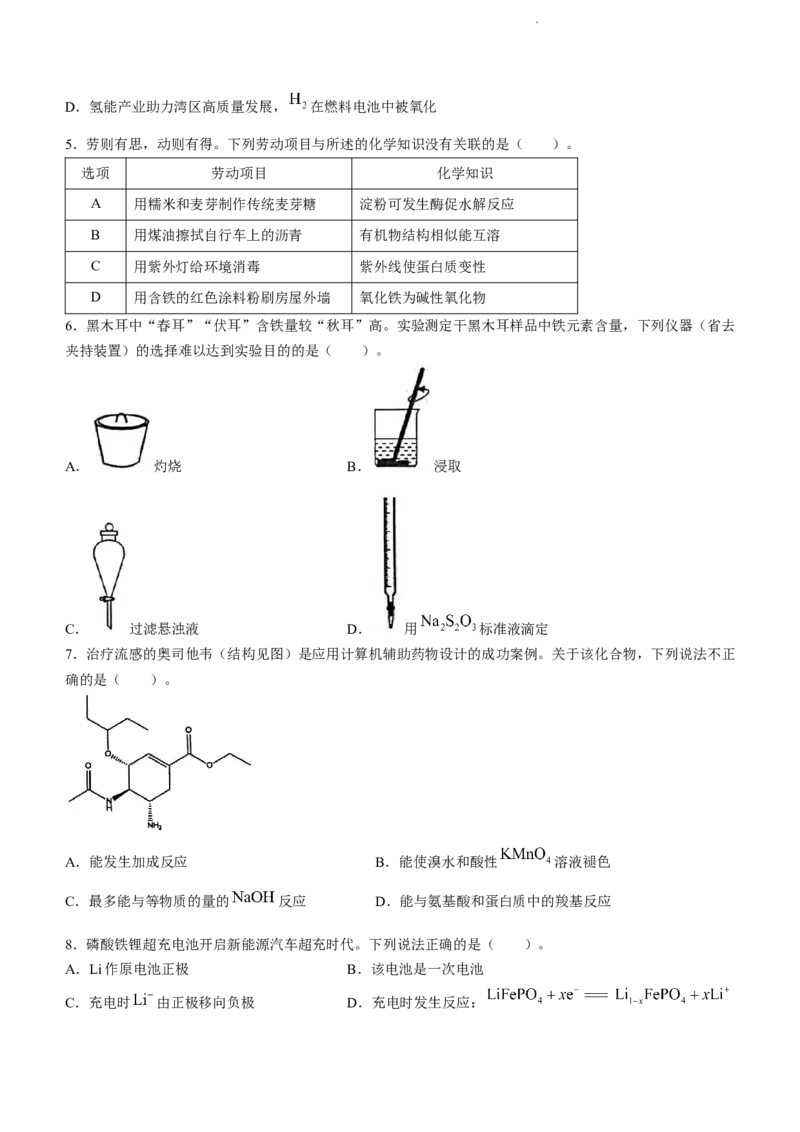
7.治疗流感的奥司他韦(结构见图)是应用计算机辅助药物设计的成功案例。关于该化合物,下列说法不正
确的是( )。
A.能发生加成反应 B.能使溴水和酸性 溶液褪色
C.最多能与等物质的量的 反应 D.能与氨基酸和蛋白质中的羧基反应
8.磷酸铁锂超充电池开启新能源汽车超充时代。下列说法正确的是( )。
A.Li作原电池正极 B.该电池是一次电池
C.充电时 由正极移向负极 D.充电时发生反应:
学科网(北京)股份有限公司9.如图为铜或镁元素的部分价类二维图,下列叙述不正确的是( )。
A.可能存在a→d→e的直接转化
B.d可能溶于过量的氨水
C.若新制的d能用于检验醛基,则此时生成b
D.蒸干c的水溶液均能得到原溶质
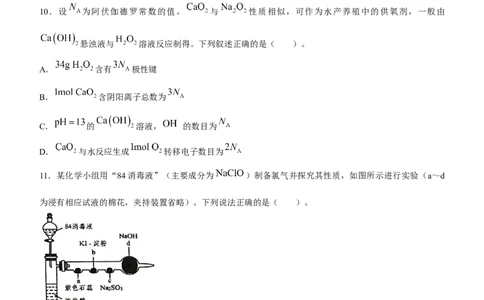
10.设 为阿伏伽德罗常数的值。 与 性质相似,可作为水产养殖中的供氧剂,一般由
悬浊液与 溶液反应制得。下列叙述正确的是( )。
A. 含有 极性键
B. 含阴阳离子总数为
C. 的 溶液, 的数目为
D. 与水反应生成 转移电子数目为
11.某化学小组用“84消毒液”(主要成分为 )制备氯气并探究其性质,如图所示进行实验(a~d
为浸有相应试液的棉花,夹持装置省略)。下列说法正确的是( )。
A.具支试管中产生黄绿色气体,体现了浓盐酸的挥发性
B.a处棉花变红而不褪色
C.b处棉花变为蓝色,说明氧化性:
D.c处无明显现象,说明未发生化学反应
12.物质间转化有规律。下列方程式符合规律且正确的是( )。
A.酸性氧化物+水→酸:
学科网(北京)股份有限公司B.较强酸+较弱酸盐→较弱酸+较强酸盐:
C.酸+碱→盐+水:
D.活泼金属+水→碱+氢气:
13.已知前四周期元素X、Y、Z、R的原子序数依次增大。X是最轻的元素,Y的p轨道比s轨道少2个电
子,Z与Y同周期,Z的最简氢化物水溶液呈碱性,R元素常被称为“21世纪金属”,广泛用作航空材料。
元素Y和R组成的某气态团簇分子结构如图所示。下列说法正确的是( )。
A.最简氢化物熔沸点比较:Y<Z
B.元素X分别与Y、Z组成的常见化合物均为极性分子
C.基态Y、Z原子核外电子均有5种空间运动状态
D.该气态团簇分子的分子式为RY
14.下表中陈述Ⅰ与陈述Ⅱ均正确,且具有因果关系的是( )。
选项 陈述Ⅰ 陈述Ⅱ
A 石英坩埚可用于熔融烧碱
熔点高
B 氨是工业制硝酸的原料
具有还原性
C 铜与稀硝酸反应,试管上方气体变红 NO为红棕色气体
D 可用于除去工业废水中的 是难溶物
15.黄铵铁矾 能催化 形成自由基(过程可能的机理如图所示),氧化去
除废水中的偶氮染料。下列说法不正确的是( )。
A.图中 指黄铵铁矾 B.图所示过程 可生成
学科网(北京)股份有限公司C.反应③有极性共价键的断裂和形成 D.温度越高,偶氮染料去除率越大
16.我国研发的“无淡化海水原位直接电解制氢技术”装置如图所示,阴、阳极材料均为附着有 的
催化电极网,表面的 可选择性地紧密结合水电离出的 。下列说法不正确的是( )。
A.气体b为
B. 负电层可减少副产物 的生成
C. 等电极垢在阳极产生,应定期更换
D.与海水淡化间接制氢相比,原位直接制氢成本低
二、非选择题:本题共4小题,共56分。
17.(14分)镁是一种活泼金属,常温下能与水缓慢反应。某实验小组将打磨后的镁条投入 滤液中,
发现立即产生大量气泡,实验探究原因。
(1)重复实验:配制 溶液,除托盘天平、烧杯、量筒、玻璃棒外,还需用到的
玻璃仪器有__________,保存时需注意__________。向 溶液中加入
溶液,产生白色沉淀后过滤,得到 滤液。取少许 滤液,投入 打
磨后的镁条,快速产生大量气泡。
(2)实验探究镁与 滤液快速产生气体的原因。
【查阅资料】体积较小的阴离子,能够“钻入” 膜,达到使其溶解的效果。 对该反应无影响。
【提出猜想】可能是 或 促进镁与水的反应。
【实验探究】完成下列表格。
序号 实验操作 实验现象
Ⅰ 将 打磨后的镁条投入 水中 细微气泡附着
学科网(北京)股份有限公司Ⅱ 将 打磨后的镁条投入 __________ 细微气泡附着
溶液中
Ⅲ 将 打磨后的镁条投入__________中 细小气泡放出
【实验结论】 能促进镁与水的反应,溶液中 离子无影响。
(3)对比发现镁与 滤液的反应速率比实验Ⅲ更快。经讨论,猜想 滤液中存在微量银离子,可能
形成了微小 原电池,进一步加快反应速率。
【提出猜想】 和 共同加快镁与水反应速率。
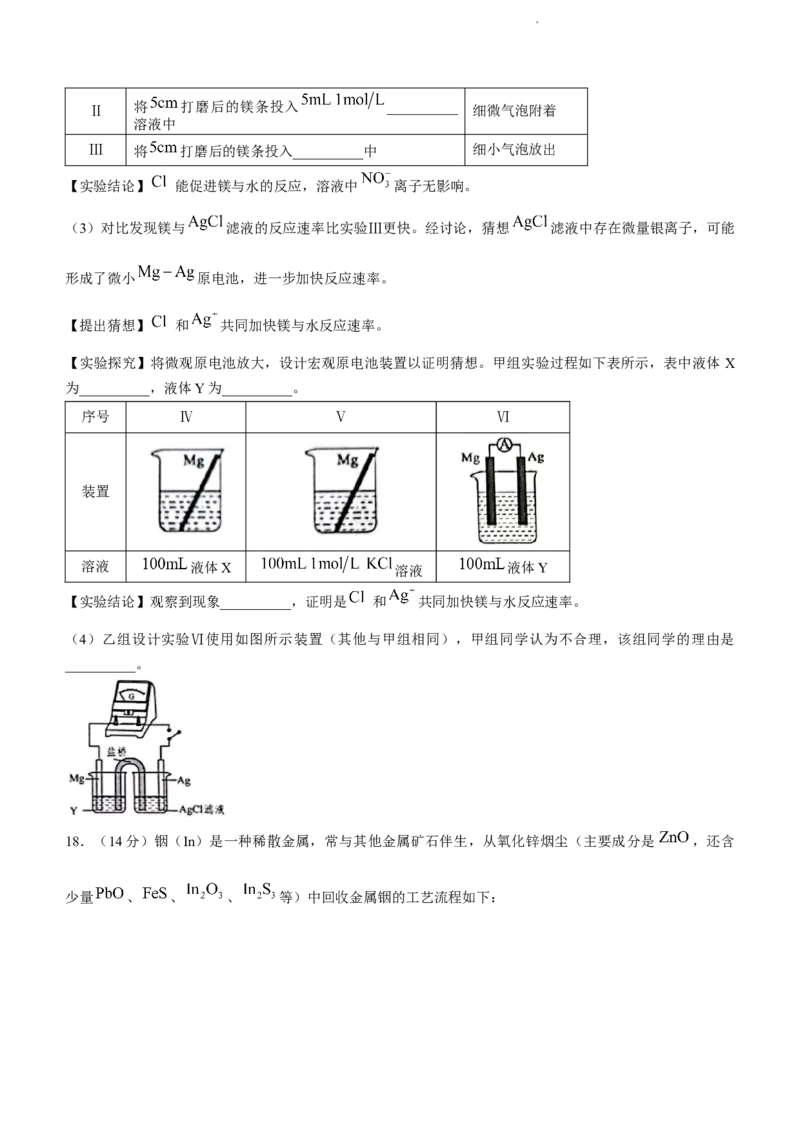
【实验探究】将微观原电池放大,设计宏观原电池装置以证明猜想。甲组实验过程如下表所示,表中液体 X
为__________,液体Y为__________。
序号 Ⅳ Ⅴ Ⅵ
装置
溶液 液体X 溶液 液体Y
【实验结论】观察到现象__________,证明是 和 共同加快镁与水反应速率。
(4)乙组设计实验Ⅵ使用如图所示装置(其他与甲组相同),甲组同学认为不合理,该组同学的理由是
__________。
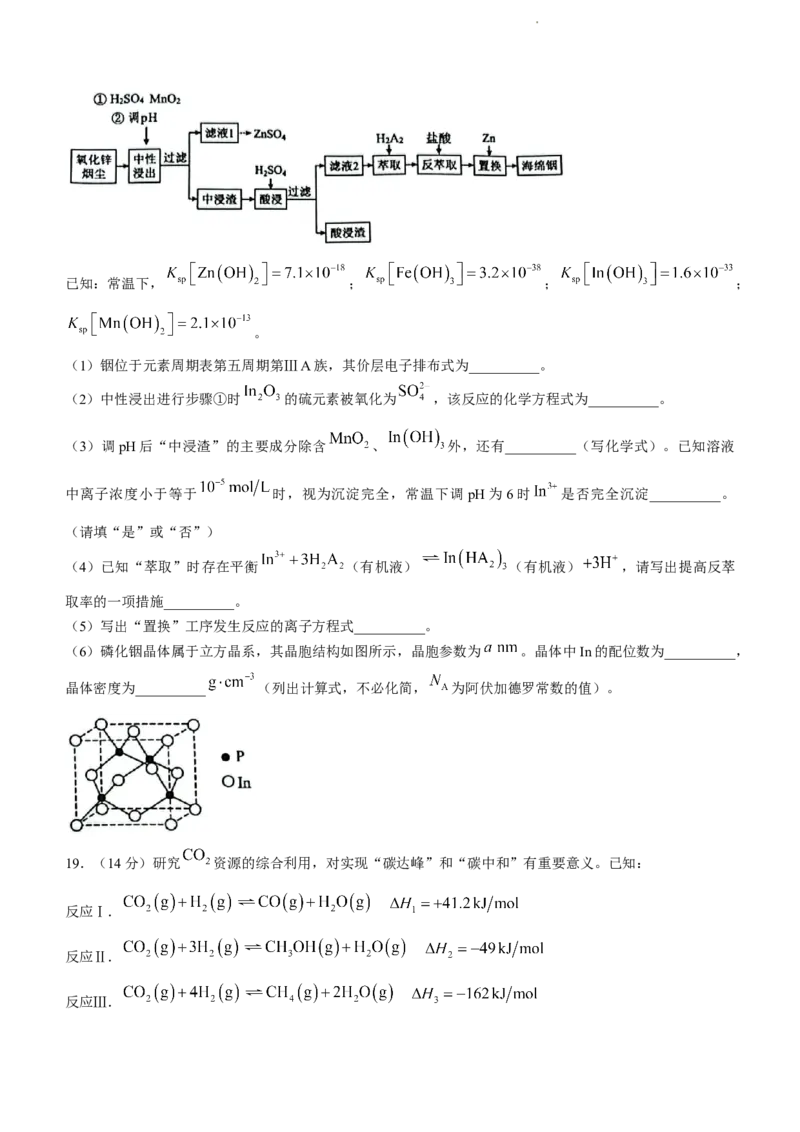
18.(14分)铟(In)是一种稀散金属,常与其他金属矿石伴生,从氧化锌烟尘(主要成分是 ,还含
少量 、 、 、 等)中回收金属铟的工艺流程如下:
学科网(北京)股份有限公司已知:常温下, ; ; ;
。
(1)铟位于元素周期表第五周期第ⅢA族,其价层电子排布式为__________。
(2)中性浸出进行步骤①时 的硫元素被氧化为 ,该反应的化学方程式为__________。
(3)调pH后“中浸渣”的主要成分除含 、 外,还有__________(写化学式)。已知溶液
中离子浓度小于等于 时,视为沉淀完全,常温下调 pH为6时 是否完全沉淀__________。
(请填“是”或“否”)
(4)已知“萃取”时存在平衡 (有机液) (有机液) ,请写出提高反萃
取率的一项措施__________。
(5)写出“置换”工序发生反应的离子方程式__________。
(6)磷化铟晶体属于立方晶系,其晶胞结构如图所示,晶胞参数为 。晶体中In的配位数为__________,
晶体密度为__________ (列出计算式,不必化简, 为阿伏加德罗常数的值)。
19.(14分)研究 资源的综合利用,对实现“碳达峰”和“碳中和”有重要意义。已知:
反应Ⅰ.
反应Ⅱ.
反应Ⅲ.
学科网(北京)股份有限公司(1)低温自发的反应是__________(填反应序号)。
(2) 温度下( 为气态),向恒容密闭容器中充入 和 ,发生上述反应,下列表明反应Ⅱ已经
达到平衡状态的是__________。
A.压强保持不变 B. 与 的物质的量之比为
C.混合气体的密度保持不变 D.混合气体的平均相对分子质量保持不变
(3) 时,反应Ⅰ的速率方程为 ,其中x表示相应气体的物质的量分数,
为平衡常数(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数),k为反应的速率常数。已知
保持 不变,达到平衡时, ,此时反应Ⅰ的速率 __________ (用含
k的代数式表示)。
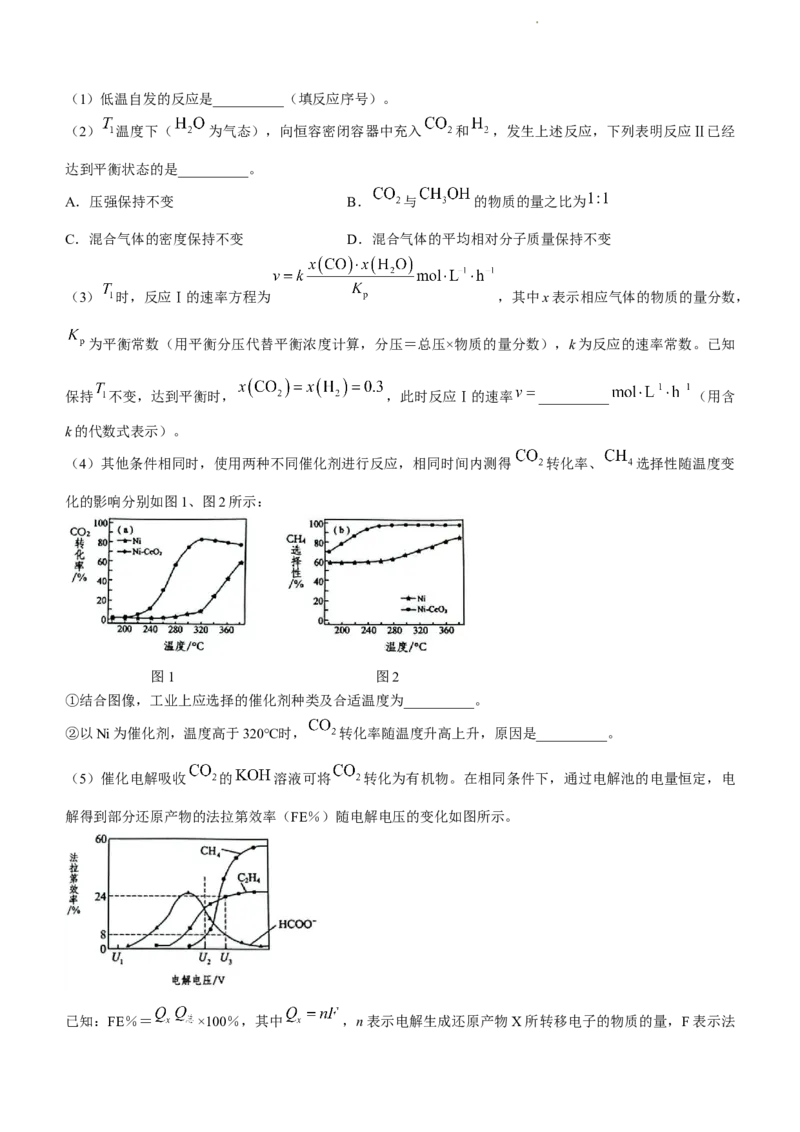
(4)其他条件相同时,使用两种不同催化剂进行反应,相同时间内测得 转化率、 选择性随温度变
化的影响分别如图1、图2所示:
图1 图2
①结合图像,工业上应选择的催化剂种类及合适温度为__________。
②以Ni为催化剂,温度高于320℃时, 转化率随温度升高上升,原因是__________。
(5)催化电解吸收 的 溶液可将 转化为有机物。在相同条件下,通过电解池的电量恒定,电
解得到部分还原产物的法拉第效率(FE%)随电解电压的变化如图所示。
已知:FE%= ×100%,其中 ,n表示电解生成还原产物X所转移电子的物质的量,F表示法
学科网(北京)股份有限公司拉第常数。
①当电解电压为 时,电解过程中含碳还原产物的FE%为0,阴极主要还原产物为__________(填化学
式)。
②当电解电压为 时,阴极由 生成 的电极反应式为__________。
③当电解电压为 时,电解生成的 和 的物质的量之比为__________。
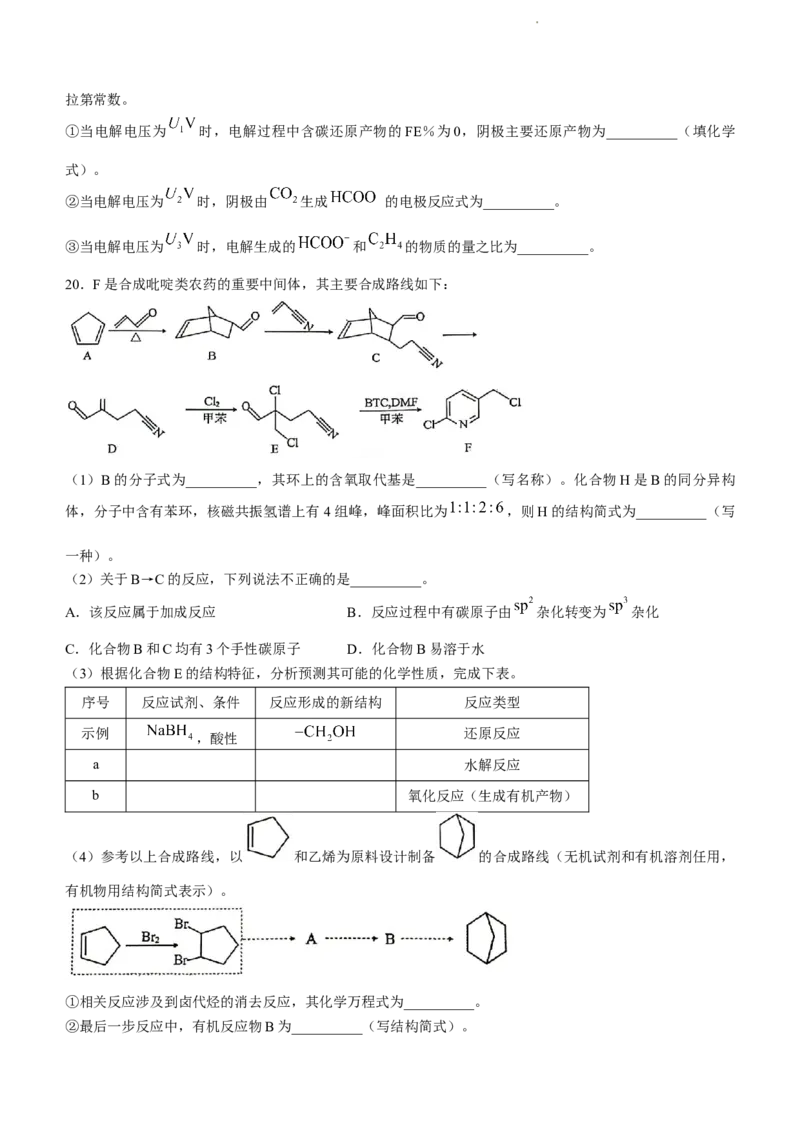
20.F是合成吡啶类农药的重要中间体,其主要合成路线如下:
(1)B的分子式为__________,其环上的含氧取代基是__________(写名称)。化合物H是B的同分异构
体,分子中含有苯环,核磁共振氢谱上有 4组峰,峰面积比为 ,则H的结构简式为__________(写
一种)。
(2)关于B→C的反应,下列说法不正确的是__________。
A.该反应属于加成反应 B.反应过程中有碳原子由 杂化转变为 杂化
C.化合物B和C均有3个手性碳原子 D.化合物B易溶于水
(3)根据化合物E的结构特征,分析预测其可能的化学性质,完成下表。
序号 反应试剂、条件 反应形成的新结构 反应类型
示例 还原反应
,酸性
a 水解反应
b 氧化反应(生成有机产物)
(4)参考以上合成路线,以 和乙烯为原料设计制备 的合成路线(无机试剂和有机溶剂任用,
有机物用结构简式表示)。
①相关反应涉及到卤代烃的消去反应,其化学万程式为__________。
②最后一步反应中,有机反应物B为__________(写结构简式)。
学科网(北京)股份有限公司学科网(北京)股份有限公司2023~2024 学年度第一学期教学质量检查
高三化学参考答案
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16
答案 B B A D D C C C D D C B A B D C
17.(14分)
(1) 容量瓶、胶头滴管(2分) 避光(1分,使用棕色试剂瓶等合理表述均给分)
(2) (1分) 溶液(2分)
(3)蒸馏水(2分) 溶液(2分)
实验Ⅴ中气泡产生的速率比实验Ⅳ快,实验Ⅵ中气泡产生的速率比实验Ⅴ快(2分)
(4)使用盐桥改变单位时间离子迁移量使得Ⅴ、Ⅵ速率不可比。(或存在Mg置换 滤液中 的副反
应,使得Ⅴ、Ⅵ速率不可比。2分,答 滤液应为 溶液也可给分,其他合理表述也可给分。)
18.(14分)
(1) (1分)
(2) (2分)
(3) 、 (2分) 是(2分)
(4)增大盐酸的浓度(2分)
(5) (1分)
(6)4(2分) (或 ,2分)
19.(14分)
(1)Ⅱ、Ⅲ(1分)
(2)AD(2分》
(3) (2分)
(4)① (1分) 320℃(1分)
②反应未达到平衡,催化剂活性随升温增强加快速率,使得 转化率上升。(2分。反应未达到平衡,温
学科网(北京)股份有限公司度升高速率加快, 转化率上升。给1分)
(5)① (1分) ② (2分) ③ (2分)
20.(14分)
(1) (1分) 醛基(1分)
或 (2分)
(2)CD(2分)
(3)(每空1分,共4分,合理答案均可给分)
序号 反应试剂、条件 反应形成的新结构
示例
,酸性
a ,水溶液,加热 或 (写对氰基水解为羧酸
钠盐也给分)
b 新制氢氧化铜,加热 (写对氰基被氧化为羧基也给分)
(4)① (2分)
② (2分)
学科网(北京)股份有限公司