文档内容
2023-2024 学年度第一学期高三期末调研考试
化学试题
考生注意:
1.答卷前,考生务必将自己的姓名、考生号、考场号、座们号填写在答题卡.
2.回答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑,如需改
动,用橡皮擦干净后,再涂选其它答案标号.回答非选择题时,用黑色墨水签字笔在答题卡上书
写作答,在试题卷上作答,答案无效.
3.考试结束后,将本试卷和答题卡一并交回.
可能用到的相对原子质量:H-1 B-11 C-12 N-14 O-16 Na-23 P-31 Cl-35.5 Ca-40
Fe-56
一、选择题(本题包括14小题,每小题3分,共42分.每小题只有一个选项符合题意)
1.中华优秀传统文化是中华文明的智慧结晶和精华所在.下列说法正确的是( )
A.曾侯乙编钟是青铜制品,可用足量硝酸处理其表面的铜锈
B.《天工开物》中“取入缸中浸三个时,漉入釜中……”,使用了过滤操作
C.《周易》记载“泽中有火……上火下泽”,其描述的是CO在沼泽表面燃烧的现象
D.《本草纲目》记载“灶中所烧薪柴之灰,令人以灰淋汁,取碱浣衣”中“碱”是氢氧化钠
2.我国著名的化工专家侯德榜发明的联合制碱法,极大地提升了中国制碱工业的效率和水平,其中一步重要
的反应: .下列相应表达正确的是( )
A. 的结构示意图:
B.元素的电负性:
C. 的空间填充模型:
D. 电离方程式:
3.化学创造美好生活.下列选项中生产活动和化学原理关联错误的是( )
选项 生产活动 化学原理
A 冬季来临时,用石灰浆涂抹树皮 石灰浆吸收空气中的 可减少植物的光合作用
B 用明矾净水 明矾溶于水产生的氢氧化铝胶体具有吸附性
C 葡萄酒中添加少量 杀菌且可防止营养物质被氧化
D 用食醋清洗水垢(主要成分为 ) 水垢中的碳酸钙能被醋酸溶解
学科网(北京)股份有限公司4.硝酸银光度法测定环境样品中微量砷的原理为
.下列说法正确的是( )
A.物质的沸点: B.热稳定性:
C. 和 中As、N杂化方式相同 D. 的空间构型为平面三角形
5.元素周期表中ⅡA族元素及其化合物应用广泛.铍常用于宇航工程材料,其化合物性质与铝的化合物性质十
分相似;工业上电解氯化镁可以得到氯气; 可用于制杀虫剂、发光漆等, 与盐酸反应可以释放出
;硫酸钡在医学上可用于胃肠道造影剂.下列反应的离子方程式书写正确的是( )
A. 与 溶液反应:
B.用Pt电极电解 溶液:
C. 与浓硝酸反应:
D. 溶液溶液与少量 反应:
6.制取物质、探究物质的性质是学习化学必备的素养之一.实验室从含碘废液(除水外含 、 、 等)
中回收碘,其实验流程如下.
下列说法正确的是( )
A.操作Ⅰ为蒸馏 B. 溶液的作用是还原剂
C.物质X为硫酸钠 D.上述流程中可能用到的仪器有分液漏斗、坩埚
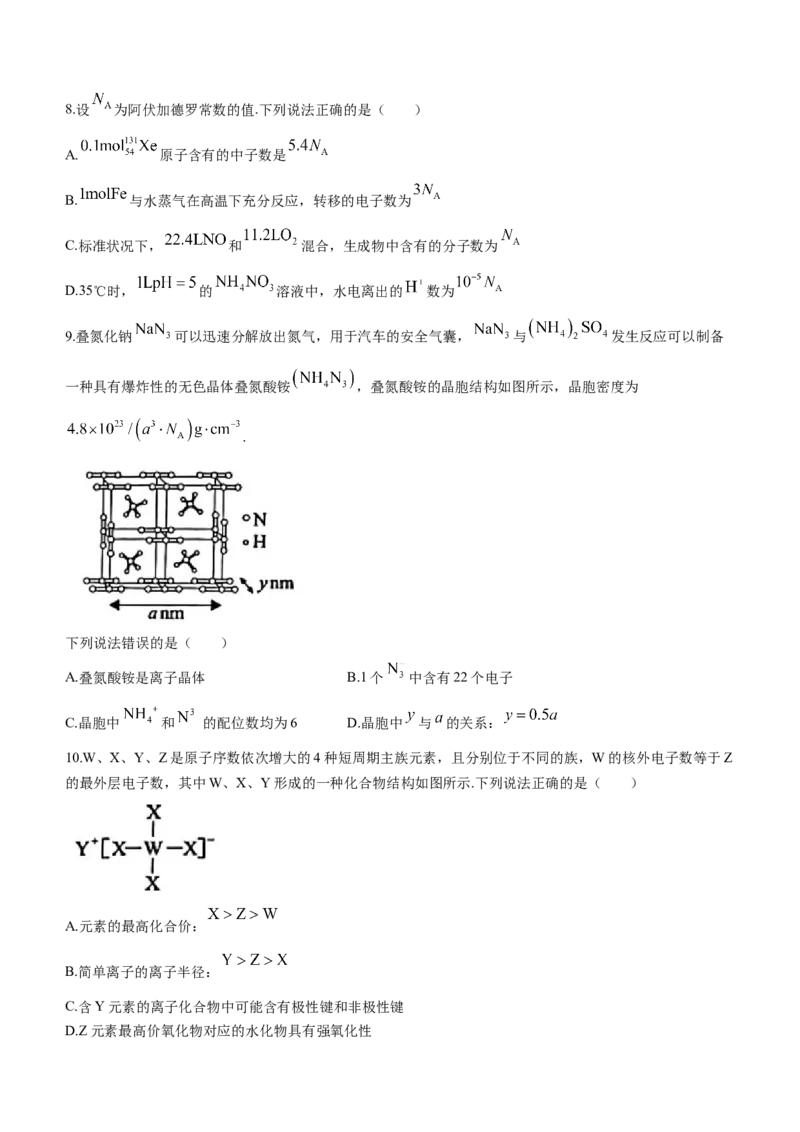
7.锌在人体生长发育、免疫、保持味觉平衡等方面起着极其重要的作用.Zn的某种化合物M是很好的补锌剂,
其结构如图所示.下列说法错误的是( )
A.M可以与水形成氢键,易溶于水 B.氧原子的配位能力比氮原子强
C.1 mol化合物M中含有 键20 mol D.Zn的基态原子的核外电子填充了7种原子轨道
学科网(北京)股份有限公司8.设 为阿伏加德罗常数的值.下列说法正确的是( )
A. 原子含有的中子数是
B. 与水蒸气在高温下充分反应,转移的电子数为
C.标准状况下, 和 混合,生成物中含有的分子数为
D.35℃时, 的 溶液中,水电离出的 数为
9.叠氮化钠 可以迅速分解放出氮气,用于汽车的安全气囊, 与 发生反应可以制备
一种具有爆炸性的无色晶体叠氮酸铵 ,叠氮酸铵的晶胞结构如图所示,晶胞密度为
.
下列说法错误的是( )
A.叠氮酸铵是离子晶体 B.1个 中含有22个电子
C.晶胞中 和 的配位数均为6 D.晶胞中 与 的关系:
10.W、X、Y、Z是原子序数依次增大的4种短周期主族元素,且分别位于不同的族,W的核外电子数等于Z
的最外层电子数,其中W、X、Y形成的一种化合物结构如图所示.下列说法正确的是( )
A.元素的最高化合价:
B.简单离子的离子半径:
C.含Y元素的离子化合物中可能含有极性键和非极性键
D.Z元素最高价氧化物对应的水化物具有强氧化性
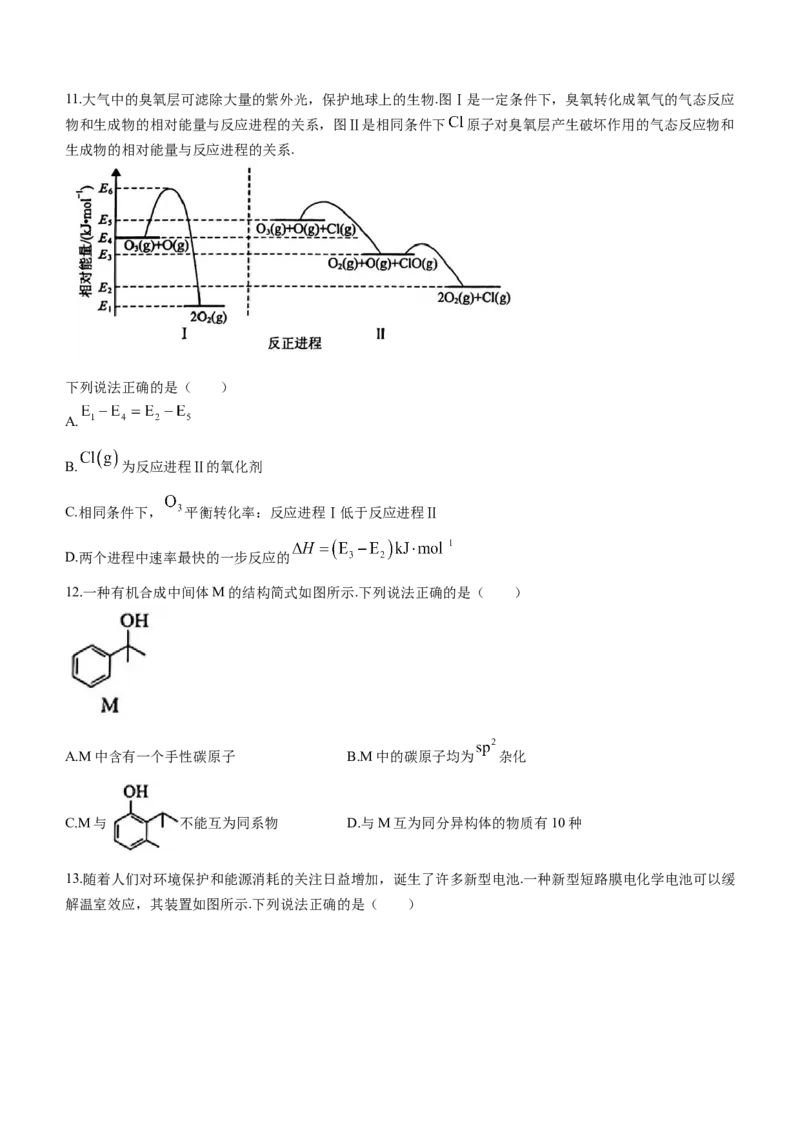
学科网(北京)股份有限公司11.大气中的臭氧层可滤除大量的紫外光,保护地球上的生物.图Ⅰ是一定条件下,臭氧转化成氧气的气态反应
物和生成物的相对能量与反应进程的关系,图Ⅱ是相同条件下 原子对臭氧层产生破坏作用的气态反应物和
生成物的相对能量与反应进程的关系.
下列说法正确的是( )
A.
B. 为反应进程Ⅱ的氧化剂
C.相同条件下, 平衡转化率:反应进程Ⅰ低于反应进程Ⅱ
D.两个进程中速率最快的一步反应的
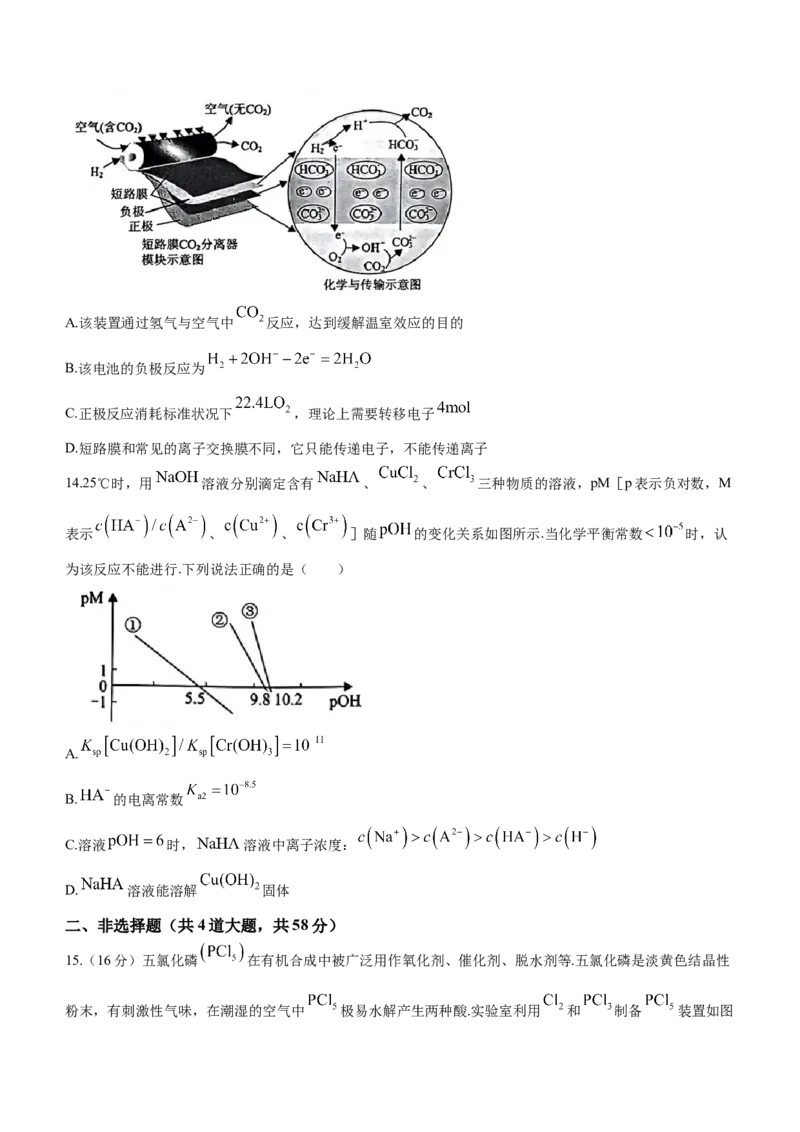
12.一种有机合成中间体M的结构简式如图所示.下列说法正确的是( )
A.M中含有一个手性碳原子 B.M中的碳原子均为 杂化
C.M与 不能互为同系物 D.与M互为同分异构体的物质有10种
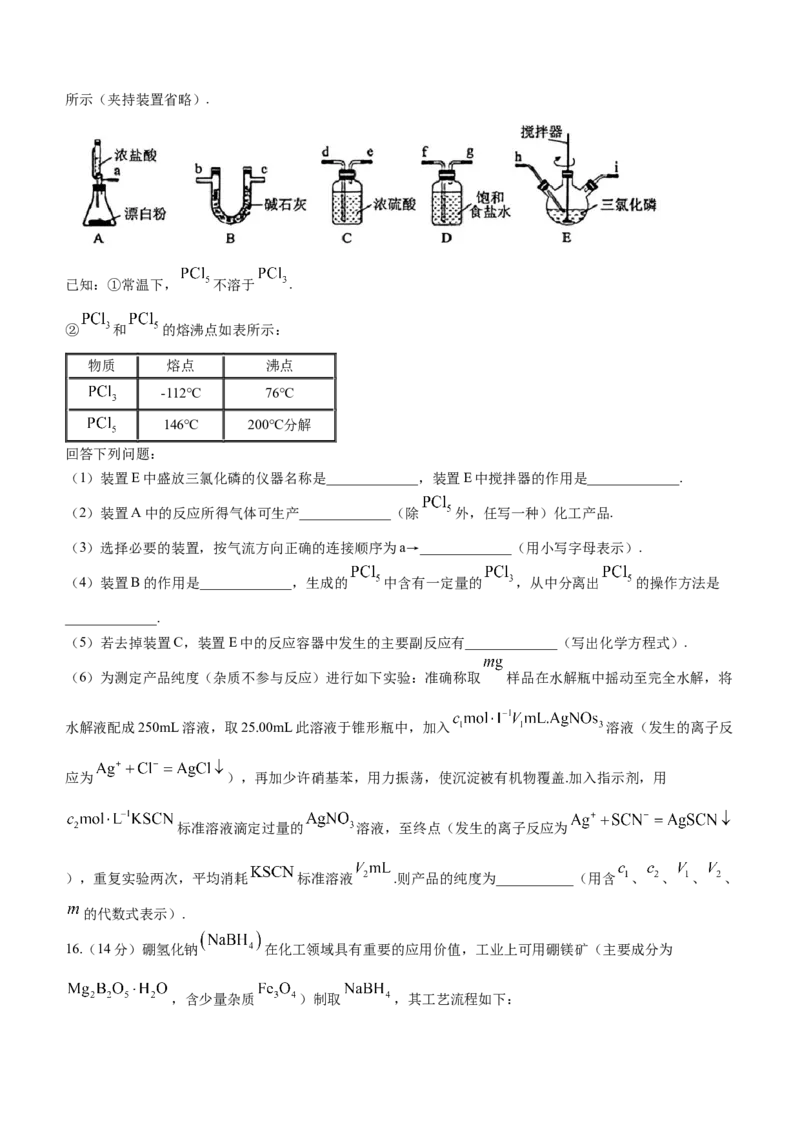
13.随着人们对环境保护和能源消耗的关注日益增加,诞生了许多新型电池.一种新型短路膜电化学电池可以缓
解温室效应,其装置如图所示.下列说法正确的是( )
学科网(北京)股份有限公司A.该装置通过氢气与空气中 反应,达到缓解温室效应的目的
B.该电池的负极反应为
C.正极反应消耗标准状况下 ,理论上需要转移电子
D.短路膜和常见的离子交换膜不同,它只能传递电子,不能传递离子
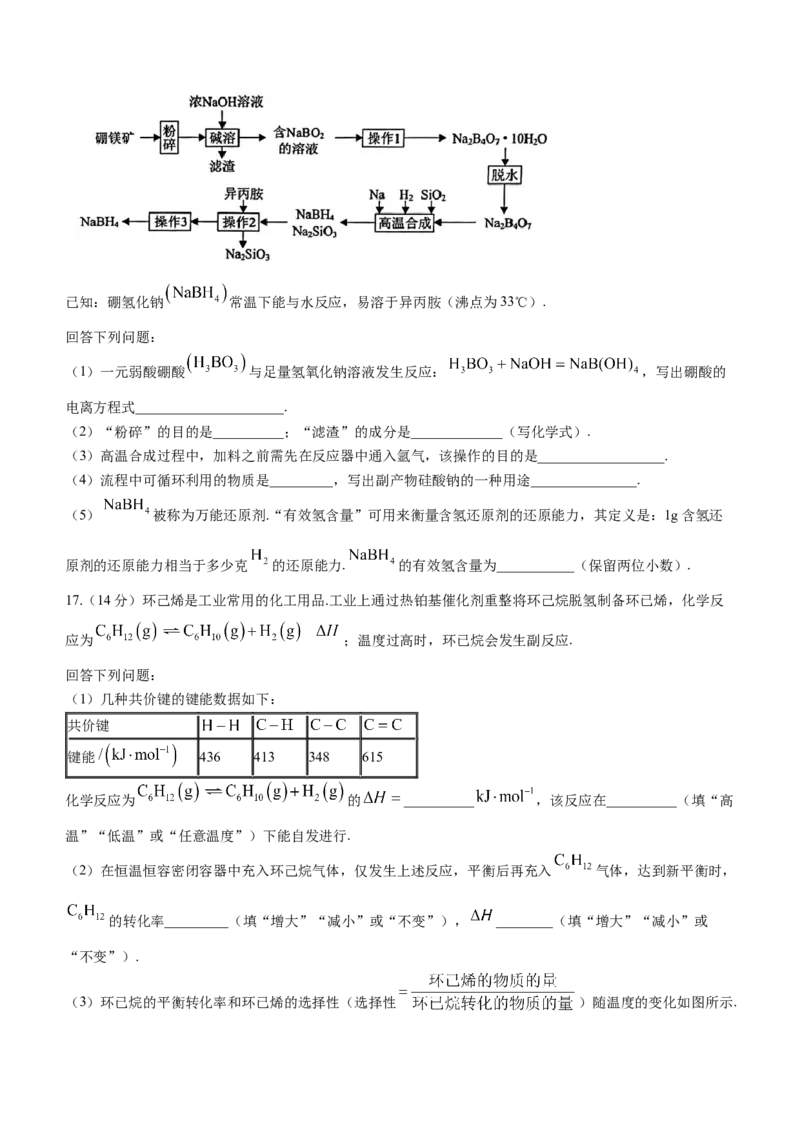
14.25℃时,用 溶液分别滴定含有 、 、 三种物质的溶液,pM[p表示负对数,M
表示 、 、 ]随 的变化关系如图所示.当化学平衡常数 时,认
为该反应不能进行.下列说法正确的是( )
A.
B. 的电离常数
C.溶液 时, 溶液中离子浓度:
D. 溶液能溶解 固体
二、非选择题(共4道大题,共58分)
15.(16分)五氯化磷 在有机合成中被广泛用作氧化剂、催化剂、脱水剂等.五氯化磷是淡黄色结晶性
粉末,有刺激性气味,在潮湿的空气中 极易水解产生两种酸.实验室利用 和 制备 装置如图
学科网(北京)股份有限公司所示(夹持装置省略).
已知:①常温下, 不溶于 .
② 和 的熔沸点如表所示:
物质 熔点 沸点
-112℃ 76℃
146℃ 200℃分解
回答下列问题:
(1)装置E中盛放三氯化磷的仪器名称是_____________,装置E中搅拌器的作用是_____________.
(2)装置A中的反应所得气体可生产_____________(除 外,任写一种)化工产品.
(3)选择必要的装置,按气流方向正确的连接顺序为a→_____________(用小写字母表示).
(4)装置B的作用是_____________,生成的 中含有一定量的 ,从中分离出 的操作方法是
_____________.
(5)若去掉装置C,装置E中的反应容器中发生的主要副反应有_____________(写出化学方程式).
(6)为测定产品纯度(杂质不参与反应)进行如下实验:准确称取 样品在水解瓶中摇动至完全水解,将
水解液配成250mL溶液,取25.00mL此溶液于锥形瓶中,加入 溶液(发生的离子反
应为 ),再加少许硝基苯,用力振荡,使沉淀被有机物覆盖.加入指示剂,用
标准溶液滴定过量的 溶液,至终点(发生的离子反应为
),重复实验两次,平均消耗 标准溶液 .则产品的纯度为___________(用含 、 、 、 、
的代数式表示).
16.(14分)硼氢化钠 在化工领域具有重要的应用价值,工业上可用硼镁矿(主要成分为
,含少量杂质 )制取 ,其工艺流程如下:
学科网(北京)股份有限公司已知:硼氢化钠 常温下能与水反应,易溶于异丙胺(沸点为33℃).
回答下列问题:
(1)一元弱酸硼酸 与足量氢氧化钠溶液发生反应: ,写出硼酸的
电离方程式_____________________.
(2)“粉碎”的目的是__________;“滤渣”的成分是_____________(写化学式).
(3)高温合成过程中,加料之前需先在反应器中通入氩气,该操作的目的是__________________.
(4)流程中可循环利用的物质是_________,写出副产物硅酸钠的一种用途_______________.
(5) 被称为万能还原剂.“有效氢含量”可用来衡量含氢还原剂的还原能力,其定义是:1g含氢还
原剂的还原能力相当于多少克 的还原能力. 的有效氢含量为___________(保留两位小数).
17.(14分)环己烯是工业常用的化工用品.工业上通过热铂基催化剂重整将环己烷脱氢制备环已烯,化学反
应为 ;温度过高时,环已烷会发生副反应.
回答下列问题:
(1)几种共价键的键能数据如下:
共价键
键能 436 413 348 615
化学反应为 的 __________ ,该反应在__________(填“高
温”“低温”或“任意温度”)下能自发进行.
(2)在恒温恒容密闭容器中充入环己烷气体,仅发生上述反应,平衡后再充入 气体,达到新平衡时,
的转化率_________(填“增大”“减小”或“不变”), ________(填“增大”“减小”或
“不变”).
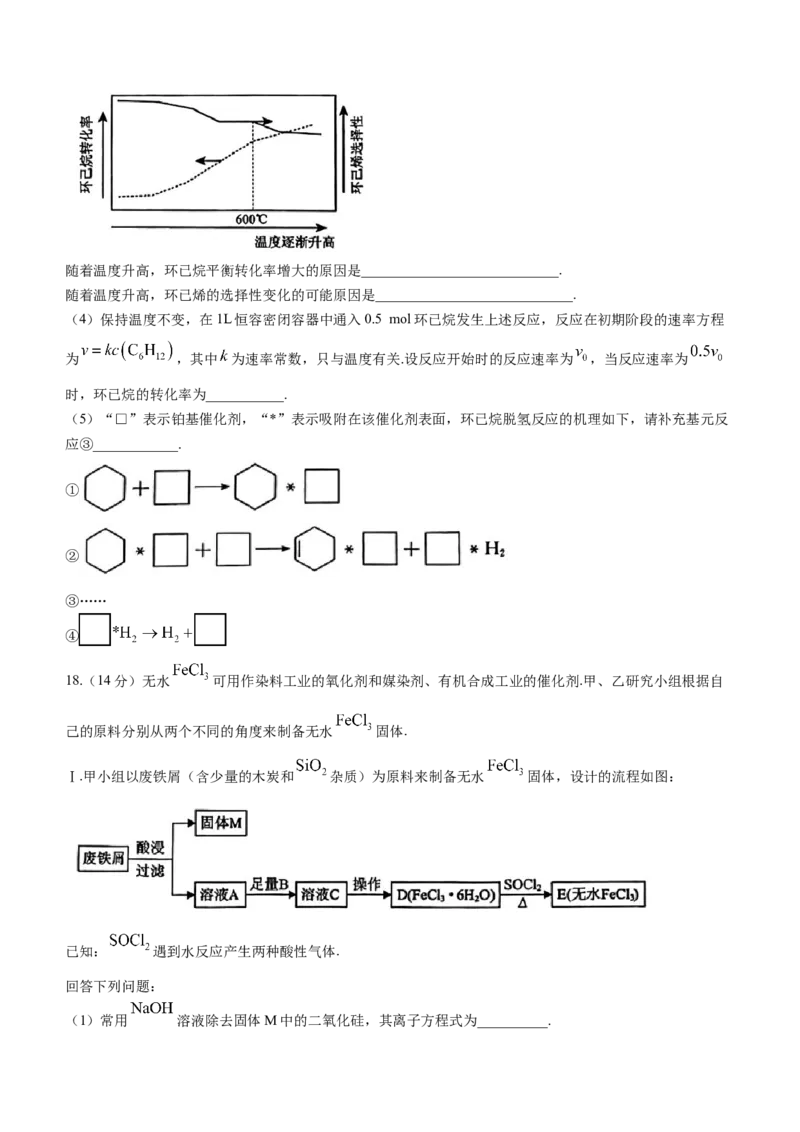
(3)环已烷的平衡转化率和环已烯的选择性(选择性 )随温度的变化如图所示.
学科网(北京)股份有限公司随着温度升高,环已烷平衡转化率增大的原因是____________________________.
随着温度升高,环已烯的选择性变化的可能原因是____________________________.
(4)保持温度不变,在1L恒容密闭容器中通入0.5 mol环已烷发生上述反应,反应在初期阶段的速率方程
为 ,其中 为速率常数,只与温度有关.设反应开始时的反应速率为 ,当反应速率为
时,环已烷的转化率为___________.
(5)“□”表示铂基催化剂,“*”表示吸附在该催化剂表面,环已烷脱氢反应的机理如下,请补充基元反
应③____________.
①
②
③……
④
18.(14分)无水 可用作染料工业的氧化剂和媒染剂、有机合成工业的催化剂.甲、乙研究小组根据自
己的原料分别从两个不同的角度来制备无水 固体.
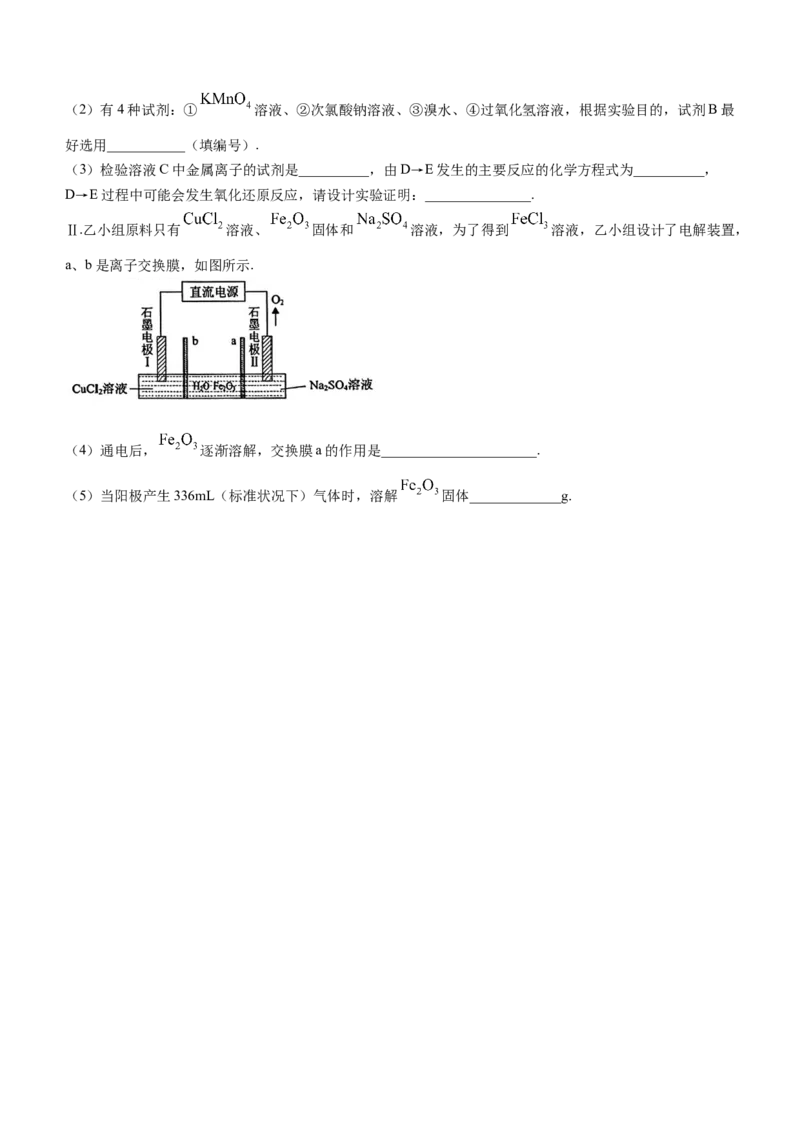
Ⅰ.甲小组以废铁屑(含少量的木炭和 杂质)为原料来制备无水 固体,设计的流程如图:
已知: 遇到水反应产生两种酸性气体.
回答下列问题:
(1)常用 溶液除去固体M中的二氧化硅,其离子方程式为__________.
学科网(北京)股份有限公司(2)有4种试剂:① 溶液、②次氯酸钠溶液、③溴水、④过氧化氢溶液,根据实验目的,试剂B最
好选用___________(填编号).
(3)检验溶液C中金属离子的试剂是__________,由D→E发生的主要反应的化学方程式为__________,
D→E过程中可能会发生氧化还原反应,请设计实验证明:_______________.
Ⅱ.乙小组原料只有 溶液、 固体和 溶液,为了得到 溶液,乙小组设计了电解装置,
a、b是离子交换膜,如图所示.
(4)通电后, 逐渐溶解,交换膜a的作用是______________________.
(5)当阳极产生336mL(标准状况下)气体时,溶解 固体_____________g.
学科网(北京)股份有限公司参考答案
一、选择题
1 2 3 4 5 6 7 8 9 10 11 12 13 14
B A A D A B B D C C A C C B
二、非选择题
15.(16分,每空2分)
(1)三颈烧瓶; 使反应物充分混合,增大反应物的接触面积
(2)漂白粉、次氯酸钠、盐酸等
(3)
(4)吸收氯气,防止污染环境,同时防止空气中的水蒸气进入装置E;过滤(控制温度蒸馏)
(5)
(6)
16.(14分,每空2分)
(1)
(2)增大硼镁矿与碱液的接触面积,提高浸取率(或提高原料的利用率)和加快反应速率(或者使反应更快
更充分) 和
(3)除去反应器中的空气,防止空气中氧气与钠、氢气反应,水与钠反应
(4)异丙胺 可做防火剂或黏合剂
(5)0.21
17.(14分,每空2分)
(1)+123;高温
(2)减小;不变
(3)正反应是吸热反应,升高温度,平衡正向移动;环已烷裂解发生副反应、环已烯易发生聚合反应
(4)50%
(5)
18.(14分,每空2分)
Ⅰ.(1)
(2)④
(3) 溶液( 、亚铁氰化钾等); ;
学科网(北京)股份有限公司取少量 于试管中,加入过量 ,振荡,向试管中加水溶解,滴加氯化钡溶液,若生成白色
沉淀,则证明脱水过程发生了氧化还原反应(取少量 于试管中,加入过量 ,振荡,向试
管中加水溶解,滴加铁氰化钾溶液,若生成蓝色沉淀,则证明脱水过程发生了氧化还原反应).
Ⅱ.(4)质子通过(质子交换膜) (5)1.6
学科网(北京)股份有限公司