文档内容
瓜州县第一中学 2023 一 2024 学年度第一学期期末考试试卷
高三化学
2024.1
注意事项:
1.本试卷分选择题和非选择题两部分。满分100分,考试时间75分钟。
2.考生作答时,请将答案答在答题卡上。选择题每小题选出答案后,用2B铅笔把答题卡上对应
题目的答案标号涂黑;非选择题请用直径0.5毫米黑色墨水签字笔在答题卡上各题的答题区域
内作答,超出答题区域书写的答案无效,在试题卷、草稿纸上作答无效。
3.本试卷命题范围:高考范围。
4.可能用到的相对原子质量:H1 C12 N14 O16 Na23 S32 K39 Ni59 Zn65 La139
一、选择题(本题共14小题,每小题3分,共42分。每小题只有一个选项符合题意)
1.中国古文化源远流长,留下不少脍炙人口的古诗词,不少古诗词清晰的描绘了我国古代人民的生活、生产
场景,下面的“诗”情“化”意,分析不正确的是
A. “粉身碎骨浑不怕,要留清白在人间”中涉及化学变化
B. “日照澄州江雾开”,雾是一种气溶胶,受阳光照射时会产生丁达尔现象
C. “美人首饰侯王印,尽是沙中浪底来”,说明金以单质的形式存在于自然界
D. “绿蚁新醅酒”,“新醅酒”即新酿的酒,葡萄糖发生水解反应生成乙醇
2.下列化学用语或图示表达正确的是
A氯离子的结构示意图: B.基态H的电子排布式为1p1
C.CO 的电子式: D.CH 的空间充填(比列)模型:
2 4
3.N 为阿伏伽德罗常数的值,下列说法不正确的是
A
A.1molHCN中含π键的数目为N
A
B.6.5gZn与一定量浓硫酸反应完全溶解,转移的电子数为0.2N
A
C,将1molNH,CI溶于稀氨水中使溶液呈中性,溶液中 数目为N
A
D.23gNa与O 充分反应生成NaO和NaO 的混合物,消耗O 的分子数在0.25N 和0.5N 之间
2 2 2 2 2 A A
4.[Co(NH)]Cl 是一种重要的化工产品。实验室可利用CoCl 制取该配合物:
3 6 3 2
2CoCl +10NH+2NHCl+H O=2[Co(NH)]Cl +2H O。下列叙述正确的是
2 3 4 2 2 3 6 3 2
A. 和NH 的中心原子价层电子对数不同
3
B.基态Co3+核外电子排布式为[Ar]3d7
C.1mol[Co(NH )]3+中含6mol配位键
3 6
D.基态Cl原子核外有15种运动状态不同的电子
学科网(北京)股份有限公司5.下列离子方程式书写正确的是
A.用酸性高锰酸钾标准溶液滴定草酸:2 +16H++5 =2Mn2++10CO ↑+8H O
2 2
B.向C HONa溶液中通入少量CO:C HO-+CO +H O=C HOH+
6 5 2 6 5 2 2 6 5
C.向碳酸氢铵溶液中加入足量石灰水:Ca2++ +OH-=CaCO ↓+H O
3 2
D.向FeI 溶液中通入足量Cl:2Fe2++2I-+2Cl=2Fe3++I +4Cl-
2 2 2 2
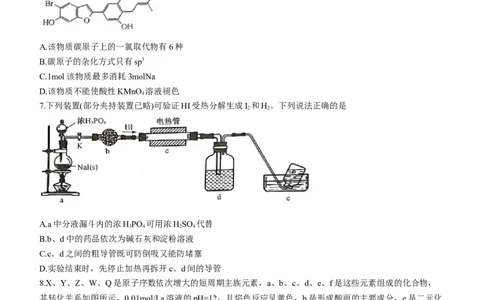
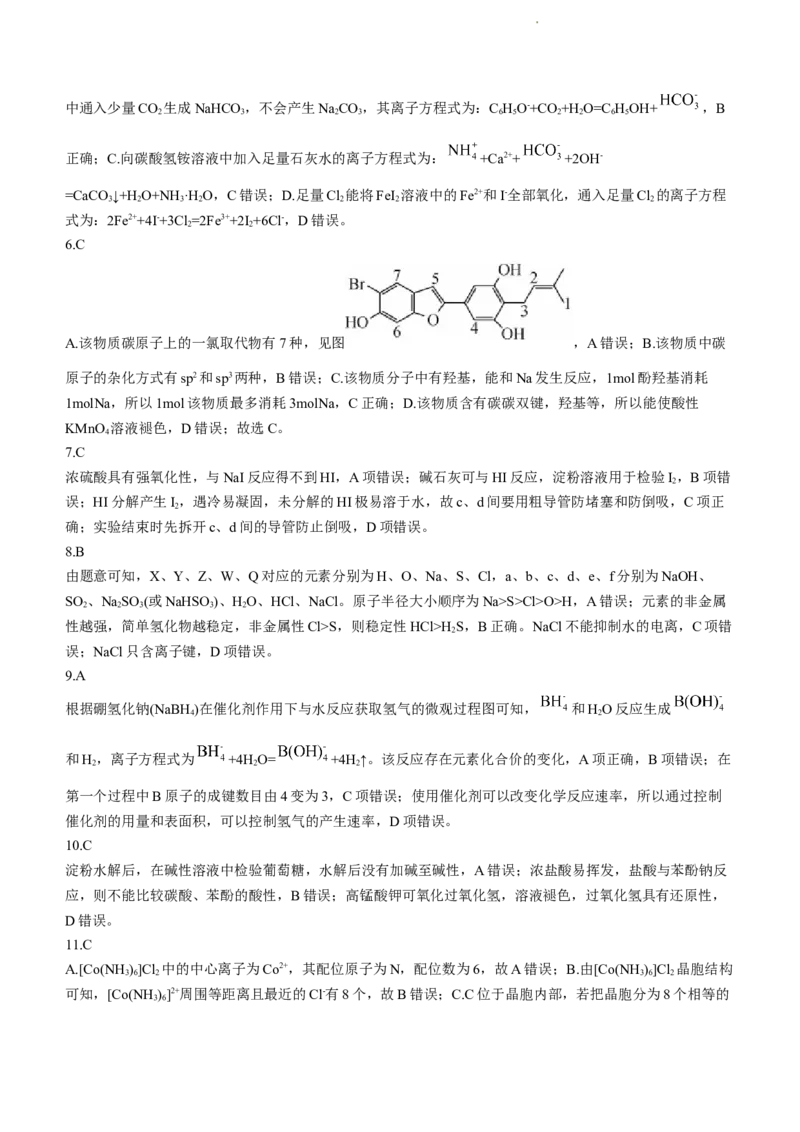
6.中药桑白皮中的一种活性物质的结构如图所示。下列说法正确的是
A.该物质碳原子上的一氯取代物有6种
B.碳原子的杂化方式只有sp3
C.1mol该物质最多消耗3molNa
D.该物质不能使酸性KMnO 溶液褪色
4
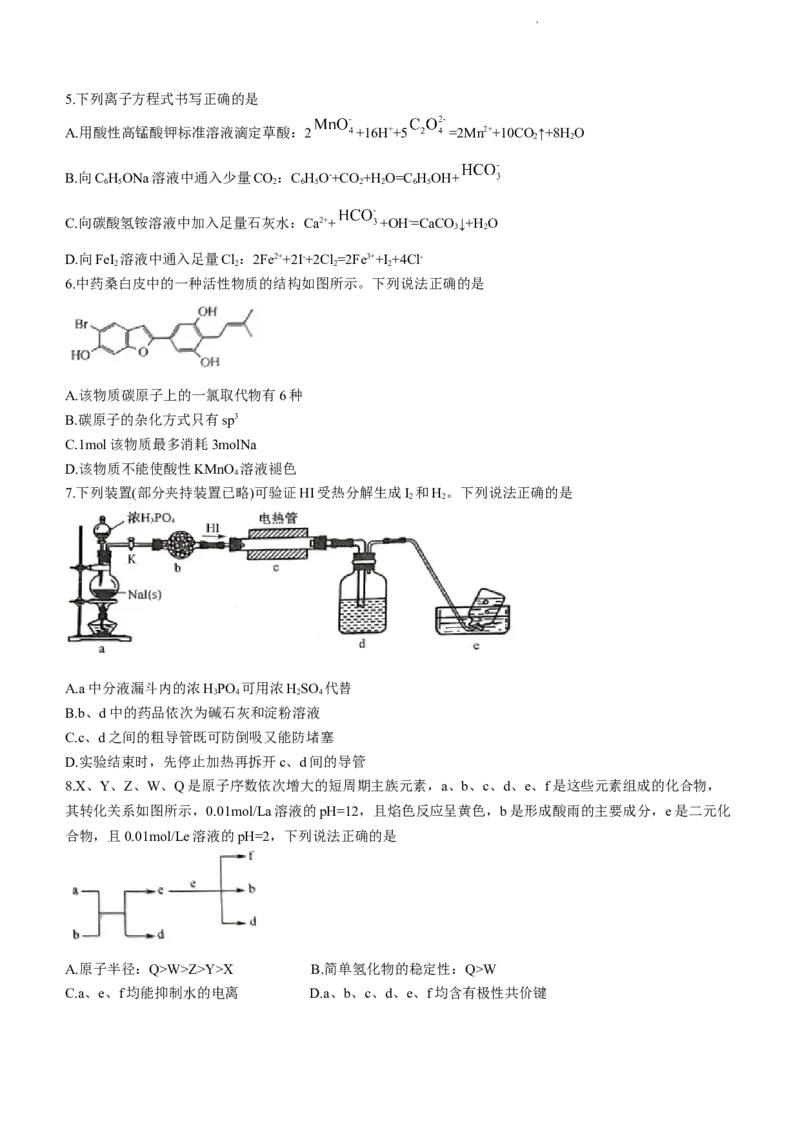
7.下列装置(部分夹持装置已略)可验证HI受热分解生成I 和H。下列说法正确的是
2 2
A.a中分液漏斗内的浓HPO 可用浓HSO 代替
3 4 2 4
B.b、d中的药品依次为碱石灰和淀粉溶液
C.c、d之间的粗导管既可防倒吸又能防堵塞
D.实验结束时,先停止加热再拆开c、d间的导管
8.X、Y、Z、W、Q是原子序数依次增大的短周期主族元素,a、b、c、d、e、f是这些元素组成的化合物,
其转化关系如图所示,0.01mol/La溶液的pH=12,且焰色反应呈黄色,b是形成酸雨的主要成分,e是二元化
合物,且0.01mol/Le溶液的pH=2,下列说法正确的是
A.原子半径:Q>W>Z>Y>X B.简单氢化物的稳定性:Q>W
C.a、e、f均能抑制水的电离 D.a、b、c、d、e、f均含有极性共价键
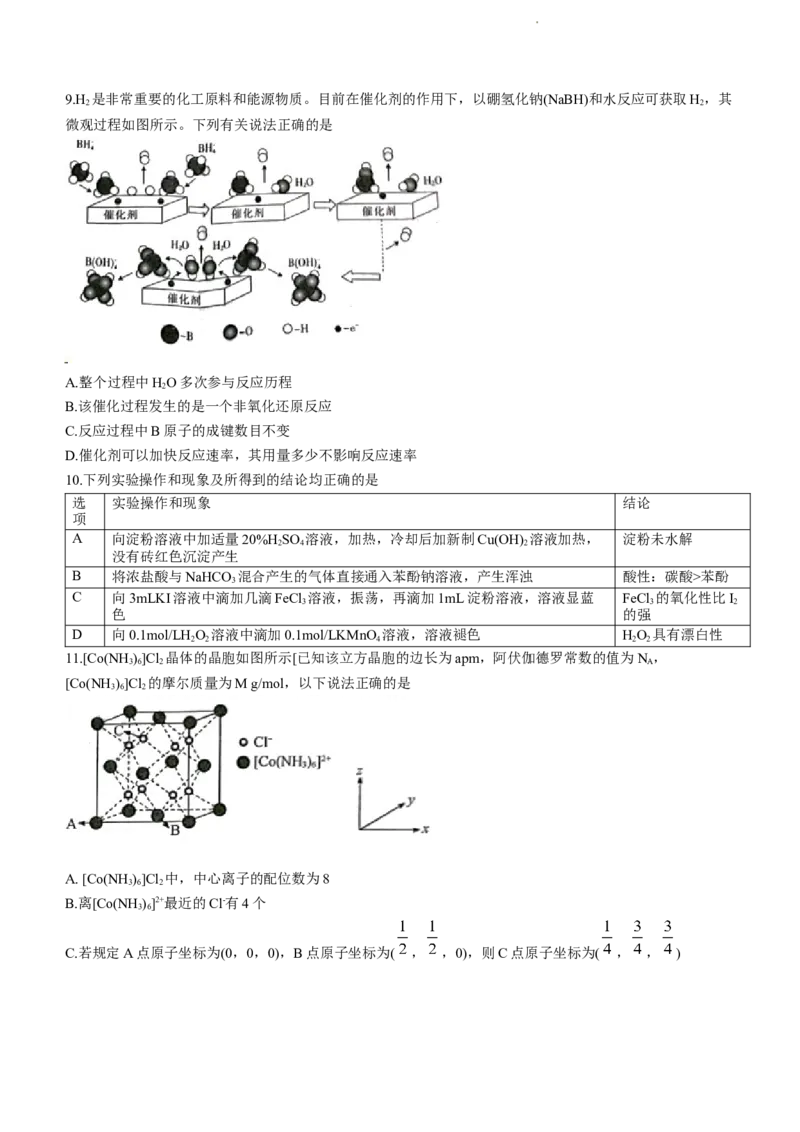
学科网(北京)股份有限公司9.H 是非常重要的化工原料和能源物质。目前在催化剂的作用下,以硼氢化钠(NaBH)和水反应可获取H,其
2 2
微观过程如图所示。下列有关说法正确的是
A.整个过程中HO多次参与反应历程
2
B.该催化过程发生的是一个非氧化还原反应
C.反应过程中B原子的成键数目不变
D.催化剂可以加快反应速率,其用量多少不影响反应速率
10.下列实验操作和现象及所得到的结论均正确的是
选 实验操作和现象 结论
项
A 向淀粉溶液中加适量20%H SO 溶液,加热,冷却后加新制Cu(OH) 溶液加热, 淀粉未水解
2 4 2
没有砖红色沉淀产生
B 将浓盐酸与NaHCO 混合产生的气体直接通入苯酚钠溶液,产生浑浊 酸性:碳酸>苯酚
3
C 向3mLKI溶液中滴加几滴FeCl 溶液,振荡,再滴加1mL淀粉溶液,溶液显蓝 FeCl 的氧化性比I
3 3 2
色 的强
D 向0.1mol/LH O 溶液中滴加0.1mol/LKMnO 溶液,溶液褪色 HO 具有漂白性
2 2 4 2 2
11.[Co(NH)]Cl 晶体的晶胞如图所示[已知该立方晶胞的边长为apm,阿伏伽德罗常数的值为N ,
3 6 2 A
[Co(NH )]Cl 的摩尔质量为M g/mol,以下说法正确的是
3 6 2
A. [Co(NH )]Cl 中,中心离子的配位数为8
3 6 2
B.离[Co(NH )]2+最近的Cl-有4个
3 6
C.若规定A点原子坐标为(0,0,0),B点原子坐标为( , ,0),则C点原子坐标为( , , )
学科网(北京)股份有限公司D. [Co(NH )]Cl 晶体的密度为 ×1021g/cm3
3 6 2
12.铍是非常重要的军工金属,也是非常重要的战略资源。某工厂以含氟铍矿(主要成分是BeO、Fe O、SiO
2 3 2
等)为原料,生产金属铍的工艺流程如下:
已知:BeO是两性氧化物,Be(OH) 是两性氢氧化物。下列说法错误的是
2
A.实验室进行操作a用到三种玻璃仪器
B.碱溶时,BeO发生的离子反应为BeO+2OH-= +H O
2
C.“沉渣”和“浸渣”的成分分别为Fe(OH) 、HSiO
3 2 3
D.从该流程可知,BeO属于电解质
13.当前,随着CO 的排放,如何解决CO 的污染成为世界各国研究的课题,我国科学家提出电化学原理将其
2 2
转化为多种燃料,装置如图,下列说法正确的是
A.电极A与外接电源的正极相连
B.生成CH 的电极反应式:CO+8H++8e-=CH +2H O
4 2 4 2
C.若右侧KOH减少5.6g,电路中通过电子为0.2N
A
D.电极电势:A>B
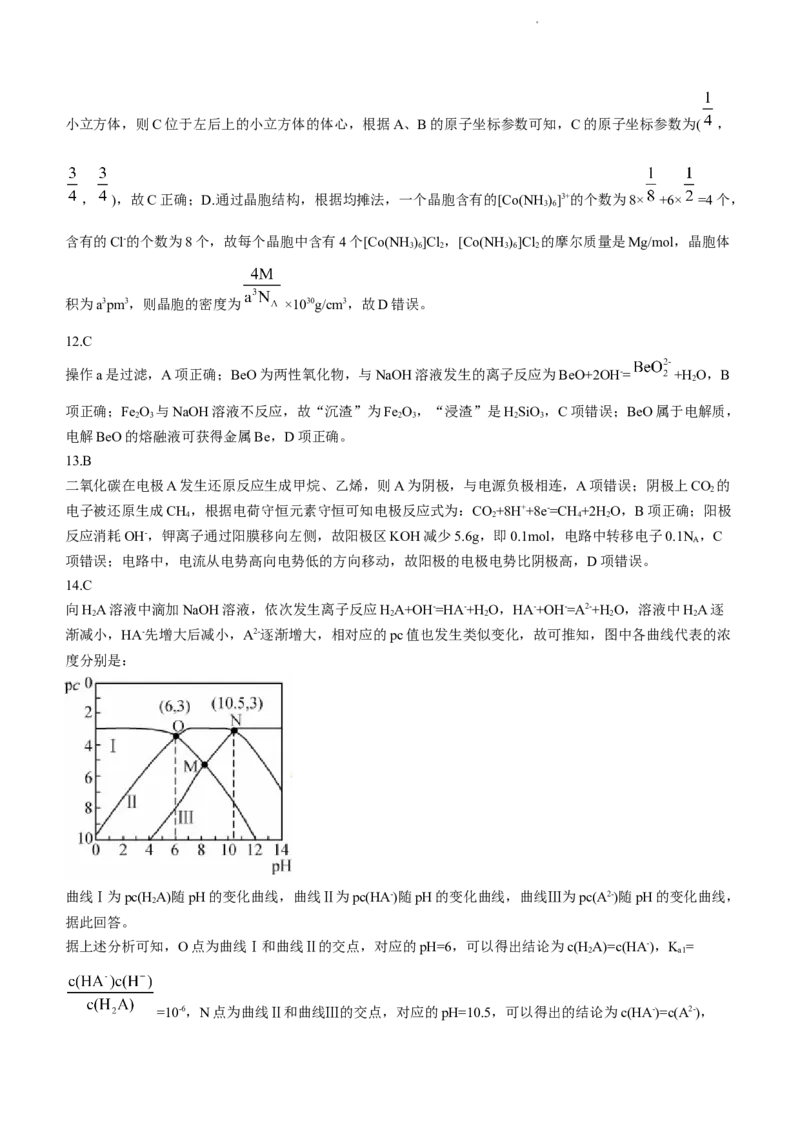
14.已知pc(B)=-lgc(B),室温下将NaOH溶液滴加到一定浓度的某二元弱酸(H A)中,部分微粒的pc值随溶液
2
pH值变化如图所示,下列说法错误的是
A.K (H A)的数量级为10-11
a2 2
学科网(北京)股份有限公司B.M点,pH=
C.NaHA溶液,c(H+)>c(OH-)
D.N点,c(Na+)+c(H+)=c(OH-)+2c(HA-)+c(A2-)
二、非选择题(本题共4小题,共58分
15.(14分)过二硫酸铵[(NH )SO]常作为氧化剂和漂白剂,被泛应用于蓄电池工业。实验室模拟制备
4 2 2 8
(NH )SO 的装置如图所示,回答下列问题:
4 2 2 8
(1)装置A中发生反应的化学方程式为______________。
(2)装置B中发生反应的化学方程式为______________。
(3)充分反应后,将装置B中混合液经--系列操作得到晶体,然后用无水乙醇洗涤,用无水乙醇洗涤的目的是
______________。
(4)烘干产品时,用红外灯低温烘干,可能的原因是_______________。
(5)过二硫酸铵可用于检验废水中的Cr3+是否超标,溶液会变成橙色(Cr3+被氧化成 ),反应的离子方程
式为_________________。
(6)为了检测(NH )SO 的纯度,取2.5g的(NH )SO 晶体配成100mL溶液。移取20.00mL(NH )SO 溶液于锥
4 2 2 8 4 2 2 8 4 2 2 8
形瓶中,加入过量的KI溶液,然后加入几滴淀粉溶液,再用0.2000mol/LNa SO 标准溶液滴定,发生反应:
2 2 3
I+2 =2I-+ 。重复上述操作三次,平均消耗NaSO 标准溶液18.00mL,滴定终点时溶液颜色的变
2 2 2 3
化为__________,制得(NH )SO 晶体的纯度为_______%。(保留小数点后两位)
4 2 2 8
16.(14分)次磷酸钠(NaH PO )是具有珍珠光泽的晶体或白色结晶性粉末,易溶于水、乙醇、甘油,微溶于氨水,
2 2
不溶于乙醚。次磷酸钠(NaH PO )广泛应用于化学镀镍,其制备与镀镍过程如图所示:
2 2
据此回答下列问题:
学科网(北京)股份有限公司(1)基态Ni原子的核外电子排布式为___________,PH 的分子空间构型为_______。
3
(2)“碱溶”过程中,发生反应化学方程式为__________________。
(3)“沉降池”中通入氨气的目的是__________________,“净化”操作需要过滤、洗涤、干燥,洗涤时,选
用的洗涤剂为_________。
(4)“滤液2”经分离提纯可以得HPO ,写出“镀镍”过程发生的离子反应方程式___________________,充
3 4
分反应后,向“滤液2”中,加入适量Ca(OH) 悬浊液,生成CaSO 和CaHPO 混合沉淀,此时
2 4 4
=__________[已知:K =(CaSO )=7×10-5(mol/L)2;K (CaHPO )=1×10-7(mol/L)2
sp 4 sp 4
(5)Ni和La的合金是目前使用广泛的储氢材料,该合金的晶胞结构如图所示。
①该晶体的化学式为____________。
②已知该晶体晶胞底面边长为apm,高为cpm,设N 为阿伏伽德罗常数的值,则该晶体的密度为______g/
A
cm3(用含a、c、N 的代数式表示)。
A
17.(15分)功能高分子材料H在生活中有广泛用途,阿司匹林是生活中常用的药物。以芳香内酯R为原料制备
H和阿司匹林的流程如下:
已知:CHCH=CHCH CH CHCOOH+CH CHCOOH
3 2 3 3 3 2
请回答下列问题:
(1)D分子中采取sp2杂化的碳原子数目为__________。
(2)F的名称是__________;A中的含氧官能团的名称是__________。
(3)R→A转化中i)的反应类型是__________;B的结构简式为__________。
(4)由C合成H的化学方程式为_____________________。
(5)D有多种同分异构体,同时具备下列条件的结构简式为__________。
①遇氯化铁溶液发生显色反应;
学科网(北京)股份有限公司②在酸性条件下水解产物之一能发生银镜反应;
③苯环上一溴代物只有2种。
(6)参照上述流程和相关信息,写出以环丙烷( )和乙醇为原料制备丙二酸二乙酯( )的
合成路线(无机试剂任选)_______________________。
18.(15分)甲烷催化裂解、氧气部分氧化和水煤气重整是目前制氢的常用方法。回答下列问题:
(1)甲烷隔绝空气分解,部分反应如下:
Ⅰ.CH (g)=C(s)+2H (g) H=+74.9kJ/mol
4 2 1
Ⅱ.6CH(g)=C H(g)+9H(g) H=+531 kJ/mol
4 6 6 2 △ 2
Ⅲ.2CH(g)=-C H(g)+2H(g) H=+202 kJ/mol
4 2 4 2 △ 3
①反应Ⅰ的△S_______(填“>”或“<”)0。
△
②C H(g)+3H(g)=3C H(g)的△H=________kJ/mol。
6 6 2 2 4
(2)CH 用水蒸气重整制氢包含的反应为:
4
Ⅰ.水蒸气重整:CH(g)+HO(g) CO(g)+3H(g) H=+206kJ/mol
4 2 2
△
Ⅱ.水煤气变换:CO(g)+HO(g) CO(g)+H(g) H=-41.2kJ/mol
2 2 2
△
平衡时各物质的物质的量分数如图1所示。
①为提高CH 的平衡转化率,除压强、温度外,还可采取的措施是___________(写一条)。
4
②温度高于T℃时,CO 的物质的量分数开始减小,其原因是________________。
1 2
③T℃时,容器中 =____________。
2
学科网(北京)股份有限公司(3)甲烷部分氧化反应为CH4(g)+ O2(g)=CO(g)+2H2(g) H=-36kJ/mol。已知甲烷部分氧化、甲烷水蒸气重
△
整、水煤气变换反应的平衡常数的自然对数lnKp与温度的关系如图2所示。
①图中Q点时,反应CO(g)+CH (g)=2CO(g)+2H(g)的lnK=_____________。
2 4 2
②在某恒压密闭容器中充入1molCH 和1molH O(g)在某温度下发生水蒸气重整反应达到平衡时,CH 的转化
4 2 4
率为50%,容器总压强为1atm。H 的平衡分压p(H )=_________atm;此温度下反应的lnKp=_________。(已
2 2
知:ln3≈1.1,ln4≈1.4)
瓜州县第一中学 2023--2024 学年度第一学期期末考试试卷
高三化学参考答案、提示及评分细则
1.D
酿酒过程中,葡萄糖发生氧化还原反应生成乙醇,答案选D。
2.D
A.氯离子的结构示意图为 ,A错误;B.基态H的电子排布式为1s1,B错误;C.CO2的电子式
为: ,C错误;D.氢原子半径小于碳原子半径,D正确。
3.A
A.HCN的结构为H-C≡N,故1molHCN中有2N 个π键,A项错误;B.0.1mol锌完全反应生成0.1mol锌离子,
A
转移了0.2mol电子,转移电子数一定为0.2N ,B项正确;C.将1molNH Cl溶于稀氨水中使溶液呈中性,则
A 4
n(H+)=n(OH-),根据电荷守恒,n( )=n(Cl-),溶液中Cl-数目为N ,则 数目也为N ,C项正确;D.根
A A
据方程式:4Na+O=2Na O,23gNa与O 充分反应生成NaO,消耗O 的分子数0.25mol,同理,
2 2 2 2 2
2Na+O=Na O,23gNa与O 反应生成NaO,消耗O 的分子数0.5mol,生成NaO和NaO 的混合物,消耗
2 2 2 2 2 2 2 2 2 2
O 的分子数在0.25N 和0.5N 之间,故D正确。
2 A A
4.C
A. 和NH 中心原子的价层电子对数均为4,A错误;B.基态Co3+核外电子排布式为[Ar]3d6,B错误;C.
3
每个NH 配体与中心Co3+间形成一根配位键,故1mol该配离子中含6mol配位键,C正确;D.基态Cl原子核
3
外有17种运动状态不同的电子,D错误;故选C。
5.B
A.HC O 为弱电解质,不能拆成离子形式,用酸性高锰酸钾标准溶液滴定草酸的离子方程式为:2
2 2 4
+16H++5 H C O=2Mn2++10CO ↑+8H O,A错误;B.酸性强弱顺序为:碳酸>苯酚> ,向C HONa溶液
2 2 4 2 2 6 5
学科网(北京)股份有限公司中通入少量CO 生成NaHCO ,不会产生NaCO,其离子方程式为:C HO-+CO +H O=C HOH+ ,B
2 3 2 3 6 5 2 2 6 5
正确;C.向碳酸氢铵溶液中加入足量石灰水的离子方程式为: +Ca2++ +2OH-
=CaCO ↓+H O+NH ·H O,C错误;D.足量Cl 能将FeI 溶液中的Fe2+和I-全部氧化,通入足量Cl 的离子方程
3 2 3 2 2 2 2
式为:2Fe2++4I-+3Cl=2Fe3++2I +6Cl-,D错误。
2 2
6.C
A.该物质碳原子上的一氯取代物有7种,见图 ,A错误;B.该物质中碳
原子的杂化方式有sp2和sp3两种,B错误;C.该物质分子中有羟基,能和Na发生反应,1mol酚羟基消耗
1molNa,所以1mol该物质最多消耗3molNa,C正确;D.该物质含有碳碳双键,羟基等,所以能使酸性
KMnO 溶液褪色,D错误;故选C。
4
7.C
浓硫酸具有强氧化性,与NaI反应得不到HI,A项错误;碱石灰可与HI反应,淀粉溶液用于检验I,B项错
2
误;HI分解产生I,遇冷易凝固,未分解的HI极易溶于水,故c、d间要用粗导管防堵塞和防倒吸,C项正
2
确;实验结束时先拆开c、d间的导管防止倒吸,D项错误。
8.B
由题意可知,X、Y、Z、W、Q对应的元素分别为H、O、Na、S、Cl,a、b、c、d、e、f分别为NaOH、
SO 、NaSO (或NaHSO)、HO、HCl、NaCl。原子半径大小顺序为Na>S>Cl>O>H,A错误;元素的非金属
2 2 3 3 2
性越强,简单氢化物越稳定,非金属性Cl>S,则稳定性HCl>H S,B正确。NaCl不能抑制水的电离,C项错
2
误;NaCl只含离子键,D项错误。
9.A
根据硼氢化钠(NaBH )在催化剂作用下与水反应获取氢气的微观过程图可知, 和HO反应生成
4 2
和H,离子方程式为 +4H O= +4H ↑。该反应存在元素化合价的变化,A项正确,B项错误;在
2 2 2
第一个过程中B原子的成键数目由4变为3,C项错误;使用催化剂可以改变化学反应速率,所以通过控制
催化剂的用量和表面积,可以控制氢气的产生速率,D项错误。
10.C
淀粉水解后,在碱性溶液中检验葡萄糖,水解后没有加碱至碱性,A错误;浓盐酸易挥发,盐酸与苯酚钠反
应,则不能比较碳酸、苯酚的酸性,B错误;高锰酸钾可氧化过氧化氢,溶液褪色,过氧化氢具有还原性,
D错误。
11.C
A.[Co(NH )]Cl 中的中心离子为Co2+,其配位原子为N,配位数为6,故A错误;B.由[Co(NH )]Cl 晶胞结构
3 6 2 3 6 2
可知,[Co(NH )]2+周围等距离且最近的Cl-有8个,故B错误;C.C位于晶胞内部,若把晶胞分为8个相等的
3 6
学科网(北京)股份有限公司小立方体,则C位于左后上的小立方体的体心,根据A、B的原子坐标参数可知,C的原子坐标参数为( ,
, ),故C正确;D.通过晶胞结构,根据均摊法,一个晶胞含有的[Co(NH )]3+的个数为8× +6× =4个,
3 6
含有的Cl-的个数为8个,故每个晶胞中含有4个[Co(NH )]Cl ,[Co(NH )]Cl 的摩尔质量是Mg/mol,晶胞体
3 6 2 3 6 2
积为a3pm3,则晶胞的密度为 ×1030g/cm3,故D错误。
12.C
操作a是过滤,A项正确;BeO为两性氧化物,与NaOH溶液发生的离子反应为BeO+2OH-= +H O,B
2
项正确;Fe O 与NaOH溶液不反应,故“沉渣”为Fe O,“浸渣”是HSiO,C项错误;BeO属于电解质,
2 3 2 3 2 3
电解BeO的熔融液可获得金属Be,D项正确。
13.B
二氧化碳在电极A发生还原反应生成甲烷、乙烯,则A为阴极,与电源负极相连,A项错误;阴极上CO 的
2
电子被还原生成CH,根据电荷守恒元素守恒可知电极反应式为:CO+8H++8e-=CH +2H O,B项正确;阳极
4 2 4 2
反应消耗OH-,钾离子通过阳膜移向左侧,故阳极区KOH减少5.6g,即0.1mol,电路中转移电子0.1N ,C
A
项错误;电路中,电流从电势高向电势低的方向移动,故阳极的电极电势比阴极高,D项错误。
14.C
向HA溶液中滴加NaOH溶液,依次发生离子反应HA+OH-=HA-+H O,HA-+OH-=A2-+H O,溶液中HA逐
2 2 2 2 2
渐减小,HA-先增大后减小,A2-逐渐增大,相对应的pc值也发生类似变化,故可推知,图中各曲线代表的浓
度分别是:
曲线Ⅰ为pc(HA)随pH的变化曲线,曲线Ⅱ为pc(HA-)随pH的变化曲线,曲线Ⅲ为pc(A2-)随pH的变化曲线,
2
据此回答。
据上述分析可知,O点为曲线Ⅰ和曲线Ⅱ的交点,对应的pH=6,可以得出结论为c(HA)=c(HA-),K =
2 a1
=10-6,N点为曲线Ⅱ和曲线Ⅲ的交点,对应的pH=10.5,可以得出的结论为c(HA-)=c(A2-),
学科网(北京)股份有限公司K = =10-10.5,故K (H A)的数量级为10-11,A正确;M点c(HA)=c(A2-),因此K ·K =
a2 a2 2 2 a1 a2
× =c2(H+),两边同时取负对数变形可得pH= ,B正确;由上述分析
可知K =10-10.5,K = =10-8,K >K ,NaHA的水解程度大于电离程度,因此溶液显碱性,C错误;N点
a2 h2 h2 a2
存在电荷守恒c(Na+)+c(H+)=c(OH-)+c(HA-)+2c(A2-),此时c(HA-)=c(A2-),代入可得c(Na+)+c(H+)=c(OH-)
+2c(HA-)+c(A2-),D正确。
15.(1)NH·H O+CaO=NH↑+Ca(OH) (2分)
3 2 3 2
(2)H O+2H SO +2NH=(NH)SO+2H O(2分)
2 2 2 4 3 4 2 2 8 2
(3)洗除晶体表面的杂质,同时乙醇易挥发,便于晶体干燥(或其他合理答案)(2分)
(4)(NH )SO 产品受热易分解(2分)
4 2 2 8
(5)2Cr3++3 +7H O=6 + +14H+(2分)
2
(6)溶液由蓝色恰好变为无色,且半分钟内不恢复蓝色(2分);82.08(2分)
16.(1)[Ar]3d84s2(或1s22s22p63s23p63d84s2)(1分);三角锥形(1分)
(2)P +3NaOH+3HO=3NaH PO +PH↑(2分)
4 2 2 2 3
(3)降低NaH PO 溶解度,使其析出,与杂质分离(2分);乙醚(1分)
2 2
(4)2Ni2++ +2H O=2Ni+H PO +3H+(2分);700(2分)
2 3 4
(5)①LaNi(1分);② (2分)
5
17.(1)7(2分)
(2)乙酸(1分);(酚)羟基、羧基(2分)
(3)水解反应(或取代反应)(1分); (2分)
(4)nHOOC-COOH+nHOCH CHOH +(2n-1)HO(2分)
2 2 2
(5) (2分)
学科网(北京)股份有限公司(6)
(3分)
18.(1)①>(1分);②+75(2分)
(2)①增加起始时 (或及时从产物中分离出H)(2分)
2
②反应Ⅱ为放热反应,从T℃升高温度,平衡向逆反应方向移动因素大于CO浓度增加向正反应方向移动因
1
素,净结果是平衡逆向移动(或其他合理表述)(2分)
③7(或7:1)(2分)
(3)①0(2分);②0.5;-0.3(各2分)
学科网(北京)股份有限公司