文档内容
让更多的孩子得到更好的教育
中考总复习:实验方案的设计和评价(提高)
撰稿:熊亚军 审稿:李伟
【巩固练习】
一、选择题 (每小题只有一个选项符合题意)
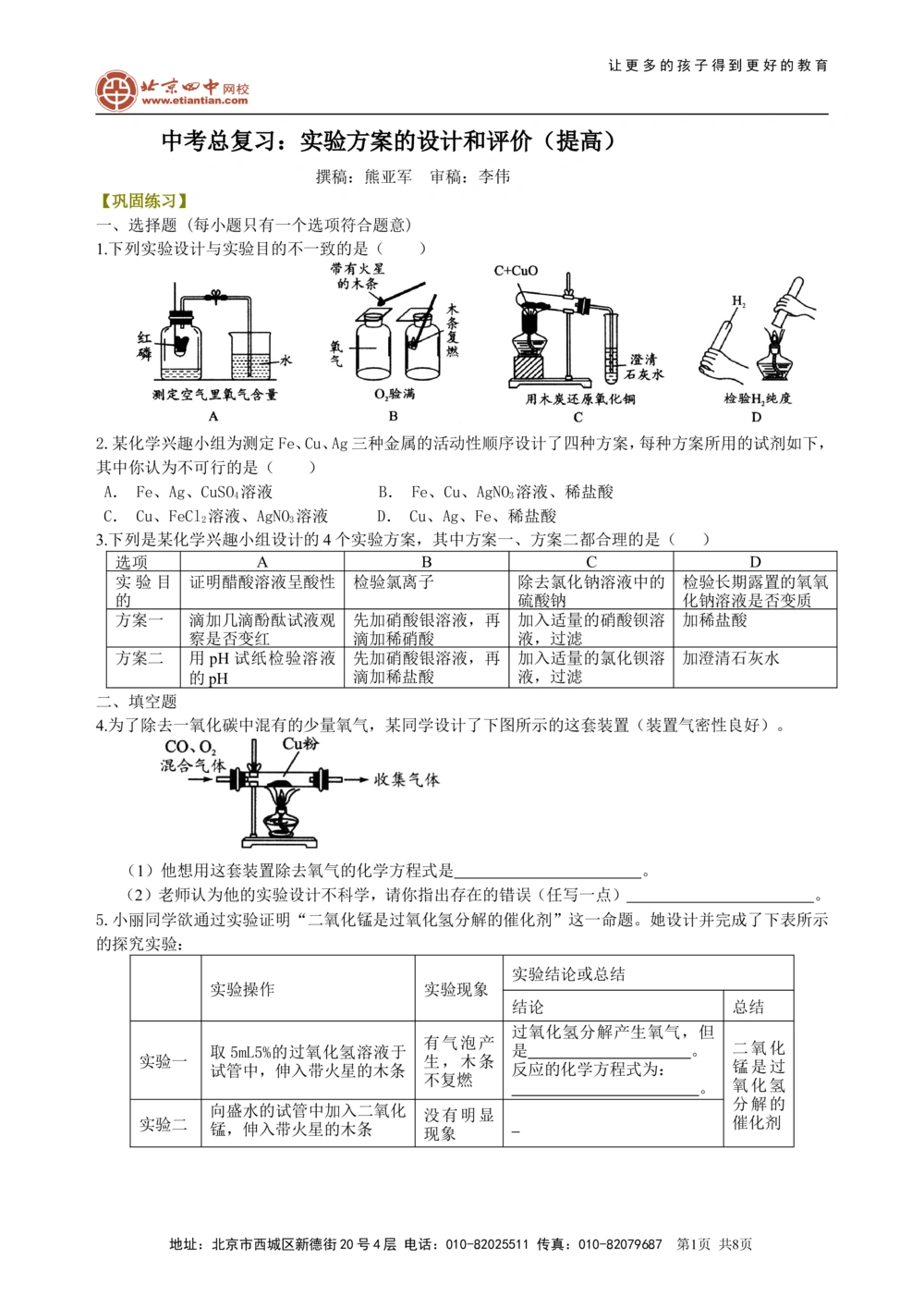
1.下列实验设计与实验目的不一致的是( )
2.某化学兴趣小组为测定Fe、Cu、Ag三种金属的活动性顺序设计了四种方案,每种方案所用的试剂如下,
其中你认为不可行的是( )
A. Fe、Ag、CuSO 溶液 B. Fe、Cu、AgNO 溶液、稀盐酸
4 3
C. Cu、FeCl 溶液、AgNO 溶液 D. Cu、Ag、Fe、稀盐酸
2 3
3.下列是某化学兴趣小组设计的4个实验方案,其中方案一、方案二都合理的是( )
选项 A B C D
实验目 证明醋酸溶液呈酸性 检验氯离子 除去氯化钠溶液中的 检验长期露置的氧氧
的 硫酸钠 化钠溶液是否变质
方案一 滴加几滴酚酞试液观 先加硝酸银溶液,再 加入适量的硝酸钡溶 加稀盐酸
察是否变红 滴加稀硝酸 液,过滤
方案二 用pH试纸检验溶液 先加硝酸银溶液,再 加入适量的氯化钡溶 加澄清石灰水
的pH 滴加稀盐酸 液,过滤
二、填空题
4.为了除去一氧化碳中混有的少量氧气,某同学设计了下图所示的这套装置(装置气密性良好)。
(1)他想用这套装置除去氧气的化学方程式是 。
(2)老师认为他的实验设计不科学,请你指出存在的错误(任写一点) 。
5.小丽同学欲通过实验证明“二氧化锰是过氧化氢分解的催化剂”这一命题。她设计并完成了下表所示
的探究实验:
实验结论或总结
实验操作 实验现象
结论 总结
过氧化氢分解产生氧气,但
有气泡产
取5mL5%的过氧化氢溶液于 是 。 二氧化
实验一 生,木条
试管中,伸入带火星的木条 反应的化学方程式为: 锰是过
不复燃
。 氧化氢
分解的
向盛水的试管中加入二氧化 没有明显
实验二 锰,伸入带火星的木条 现象 催化剂
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第1页 共8页让更多的孩子得到更好的教育
二氧化锰能加快过氧化氢的
实验三 分解
(1)请你帮小丽同学填写上表中未填完的空格。
(2)在小丽的探究实验中,“实验一”和“实验二”起的作用是 。
(3)小英同学认为仅由上述实验还不能完全得出表内的“总结”,她利用“实验三”反应后试管内的
剩余物继续实验最终完成了对“命题”的实验证明。
小英接下来的实验操作、现象和结论是:倾倒掉反应后的液体,向剩余的固体中重新加人过氧化氢溶
液,有 ,说明MnO 仍然能加快过氧化氢的分解速率(化学性质没变) 。
2
6.已知某金属X有下列相关信息:①它的主要矿物的化学成分是XO;②它主要通过热还原法冶炼而成;
2 3
③它的年产量位于金属之首。
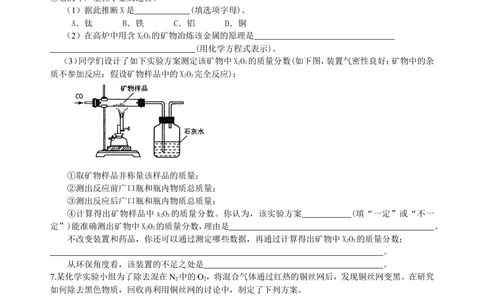
(1)据此推断X是 (填选项字母)。
A.钛 B.铁 C.铝 D.铜
(2)在高炉中用含XO 的矿物冶炼该金属的原理是
2 3
(用化学方程式表示)。
(3)同学们设计了如下实验方案测定该矿物中XO 的质量分数(如下图,装置气密性良好;矿物中的杂
2 3
质不参加反应;假设矿物样品中的XO 完全反应):
2 3
①取矿物样品并称量该样品的质量;
②测出反应前广口瓶和瓶内物质总质量;
③测出反应后广口瓶和瓶内物质总质量;
④计算得出矿物样品中xO 的质量分数。你认为,该实验方案 (填“一定”或“不一
2 3
定”)能准确测出矿物中XO 的质量分数,理由是 。
2 3
不改变装置和药品,你还可以通过测定哪些数据,再通过计算得出矿物中XO 的质量分数:
2 3
。
从环保角度看,该装置的不足之处是 。
7.某化学实验小组为了除去混在N 中的O,将混合气体通过红热的铜丝网后,发现铜丝网变黑。在研究
2 2
如何除去黑色物质,回收再利用铜丝网的讨论中,制定了下列方案。
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第2页 共8页让更多的孩子得到更好的教育
请根据以上方案回答:
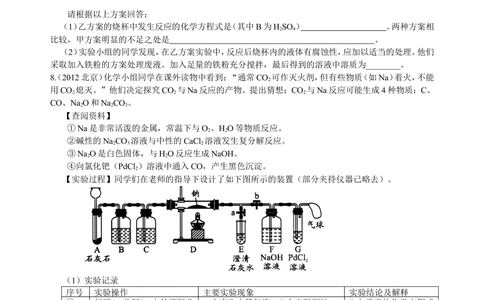
(1)乙方案的烧杯中发生反应的化学方程式是(其中B为HSO ) 。两种方案相
2 4
比较,甲方案明显的不足之处是 。
(2)实验小组的同学发现,在乙方案实验中,反应后烧杯内的液体有腐蚀性,应加以适当的处理。他们
采取加入铁粉的方案处理废液。加入足量的铁粉充分搅拌,最后得到的溶液中溶质为________。
8(. 2012北京)化学小组同学在课外读物中看到:“通常CO 可作灭火剂,但有些物质(如Na)着火,不能
2
用CO 熄灭。”他们决定探究CO 与Na反应的产物。提出猜想:CO 与Na反应可能生成4种物质:C、
2 2 2
CO、NaO和NaCO。
2 2 3
【查阅资料】
①Na是非常活泼的金属,常温下与O、HO等物质反应。
2 2
②碱性的NaCO 溶液与中性的CaCl 溶液发生复分解反应。
2 3 2
③NaO是白色固体,与HO反应生成NaOH。
2 2
④向氯化钯(PdCl )溶液中通入CO,产生黑色沉淀。
2
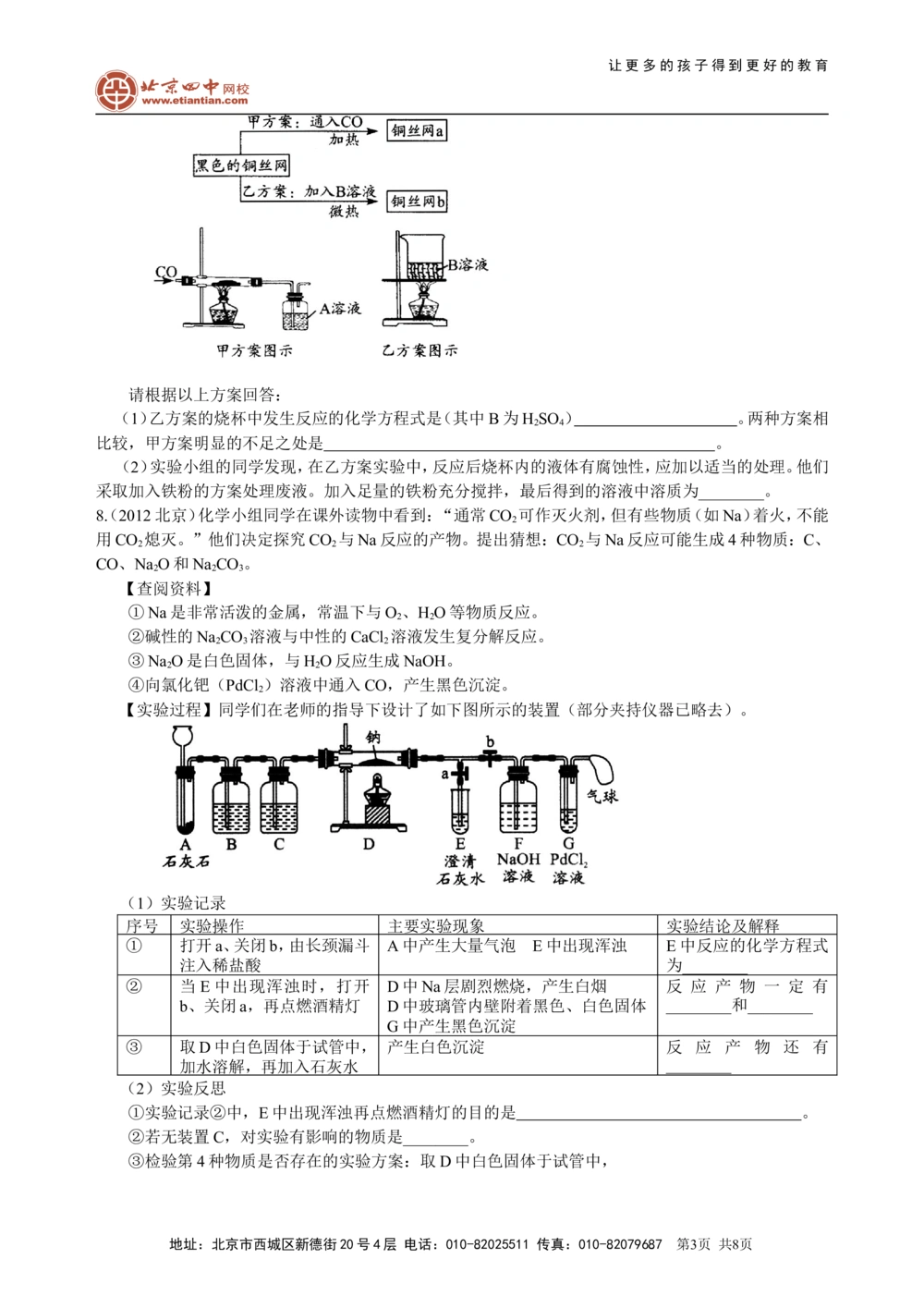
【实验过程】同学们在老师的指导下设计了如下图所示的装置(部分夹持仪器已略去)。
(1)实验记录
序号 实验操作 主要实验现象 实验结论及解释
① 打开a、关闭b,由长颈漏斗 A中产生大量气泡 E中出现浑浊 E中反应的化学方程式
注入稀盐酸 为________
② 当E中出现浑浊时,打开 D中Na层剧烈燃烧,产生白烟 反 应 产 物 一 定 有
b、关闭a,再点燃酒精灯 D中玻璃管内壁附着黑色、白色固体 ________和________
G中产生黑色沉淀
③ 取D中白色固体于试管中, 产生白色沉淀 反 应 产 物 还 有
加水溶解,再加入石灰水 ________
(2)实验反思
①实验记录②中,E中出现浑浊再点燃酒精灯的目的是 。
②若无装置C,对实验有影响的物质是________。
③检验第4种物质是否存在的实验方案:取D中白色固体于试管中,
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第3页 共8页让更多的孩子得到更好的教育
。
9.工业上用天然气和水蒸气在高温条件下发生反应(化学方程式为 CH+H O 高温 C O+3H ),
4 2 2
得到的CO和H 的混合气被称为合成气。合成气在工业上可用于合成一系列化工原料和新型燃料,还可
2
用于冶炼某些金属。某化学兴趣小组的同学在实验室模拟了合成气的制备,并设计实验验证合成气的还
原性。
(1)用甲烷和水蒸气在高温条件下反应得到合成气。根据化学方程式CH+H O 高温 C O+3H,合成
4 2 2
气中CO和H 的质量比为________。
2
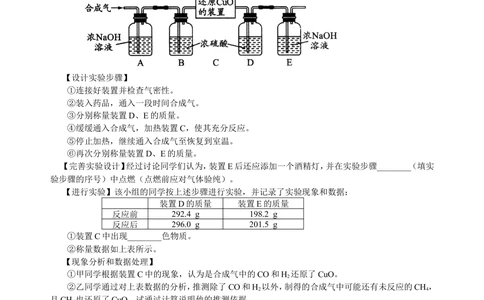
(2)用合成气还原足量氧化铜。实验装置如下图所示:
【设计实验步骤】
①连接好装置并检查气密性。
②装入药品,通入一段时间合成气。
③分别称量装置D、E的质量。
④缓缓通入合成气,加热装置C,使其充分反应。
⑤停止加热,继续通入合成气至恢复到室温。
⑥再次分别称量装置D、E的质量。
【完善实验设计】经过讨论同学们认为,装置E后还应添加一个酒精灯,并在实验步骤________(填实
验步骤的序号)中点燃(点燃前应对气体验纯)。
【进行实验】该小组的同学按上述步骤进行实验,并记录了实验现象和数据:
装置D的质量 装置E的质量
反应前 292.4 g 198.2 g
反应后 296.0 g 201.5 g
①装置C中出现________色物质。
②称量数据如上表所示。
【现象分析和数据处理】
①甲同学根据装置C中的现象,认为是合成气中的CO和H 还原了CuO。
2
②乙同学通过对上表数据的分析,推测除了CO和H 以外,制得的合成气中可能还有未反应的CH,
2 4
且CH 也还原了CuO。试通过计算说明他的推测依据 。
4
。
【拓展探究】该小组同学对于CH 是否真的能够还原氧化铜提出了质疑并进行探究。查阅资料:甲
4
烷具有还原性,可以还原氧化铜,生成CO 和HO;白色的无水硫酸铜遇水会变成蓝色。
2 2
【实验设计】该小组同学拟用纯净的甲烷气体如下图所示装置进行实验。
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第4页 共8页让更多的孩子得到更好的教育
①上图装置F中盛放的试剂名称是________。
②上图装置的正确连接顺序是________(填字母,且每套装置限用一次)。
10.叠氮化钠(NaN )被广泛应用于汽车安全气囊,某兴趣小组对其进行下列研究。
3
【应用研究】
(1)汽车经撞击后,30毫秒内引发NaN ,迅速分解为Na、N,反应的化学方程式为________。
3 2
【制备研究】
(2)将金属钠与液态氨反应得NaNH ,再将NaNH 与NO反应可生成NaN 、NaOH和气体X,该反应
2 2 2 3
的化学方程式为2NaNH +N O==NaN +NaOH+X,实验室检验X气体使用的试纸是湿润的________。
2 2 3
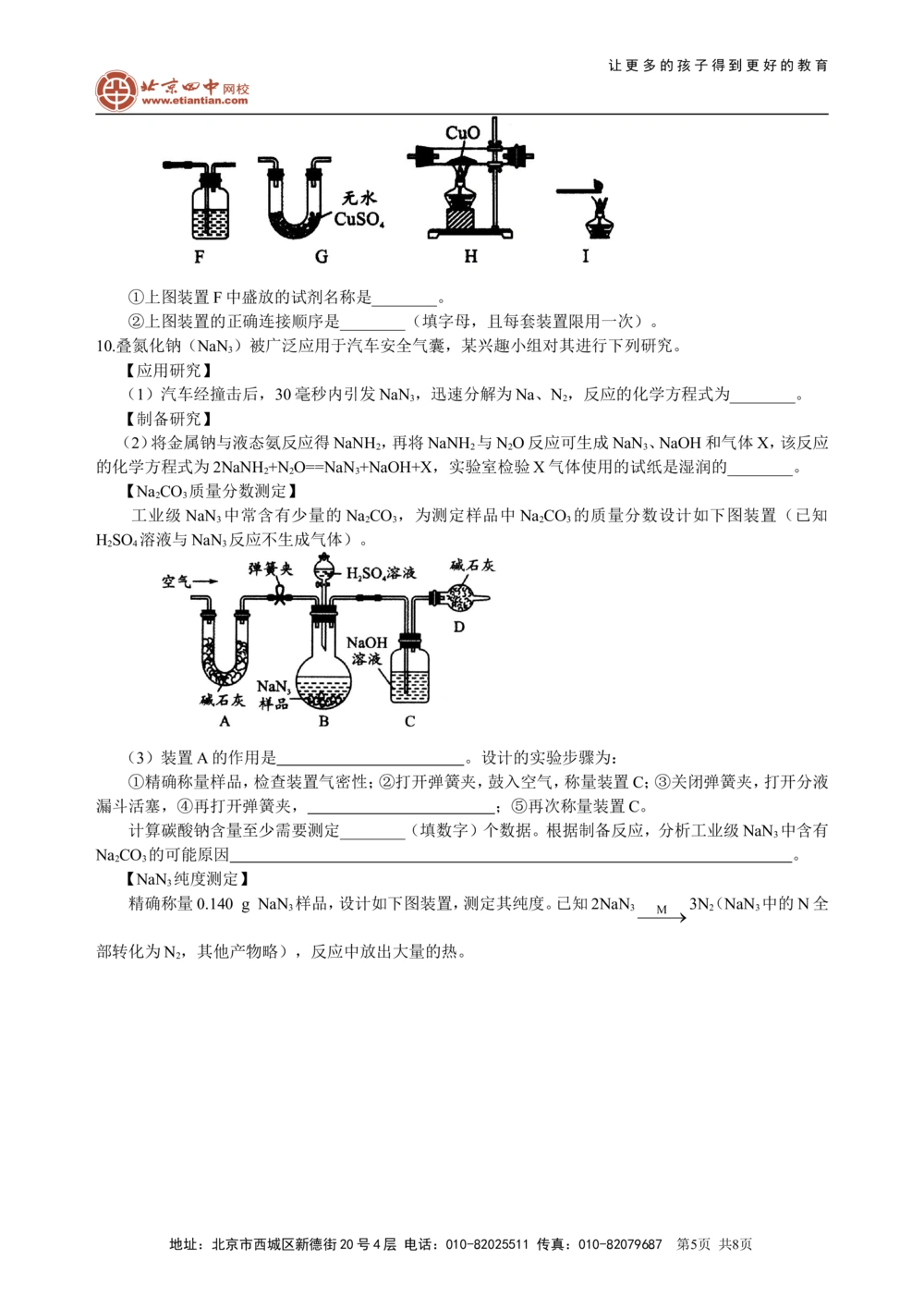
【NaCO 质量分数测定】
2 3
工业级NaN 中常含有少量的NaCO ,为测定样品中NaCO 的质量分数设计如下图装置(已知
3 2 3 2 3
HSO 溶液与NaN 反应不生成气体)。
2 4 3
(3)装置A的作用是 。设计的实验步骤为:
①精确称量样品,检查装置气密性;②打开弹簧夹,鼓入空气,称量装置C;③关闭弹簧夹,打开分液
漏斗活塞,④再打开弹簧夹, ;⑤再次称量装置C。
计算碳酸钠含量至少需要测定________(填数字)个数据。根据制备反应,分析工业级NaN 中含有
3
NaCO 的可能原因 。
2 3
【NaN 纯度测定】
3
精确称量0.140 g NaN 样品,设计如下图装置,测定其纯度。已知2NaN 3N(NaN 中的N全
3 3 2 3
部转化为N,其他产物略),反应中放出大量的热。
2
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第5页 共8页让更多的孩子得到更好的教育
(4)检查该装置气密性的方法是连接好装置,从水准瓶注水,量气管中液面与右边液面形成高度差,做
好标记,一段时间后,两边高度差________(填“变大”“变小”或“不变”),说明气密性良好。
(5)使小试管中的NaN 样品与M溶液接触的操作是 。
3
(6)使用冷水冷凝的目的是 。反应前应将液面调节到
量气管的“0”刻度,并使两边液面相平,反应后读数时,还需要进行的操作是
。
(7)常温下测得量气管读数为67.2 mL(N 的密度为1.25 g/L),则实验中选用的量气管规格合适的
2
是________(填字母序号)。
A.100 mL B.1 L C.2 L
(8)NaN 样品的纯度是 。
3
【答案与解析】
1.【答案】B
【解析】本题考查化学实验。验满氧气应将带火星的木条放置在集气瓶口部;将木条伸入到集气瓶中是
检验氧气,故B项的实验设计与实验目的不符。
2.【答案】D
【解析】本题考查金属活动性检验的方法,可利用金属与酸、盐反应的性质判断。
3.【答案】D
【解析】A中方案一,酸不能使酚酞变色,不能利用酚酞来证明醋酸显酸性;B中方案二,滴加稀盐酸时
使溶液中混进了Cl-,则不能检验原溶液中的Cl-;C中方案一,会产生新的杂质硝酸钠。
4.【答案】(1)2Cu+O △ 2 C uO (2)CO和O 混合加热会发生反应,甚至爆炸
2 2
5.【答案】 (1)
实验一 反应慢 2HO=2HO + O↑
2 2 2 2
实验二 二氧化锰加入水中不产生氧气
实验三 向盛有 5mL5%过氧化氢溶液 有大量气泡产生,带
的试管中加入二氧化锰,伸入 火星的木条迅速复燃
带火星的木条
(2)对比(或对照) (3)大量气泡产生
6.【答案】
(1)B (2)3CO+FeO 2Fe+3CO
2 3 2
(3)不一定 生成的二氧化碳气体不一定被石灰水完全吸收(或石灰水可能吸收空气中的二氧化碳)
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第6页 共8页让更多的孩子得到更好的教育
分别测出反应前玻璃管和矿物样品的总质量、反应后玻璃管和剩余固体总质量 无尾气处理装置
7.【答案】
(1)CuO+HSO △ C uSO +H O 需要制取CO且CO有毒;尾气CO未处理;实验装置复杂等
2 4 4 2
(2)大于 (3)FeSO
4
8.【答案】
(1)①CO+Ca(OH) ==CaCO↓+H O ②C CO ③NaCO
2 2 3 2 2 3
(2)①排出装置中的空气,防止空气的干扰 ②水 ③加水溶解,加入过量的CaCl 溶液使其沉淀完
2
全,静置,向上层清液中滴加酚酞溶液。若溶液变红,则产物中有NaO;若溶液不变色,则产物中没有
2
NaO
2
【解析】
(1)①加入稀盐酸能产生使澄清石灰水变浑浊的气体,即CO 与Ca(OH) 发生反应生成了CaCO 沉淀
2 2 3
和HO;②根据D中发生的现象内壁附着黑色物质说明产生了碳,根据C中产生黑色沉淀说明产物中有
2
CO;③D中固体放于试管中加水溶解,再加入石灰水产生白色沉淀,说明产物中有NaCO。
2 3
(2)由于空气中含有多种气体,为防止空气的干扰,应将装置中的空气排净;没有装置C,水能与Na发
生反应产生H,对实验产物有影响;③检验第4种物质的存在,可加入水溶解,再加入过量的CaCl 溶液
2 2
使沉淀完全(除去碳酸钠),静置后向上层清液中滴加酚酞试液,若溶液变红,说明溶液仍显碱性,则产物
中有NaO,若溶液不变色,则产物中没有NaO。
2 2
9. 【答案】
(1)14∶3
(2)【完善实验设计】②
【进行实验】红
【现象分析和数据处理】如果只有CO和H ,还原足量CuO,合成气中CO与H 的分子个数比为
2 2
1∶3,生成物中碳元素与氢元素的质量比为2∶1;如果只有CH 还原足量CuO,生成物中碳元素与氢元
4
素的质量比为3∶1;现测得CO 的质量:201.5 g-198.2 g=3.3 g,HO的质量:296.0 g-292.4 g=3.6 g。
2 2
生成物中碳元素与氢元素的质量比: ,9∶4介于2∶1和3∶1之间。由
此可推测出,除了CO和H 以外,制得的合成气中可能还有未反应的CH,且CH4也还原了CuO。
2 4
【实验设计】澄清石灰水 HGFI
【解析】
(1)根据化学方程式知合成气中CO和H 的质量比为28∶6=14∶3。
2
(2)为了检验合成气是否纯净应在步骤②中对气体验纯;装置C中黑色粉末变红色;根据表中数据可
以确定生成物中碳元素与氢元素的质量比,根据质量比与反应物中只有CO和H 或只有CH 时碳元素与
2 4
氢元素的质量比较,从而找出推测的依据。利用澄清的石灰水可以检验是否有CO 生成;连接仪器时应先
2
通过H,再通过G,利用无水CuSO 是否变蓝确定是否有水生成,利用澄清的石灰水是否变浑浊来确定是
4
否有CO 生成,最后将剩余的气体通过点燃除掉。
2
10.【答案】
(1)2NaN 2Na+3N↑ (2)红色石蕊试纸
3 2
(3)除去空气中的二氧化碳 缓缓鼓入空气 3
生成NaN 的同时有NaOH生成;NaOH吸收空气中的CO,生成了NaCO
3 2 2 3
(4)不变 (5)将锥形瓶倾斜,使样品与M溶液接触
(6)降低气体温度(防止量气管中水喷出) 调节两边液面相平 (7)A
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第7页 共8页让更多的孩子得到更好的教育
(8)m (N )=67.2 mL×10-3 L/mL×1.25 g/L=0.084 g
2
设样品中NaN 的质量为x。
3
2NaN ~ 3N
3 2
130 84
x 0.084 g
,x=0.13 g
【解析】(1)写方程式时不要忘记条件是撞击。(2)根据质量守恒定律,推知X为NH ,NH 使湿润红色
3 3
石蕊试纸变蓝。(3)为防止空气中的CO,被C装置吸收,影响实验结果,用A装置中的碱石灰除去空气
2
中的CO;为了使反应后产生的CO 全部被NaOH溶液吸收,应鼓入空气排出圆底烧瓶内的CO;首先称
2 2 2
量样品质量,然后称量装置C反应前和反应后的质量,两次质量差就是生成CO 的质量,根据CO 的质量
2 2
计算出样品中NaCO 的质量,从而计算样品中NaCO 的质量分数,所以至少称量三次,测得三个数据。
2 3 2 3
(4)若装置漏气则量气管液面与右边液面不可能形成高度差。(5)将锥形瓶倾斜使M溶液进入小试管中。
(6)因反应放出大量的热,以防热的气流速率太快,将量气管中的水喷出,所以用冷水冷却气体;调节水
准瓶的高度,使两边液面相平,在两边压强相同的条件下读得的数据更准确。(7)根据实验测67.2 mL
M,用量程是100 mL的量气管,若用较大量程的量气管,导致误差偏大;(8)根据m= ·V,可计算出氮
气的质量,由氮气质量计算出样品中NaN 的质量,从而确定样品中NaN 的纯度。
3 3
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第8页 共8页