文档内容
机密★启用前 试卷类型:A
(试题卷)
2025 年山东省普通高校招生等级性考试
化 学
注意事项:
1. 答题前,学生务必在练习卷、答题卡规定的地方填写自己的学校、准考
证号、姓名。学生要认真核对答题卡上粘贴的条形码的“准考证号、姓名”
与学生本人准考证号、姓名是否一致。
2. 回答选择题时,选出每小题答案后,用 2B铅笔把答题卡上对应题目的答
案标号涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。
3. 回答非选择题时,将答案写在答题卡上。写在本练习卷上无效。
4. 可能用到的相对原子质量:H 1 O 16 Na 23 K 39
5. 答题结束后,学生必须将练习卷和答题卡一并交回。
(本部分需要考生认真、准确填写,不得有误)
考生考号
考生姓名
考场号
考生座位号
H 化学试题 第1页(共12页)
学科网(北京)股份有限公一、 选择题:本题共10小题,每小题 2分,共20分。每小题只有一个选项符合
题目要求。
1. 下列在化学史上产生重要影响的成果中,不涉及氧化还原反应的是( )
A. 侯德榜发明了以
H 化学试题 第2页(共12页)
学科网(北京)股份有限公
N H
3
, C O
2
和 N a C l 为原料的联合制碱法
B. 戴维电解盐酸得到H 和Cl ,从而提出了酸的含氢学说
2 2
C. 拉瓦锡基于金属和 O
2
的反应提出了燃烧的氧化学说
D. 哈伯发明了以N 和H 为原料合成氨的方法
2 2
2. 化学应用体现在生活的方方面面,下列用法不合理的是( )
A.用明矾净化黄河水 B.用漂白粉漂白蚕丝制品
C.用食醋去除水壶中水垢 D.用小苏打作烘焙糕点膨松剂
3. 实验室中,下列试剂保存方法正确的是( )
A.液溴加水封保存在广口试剂瓶中 B.硝酸银溶液保存在棕色细口试剂瓶中
C.高锰酸钾与苯酚存放在同一药品柜中 D.金属锂保存在盛有煤油的广口试剂瓶中
NaOH 400mL
4. 称取1.6g固体 配制 浓度约为
0 .1 m o l L − 1
的
N a O H
溶液,下列仪器中
不需要使用的是( )
A. 1 0 0 m L 烧杯 B.500mL容量瓶
C. 5 0 0 m L 量筒 D. 5 0 0 m L 细口试剂瓶(具橡胶塞)
5. 下列实验涉及反应的离子方程式书写正确的是( )
A. 用NaOH溶液吸收少量 S O
2
: S O
2
+ O H − = H S O −3
O :Na O +H O=2Na+ +2OH− +O
B. 用Na O 和水制备少量 2 2 2 2 2
2 2
C. 用MnO 和浓盐酸制备
2
C l
2
: M n O
2
+ 4 H + + 2 C l −
M n 2 + + C l
2
+ 2 H
2
O
D. 用稀硝酸溶解少量 C u 粉: 3 C u + 8 H + + 8 N O −3 = 3 C u ( N O
3
)
2
+ 2 N O + 4 H
2
O
6. 第70号元素镱(Yb)的基态原子价电子排布式为 4 f 1 4 6 s 2 。下列说法正确的是( )
A. 1 7 4
7 0
Y b 的中子数与质子数之差为104 B.174Yb与176Yb是同一种核素
70 70
C.基态Yb原子核外共有10个d电子 D.Yb位于元素周期表中第6周期7. 用硫酸和
H 化学试题 第3页(共12页)
学科网(北京)股份有限公
N a N
3
可制备一元弱酸 H N
3
。下列说法错误的是( )
A. N a N
3
的水溶液显碱性
B. N −3 的空间构型为V形
C. N a N
3
为含有共价键的离子化合物
D. N −3 的中心N原子所有价电子均参与成键
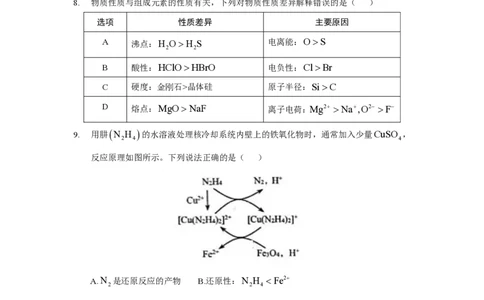
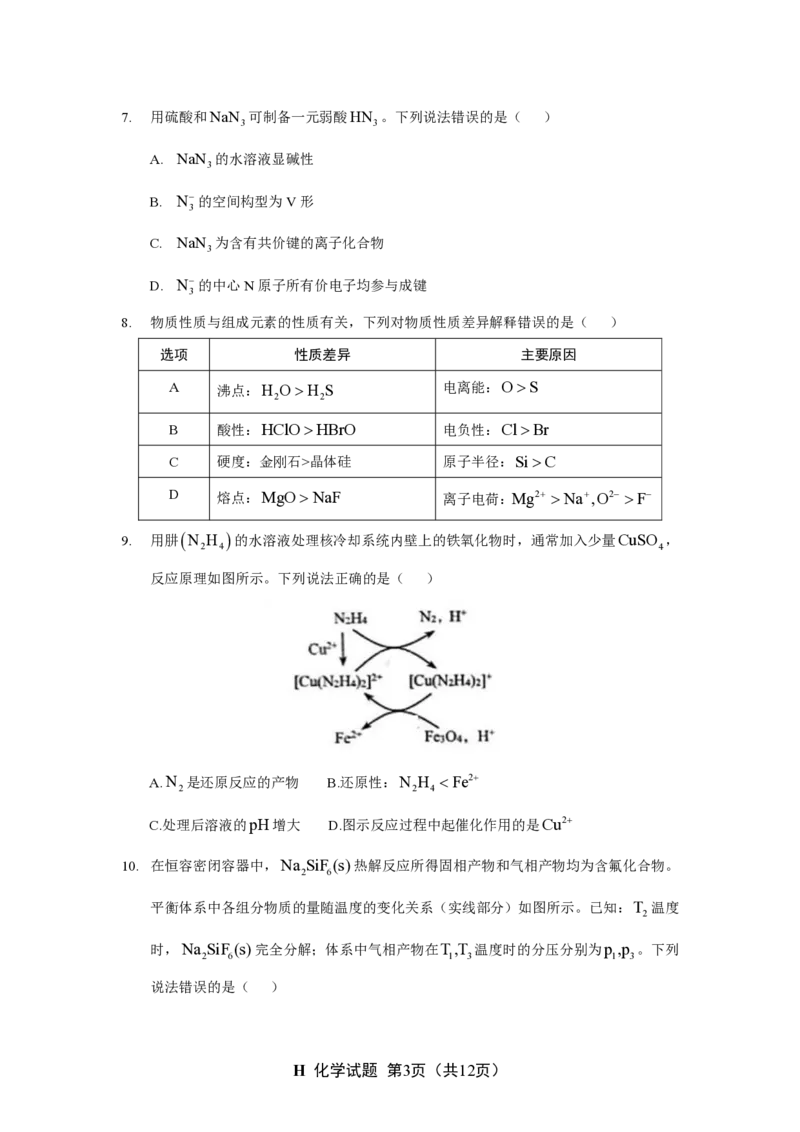
8. 物质性质与组成元素的性质有关,下列对物质性质差异解释错误的是( )
选项 性质差异 主要原因
A 沸点: H
2
O H
2
S 电离能: O S
B 酸性:HClOHBrO 电负性: C l B r
C 硬度:金刚石>晶体硅 原子半径: S i C
D 熔点: M g O N a F 离子电荷: M g 2 + N a + , O 2 − F −
9. 用肼 ( N
2
H
4
) 的水溶液处理核冷却系统内壁上的铁氧化物时,通常加入少量 C u S O
4
,
反应原理如图所示。下列说法正确的是( )
A. N
2
是还原反应的产物 B.还原性:N H Fe2+
2 4
C.处理后溶液的 p H 增大 D.图示反应过程中起催化作用的是Cu2+
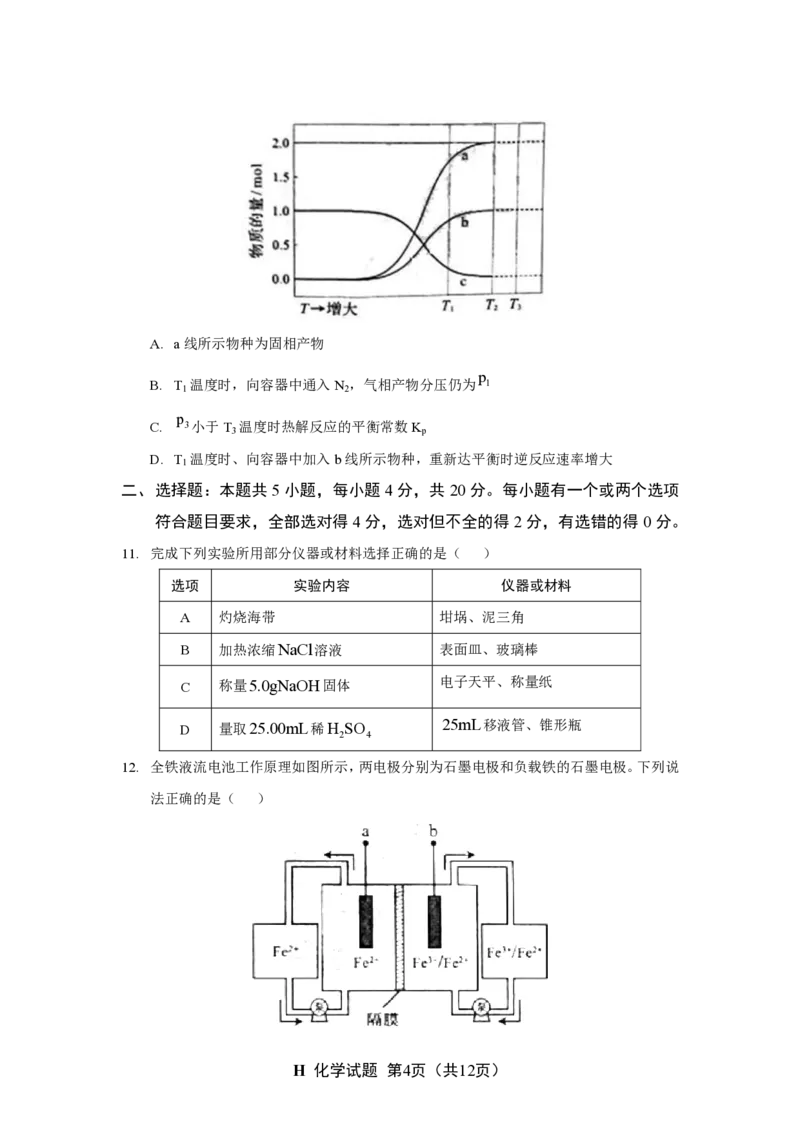
10. 在恒容密闭容器中,Na SiF (s)热解反应所得固相产物和气相产物均为含氟化合物。
2 6
平衡体系中各组分物质的量随温度的变化关系(实线部分)如图所示。已知:T 温度
2
时, N a
2
S i F
6
( s ) 完全分解;体系中气相产物在 T
1
, T
3
温度时的分压分别为 p
1
, p
3
。下列
说法错误的是( )A. a线所示物种为固相产物
p
B. T 温度时,向容器中通入N ,气相产物分压仍为 1
1 2
C.
H 化学试题 第4页(共12页)
学科网(北京)股份有限公
p
3 小于T 温度时热解反应的平衡常数K
3 p
D. T 温度时、向容器中加入b线所示物种,重新达平衡时逆反应速率增大
1
二、 选择题:本题共 5 小题,每小题 4 分,共 20 分。每小题有一个或两个选项
符合题目要求,全部选对得 4 分,选对但不全的得 2 分,有选错的得 0 分。
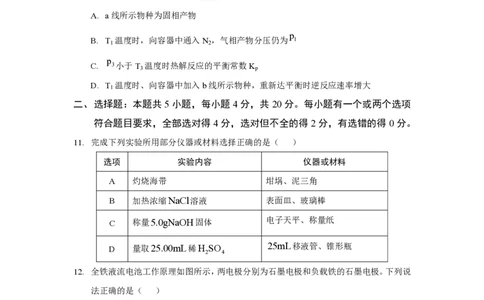
11. 完成下列实验所用部分仪器或材料选择正确的是( )
选项 实验内容 仪器或材料
A 灼烧海带 坩埚、泥三角
B 加热浓缩 N a C l 溶液 表面皿、玻璃棒
C 称量 5 . 0 g N a O H 固体 电子天平、称量纸
D 量取 2 5 . 0 0 m L 稀 H
2
S O
4
25mL移液管、锥形瓶
12. 全铁液流电池工作原理如图所示,两电极分别为石墨电极和负载铁的石墨电极。下列说
法正确的是( )A. 隔膜为阳离子交换膜
B. 放电时,a极为负极
C. 充电时,隔膜两侧溶液
H 化学试题 第5页(共12页)
学科网(北京)股份有限公
F e 2 + 浓度均减小
D. 理论上,Fe3+每减少1mol,Fe2+总量相应增加2mol
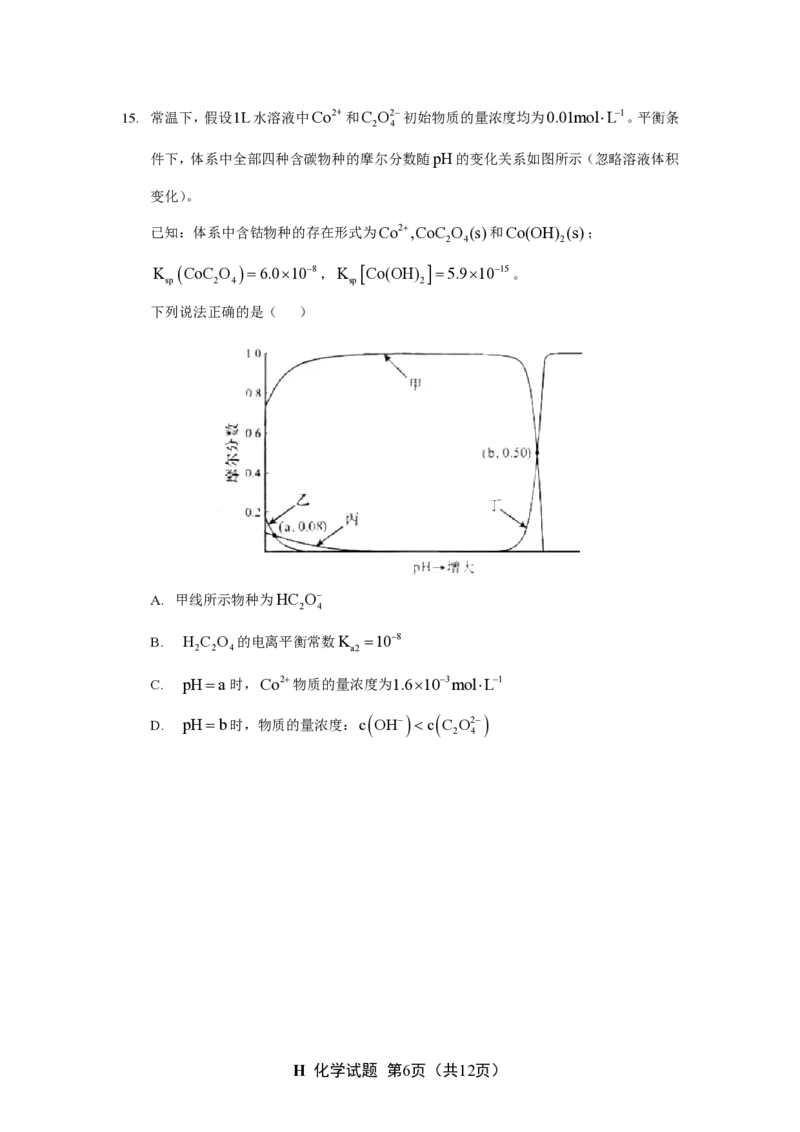
13. 钢渣中富含CaO,SiO ,FeO,Fe O 等氧化物,实验室利用酸碱协同法分离钢渣中的
2 2 3
Ca,Si,Fe元素,流程如下。
已知: F e
2
( C
2
O
4
)
3
能溶于水;K (CaC O )=2.310−9,K (FeC O )=3.210−7。
sp 2 4 sp 2 4
下列说法错误的是( )
A. 试剂X可选用Fe粉
B. 试剂Y可选用盐酸
C. “分离”后Fe元素主要存在于滤液Ⅱ中
D. “酸浸”后滤液Ⅰ的pH过小会导致滤渣Ⅱ质量减少
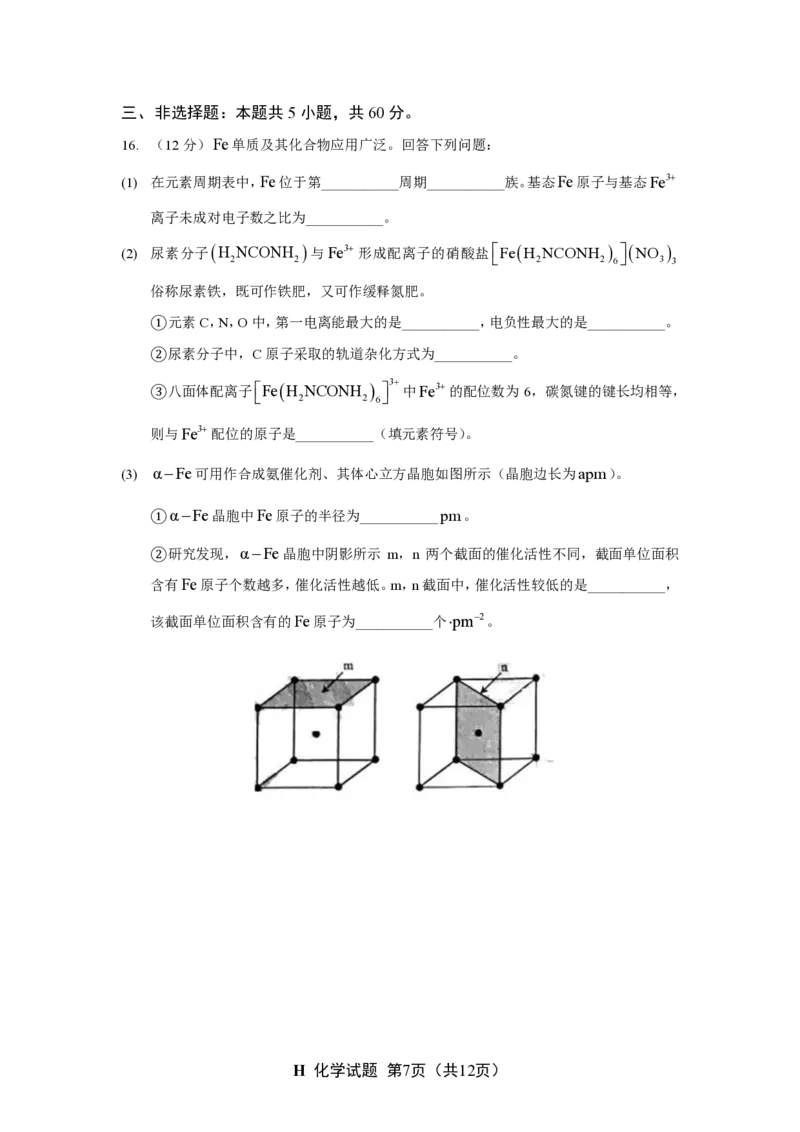
14. 以异丁醛 ( M ) 为原料制备化合物Q的合成路线如下,下列说法错误的是( )
A. M系统命名为2-甲基丙醛
B. 若 M + X → N 原子利用率为100%,则X是甲醛
C. 用酸性 K M n O
4
溶液可鉴别N和Q
D. P→Q过程中有CH COOH生成
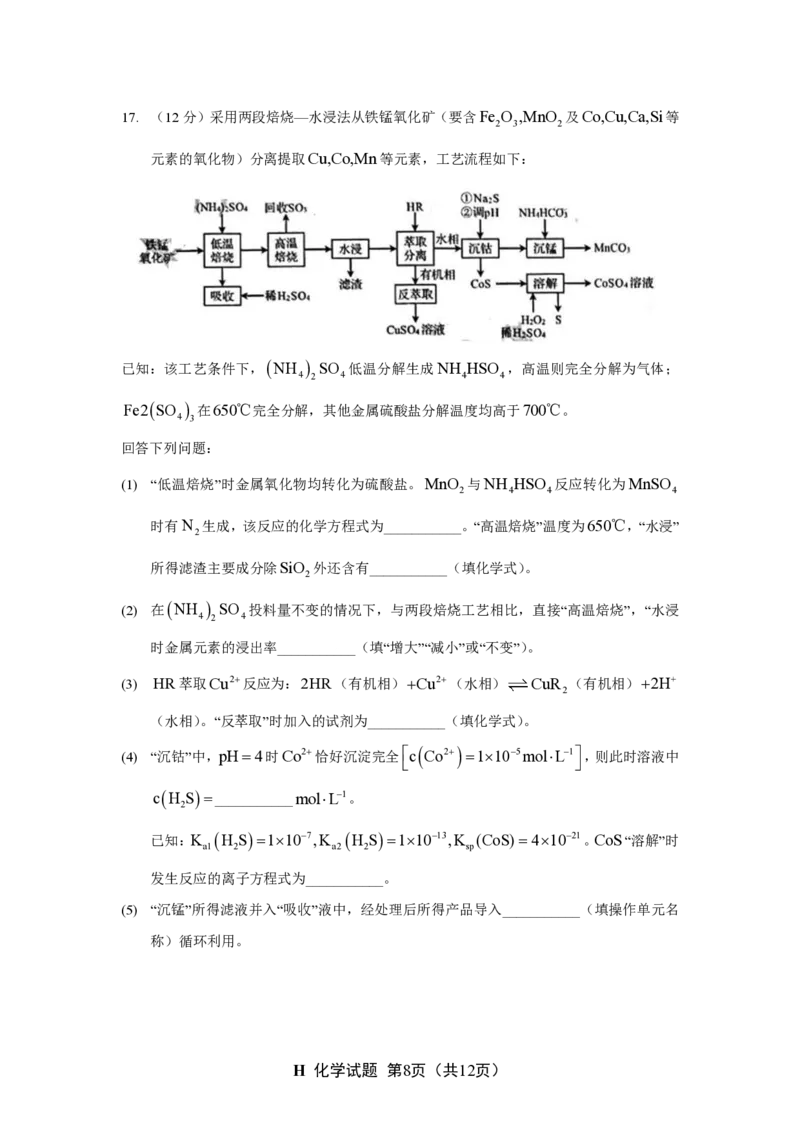
315. 常温下,假设
H 化学试题 第6页(共12页)
学科网(北京)股份有限公
1 L 水溶液中 C o 2 + 和 C
2
O 24 − 初始物质的量浓度均为 0 .0 1 m o l L − 1 。平衡条
件下,体系中全部四种含碳物种的摩尔分数随 p H 的变化关系如图所示(忽略溶液体积
变化)。
已知:体系中含钴物种的存在形式为 C o 2 + , C o C
2
O
4
( s ) 和 C o ( O H )
2
( s ) ;
K (CoC O )=6.010−8,
sp 2 4
K
sp
C o ( O H )
2
= 5 .9 1 0 − 1 5 。
下列说法正确的是( )
A. 甲线所示物种为 H C
2
O −4
B. H C O 的电离平衡常数K =10−8
2 2 4 a2
C. p H = a 时, C o 2 + 物质的量浓度为 1 .6 1 0 − 3 m o l L − 1
D. p H = b 时,物质的量浓度: c ( O H − ) c ( C
2
O 24 − )三、 非选择题:本题共5小题,共 60分。
16. (12分)
H 化学试题 第7页(共12页)
学科网(北京)股份有限公
F e 单质及其化合物应用广泛。回答下列问题:
(1) 在元素周期表中, F e 位于第___________周期___________族。基态 F e 原子与基态 F e 3 +
离子未成对电子数之比为___________。
(2) 尿素分子 ( H
2
N C O N H
2
) 与 F e 3 + 形成配离子的硝酸盐Fe(H NCONH ) (NO )
2 2 6 3 3
俗称尿素铁,既可作铁肥,又可作缓释氮肥。
①元素C,N,O中,第一电离能最大的是___________,电负性最大的是___________。
②尿素分子中,C原子采取的轨道杂化方式为___________。
③八面体配离子Fe(H NCONH ) 3+ 中
2 2 6
F e 3 + 的配位数为 6,碳氮键的键长均相等,
则与 F e 3 + 配位的原子是___________(填元素符号)。
(3) α − F e 可用作合成氨催化剂、其体心立方晶胞如图所示(晶胞边长为 a p m )。
① α − F e 晶胞中 F e 原子的半径为___________ p m 。
②研究发现, α − F e 晶胞中阴影所示 m,n 两个截面的催化活性不同,截面单位面积
含有 F e 原子个数越多,催化活性越低。m,n截面中,催化活性较低的是___________,
该截面单位面积含有的 F e 原子为___________个 p m − 2 。17. (12分)采用两段焙烧—水浸法从铁锰氧化矿(要含
H 化学试题 第8页(共12页)
学科网(北京)股份有限公
F e
2
O
3
, M n O
2
及 C o , C u , C a , S i 等
元素的氧化物)分离提取 C u ,C o ,M n 等元素,工艺流程如下:
已知:该工艺条件下, ( N H
4
)
2
S O
4
低温分解生成NH HSO ,高温则完全分解为气体;
4 4
F e 2 ( S O
4
)
3
在 6 5 0 ℃ 完全分解,其他金属硫酸盐分解温度均高于 7 0 0 ℃ 。
回答下列问题:
(1) “低温焙烧”时金属氧化物均转化为硫酸盐。 M n O
2
与 N H
4
H S O
4
反应转化为 M n S O
4
时有 N
2
生成,该反应的化学方程式为___________。“高温焙烧”温度为650℃,“水浸”
所得滤渣主要成分除 S i O
2
外还含有___________(填化学式)。
(2) 在 ( N H
4
)
2
S O
4
投料量不变的情况下,与两段焙烧工艺相比,直接“高温焙烧”,“水浸
时金属元素的浸出率___________(填“增大”“减小”或“不变”)。
(3) H R 萃取 C u 2 + 反应为: 2 H R (有机相) + C u 2 + (水相) C u R
2
(有机相) + 2 H +
(水相)。“反萃取”时加入的试剂为___________(填化学式)。
(4) “沉钴”中,pH=4时 C o 2 + 恰好沉淀完全 c ( C o 2 + ) = 1 1 0 − 5 m o l L − 1 ,则此时溶液中
c(H S)=___________
2
m o l L − 1 。
已知:K (H S)=110−7,K (H S)=110−13,K (CoS)=410−21。
a1 2 a2 2 sp
C o S “溶解”时
发生反应的离子方程式为___________。
(5) “沉锰”所得滤液并入“吸收”液中,经处理后所得产品导入___________(填操作单元名
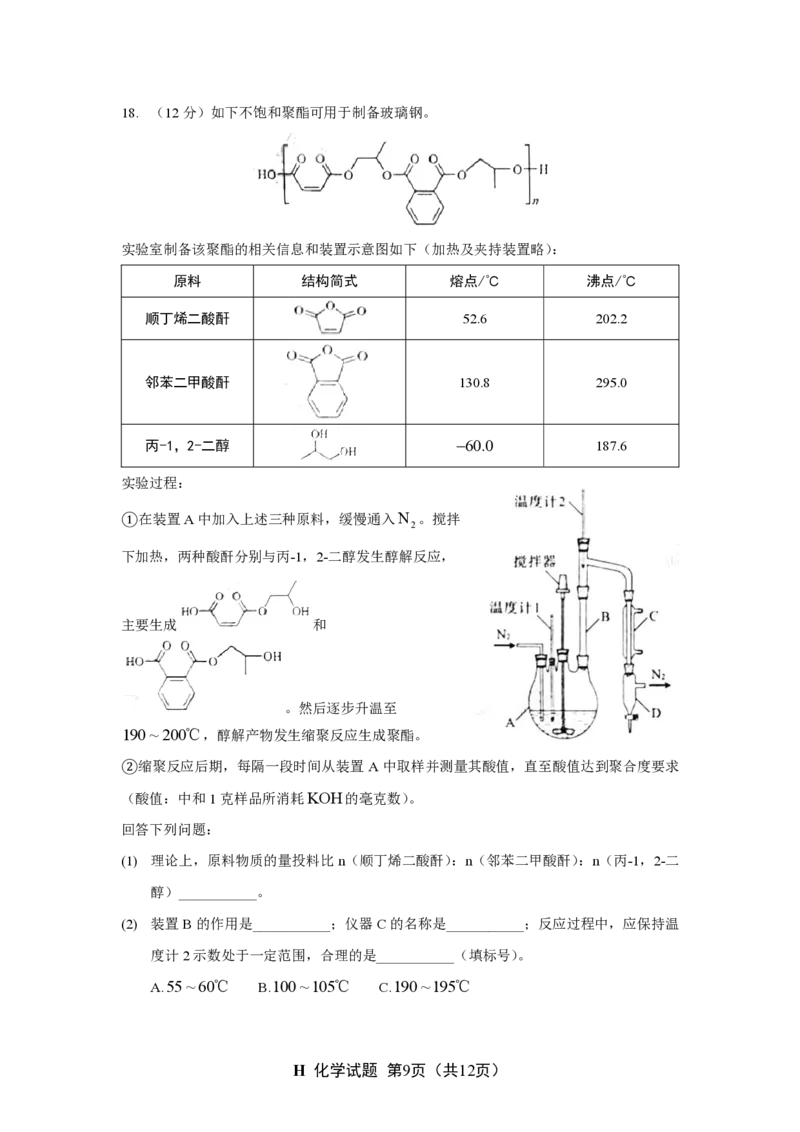
称)循环利用。18. (12分)如下不饱和聚酯可用于制备玻璃钢。
实验室制备该聚酯的相关信息和装置示意图如下(加热及夹持装置略):
原料 结构简式 熔点/℃ 沸点/℃
顺丁烯二酸酐 52.6 202.2
邻苯二甲酸酐 130.8 295.0
丙-1,2-二醇
H 化学试题 第9页(共12页)
学科网(北京)股份有限公
− 6 0 .0 187.6
实验过程:
①在装置A中加入上述三种原料,缓慢通入N 。搅拌
2
下加热,两种酸酐分别与丙-1,2-二醇发生醇解反应,
主要生成 和
。然后逐步升温至
1 9 0 ~ 2 0 0 ℃ ,醇解产物发生缩聚反应生成聚酯。
②缩聚反应后期,每隔一段时间从装置 A 中取样并测量其酸值,直至酸值达到聚合度要求
(酸值:中和1克样品所消耗 K O H 的毫克数)。
回答下列问题:
(1) 理论上,原料物质的量投料比 n(顺丁烯二酸酐):n(邻苯二甲酸酐):n(丙-1,2-二
醇)___________。
(2) 装置B的作用是___________;仪器C的名称是___________;反应过程中,应保持温
度计2示数处于一定范围,合理的是___________(填标号)。
A.55~60℃ B.100~105℃ C.190~195℃(3) 为测定酸值,取
H 化学试题 第10页(共12页)
学科网(北京)股份有限公
a g 样品配制 2 5 0 . 0 0 m L 溶液.移取 2 5 . 0 0 m L 溶液,用 c m o l L − 1 K O H
—乙醇标准溶液滴定至终点,重复实验,数据如下:
序号 1 2 3 4 5
滴定前读数/ m L 0.00 24.98 0.00 0.00 0.00
滴定后读数/ m L 24.98 49.78 24.10 25.00 25.02
应舍弃的数据为___________(填序号);测得该样品的酸值为___________(用含a,c
的代数式表示)。若测得酸值高于聚合度要求,可采取的措施为___________(填标号)。
A.立即停止加热 B.排出装置D内的液体 C.增大 N
2
的流速
(4) 实验中未另加催化剂的原因是___________。
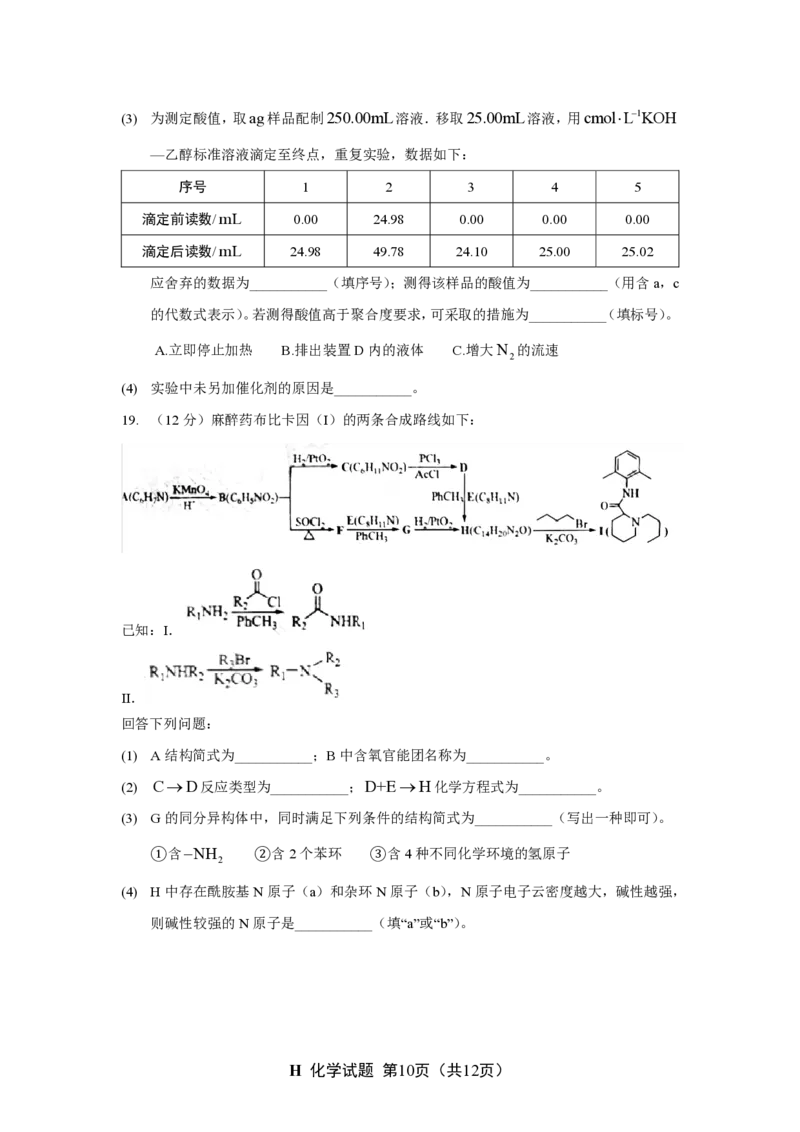
19. (12分)麻醉药布比卡因(I)的两条合成路线如下:
已知:Ⅰ.
Ⅱ.
回答下列问题:
(1) A结构简式为___________;B中含氧官能团名称为___________。
(2) C → D 反应类型为___________; D + E → H 化学方程式为___________。
(3) G的同分异构体中,同时满足下列条件的结构简式为___________(写出一种即可)。
①含−NH ②含2个苯环 ③含4种不同化学环境的氢原子
2
(4) H中存在酰胺基N原子(a)和杂环N原子(b),N原子电子云密度越大,碱性越强,
则碱性较强的N原子是___________(填“a”或“b”)。(5) 结合路线信息,用
H 化学试题 第11页(共12页)
学科网(北京)股份有限公
H
2
/ P t O
2
催化加氢时,下列有机物中最难反应的是___________(填
标号)。
A.苯( ) B.吡啶( )
C.环已-1,3-二烯( ) D.环己-1,4-二烯( )
(6) 以 , 为主要原料合成 。
利用上述信息补全合成路线。
20. (12分)利用 C a S 循环再生可将燃煤尾气中的 S O
2
转化生产单质硫,涉及的主要反应
如下:
Ⅰ. C a S ( s ) + 2 S O
2
( g ) C a S O
4
( s ) + S
2
( g ) Δ H
1
Ⅱ. C a S O
4
( s ) + 4 H
2
( g ) C a S ( s ) + 4 H
2
O ( g ) Δ H
2
Ⅲ. S O
2
( g ) + 3 H
2
( g ) H
2
S ( g ) + 2 H
2
O ( g ) H
3
恒容条件下,按 1 m o l C a S , 1 m o l S O
2
和 0 .1 m o l H
2
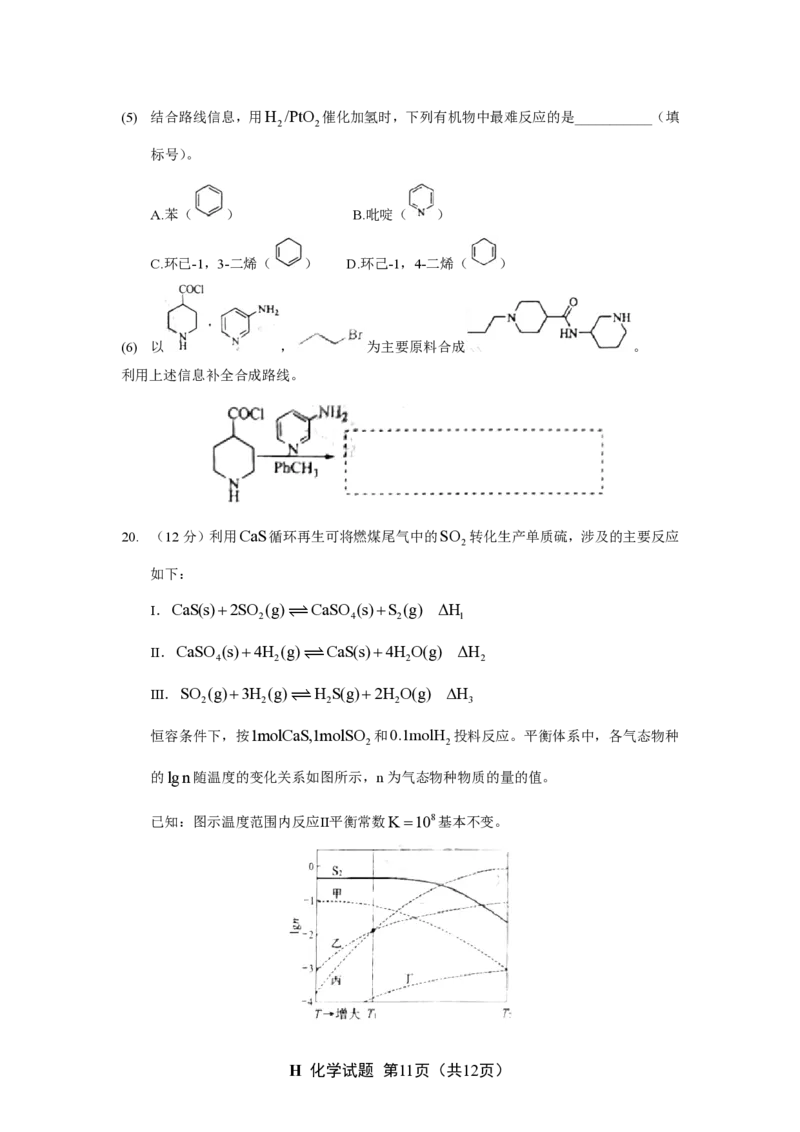
投料反应。平衡体系中,各气态物种
的 l g n 随温度的变化关系如图所示,n为气态物种物质的量的值。
已知:图示温度范围内反应Ⅱ平衡常数K=108基本不变。回答下列问题:
(1) 反 应
H 化学试题 第12页(共12页)
学科网(北京)股份有限公
4 H
2
( g ) + 2 S O
2
( g ) 4 H
2
O ( g ) + S
2
( g ) 的 焓 变 Δ H = ___________ ( 用 含
Δ H
1
,Δ H
2
的代数式表示)。
(2) 乙线所示物种为___________(填化学式)。反应Ⅲ的焓变 Δ H
3
___________0(填“>”“<”
或“=”)。
(3) T 温度下,体系达平衡时,乙线、丙线所示物种的物质的量相等,若丁线所示物种为
1
a m o l ,则 S
2
为___________ m o l (用含a的代数式表示);此时, C a S 与 C a S O
4
物质
的量的差值 n ( C a S ) − n ( C a S O
4
) = ___________ m o l (用含a的最简代数式表示)。
(4) T
2
温度下,体系达平衡后,压缩容器体积 S
2
产率增大。与压缩前相比,重新达平衡时,
H
2
S 与 H
2
n(H S)
物质的量之比 2 ___________(填“增大”“减小”或“不变”),
n(H )
2
H
2
O 物质
的量 n ( H
2
O ) ___________(填“增大”“减小”或“不变”)。