文档内容
2025 届云南三校高考备考实用性联考卷(七)
化学评分细则
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
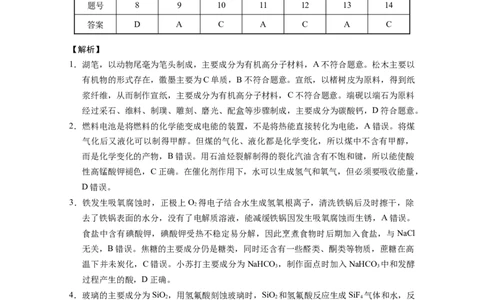
题号 1 2 3 4 5 6 7
答案 D C D B B B D
题号 8 9 10 11 12 13 14
答案 D A C A C A C
【解析】
1.湖笔,以动物尾毫为笔头制成,主要成分为有机高分子材料,A不符合题意。松木主要以
有机物的形式存在,徽墨主要为C单质,B不符合题意。宣纸,以楮树皮为原料,得到纸
浆纤维,从而制作宣纸,主要成分为有机高分子材料,C不符合题意。端砚以端石为原料
经过采石、维料、制璞、雕刻、磨光、配盒等步骤制成,主要成分为碳酸钙,D符合题意。
2.燃料电池是将燃料的化学能变成电能的装置,不是将热能直接转化为电能,A错误。将煤
气化后又液化可以制得甲醇。但煤的气化、液化都是化学变化,所以煤中不含有甲醇,
而是化学变化的产物,B错误。用石油烃裂解制得的裂化汽油含有不饱和键,所以能使酸
性高锰酸钾褪色,C正确。在催化剂作用下,水可以生成氢气和氧气,但必须要吸收能量,
D错误。
3.铁发生吸氧腐蚀时,正极上O 得电子结合水生成氢氧根离子,清洗铁锅后及时擦干,除
2
去了铁锅表面的水分,没有了电解质溶液,能减缓铁锅因发生吸氧腐蚀而生锈,A错误。
食盐中含有碘酸钾,碘酸钾受热不稳定易分解,因此烹煮食物时后期加入食盐,与NaCl
无关,B错误。焦糖的主要成分仍是糖类,同时还含有一些醛类、酮类等物质,蔗糖在高
温下并未炭化,C错误。小苏打主要成分为NaHCO ,制作面点时加入NaHCO 中和发酵
3 3
过程产生的酸,D正确。
4.玻璃的主要成分为SiO,用氢氟酸刻蚀玻璃时,SiO 和氢氟酸反应生成SiF 气体和水,反
2 2 4
应的方程式为SiO+4HF=SiF↑+2H O,A错误。氯气具有强氧化性,可以氧化硫代
2 4 2
硫酸根成硫酸根,氯气被还原为氯离子,反应的离子方程式为 +4Cl+5H O=
2 2
+8Cl−+10H+,B正确。试管壁上的银镜用稀硝酸清洗,银溶于稀硝酸生成硝酸银和
一氧化氮气体,该反应的离子方程式为 = ,C错
误。用草酸标准溶液测定高锰酸钾溶液的浓度, 被氧化为 , 属于弱
化学评分细则·第1页(共7页)
学科网(北京)股份有限公司酸,该反应的离子方程式为 = ,D错
误。
5.NO和CO 为等电子体有相似的结构为直线形分子,A正确。次氯酸的电子式为 ,
2 2
B错误。激发态Li原子的价层电子可能将2s电子激发到2p能级,C正确。σ键形成头碰
头,D正确。
6.该试验装置不需在试管口放置棉花,铁粉密度大不易阻塞导气管,A错误。由于该实验中
的反应生成 ,因此要使用稀盐酸先溶解,然后分别用硫氰化钾溶液、铁氰化钾溶液
来检验三价铁,二价铁,B正确。用木柴点燃肥皂泡检验生成的氢气,发现火焰为黄色,
是因为肥皂里面含有钠元素,焰色反应为黄色,而氢气燃烧的火焰颜色为淡蓝色,C错误。
酒精灯放在铁粉下方加热可以产生高温,且不影响水的蒸发,若移至湿棉花下方则难以
产生高温,则实验效果不好,D错误。
7.MgCl 溶液、AlCl 溶液与少量NaOH溶液反应时现象相同,分别产生白色 Mg(OH) 、
2 3 2
Al(OH) 沉淀,过量NaOH溶液反应时现象不相同,Al(OH) 沉淀能溶解,但Mg(OH) 不
3 3 2
能,从而能比较Mg(OH) 和Al(OH) 碱性的强弱,从而能比较Mg和Al的金属性强弱,A
2 3
能实现实验目的。在一支试管中依次加入一定量的乙醇、浓硫酸、乙酸,并且放入几粒
碎瓷片,另一支试管中加入适量饱和碳酸钠溶液,用酒精灯小心加热,乙酸与乙醇在浓
硫酸存在、加热条件下发生酯化反应生成乙酸乙酯和水,在饱和碳酸钠溶液液面上收集
乙酸乙酯,B能实现实验目的。向盛有 CuSO 溶液的试管中滴加氨水,首先产生蓝色
4
Cu(OH) 沉淀,继续滴加氨水,沉淀溶解得到深蓝色的[Cu(NH )]SO 溶液,然后再加入
2 3 4 4
乙醇,可制备 晶体,C能实现实验目的。硫酸铁溶液不能制备氢氧化铁胶
体。主要原因在于硫酸是难挥发性酸,无法从溶液中挥发,导致生成的氢氧化铁胶体会
立即聚沉,无法制得纯净的氢氧化铁胶体,D不能实现实验目的。
8.阿魏萜宁的分子式为C H O ,A正确。由分子结构可知,与醇羟基相连的C原子共与3
22 30 4
个不同化学环境的C原子相连,且这3个C原子上均连接了H原子,因此,该有机物发
生消去反应时,其消去反应产物最多有3种,B正确。该有机物酸性条件下的水解产物有
2种,其中一种含有碳碳双键和2个醇羟基,这种水解产物既能通过发生加聚反应生成高
聚物,也能通过缩聚反应生成高聚物;另一种水解产物含有羧基和酚羟基且羟基的两个
邻位上均有氢原子,其可以发生缩聚反应生成高聚物,C正确。该有机物分子中含有酚羟
基且其邻位上有H原子,故其可与浓溴水发生取代反应;还含有碳碳双键,故其可与
发生加成,因此,1mol该物质与 充分反应后,最多可消耗3mol ,D错误。
9.108g 的物质的量为 1mol,一个 分子中含有 16条 键,A正确。
化学评分细则·第2页(共7页)
学科网(北京)股份有限公司在水溶液中发生水解,1L1mol·L−1NH NO 溶液中含 的数目小于N ,B错误。
4 3 A
1molN 和3molH 在高温高压催化剂作用下,反应为可逆反应,充分反应生成NH 的数
2 2 3
目小于 ,C错误。NaO 与 反应,生成11.2L O ,转移电子数目为 。由于未给
2 2 2
出气体所处的状态,无法求出生成气体的物质的量,也无法得出转移电子数目,D错误。
10.三聚氰胺分子中含有氨基,氨基上还有一对孤对电子,所以氨基中的氮原子为sp3,A错
误。该反应为缩聚反应,线性聚合反应还要生成(n−1)的水,B错误。三聚氰胺分子六
元环上的碳、氮原子均为sp2杂化,所以该六元环为平面六边形,与之相连的氮原子也在
同一平面上,C正确。该线性聚合物不含酰胺基,D错误。
11.步骤Ⅰ涉及的是碳氢键的断裂和氢氧键的形成,步骤Ⅱ中涉及碳氧键的形成,A正确。
直接参与化学键变化的元素被替换为更重的同位素时,反应速率会变慢,则此时正反应
活化能会增大,根据图示可知, 与 反应的能量变化应为图中曲线a,B错误。
与 反应时,因直接参与化学键变化的元素被替换为更重的同位素时,步骤
Ⅰ 的 活 化 能 增 大 , 反 应 速 率 会 变 慢 , 则 CHDOD 更 难 获 得 , 故 产 率 :
2
,C错误。过渡态1比过渡态2相对
能量高,所以更不稳定,D错误。
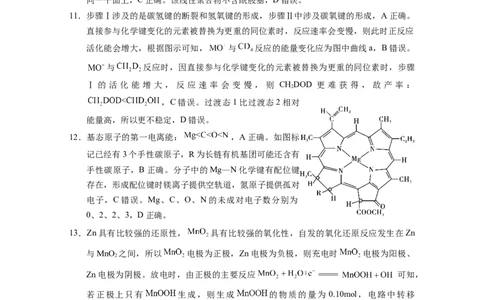
12.基态原子的第一电离能: ,A正确。如图标
记已经有3个手性碳原子,R为长链有机基团可能还含有
手性碳原子,B正确。分子中的Mg—N化学键有配位键
存在,形成配位键时镁离子提供空轨道,氮原子提供孤对
电子,C错误。Mg、C、O、N的未成对电子数分别为
0、2、2、3,D正确。
13.Zn具有比较强的还原性, 具有比较强的氧化性,自发的氧化还原反应发生在Zn
与MnO 之间,所以 电极为正极,Zn电极为负极,则充电时 电极为阳极、
2
Zn电极为阴极。放电时,由正极的主要反应 = 可知,
若正极上只有 生成,则生成 的物质的量为 0.10mol,电路中转移
0.10mol 电子,Zn 电极质量减少 3.25g(物质的量为 0.050mol),但是正极上还有
生成,因此, 电极生成了0.10mol , 电极质量大于3.25g,A
错误。充电时该装置为电解池,电解池中阳离子向阴极迁移,即 向Zn电极方向迁
移,B正确。放电时 电极为正极,正极上检测到 和少量 ,则正
极上主要发生的电极反应是 = ,C正确。放电时,负
化学评分细则·第3页(共7页)
学科网(北京)股份有限公司极的电极反应为 = ,MnO 电极为正极电势较高,D正确。
2
14 . 在 溶 液 中 存 在 平 衡 : CHCOOH CHCOO−+H+ ( ① ) 、 Ag++CH COO−
3 3 3
CHCOOAg(aq)(②),Ag+的水解平衡Ag++H O AgOH+H+(③),随着pH的增大,
3 2
c(H+)减小,平衡①③正向移动,c(CHCOOH)、c(Ag+)小,pH较小时(约小于 7.8)
3
CHCOO−浓度增大的影响大于Ag+浓度减小的影响,CHCOOAg浓度增大,pH较大时
3 3
(约大于7.8)CHCOO−浓度增大的影响小于Ag+浓度减小的影响,CHCOOAg浓度减
3 3
小,故曲线Ⅰ表示 CHCOOH 的物质的量分数随 pH 变化的关系,曲线Ⅱ表示
3
CHCOO−的物质的量分数随pH变化的关系,曲线Ⅲ表示CHCOOAg的物质的量分数随
3 3
pH变化的关系。根据分析,曲线Ⅰ表示 的变化情况,A正确。由图可知,当
c(CHCOOH)=c(CHCOO−)时(即曲线Ⅰ和曲线Ⅱ的交点),溶液的 pH=m,则
3 3
CHCOOH的电离平衡常数K= =10−m,B正确。根据物料守恒,pH=n
3 a
时溶液中c(CHCOOAg)=0.02mol/L,同时有 的水解平衡Ag++H O AgOH+H+存
3 2
在,所以 c(Ag+)<0.08mol/L,C错误。pH=n时 =10−m,c(CHCOO−)=
3
=10n−mc(CHCOOH) , Ag++CH COO− CHCOOAg(aq) 的 K=
3 3 3
, c(Ag+)= , 由 图 可 知 pH=n 时 ,
c(CHCOOH)=c(CHCOOAg),代入整理得c(Ag+)= mol/L,D正确。
3 3
二、非选择题:本题共4小题,共58分。
15.(除特殊标注外,每空1分,共15分)
(1)粉碎固体增大固液接触面积,搅拌,升温等
(2)无法完全除去Fe元素(2分)
(3) = (2分)
(4) (2分)
(5)①负阳
② = (2分)
化学评分细则·第4页(共7页)
学科网(北京)股份有限公司(6) (2分)升高
【解析】由题中信息可知,用硫酸处理含有Co、Zn、Pb、Fe的单质或氧化物的废渣,得
到含有 、 、 、 、 等离子的溶液,Pb的单质或氧化物与硫酸反应
生成难溶的 ,则“滤渣1”为“酸浸”时生成的 ;向滤液中加入 将
氧化为 ,然后加入ZnO调节pH=4使 完全转化为 ,则“滤渣2”的
主要成分为 ,滤液中的金属离子主要是 、 和 ;最后“氧化沉
钴”,加入强氧化剂 ,将溶液中 氧化为 ,在 时 形成
沉淀,而 则被还原为 , 还会与溶液中的 发生归中反
应生成 ,得到 和 的混合物,“除钴液”主要含有ZnSO 、KSO ,
4 2 4
据此解答。
(3)由分析可知,该过程发生两个氧化还原反应,根据分析中两个反应的反应物、产物
与反应环境(pH=5),结合得失电子守恒、电荷守恒和原子守恒可写出其离子方程式为
= 。
( 4 ) 当 溶 液 时 , 恰 好 完 全 沉 淀 , 此 时 溶 液 中
,则 ,则
。 “ 除 钴 液 ” 的 , 即 , 则
, 此 时 溶 液 中
。
16.(除特殊标注外,每空2分,共14分)
(1) 容量瓶(1分)胶头滴管(1分)(错别字不得分)
(2)将生成的二氧化硫排入后续装置中,使其充分被吸收防止倒吸(1分)
(3) (或 )偏大I+SO+2H O=4H++2I−+
2 2 2
(4)催化剂(1分)不变
【解析】由题中信息可知,利用“燃烧—碘酸钾滴定法”测定钢铁中硫含量的实验中,
将氧气经干燥、净化后通入管式炉中将钢铁中硫氧化为 ,然后将生成的 导入碘
化学评分细则·第5页(共7页)
学科网(北京)股份有限公司液中吸收,通过消耗 碱性标准溶液的体积来测定钢铁中硫的含量。
(1)取 的碱性溶液和一定量的 固体,配制
碱性标准溶液(稀释了 50 倍后 的浓度为 ),还需要用
容量瓶配制标准溶液,还需要用胶头滴管定容。
(2)装置F中通气管末端多孔玻璃泡内置一密度小于水的磨砂浮子,其目的是防止倒吸,
因为磨砂浮子的密度小于水,若球泡内水面上升,磨砂浮子也随之上升,磨砂浮子可以
作为一个磨砂玻璃塞将导气管的出气口堵塞上,从而防止倒吸。
( 3 ) 由 S 元 素 守 恒 及 = 、 =
可得关系式3S~ ~ ~ ,若滴定消耗 碱性标准溶液 ,则
,
,样品中硫的质量分数是
。
(4)若装置D中瓷舟未加盖,燃烧时产生粉尘中含有铁的氧化物,铁的氧化物能催化
的氧化反应从而促进 的生成,因此,粉尘在该过程中的作用是催化剂;若滴定
过程中,有少量 不经 直接将 氧化成 ,从电子转移守恒的角度分析,
得到 被还原为 ,仍能得到关系式3S~ ~ ,测定结果不会变。
17.(除特殊标注外,每空2分,共14分)
(1)
(2)(a+c−2b)
(3)0.05
(4)5.0正向进行(1分)>(1分)
(5)404.44
【解析】(2)根据盖斯定律可知,①+③−② 2可得FeSO ·7HO(s)+FeSO·HO(s)=
4 2 4 2
2FeSO ·4HO(s),则 (a+c−2b) 。
4 2
(3)660K 时, ,因此,该反应用二氧化硫表示的反应速率
。
化学评分细则·第6页(共7页)
学科网(北京)股份有限公司(4)720K 时, ,因此,该反应的平衡总压 、平衡常数
2.5×2.5=6.25 大 于 , 则 此 时 反 应 正 向 进 行 ,
。
(5)提高温度,上述容器中进一步发生反应 (Ⅱ),在同
温同压下,不同气体的物质的量之比等于其分压之比,则 、
, 联 立 方 程 组 , 可 得 , 则 ,
。
18.(除特殊标注外,每空2分,共15分)
(1)羟基、碳碳双键(对一个得一分,多填一个扣一分,错别字不得分)
(2)5−甲基−1,3−苯二胺17
(3)
(4)取代反应(1分)
(5)
(6)9 、 (任写一种)
【解析】(6) 邻、间、对3种、 共6种,满足核磁共
振氢谱峰面积之比为6∶2∶1∶1的结构简式可为 、 。
化学评分细则·第7页(共7页)
学科网(北京)股份有限公司