文档内容
2025 年内蒙古自治区普通高等学校招生考试适应性测试
化学
注意事项:
1.答卷前考生务必将自己的姓名、考生号、座位号填写在答题卡上。本试卷满分100分。
2.作答时,将答案写在答题卡上。写在试卷上无效。
3.考试结束后,将试卷和答题卡一并交回。
可能用到的相对原子质量:
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一
项符合题目要求。
1. 内蒙古自治区作为我国重要的能源和战略资源基地,拥有丰富的自然资源。下列说法正确的是
A. 天然气的主要成分是CO和H B. 有色金属是指铜、金等有颜色的金属
2
C. 煤的直接液化是物理变化 D. 稀土元素是金属元素
的
2. 下列化学用语或表述正确 是
A. NaO 电子式: B. 209Bi和210Bi:互为同素异形体
2 2
C. CH 的空间结构:正方形 D. 基态Fe2+的价电子排布式:3d54s1
4
3. 化学革新催化体育发展,科技赋能铸就赛场荣光。下列有关说法正确的是
A. 碳纤维复合材料可增强羽毛球拍的强度,其成分属于单质
B. 聚氨酯泳衣能有效提升游泳速度,其成分属于天然高分子
C. 氯乙烷气雾剂可缓解运动扭伤疼痛,氯乙烷是乙烷的同系物
D. 防滑粉可吸汗防滑,其主要成分碳酸镁属于无机盐
4. 下列有关物质的工业制备反应正确的是
.
A 侯氏制碱:
B. 制硝酸: (浓)
C. 制氯气:
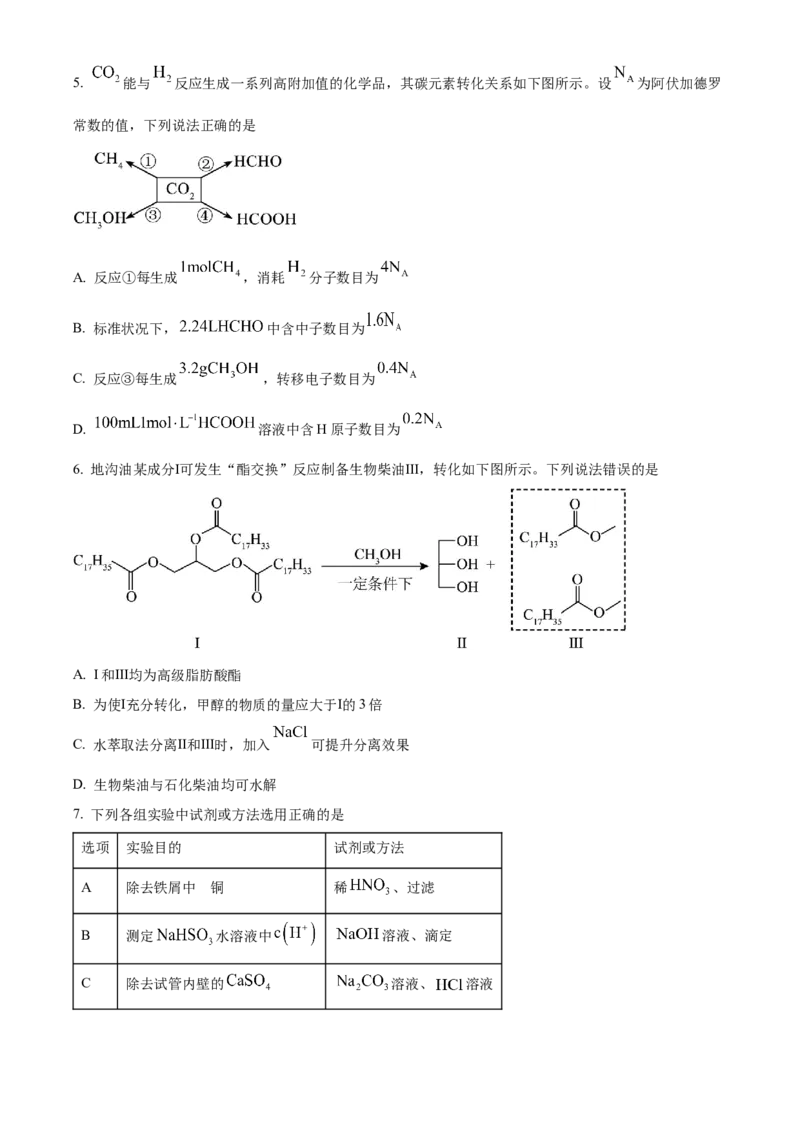
D. 冶炼铝:5. 能与 反应生成一系列高附加值的化学品,其碳元素转化关系如下图所示。设 为阿伏加德罗
常数的值,下列说法正确的是
A. 反应①每生成 ,消耗 分子数目为
B. 标准状况下, 中含中子数目为
C. 反应③每生成 ,转移电子数目为
D. 溶液中含H原子数目为
6. 地沟油某成分Ⅰ可发生“酯交换”反应制备生物柴油Ⅲ,转化如下图所示。下列说法错误的是
A. Ⅰ和Ⅲ均为高级脂肪酸酯
B. 为使Ⅰ充分转化,甲醇的物质的量应大于Ⅰ的3倍
C. 水萃取法分离Ⅱ和Ⅲ时,加入 可提升分离效果
D. 生物柴油与石化柴油均可水解
7. 下列各组实验中试剂或方法选用正确的是
选项 实验目的 试剂或方法
A 除去铁屑中 铜的稀 、过滤
B 测定 水溶液中 溶液、滴定
C 除去试管内壁的 溶液、 溶液D 分离乙醇和乙酸乙酯 直接分液
A. A B. B C. C D. D
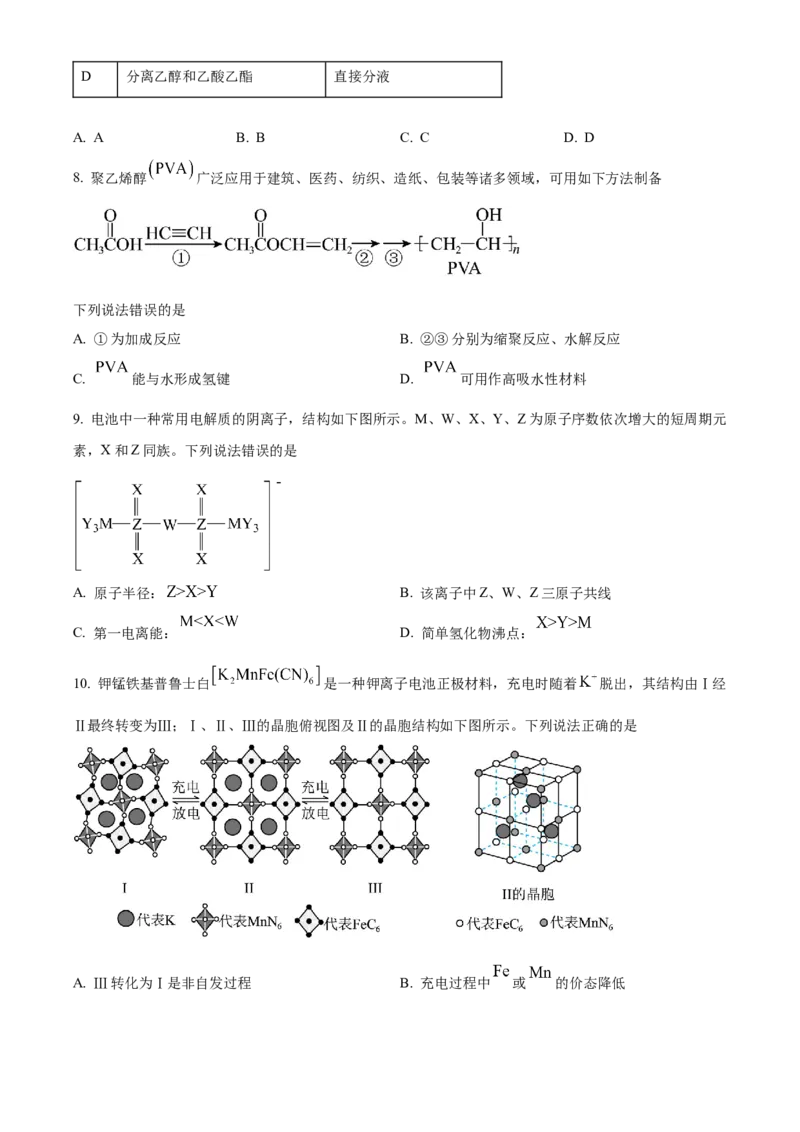
8. 聚乙烯醇 广泛应用于建筑、医药、纺织、造纸、包装等诸多领域,可用如下方法制备 。
下列说法错误的是
A. ①为加成反应 B. ②③分别为缩聚反应、水解反应
C. 能与水形成氢键 D. 可用作高吸水性材料
9. 电池中一种常用电解质的阴离子,结构如下图所示。M、W、X、Y、Z为原子序数依次增大的短周期元
素,X和Z同族。下列说法错误的是
A. 原子半径: B. 该离子中Z、W、Z三原子共线
C. 第一电离能: D. 简单氢化物沸点:
10. 钾锰铁基普鲁士白 是一种钾离子电池正极材料,充电时随着 脱出,其结构由Ⅰ经
Ⅱ最终转变为Ⅲ;Ⅰ、Ⅱ、Ⅲ的晶胞俯视图及Ⅱ的晶胞结构如下图所示。下列说法正确的是
A. Ⅲ转化为Ⅰ是非自发过程 B. 充电过程中 或 的价态降低C. 晶体Ⅱ的化学式为 D. 晶胞Ⅲ中 键数目为24
阅读下列材料,完成下列小题。
随着锂离子电池在众多领域的广泛应用,其废旧电池的回收工作愈发显得意义重大。现行的回收工艺通常
采用酸浸碱浸的方法,从锂离子电池正极材料 (含少量金属 )中提取 和 ,得到的
和 在空气中煅烧,可实现 的再生。与此同时,为达成绿色回收 和 的目标,
科研人员正在研究一种新型电解回收工艺。已知: 。
11. 一种现行回收工艺的流程如下图所示。下列说法正确的是
A. “浸取”反应中,正极材料成分为还原剂
B. “浸取”时 转化为 和
C. 滤液2中
D. 再生:
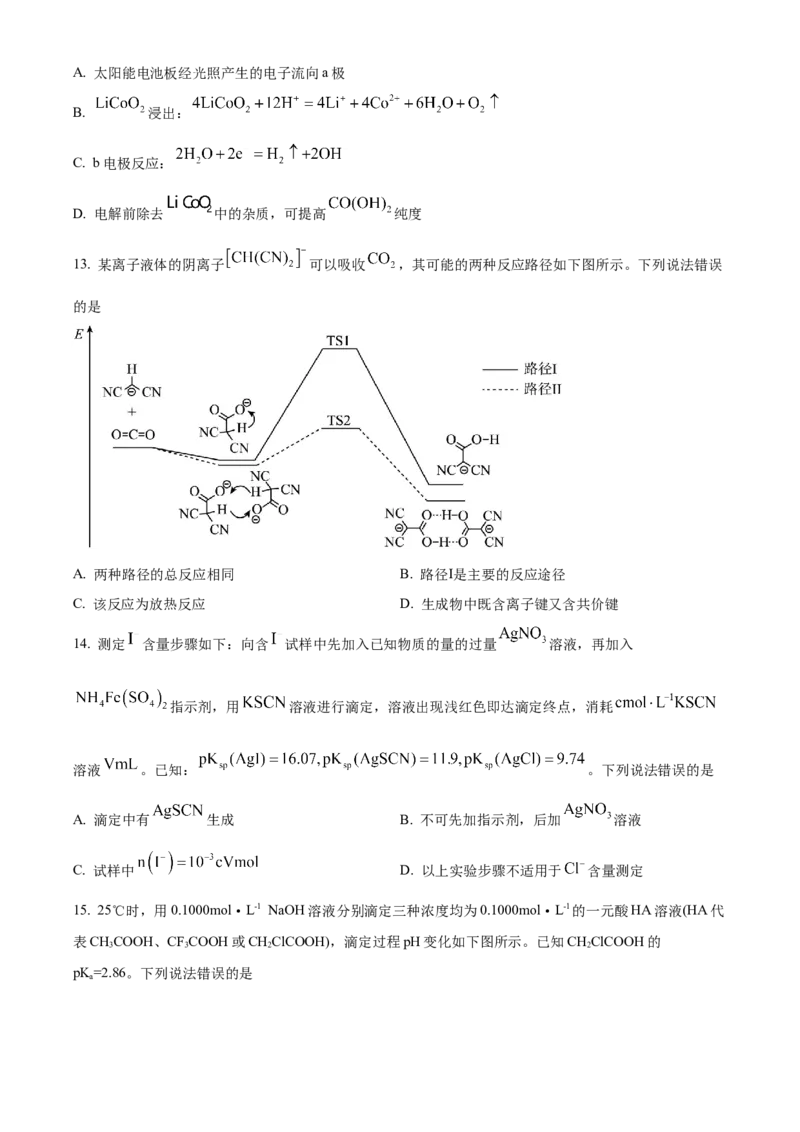
12. 电解回收工艺的原理如下图所示。下列说法错误的是A. 太阳能电池板经光照产生的电子流向a极
B. 浸出:
C. b电极反应:
D. 电解前除去 中的杂质,可提高 纯度
13. 某离子液体的阴离子 可以吸收 ,其可能的两种反应路径如下图所示。下列说法错误
的是
A. 两种路径的总反应相同 B. 路径Ⅰ是主要的反应途径
C. 该反应为放热反应 D. 生成物中既含离子键又含共价键
14. 测定 含量步骤如下:向含 试样中先加入已知物质的量的过量 溶液,再加入
指示剂,用 溶液进行滴定,溶液出现浅红色即达滴定终点,消耗
溶液 。已知: 。下列说法错误的是
A. 滴定中有 生成 B. 不可先加指示剂,后加 溶液
C. 试样中 D. 以上实验步骤不适用于 含量测定
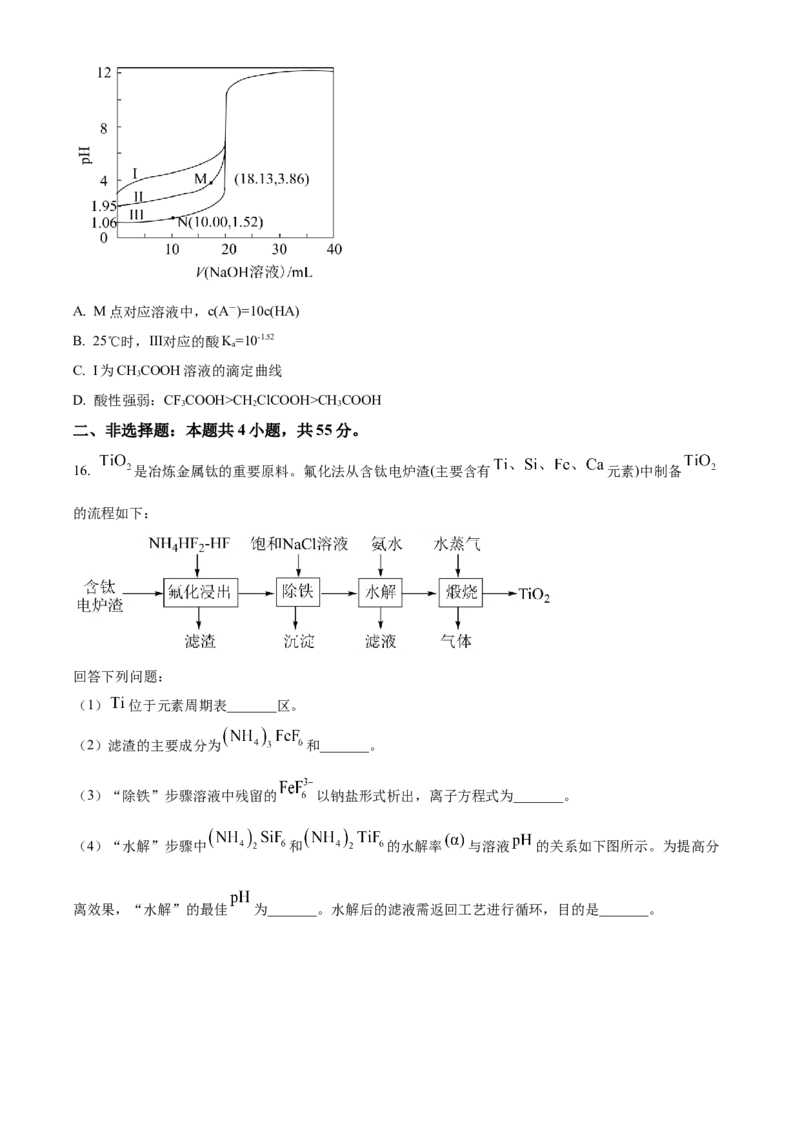
15. 25℃时,用0.1000mol·L-1 NaOH溶液分别滴定三种浓度均为0.1000mol·L-1的一元酸HA溶液(HA代
表CHCOOH、CFCOOH或CHClCOOH),滴定过程pH变化如下图所示。已知CHClCOOH的
3 3 2 2
pK=2.86。下列说法错误的是
aA. M点对应溶液中,c(A-)=10c(HA)
B. 25℃时,Ⅲ对应的酸K=10-1.52
a
C. Ⅰ为CHCOOH溶液的滴定曲线
3
D. 酸性强弱:CFCOOH>CH ClCOOH>CH COOH
3 2 3
二、非选择题:本题共4小题,共55分。
16. 是冶炼金属钛的重要原料。氟化法从含钛电炉渣(主要含有 元素)中制备
的流程如下:
回答下列问题:
(1) 位于元素周期表_______区。
(2)滤渣的主要成分为 和_______。
(3)“除铁”步骤溶液中残留的 以钠盐形式析出,离子方程式为_______。
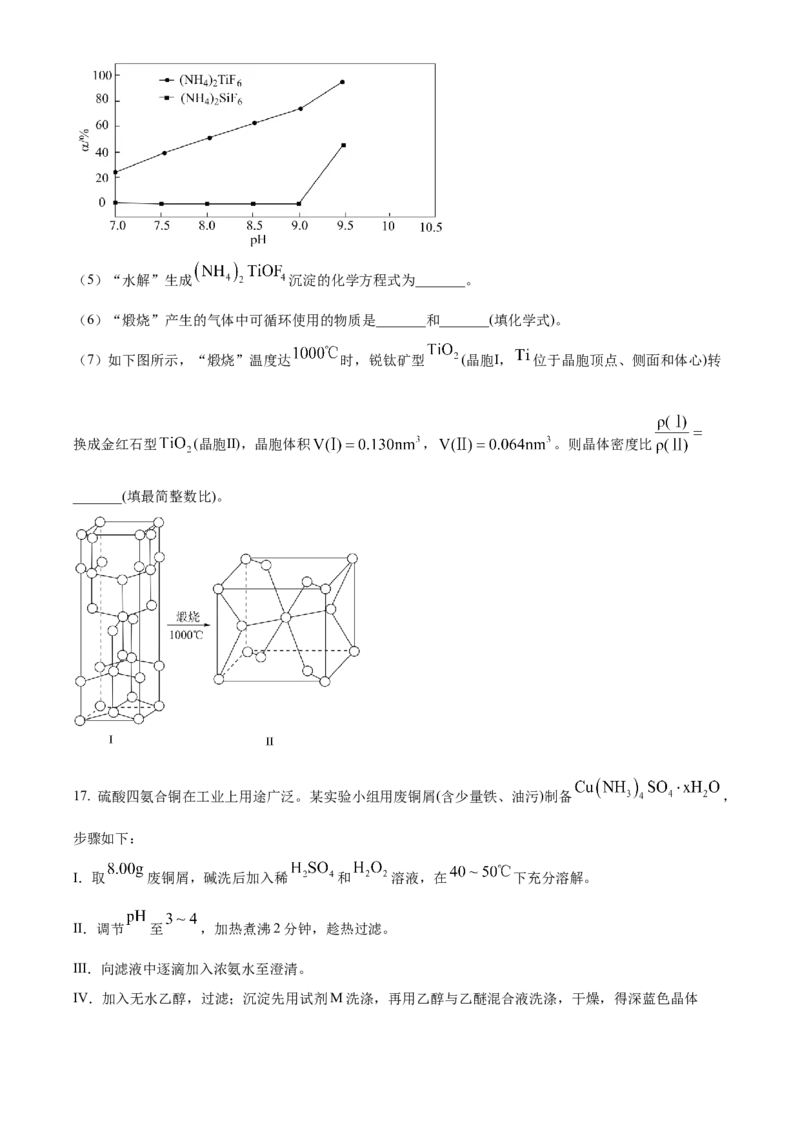
(4)“水解”步骤中 和 的水解率 与溶液 的关系如下图所示。为提高分
离效果,“水解”的最佳 为_______。水解后的滤液需返回工艺进行循环,目的是_______。(5)“水解”生成 沉淀的化学方程式为_______。
(6)“煅烧”产生的气体中可循环使用的物质是_______和_______(填化学式)。
(7)如下图所示,“煅烧”温度达 时,锐钛矿型 (晶胞Ⅰ, 位于晶胞顶点、侧面和体心)转
换成金红石型 (晶胞Ⅱ),晶胞体积 , 。则晶体密度比
_______(填最简整数比)。
17. 硫酸四氨合铜在工业上用途广泛。某实验小组用废铜屑(含少量铁、油污)制备 ,
步骤如下:
Ⅰ.取 废铜屑,碱洗后加入稀 和 溶液,在 下充分溶解。
Ⅱ.调节 至 ,加热煮沸2分钟,趁热过滤。
Ⅲ.向滤液中逐滴加入浓氨水至澄清。
Ⅳ.加入无水乙醇,过滤;沉淀先用试剂M洗涤,再用乙醇与乙醚混合液洗涤,干燥,得深蓝色晶体。
已知:硫酸四氨合铜溶液是深蓝色; 。
回答下列问题:
(1)步骤Ⅰ碱洗的目的是_______。
(2)步骤Ⅱ可除去溶液中的_______和_______(填离子符号或化学式)。
(3)步骤Ⅲ的实验现象为_______。
(4)步骤Ⅳ中试剂M应选用_______(填标号)。
A. 乙醇和浓氨水混合溶液 B. 蒸馏水
C. 乙醇和稀硫酸混合溶液 D. 溶液
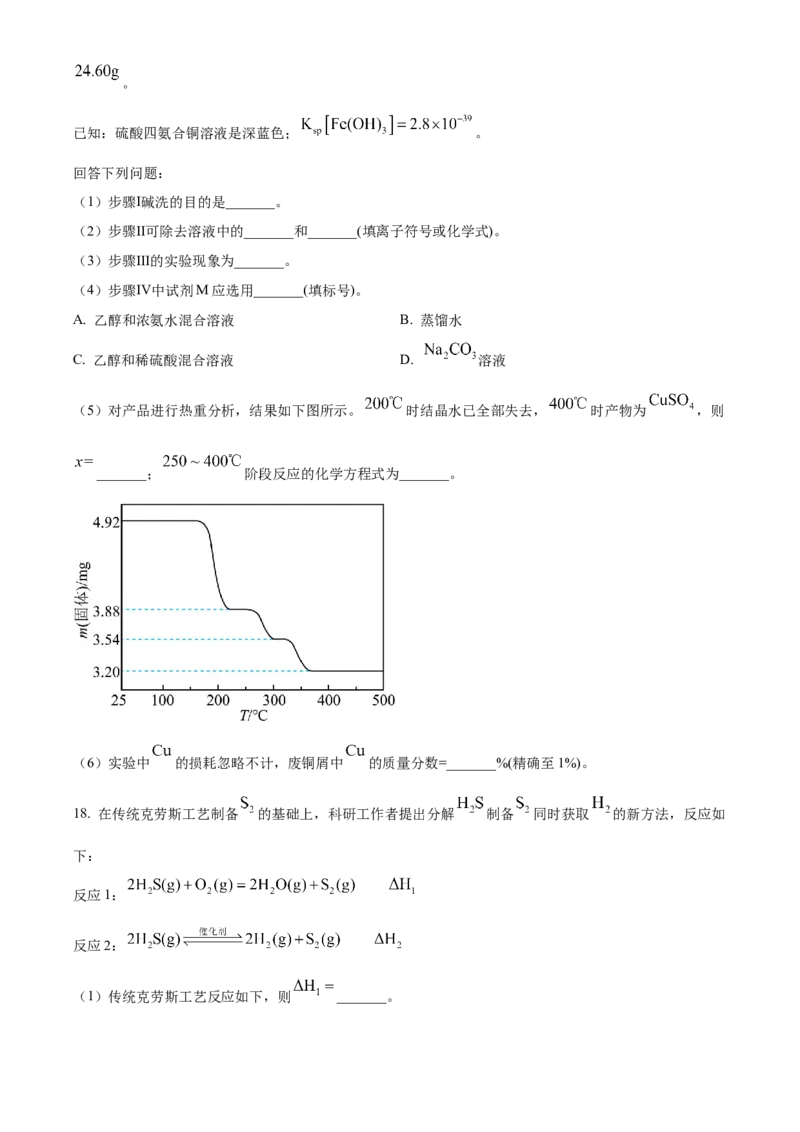
(5)对产品进行热重分析,结果如下图所示。 时结晶水已全部失去, 时产物为 ,则
_______; 阶段反应的化学方程式为_______。
(6)实验中 的损耗忽略不计,废铜屑中 的质量分数=_______%(精确至1%)。
18. 在传统克劳斯工艺制备 的基础上,科研工作者提出分解 制备 同时获取 的新方法,反应如
下:
反应1:
反应2:
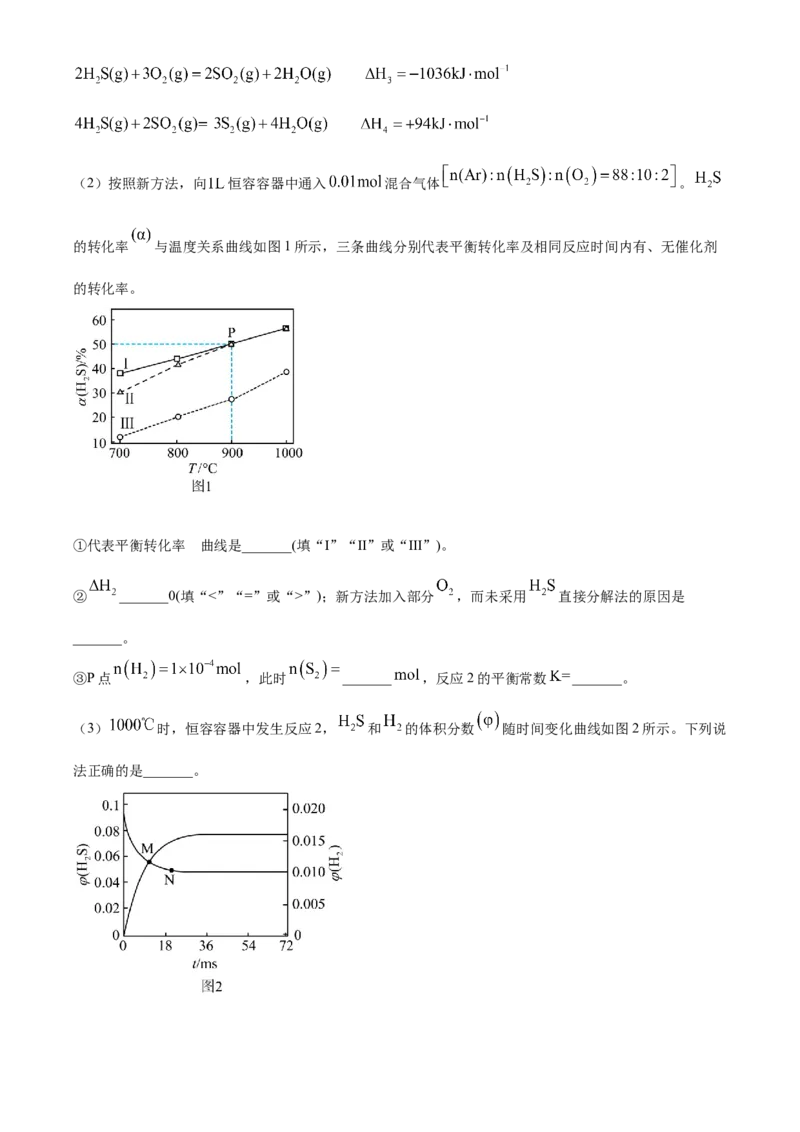
(1)传统克劳斯工艺反应如下,则 _______。(2)按照新方法,向 恒容容器中通入 混合气体 。
的转化率 与温度关系曲线如图1所示,三条曲线分别代表平衡转化率及相同反应时间内有、无催化剂
的转化率。
的
①代表平衡转化率 曲线是_______(填“Ⅰ”“Ⅱ”或“Ⅲ”)。
② _______0(填“<”“=”或“>”);新方法加入部分 ,而未采用 直接分解法的原因是
_______。
③P点 ,此时 _______ ,反应2的平衡常数 _______。
(3) 时,恒容容器中发生反应2, 和 的体积分数 随时间变化曲线如图2所示。下列说
法正确的是_______。A. 反应2在M点达到化学平衡状态 B. 时,通入 不变
C. 的反应速率: D. 时,降低温度, 的产率增加
(4) 可催化分解 。形成立方 时, 的 轨道分裂为两组。请参照基态原子核外电子排
布规律将 的价电子填充至图3中,完成轨道表示式_______。
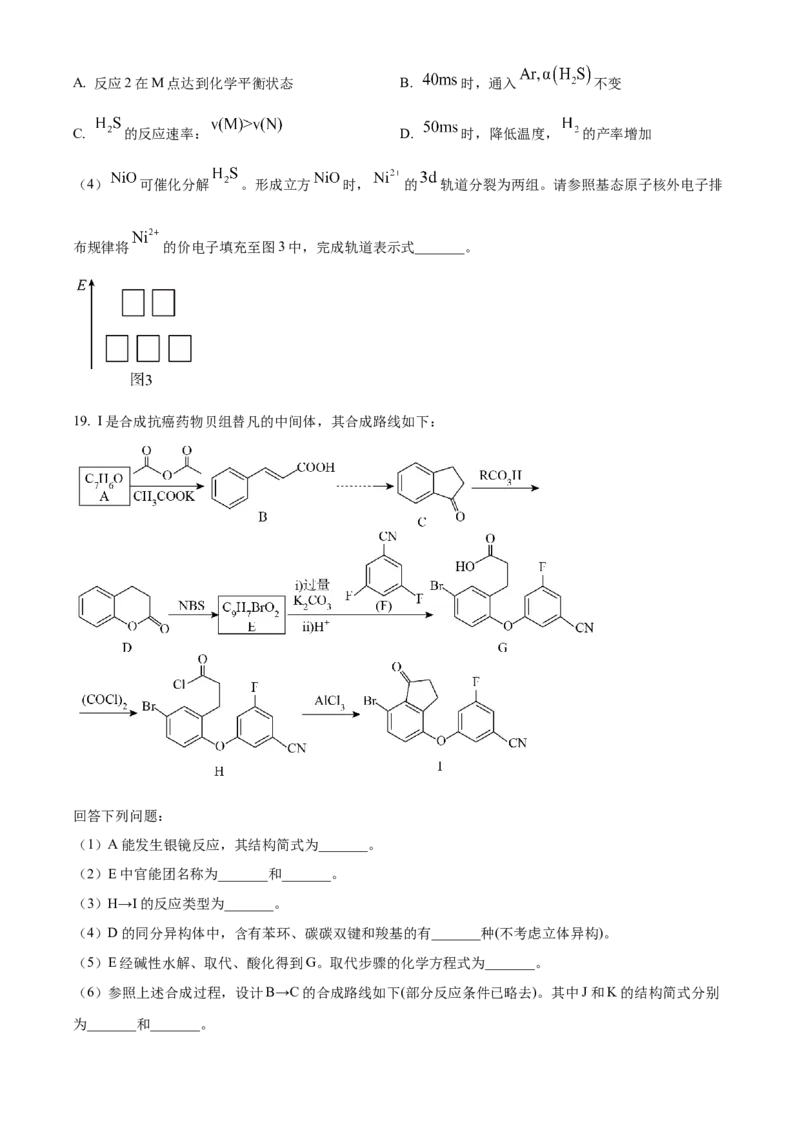
19. I是合成抗癌药物贝组替凡的中间体,其合成路线如下:
回答下列问题:
(1)A能发生银镜反应,其结构简式为_______。
(2)E中官能团名称为_______和_______。
(3)H→I的反应类型为_______。
(4)D的同分异构体中,含有苯环、碳碳双键和羧基的有_______种(不考虑立体异构)。
(5)E经碱性水解、取代、酸化得到G。取代步骤的化学方程式为_______。
(6)参照上述合成过程,设计B→C的合成路线如下(部分反应条件已略去)。其中J和K的结构简式分别
为_______和_______。