文档内容
贵阳第一中学 2026 届高考适应性月考卷(二)
化学评分细则
一、选择题:本题共14小题,每小题3分。在每小题给出的四个选项中,只有一项是符合题
目要求的。
题号 1 2 3 4 5 6 7
答案 D C A A D D B
题号 8 9 10 11 12 13 14
答案 B A B B C B C
【解析】
1.二氧化硫可以抑制葡萄酒中的细菌生长,利用二氧化硫的还原性还可以作抗氧化剂,A正
确。硫酸钡可用于医疗上作检查肠胃的内服药剂,即“钡餐”,B正确。二氧化硅为制作
光导纤维的原材料,其为酸性氧化物遇强碱会反应,C正确。玻璃钢是纤维增强塑料,不
是金属材料,D错误。
2. 是离子化合物,电子式为 ,A正确。 是三角锥形分子,
分子的球棍模型: ,B正确。中子数为1的氦核素,质量数为3,C错误。Cr是
24 号元素,基态 Cr 原子价层电子排布式为 3d54s1,价层电子轨道表示式为
,D正确。
3.电解NaCl溶液可以生成氢气和氯气,两者发生化合反应生成 HCl,故过程中的物质转化
均可实现,A正确。FeCl 与NaOH溶液直接反应生成Fe(OH) 沉淀,而非Fe(OH) 胶体,
3 3 3
Fe(OH) 胶体制备需将饱和FeCl 溶液滴入沸水,B错误。Mg单质的制备需要电解熔融
3 3
, 正 确 的 物 质 转 化 : 海 水
, C 错 误 。 工 业 制
HNO 需NH 催化氧化生成NO,NO进一步氧化为NO ,NO 与水反应生成HNO ,缺少
3 3 2 2 3
NO→NO 步骤,D错误。
2
4.KHSO 晶体由K+和 构成,A正确。过量的 Na能与水反应生成 H ,H 体积大于
4 2 2
1.12L,B错误。1mol NH 中所含孤电子对数为2 N ,C错误。S 与足量O 在催化剂作
2 4 A 8 2
用下反应先生成SO ,SO 与O 反应生成SO 是可逆反应,生成SO 的数目小于0.8N ,D
2 2 2 3 3 A
错误。
学科网(北京)股份有限公司5.HI应拆开写成离子形式,A错误。NaHCO 过量会使OH-完全反应,故方程式为
3
+Ba2++2OH-=BaCO ↓+ +2H O,B错误。只能生成Al(OH) 沉淀,C错误。
3 2 3
6.A选项,过氧化钠易溶于反应液,不可实现固液分离,因此不能用启普发生器的简易装置。
B选项,CO 与NaCO 溶液反应,应为饱和NaHCO ;C选项,乙醇蒸气能使KMnO (H+)
2 2 3 3 4
褪色。
7.酚能与NaCO 溶液反应;发生消去反应只能得到1种产物(不含立体异构);碳原子有
2 3
sp2和sp3两种杂化方式;碳碳双键与溴水发生加成反应,酚与浓溴水发生取代反应。
8.W、Y、Z为不同周期不同主族的短周期元素,Z形成一个共价键,Z为H元素,W形成
+2价阳离子,W为Mg元素,Y形成共价键(其中一个为配位键),Y为B元素,W、
Y、Z的最外层电子数之和等于X的最外层电子数,X形成两个共价键,X为O元素。电
负性O>B>Mg,A正确。X为O元素,价层电子对为4,杂化方式为sp3杂化,Y为B,
周围形成四个单键,价层电子对为4,杂化方式为sp3,B错误。X为O元素,与W、Z分
别形成MgO、HO,晶体类型分别是离子晶体、分子晶体,类型不同,C正确。O2−和
2
Mg2+有相同的电子层结构,半径O2−>Mg2+,D正确。
9.钠与水反应比钠与乙醇反应剧烈,说明水中的羟基比乙醇中的羟基活泼,A正确。
CH=CHCHO中的醛基也可以使酸性高锰酸钾溶液褪色,不能检验碳碳双键的存在,B
2
错误。测定相同温度相同浓度的 CHCOONa和NaCO 溶液的pH,只能说明CHCOOH
3 2 3 3
和 的电离能力,C错误。苯酚与溴水反应生成的三溴苯酚溶于苯中,不能过滤除去,
D错误。
10.镁原子位于铁原子构成的四面体空隙中,A正确。该晶胞参数为 nm,Mg与Fe之间
的最近距离为 nm,B错误。与铁原子最近的铁原子数有12个,C正确。储氢后的
晶体化学式为 ,晶体密度为 ,D正确。
11. 在电极M上,CHCOOH失去电子生成CO ,发生氧化反应,为阳极;在电极N上,
3 2
得到电子生成 ,发生还原反应,为阴极;电极a为正极,电极b为负
极,在电解池中,阳离子向阴极移动。由装置图可知, 极为阳极, 极为阴极,所
以 电 极 的 电 势 比 电 极 的 高 , A 错 误 。 极 的 电 极 反 应 式 为
,B 正确。M 极有 1mol CHCOOH 反应时,有
3
学科网(北京)股份有限公司通 过 质 子 交 换 膜 由 左 向 右 移 动 , C 错 误 。 M 极 的 电 极 反 应 式 为
= ,根据 极的电极反应式可知,当生成
(0.1mol)苯酚时,生成 的质量为 ,D错误。
12.“酸浸”时,CaCO 与稀盐酸中的 H+反应,生成 Ca2+、CO 和 HO,离子方程式为
3 2 2
CaCO +2H+ =Ca2++HO+CO↑,A 正确。酸浸时,废渣中的 CaCO 、SrCO 、
3 2 2 3 3
MgCO 与稀盐酸反应生成Ca2+、Sr2+、Mg2+,SrSO 难溶于稀盐酸留在浸出渣1中,B正
3 4
确。由SrCl 溶液制备SrCl ·6H O需采取的操作为蒸发浓缩(控温至60~100℃),冷却
2 2 2
结晶,C 错误。“盐浸”中,浸出渣 1 含 SrSO ,加入 BaCl 后,因 K (BaSO)<
4 2 sp 4
K (SrSO ),发生沉淀转化: ,其反应的平衡常数K=
sp 4
=103.51,D正确。
13.由图知,反应①:2NH +2H+= ;
3
反应②: +NO=[(NH )(NO )]2+;
2 4 2 2
反应③:[(NH )(NO )]2++NO=[(NH )(HNO)]++H++N +H O;
4 2 2 4 2 2 2
反应④:[(NH )(HNO)]++H+=2H++N +2HO,抵消方程式两边的 1 个 H+,可得
4 2 2 2
[(NH )(HNO)]+ =H++N +2HO。由图可知,反应历程由NH 与H+发生反应①开始,
4 2 2 2 3
后H+又再次生成,因此H+是催化剂,A正确。根据化合价变化规律—“只靠近不交
叉”及化合价升降数目相等可知,反应③[(NH )(NO )]2++NO=[(NH )(HNO)]++H+
4 2 2 4 2
+N +H O~3e-,因此若2 mol NO参与反应,则反应③转移电子数为6mol,B错误。由分
2 2
析知,反应②为2 +2NO=[(NH )(NO )]2+,“多变一”,属于化合反应, C正
2 4 2 2
确。由图可知,总反应为NH 、NO、NO 等在一定条件下生成N 和HO,根据图中物质
3 2 2 2
系数可知总反应为 ===== ,D正确。
14.根据图示,两个交点,说明 为二元弱酸, ,
在曲线最左边溶液酸性较强时,主要组分是 ,所以曲线①代表 ,曲线②代
表 ,曲线③代表 ,以此解题。由分析可知,曲线①代表 ,曲线②
代表 ,A正确。结合分析可知,曲线②代表 ,曲线③代表 ,由图
可 知 , 时 , B 正 确 。 a 点 , ,
学科网(北京)股份有限公司, 同 理 可 知 , , 而 的
,水解大于电离,c(H A)大于c(A2−),C错误。结合C的分析
2
可知, 的第一步电离平衡常数 =10−6.3,D正确。
二、非选择题:本题共4小题,共58分。
15.(除特殊标注外,每空2分,共15分)
(1)三颈烧瓶(1分) 防倒吸
(2) = 或 =
( 3 ) 当 加 入 时 , 增 大 , 使
平 衡 向 左 移 动 , 促 使
析出 或
加热浓缩过程中 挥发,使 平衡向右移动,且 发
生水解生成氢氧化铜或碱式硫酸铜
(4) 中存在 ,用稀硫酸溶解该配合物时,H⁺
与 发生中和反应,使平衡正向移动,释放出Cu²⁺且抑制了铜离子的水解(从H+与
NH 配位能力强于Cu2+与NH 配位能力角度答均可给分)
3 3
(5)98.4%或0.984
【解析】(1)盛装硫酸铜溶液的仪器名称为三颈烧瓶;氨气极易溶于水,将A装置产生
的气体持续通入B装置中,使用仪器a而不使用长导管通入的原因是防倒吸。
(2)B中氨气通入硫酸铜溶液中生成四氨合铜离子,反应方程式为 =
或 = 。
( 3 ) 当 加 入 时 , 增 大 , 使
平 衡 向 左 移 动 , 促 使
析 出 ; 加 热 浓 缩 过 程 中 挥 发 , 使
平衡向右移动,且 发生水解生成氢氧化铜或碱式硫
酸铜。
(4) 中存在 ,用稀硫酸溶解该配合物时,H⁺
学科网(北京)股份有限公司与 发生中和反应,破坏了 中Cu—NH 配位键的稳定性,释放出Cu2+。
3
(5)Cu2+与过量I-作用,生成I 和CuI,反应方程式为2Cu2++4I-=2CuI↓+I ,向该溶
2 2
液中滴加 NaSO 标准溶液,I 会发生反应 I+ = +2I-,可得关系式
2 2 3 2 2
2Cu2+~I ~ ,反应消耗的 的物质的量 =0.050mol/L×0.016L×
2
=0.004mol,则溶液中含有Cu2+的物质的量n(Cu2+)= =0.004mol,根据
Cu 元素守恒可知反应产生的[Cu(NH )]SO ·HO]的物质的量是 0.004mol,其质量是
3 4 4 2
m{[Cu(NH )]SO ·HO}=0.004mol×246g/mol=0.984g , 因 此 该 物 质 的 纯 度 是
3 4 4 2
(0.984g÷1.00g)×100%=98.4%或0.984。
16.(除特殊标注外,每空2分,共14分)
(1)5d106s1(1分)
(2)硝酸(1分)
(3) =
(4)12 12 Au+HNO +4HCl=H[AuCl ]+NO↑+2HO
3 4 2
(5)提高金的浸出率(或提高金的产率,或减小金的损失,合理即可)
(6)(适度)增大溶液中c(CN-)/增大CN-的用量
【解析】(1)Cu是第四周期ⅠB族元素,Cu的价电子排布式为3d104s1,Au与Cu同族
且比Cu多两个电子层,基态Au原子的价电子排布式为5d106s1。
(2)根据流程图,步骤2中Ag溶于酸,由于硫酸银微溶,氯化银难溶,所以步骤2中浸
出应选用硝酸。
(3)步骤4浸出的目的是将单质Au转化为 进入溶液,则KCN、氧气、Au在
碱性条件下反应生成 ,根据得失电子守恒、电荷守恒和原子守恒,该反应的
离子方程式为 = 。
(4)以顶点的Au原子为研究对象,与之距离最近且相等的Cu原子位于面心,每个顶点
的Au原子被8个晶胞共用,每个面心的Cu原子被2个晶胞共用,所以Au的配位数为
=12。根据均摊法,晶胞中Au原子的个数为8× =1,Cu原子的个数为6× =3,该
合金的化学式为AuCu ,Au的质量分数为 =50.6%,为12K金。已知浓硝酸
3
与浓盐酸比例为1∶3时溶解Au效果好,HNO 被还原为NO,Au被氧化结合Cl-生成
3
[AuCl ]-,化学方程式为Au+HNO +4HCl=H[AuCl ]+NO↑+2HO。
4 3 4 2
(5)步骤6中洗涤液和滤液合并利用,可减少金的损失,因此目的是提高金的浸出率。
学科网(北京)股份有限公司( 6 ) 根 据 步 骤 7 置 换 的 总 反 应 , 结 合
知,为防止生成 沉淀影响
置换速率,可采取的措施是适度增大溶液中c(CN-),使锌元素以 形式存在。
17.(除特殊标注外,每空2分,共14分)
(1)①−90.7kJ/mol ②D
(2)① (1分) (1分) ②增大初始水碳比,平衡逆向移动,不利于尿素生成
③ 或0.125
(3)①乙醇胺含有氨基,有碱性,可与二氧化碳和水反应生成盐
② 环上连有甲基,使得活性点位减少/使结合能力下降
【 解 析 】 ( 1 ) ① 根 据 盖 斯 定 律 可 知 ,
;
② 不能表明正逆反应速率相等,当 才可以说明正
逆反应速率相等,才能判断是平衡状态,A不选。设 的变化量为x,列三段式:
, 的体积分数
为 ,故其体积分数始终保持50%不变,其体积分数不再改
变,不能判定为平衡状态,B不选。该体系为恒容环境,且该反应全部由气体参与,故
m(气)、V均为定值,密度始终保持不变,故密度不可作为判断平衡状态的依据,C不选。
CO 与H 未按照化学计量数之比进行投料,二者物质的量之比是变量,当其保持不变,
2 2
说明正逆反应速率相等,达到了平衡状态,D选。
(2)①根据反应Ⅰ可知,氨碳比 比越大,相当于增大NH 的浓度,平衡正向移
3
动,CO 平衡转化率越大,则 > ,水碳比 越小,相当于减小HO(g)的浓度,
2 2
反应Ⅰ正向移动,CO 平衡转化率越大,则 < 。
2
学科网(北京)股份有限公司②增大初始水碳比 ,相当于增大HO(g)的浓度,平衡逆向移动,不利于尿素生
2
成。
③当CO 平衡转化率为20%时,列三段式:
2
K=
当CO 平衡转化率为80%时,列三段式:
2
K= ,解得V= L或0.125L。
(3)①乙醇胺溶液能够吸收CO 的原因是乙醇胺含有氨基,有碱性,可与二氧化碳和水
2
反应生成盐;
②由题目信息可知, 中的三个位置均可能捕获CO , 环上连有甲基,使得
2
活性点位减少。
18.(除特殊标注外,每空2分,共15分)
(1)催化(1分) 无有毒气体二氧化硫产生
(2)酯基、羟基
(3)
(4)sp2和sp3 4
(5)
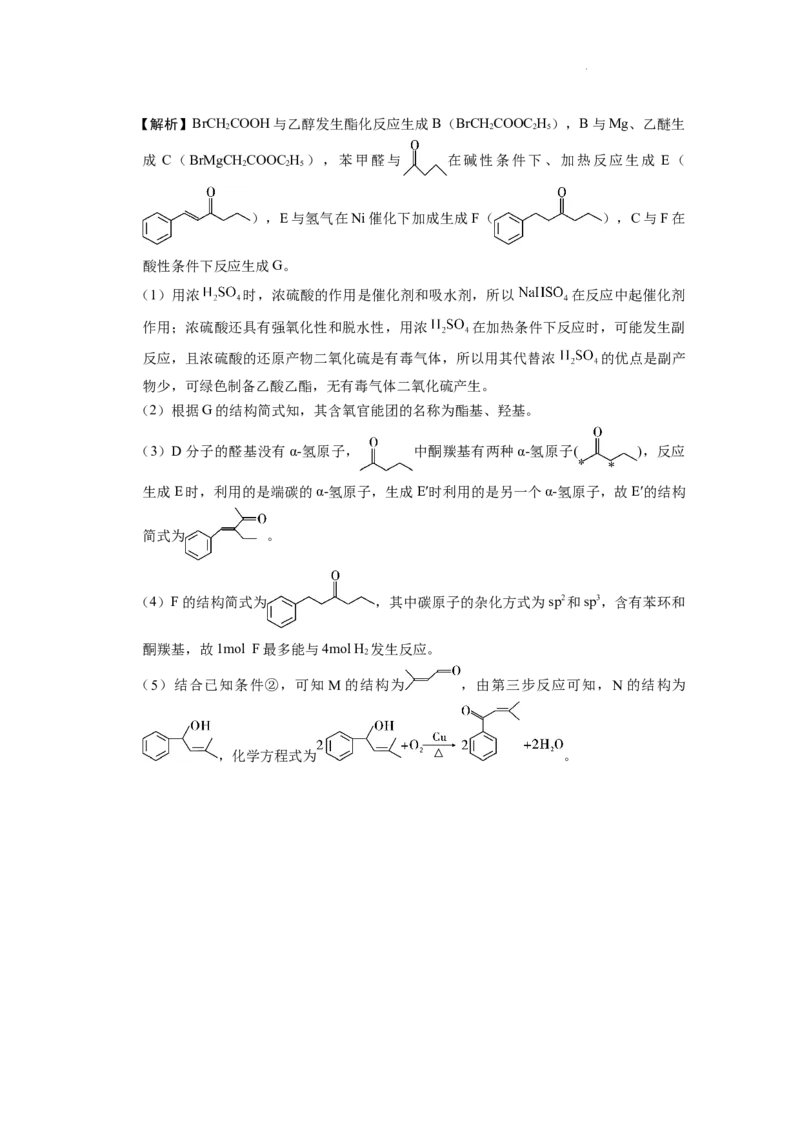
学科网(北京)股份有限公司【解析】BrCHCOOH与乙醇发生酯化反应生成B(BrCHCOOC H ),B与Mg、乙醚生
2 2 2 5
成 C(BrMgCH COOC H ),苯甲醛与 在碱性条件下、加热反应生成 E(
2 2 5
),E与氢气在Ni催化下加成生成F( ),C与F在
酸性条件下反应生成G。
(1)用浓 时,浓硫酸的作用是催化剂和吸水剂,所以 在反应中起催化剂
作用;浓硫酸还具有强氧化性和脱水性,用浓 在加热条件下反应时,可能发生副
反应,且浓硫酸的还原产物二氧化硫是有毒气体,所以用其代替浓 的优点是副产
物少,可绿色制备乙酸乙酯,无有毒气体二氧化硫产生。
(2)根据G的结构简式知,其含氧官能团的名称为酯基、羟基。
(3)D分子的醛基没有α-氢原子, 中酮羰基有两种α-氢原子( ),反应
生成E时,利用的是端碳的α-氢原子,生成E′时利用的是另一个α-氢原子,故E′的结构
简式为 。
(4)F的结构简式为 ,其中碳原子的杂化方式为sp2和sp3,含有苯环和
酮羰基,故1mol F最多能与4mol H 发生反应。
2
(5)结合已知条件②,可知 M的结构为 ,由第三步反应可知,N的结构为
,化学方程式为 。
学科网(北京)股份有限公司