文档内容
2024-2025 学年高二化学上学期第一次月考卷
(考试时间:75 分钟 试卷满分:100 分)
注意事项:
1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。答卷前,考生务必将自己的姓名、准考证号
填写在答题卡上。
2.回答第Ⅰ卷时,选出每小题答案后,用 2B 铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡
皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。
4.测试范围:第 1 章~第 2 章第 2 节(人教版 2019 选择性必修 1)。
5.难度系数:0.68
6.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Fe 56
第Ⅰ卷(选择题 共 44 分)
一、选择题:本题共 16 个小题,共 44 分。第 1~10 小题,每小题 2 分;第 11~16 小题,每小题 4 分。在
每小题给出的四个选项中,只有一项是符合题目要求的。
1.能量与科学、技术、社会、环境关系密切。下列应用中能量转化关系错误的是
氧炔焰 车用燃料电池
A.化学能→机械能 B.化学能→电能
太阳能电池 水电站发电
C.太阳能→电能 D.机械能→电能
【答案】A
【解析】A.氧炔焰是将化学能转化为热能,A 错误;
B.车用燃料电池是将化学能转化为电能,B 正确;
/C.硅太阳能电池将太阳能转化为电能,C 正确;
D.水电站能将机械能转化为电能,D 正确;
故选 A。
2.下列说法正确的是
A.升高温度能使化学反应速率增大,主要原因是增加了反应物分子中活化分子的百分数
B.增加反应物的浓度,能增大活化分子百分数,所以反应速率增大
C.测定中和反应反应热的实验中,混合溶液的温度不再变化时,该温度为终止温度
D.测定中和反应反应热的实验中,测了盐酸溶液温度的温度计未洗涤立马测定氢氧化钠溶液的温度,
会使得 偏小
【答案】A
【解析】A.升高温度,反应物分子中活化分子的数目和百分数都增大,有效碰撞的次数增大,化学反
应速率增大,A 正确;
B.增大反应物浓度,可以增大单位体积内活化分子数,但单位体积内活化分子百分数不变,B 错误;
C.酸碱恰好反应完全时放热最多,所以测定中和反应热的实验中,混合溶液温度最高时的温度为终止
温度,C 错误;
D.测盐酸溶液温度的温度计未洗涤立马测定氢氧化钠溶液的温度时,所测 NaOH 溶液的温度偏高,温
度差偏小,反应热数值偏小,但中和热△H 为负值,值越小,△H 越大,D 错误;
故答案为:A
3.下列装置及设计不能达到实验目的的是
A.测定中和反应的反应热 B.探究反应物浓度对反应速率的影响
C.测定锌与稀硫酸反应生成氢气的速率 D.探究温度对化学平衡的影响
【答案】B
【解析】A.此装置中,内外桶中间有隔热层,内外桶口与杯盖相平,吻合度高,有温度计、环形玻璃
搅拌棒,则装置的保温效果好,最高温度的测定准确,A 正确;
B.实验通过改变 NaSO 的浓度探究浓度对反应速率的影响,若 NaSO 是反应物则正确,若 NaSO
2 4 2 4 2 4
作为催化剂或反应无关的物质,其浓度变化不会影响反应速率,B 错误;
C.锌与稀硫酸反应,测定相同时间内产生的氢气体积,或者产生相同体积氢气所用的时间,可测定平
均反应速率,C 正确;
/D.NO 呈红棕色,NO 呈无色,依据热水中圆底烧瓶内气体的颜色与冷水中圆底烧瓶内气体的颜色的
2 2 4
深浅,可确定平衡移动的方向,从而确定温度对化学平衡的影响,D 正确;
故选 B。
4.化学与生产、生活密切相关。下列事实与化学反应速率无关的是
A.食盐中添加碘酸钾 B.锌粉和稀硫酸反应时常常加入少量铜粉
C.医护人员冷藏存放“新冠”疫苗 D.工业矿石冶炼前先将矿石粉碎
【答案】A
【解析】A.食盐中添加碘酸钾是防止碘缺乏病,与化学反应速率无关,A 项符合题意;
B.锌粉和稀硫酸反应时常常加入少量铜粉,可形成原电池,加快反应速率,与化学反应速率有关,B
项不符合题意;
C.医护人员冷藏存放“新冠”疫苗,可以降低温度,减慢疫苗(蛋白质)变性的速率,与化学反应速率有关,
C 项不符合题意;
D.工业矿石冶炼前先将矿石粉碎,可以增大接触面积,加快反应速率,与化学反应速率有关,D 项不
符合题意;
故选 A。
5.将 11.2g 铁粉投入到盛有 200mL3mol/L 稀盐酸的烧杯中,5min 时铁粉刚好完全溶解(溶解前后溶液体
积变化忽略不计),下列表示此反应的速率正确的是
A. B.
C. D.
【答案】C
【分析】Fe 的物质的量为 =0.2mol,由 可知,参加反应的 HCl 的物质的
量为 0.4mol,生成 FeCl 、H 的物质的量都是 0.2mol。
2 2
【解析】A.Fe 为纯固体,不能用其浓度变化量表示化学反应速率,A 错误;
B. ,B 错误;
C.在同一反应中,不同物质表示的化学反应速率之比等于化学计量数之比,则
,C 正确。
D.由 B 中可知, = =0.0067mol·L-1·s-1,D 错误;
故选 C。
6.在恒温恒容密闭容器中投入足量 ,发生反应: 。下列说法
正确的是
/A.平衡常数表达式为
B.若 的体积分数不再改变,则达到平衡
C.平衡后充入更多的 和 ,达到新平衡时其浓度均增大
D.可用单位时间内 质量变化来表示反应快慢
【答案】D
【解析】A.CaC O、CaO 呈固态,则平衡常数表达式为 K=c(CO)·c(CO),A 项错误;
2 4 2
B.分析此反应,产物中只有 、 为气体,化学计量数固定, 体积分数始终为 ,B 项错误;
C.起始投入足量 CaC O,平衡时 CO 和 CO 物质的量相等,平衡后充入等物质的量的 CO 和 CO,增
2 4 2 2
大生成物浓度平衡逆向移动,但温度不变,平衡常数不变,则达到新平衡时其浓度均不变,C 项错误;
D.任何化学反应的快慢都表现为有关物质的量随着时间变化的多少,故该反应可用单位时间内 CaO 质
量净增量比较反应快慢,D 项正确;
故选 D。
7.一定温度下的密闭容器中,可逆反应 达到平衡状态的标志是
A. 、 、 在容器中共存 B.
C.浓度商等于化学平衡常数 D.体系内物质的总质量不变
【答案】C
【解析】A. 是可逆反应,任何时刻 、 、 在容器均中共存,不
能说明反应处于平衡状态,A 不符合题意;
B.正逆反应速率之比等于化学计量数之比时:v 正(H )=3v 逆(N )说明正逆反应速率相等,则 3v 正(H )
2 2 2
=v 逆(N ),说明正逆反应速率不相等,反应未达平衡状态,B 不符合题意;
2
C.浓度商大于化学平衡常数时从逆反应建立平衡,浓度商小于化学平衡常数时从正反应建立平衡,浓
度商等于化学平衡常数,说明反应处于平衡状态,C 符合题意;
D.质量守恒,体系内物质的总质量始终不变,不能说明反应处于平衡状态,D 不符合题意;
故选 C。
8.已知:① ;
②
1molCH CHCHCH(g)转化为 的热量变化为
3 2 2 3
A.放出 9kJ B.吸收 9kJ C.放出 17kJ D.吸收 18kJ
【答案】A
【解析】由盖斯定律可知,反应①—反应②得到反应 ,则反应△H=
/(—2878kJ/mol)—(—2869kJ/mol)=—9kJ/mol,所以 1molCH CHCHCH(g)转化为 放出的热
3 2 2 3
量为 9kJ/mol×1mol=9kJ,故选 A。
9.下列说法正确的是
A.C(石墨 s) C(金刚石,s) ,则金刚石比石墨稳定
B.同温同压下, 在光照和点燃条件下的 不同
C.用 溶液和 NaOH 溶液反应测定中和热的
D. ,则碳的燃烧热等于
【答案】C
【解析】A.C(石墨 s) C(金刚石,s) ,石墨具有的能量低于金刚石,则石墨比金刚石
稳定,故 A 错误;
B.同温同压下, 在光照和点燃的条件下 相同, 与反应条件无关,只与
反应物和生成物所具有的总能量有关,故 B 错误;
C.CHCOOH 是一元弱酸,电离过程吸热,使放出热量减小,测定中和热的 ,故 C 正
3
确;
D.燃烧热是 1mol 纯净的可燃物完全燃烧生成指定产物放出的热量,碳燃烧的指定产物是二氧化碳,而
一氧化碳不是指定产物,故 D 错误;
故答案为 C。
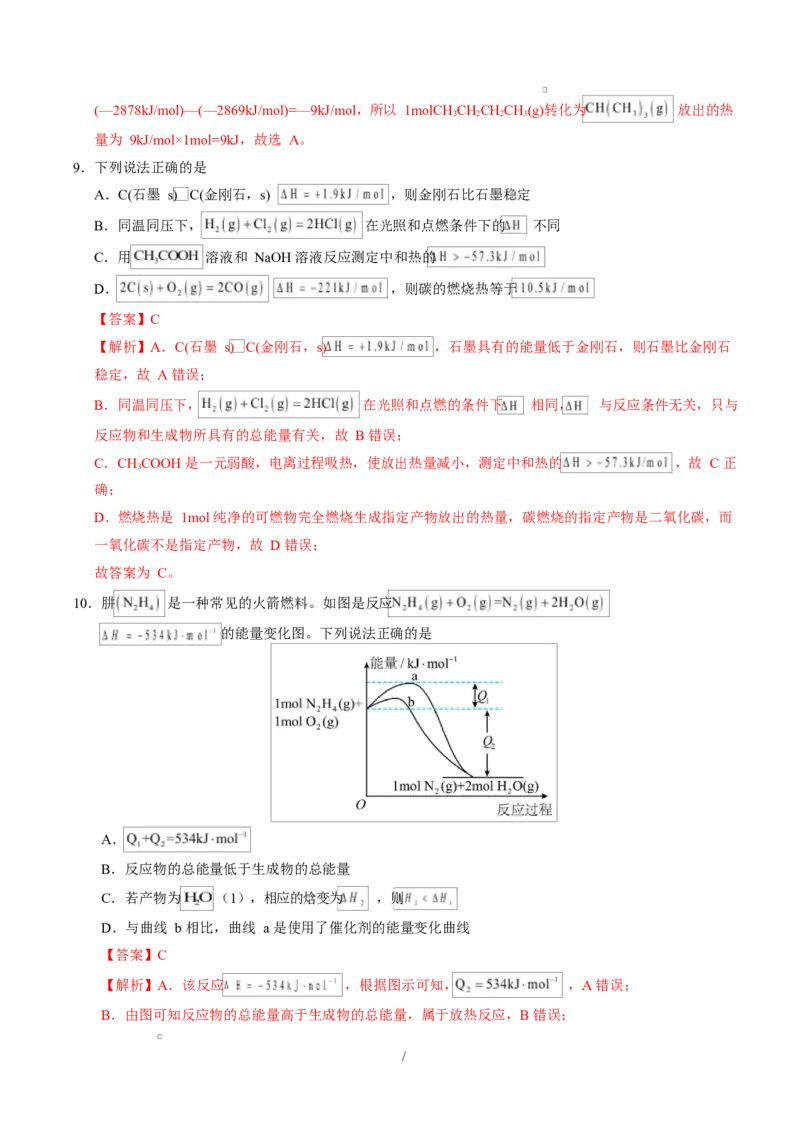
10.肼 是一种常见的火箭燃料。如图是反应
的能量变化图。下列说法正确的是
A.
B.反应物的总能量低于生成物的总能量
C.若产物为 (1),相应的焓变为 ,则
D.与曲线 b 相比,曲线 a 是使用了催化剂的能量变化曲线
【答案】C
【解析】A.该反应 ,根据图示可知, ,A 错误;
B.由图可知反应物的总能量高于生成物的总能量,属于放热反应,B 错误;
/C.若产物为 , 能量低于 ,放出热量多, ,C 正确;
D.使用催化剂可降低反应的活化能,故与曲线 a 相比,曲线 b 为使用了催化剂的图像,D 错误;
答案选 C。
11.NO 催化 生成 的过程由三步基元反应构成:
第一步: ;
第二步: ;
第三步: 。
下列说法错误的是
A.该反应会经历三个过渡态 B.第二步、第三步反应均为放热反应
C.催化剂 NO 不改变总反应的焓变 D.总反应 的
【答案】D
【解析】A.由题意可知,该反应由 NO 催化 O 生成 O 的过程由三步基元反应构成,同时通过图中信
3 2
息可知,该反应会经历三个过渡态,故 A 正确;
B.由图可知,第一步反应是吸热反应,第二步和第三步反应均为放热反应,故 B 正确;
C.NO 是反应 2O(g)═2O (g)的催化剂,催化剂不改变反应的始态和终态,不能改变总反应的焓变,故
3 2
C 正确;
D.总反应 2O(g)═2O (g),由盖斯定律:第一步反应+第二步反应+第三步反应计算反应 2O(g)═3O
3 2 3 2
(g)的ΔH=ΔH+ΔH +ΔH ,故 D 错误;
1 2 3
答案选 D。
12.已知 1mol 二氧化硅晶体中化学键的数目为 4 ,有关键能数据如表所示:
化学键 Si—O O=O Si—Si
键能/( ) 460 498.8 176
又知 ,则 1mol Si 中 Si—Si 键的数目为
A. B.2 C.3 D.4
【答案】B
【解析】设 1molSi 中含有 x mol Si-Si 键,已知 Si(s)+O(g)=SiO (s),△H=-989.2kJ·mol-1,根据△H=反
2 2
/应物总键能-生成物总键能,则有 176kJ·mol-1×x+498.8kJ·mol-1-4×460kJ·mol-1=-989.2kJ·mol-1,解得 x=2,
则 1mol Si 中含有 Si-Si 键的数目为 2NA,答案选 B。
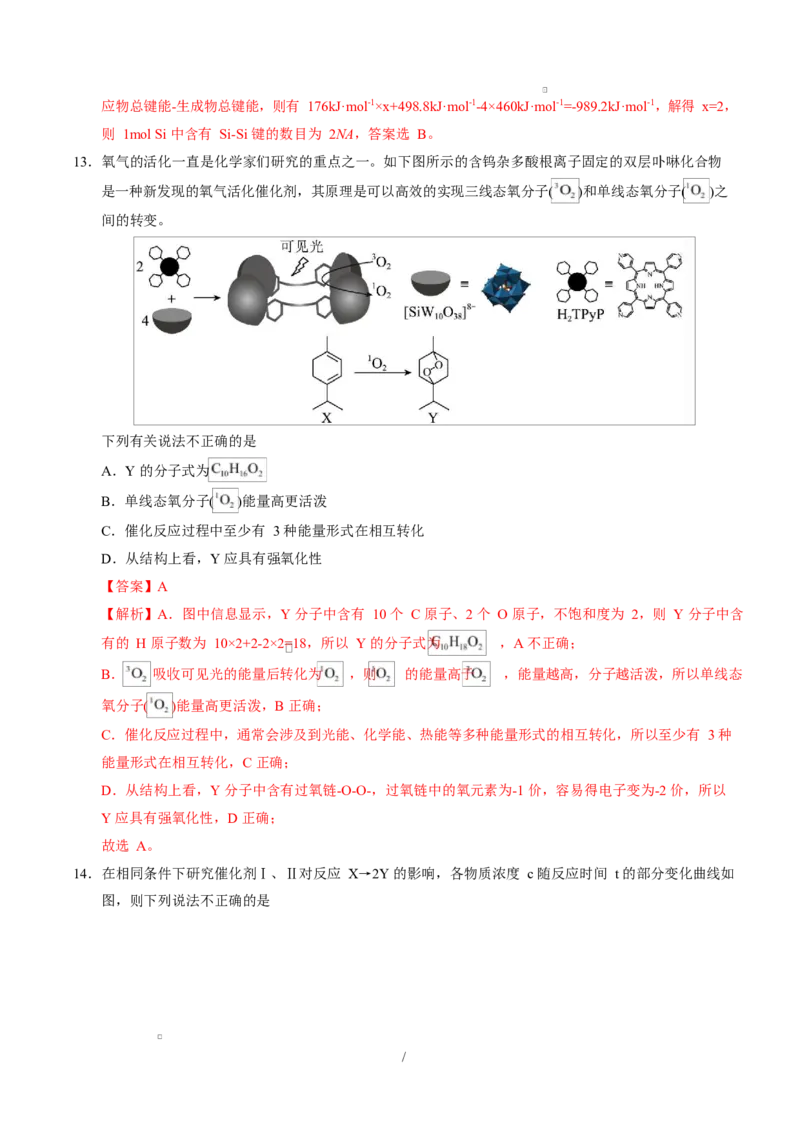
13.氧气的活化一直是化学家们研究的重点之一。如下图所示的含钨杂多酸根离子固定的双层卟啉化合物
是一种新发现的氧气活化催化剂,其原理是可以高效的实现三线态氧分子( )和单线态氧分子( )之
间的转变。
下列有关说法不正确的是
A.Y 的分子式为
B.单线态氧分子( )能量高更活泼
C.催化反应过程中至少有 3 种能量形式在相互转化
D.从结构上看,Y 应具有强氧化性
【答案】A
【解析】A.图中信息显示,Y 分子中含有 10 个 C 原子、2 个 O 原子,不饱和度为 2,则 Y 分子中含
有的 H 原子数为 10×2+2-2×2=18,所以 Y 的分子式为 ,A 不正确;
B. 吸收可见光的能量后转化为 ,则 的能量高于 ,能量越高,分子越活泼,所以单线态
氧分子( )能量高更活泼,B 正确;
C.催化反应过程中,通常会涉及到光能、化学能、热能等多种能量形式的相互转化,所以至少有 3 种
能量形式在相互转化,C 正确;
D.从结构上看,Y 分子中含有过氧链-O-O-,过氧链中的氧元素为-1 价,容易得电子变为-2 价,所以
Y 应具有强氧化性,D 正确;
故选 A。
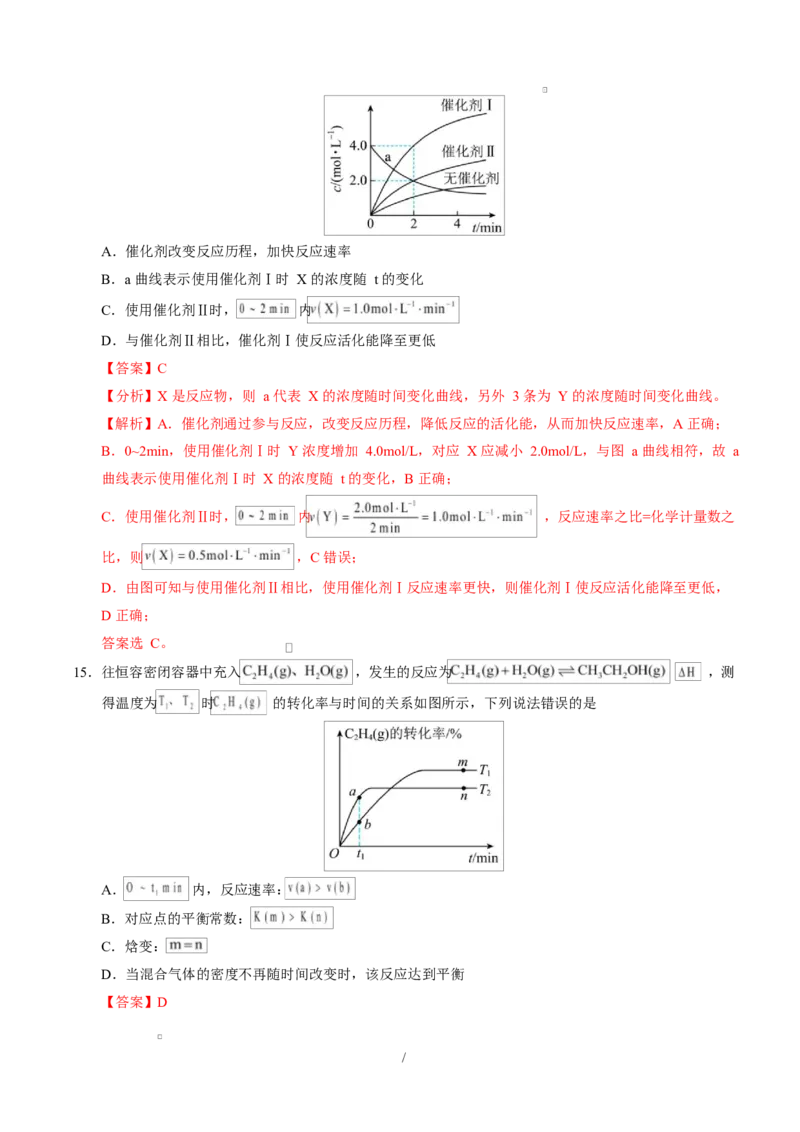
14.在相同条件下研究催化剂Ⅰ、Ⅱ对反应 X→2Y 的影响,各物质浓度 c 随反应时间 t 的部分变化曲线如
图,则下列说法不正确的是
/A.催化剂改变反应历程,加快反应速率
B.a 曲线表示使用催化剂Ⅰ时 X 的浓度随 t 的变化
C.使用催化剂Ⅱ时, 内
D.与催化剂Ⅱ相比,催化剂Ⅰ使反应活化能降至更低
【答案】C
【分析】X 是反应物,则 a 代表 X 的浓度随时间变化曲线,另外 3 条为 Y 的浓度随时间变化曲线。
【解析】A.催化剂通过参与反应,改变反应历程,降低反应的活化能,从而加快反应速率,A 正确;
B.0~2min,使用催化剂Ⅰ时 Y 浓度增加 4.0mol/L,对应 X 应减小 2.0mol/L,与图 a 曲线相符,故 a
曲线表示使用催化剂Ⅰ时 X 的浓度随 t 的变化,B 正确;
C.使用催化剂Ⅱ时, 内 ,反应速率之比=化学计量数之
比,则 ,C 错误;
D.由图可知与使用催化剂Ⅱ相比,使用催化剂Ⅰ反应速率更快,则催化剂Ⅰ使反应活化能降至更低,
D 正确;
答案选 C。
15.往恒容密闭容器中充入 ,发生的反应为 ,测
得温度为 时 的转化率与时间的关系如图所示,下列说法错误的是
A. 内,反应速率:
B.对应点的平衡常数:
C.焓变:
D.当混合气体的密度不再随时间改变时,该反应达到平衡
【答案】D
/【分析】根据“先拐先平,数值大”,T>T;
2 1
【解析】A.升高温度,反应速率加快,T>T,所以 内,反应速率: ,故 A 正确;
2 1
B.T>T,升高温度, 的转化率减小,正反应放热,对应点的平衡常数: ,故 B
2 1
正确;
C.焓变与平衡移动无关,所以焓变 ,故 C 正确;
D.反应前后气体总质量不变、容器体积不变,密度是恒量,当混合气体的密度不再随时间改变时,不
能说明该反应达到平衡,故 D 错误;
选 D。
16.向两个体积相等的恒容密闭容器中起始时均充入 1molP (g)和 6molH (g),分别在绝热、恒温两条件下发
4 2
生反应:P
4
(g)+6H
2
(g)⇌4PH
3
(g) △H,测得两容器中气体压强(kPa)与时间(min)关系
如表所示。
时间 0 2 4 6 8 10 12 14
容器 I 100p 95p 92p 90p 88p 87p 87p 87p
容器
100p 105p 100p 94p 90p 90p 90p 90p
Ⅱ
下列叙述不正确的是
A.△H<0
B.平衡时容器Ⅱ温度高于容器Ⅰ
C.容器Ⅰ6min 时气体总物质的量等于容器Ⅱ8min 时气体总物质的量
D.14min 时正反应速率:容器Ⅱ大于容器Ⅰ
【答案】C
【解析】A.分析数据表,容器Ⅰ中气体压强逐渐减小,观察此可逆反应,该反应的气体分子数逐渐减
小,说明容器Ⅰ是恒温过程,容器Ⅱ中气体压强先增大,后减小,说明它是绝热过程,且正反应是放
热反应,△H<0,故 A 正确;
B.由 A 选分析知,平衡时容器Ⅱ温度高于容器Ⅰ,故 B 正确;
C.当压强都为 90p 时,容器体积相等,温度越高,气体总物质的量越小,明显容器Ⅱ温度高于容器Ⅰ,
二者气体总物质的量不相等,故 C 错误;
D.14min 时两个容器都达到平衡,温度越高,反应速率越大,故 D 项正确。
故选 C。
第 II 卷(非选择题 共 56 分)
二、非选择题:共 4 题,共 56 分。
17.(14 分)回答下列问题:
Ⅰ.某实验小组用 0.50 mol·L-1 NaOH 溶液和 0.50 mol·L-1 硫酸溶液进行中和反应反应热的测定。实验
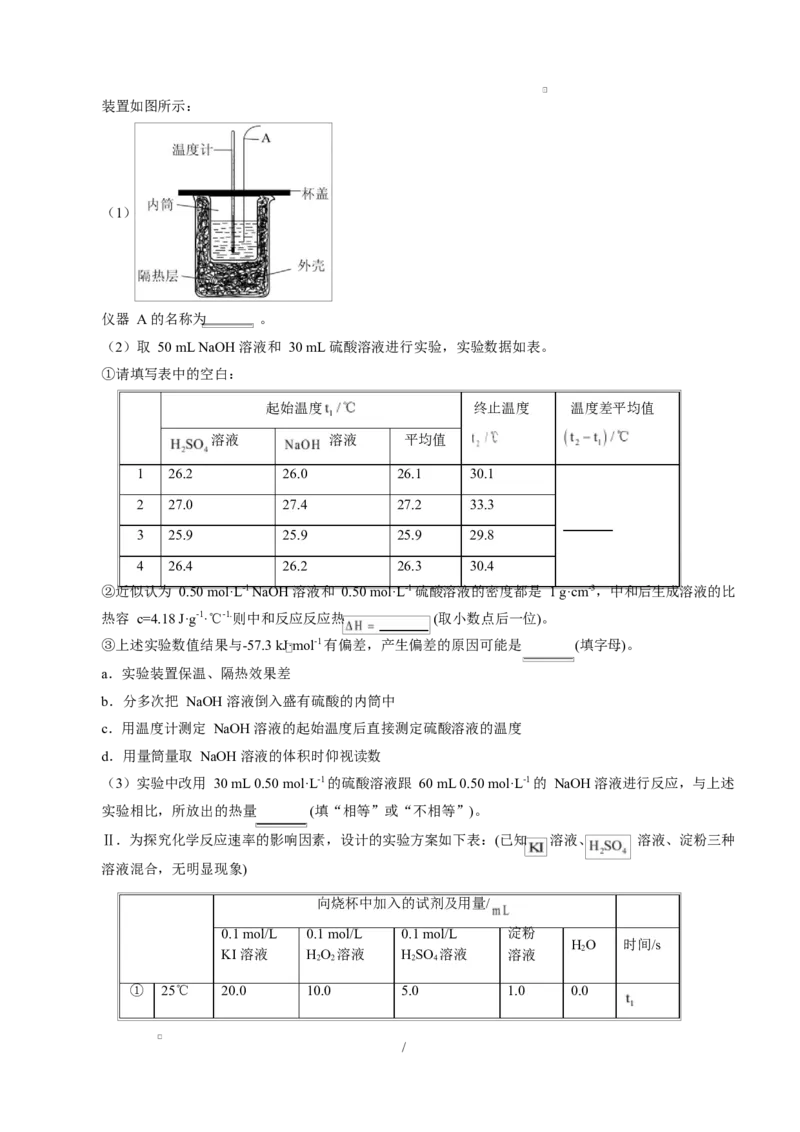
/装置如图所示:
(1)
仪器 A 的名称为 。
(2)取 50 mL NaOH 溶液和 30 mL 硫酸溶液进行实验,实验数据如表。
①请填写表中的空白:
起始温度 终止温度 温度差平均值
溶液 溶液 平均值
1 26.2 26.0 26.1 30.1
2 27.0 27.4 27.2 33.3
3 25.9 25.9 25.9 29.8
4 26.4 26.2 26.3 30.4
②近似认为 0.50 mol·L-1 NaOH 溶液和 0.50 mol·L-1 硫酸溶液的密度都是 1 g·cm-3,中和后生成溶液的比
热容 c=4.18 J·g-1·℃-1.则中和反应反应热 (取小数点后一位)。
③上述实验数值结果与-57.3 kJ·mol-1 有偏差,产生偏差的原因可能是 (填字母)。
a.实验装置保温、隔热效果差
b.分多次把 NaOH 溶液倒入盛有硫酸的内筒中
c.用温度计测定 NaOH 溶液的起始温度后直接测定硫酸溶液的温度
d.用量筒量取 NaOH 溶液的体积时仰视读数
(3)实验中改用 30 mL 0.50 mol·L-1 的硫酸溶液跟 60 mL 0.50 mol·L-1 的 NaOH 溶液进行反应,与上述
实验相比,所放出的热量 (填“相等”或“不相等”)。
Ⅱ.为探究化学反应速率的影响因素,设计的实验方案如下表:(已知 溶液、 溶液、淀粉三种
溶液混合,无明显现象)
向烧杯中加入的试剂及用量/
0.1 mol/L 0.1 mol/L 0.1 mol/L 淀粉
HO 时间/s
KI 溶液 HO 溶液 HSO 溶液 溶液 2
2 2 2 4
① 25℃ 20.0 10.0 5.0 1.0 0.0
/② 40℃ 20.0 10.0 5.0 1.0 0.0
③ 25℃ 20.0 5.0 5.0 1.0 V
(4)该实验能观察到的实验现象为: 。
(5)表中的 V= , 、 、 由小到大的顺序为 。
(6)对比实验①②可推测实验结论为 。
【答案】(1)环形玻璃搅拌器(1 分)
(2)4.0(1 分) -53.5 kJ·mol-1(2 分) abc(2 分)
(3)不相等(1 分)
(4)溶液变为蓝色(1 分)
(5)5(2 分) < < (2 分)
(6)相同条件下,温度越高,反应速率越快(2 分)
【分析】进行酸、碱反应的中和热测定时,关键性的操作是反应前后溶液的温度测定,尤其是中和反
应发生时的最高温度,既要求装置的保温效果好、实验操作规范,又要求观察温度时敏捷。
【解析】(1)仪器 为环形玻璃搅拌器;
(2)①第一次测定的温度差为 ,第二次测定的温度差为 ,第三次测定的温度差为 ,第
四次测定的温度差为 ,实验 2 的误差太大要舍去,三次温度差的平均值为 。
②50 mL 0.50 mol·L-1 NaOH氢氧化钠溶液与30 mL 0.50 mol·L-1 硫酸溶液进行中和反应,硫酸是过量的,
生成水的物质的量和消耗氢氧化钠的物质的量相等,所以生成水的物质的量为
,溶液的质量为 ,温度变化的值 ,则生
成 0.025 mol 水放出的热量 ,即 1.3376 kJ,所以实验
测得的中和热 。
③a.装置保温、隔热效果差,测得的热量偏小,中和反应反应热 偏大;
b.分多次把 溶液倒入盛有硫酸的内筒中,热量散失较多,测得温度偏低,中和反应反应热 偏
大;
c.用温度计测定 溶液的起始温度后直接测定 溶液的温度,导致温度计上残留的碱液与稀
硫酸反应,起始温度偏高,中和反应反应热 偏大;
d.量取 溶液的体积时仰视读数,会导致所量的氢氧化钠溶液体积偏大,放出的热量偏高,中和
反应反应热 偏小。
故答案为:abc;
(3)实验中改用 30 mL 0.50 mol·L-1 硫酸溶液跟 60 mL 0.50 mol·L-1 氢氧化钠溶液进行反应,与上述实
验相比,生成的水的物质的量不同,所放出的热量不相等。
(4)混合溶液中滴入 溶液,双氧水氧化碘离子生成单质碘,则该实验能观察到的实验现象为:
/溶液变为蓝色。
(5)①③是研究双氧水浓度对反应速率的影响,而整个溶液的体积要相同,则表中的 V=5,③中双氧
水浓度比①中双氧水浓度小,反应速率慢,出现蓝色现象需要的时间长,①②探究温度对反应速率的
影响,②的温度高,反应速率快,出现蓝色需要的时间短,因此 、 、 ,由小到大的顺序为 < <
。
(6)对比实验①②,②溶液变为蓝色比①快,②的温度高,反应速率快,因此可推测实验结论为相同
条件下,温度越高,反应速率越快。
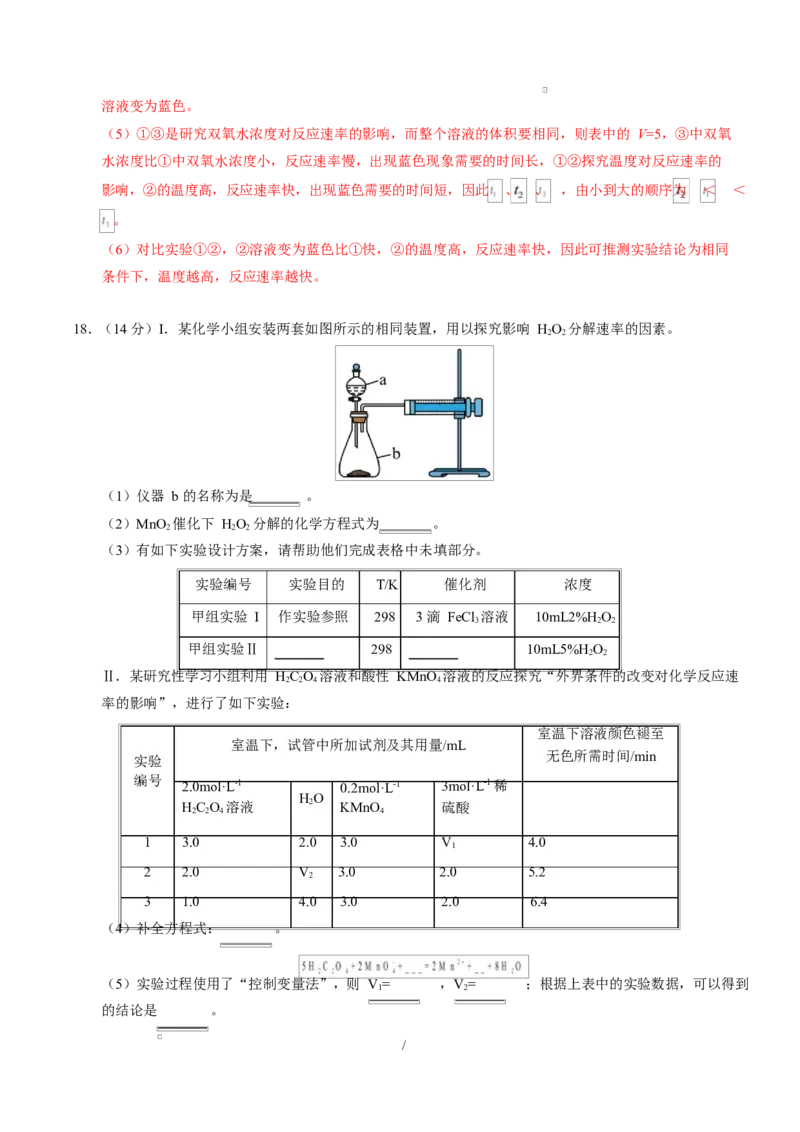
18.(14 分)I.某化学小组安装两套如图所示的相同装置,用以探究影响 HO 分解速率的因素。
2 2
(1)仪器 b 的名称为是 。
(2)MnO 催化下 HO 分解的化学方程式为 。
2 2 2
(3)有如下实验设计方案,请帮助他们完成表格中未填部分。
实验编号 实验目的 T/K 催化剂 浓度
甲组实验 I 作实验参照 298 3 滴 FeCl 溶液 10mL2%H O
3 2 2
甲组实验Ⅱ 298 10mL5%H O
2 2
Ⅱ.某研究性学习小组利用 HC O 溶液和酸性 KMnO 溶液的反应探究“外界条件的改变对化学反应速
2 2 4 4
率的影响”,进行了如下实验:
室温下溶液颜色褪至
室温下,试管中所加试剂及其用量/mL
无色所需时间/min
实验
编号
2.0mol·L-1 0.2mol·L-1 3mol·L-1 稀
HO
HC O 溶液 2 KMnO 硫酸
2 2 4 4
1 3.0 2.0 3.0 V 4.0
1
2 2.0 V 3.0 2.0 5.2
2
3 1.0 4.0 3.0 2.0 6.4
(4)补全方程式: 。
(5)实验过程使用了“控制变量法”,则 V= ,V= ;根据上表中的实验数据,可以得到
1 2
的结论是 。
/(6)该小组同学查阅已有的资料后,提出假设:生成物中的 MnSO 为该反应的催化剂,请你帮助该
4
小组同学完成实验方案验证假设。
室温下,试管中所加试剂及其用量/mL
室温下溶液颜色褪
实验 再向试管中加
2.0mol·L-1 至无色所需时间
编号 入少量固体
0.2mol·L-1 3mol·L-1 稀 /min
HO
HC O 溶液 2 KMnO 溶液 硫酸
2 2 4 4
4 3.0 2.0 3.0 2.0 _______ t
①再向试管中加入的少量固体的化学式为 。
②若该小组同学提出的假设成立,应观察到的现象是 。
【答案】(1)锥形瓶(1 分)
(2) (2 分)
(3)研究浓度对速率的影响(1 分) 3 滴 FeCl 溶液(1 分)
3
(4)5H
2
C
2
O
4
+2 +6H+= 2Mn2++10CO
2
↑+8H
2
O(2 分)
(5)2.0(1 分) 3.0(1 分) 其他条件相同时,增大草酸浓度,反应速率加快(2 分)
(6)MnSO (1 分) 与实验 1 相比,溶液褪色所需时间短(2 分)
4
【分析】I、研究外界条件的改变对化学反应速率的影响,需要控制变量,探究浓度对速率的影响时,
其他条件要保持不变;
Ⅱ某研究性学习小组利用 HC O 溶液和酸性 KMnO 溶液的反应探究“外界条件的改变对化学反应速率
2 2 4 4
的影响”,实验 1、2、3 都是改变 HC O 溶液的浓度,保持 KMnO 溶液的浓度和温度不变,通过测定
2 2 4 4
溶液颜色发生改变所需的时间,探究浓度对化学反应速率的影响,实验 4 与实验 1 进行对比,各反应
物的浓度都相同,但加入了催化剂,探究催化剂对化学反应速率的影响,据此分析;
【解析】(1)由装置图可知仪器 b 的名称为锥形瓶;
(2)HO 在 MnO 催化下分解生成水和氧气,化学方程式为: ;
2 2 2
(3)由甲组实验Ⅰ的实验目的可知,催化剂和浓度只能有一个作为变量,而浓度已为变量,催化剂就
不能再作为变量,所以甲组实验Ⅱ中催化剂与甲组实验Ⅰ中的相同,由题干的实验目的可知甲组实验
Ⅱ的实验目的为探究浓度对速率的影响,催化剂也为 3 滴 FeCl 溶液;
3
(4)HC O 溶液和酸性 KMnO 溶液发生反应,Mn 元素由+7 价降低到+2 价,则 KMnO 作氧化剂,
2 2 4 4 4
HC O 作还原剂,C 元素由+3 价升高到+4 价,从而生成 CO。利用得失电子守恒,可得出配平的离子
2 2 4 2
方程式为 5H
2
C
2
O
4
+2 +6H+=2Mn2++10CO
2
↑+8H
2
O;
(5)实验过程使用了“控制变量法”,为保证 KMnO 溶液的浓度不变,需保证混合溶液的总体积不变,
4
实验 3 中,溶液的总体积为 10mL,由此可得出,V=2.0,V=3.0;上表中的实验数据显示,HC O
1 2 2 2 4
溶液浓度越小,溶液褪色所需时间越长,则可以得到的结论是:其他条件相同时,增大草酸浓度,反
/应速率加快;
(6)①假设生成物中的MnSO 为该反应的催化剂,则应再向试管中加入的少量固体的化学式为MnSO ;
4 4
②催化剂能加快反应速率,缩短反应到达平衡的时间。若该小组同学提出的假设成立,应观察到的现
象是:与实验 1 相比,溶液褪色所需时间短。
19.(14 分)回答下列问题:
(1)在 25℃、101kPa 下,23g 乙醇 C HOH 燃烧生成 CO 和液态水时放热 683.4kJ。则表示乙醇燃烧
2 5 2
热的热化学方程为 。
(2)一定条件下 与 可发生反应: ,该反应为放热反应,
对于该反应,反应物的化学键断裂要吸收的能量 生成物的化学键形成要放出的能量(填“大于”、“小
于”或“等于”)。
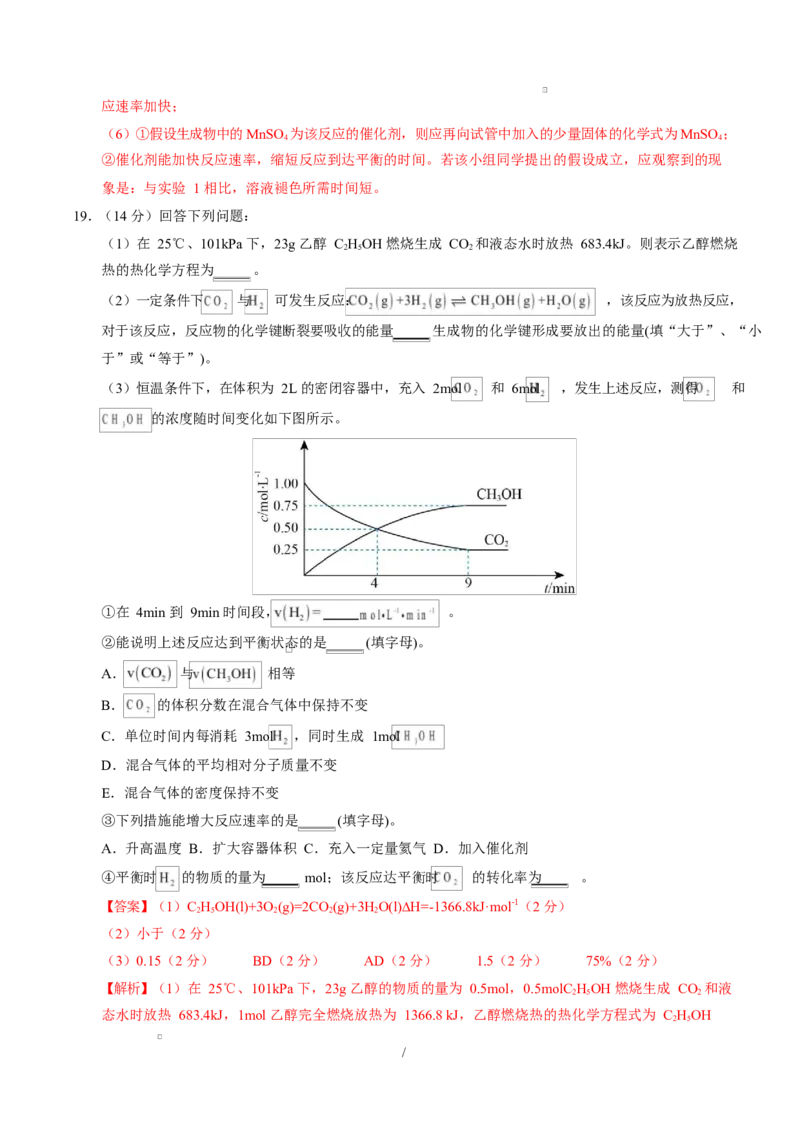
(3)恒温条件下,在体积为 2L 的密闭容器中,充入 2mol 和 6mol ,发生上述反应,测得 和
的浓度随时间变化如下图所示。
①在 4min 到 9min 时间段, 。
②能说明上述反应达到平衡状态的是 (填字母)。
A. 与 相等
B. 的体积分数在混合气体中保持不变
C.单位时间内每消耗 3mol ,同时生成 1mol
D.混合气体的平均相对分子质量不变
E.混合气体的密度保持不变
③下列措施能增大反应速率的是 (填字母)。
A.升高温度 B.扩大容器体积 C.充入一定量氦气 D.加入催化剂
④平衡时 的物质的量为 mol;该反应达平衡时 的转化率为 。
【答案】(1)C HOH(l)+3O (g)=2CO (g)+3HO(l)∆H=-1366.8kJ·mol-1(2 分)
2 5 2 2 2
(2)小于(2 分)
(3)0.15(2 分) BD(2 分) AD(2 分) 1.5(2 分) 75%(2 分)
【解析】(1)在 25℃、101kPa 下,23g 乙醇的物质的量为 0.5mol,0.5molC HOH 燃烧生成 CO 和液
2 5 2
态水时放热 683.4kJ,1mol 乙醇完全燃烧放热为 1366.8 kJ,乙醇燃烧热的热化学方程式为 C HOH
2 5
/(l)+3O (g)=2CO (g)+3HO(l) ∆H=-1366.8kJ·mol-1。
2 2 2
(2)该反应为放热反应,反应物的化学键断裂要吸收的能量小于生成物的化学键形成要放出的能量。
(3)①在 4min 到 9min 时间段,CO 的浓度变化量为 0.25mol/L,根据方程可知,H 的浓度变化量为:
2 2
, ;
②A. 与 相等,并没有指明正、逆反应方向,不能判断达到平衡状态,A 错误;
B. 的体积分数在混合气体中保持不变,达到平衡状态,B 正确;
C.单位时间内每消耗 3mol ,同时生成 1mol ,均为正反应方向,不能判断达到平衡状态,C
错误;
D.反应前后混合气体的总物质的量减少,总质量不变,当混合气体的平均相对分子质量不变时达到平
衡状态,D 正确;
E.反应前后气体的总质量不变,容器体积不变,故混合气体的密度一直保持不变,不能判断达到平衡
状态,E 错误;
故选 BD;
③A.升高温度,化学反应速率增大,A 正确;
B.扩大容器体积,各物质浓度降低,反应速率减小,B 错误;
C.充入一定量氦气,各物质浓度不变,反应速率不变,C 错误;
D.加入催化剂,反应速率增大,D 正确;
故选 AD;
④平衡时 CHOH 的物质的量浓度变化量为 0.75mol/L,可列出三段式:
3
,
平衡时 的物质的量为 ; 的平衡转化率为 。
20.(14 分)钌(Ru)是重要的催化剂元素。回答下列问题:
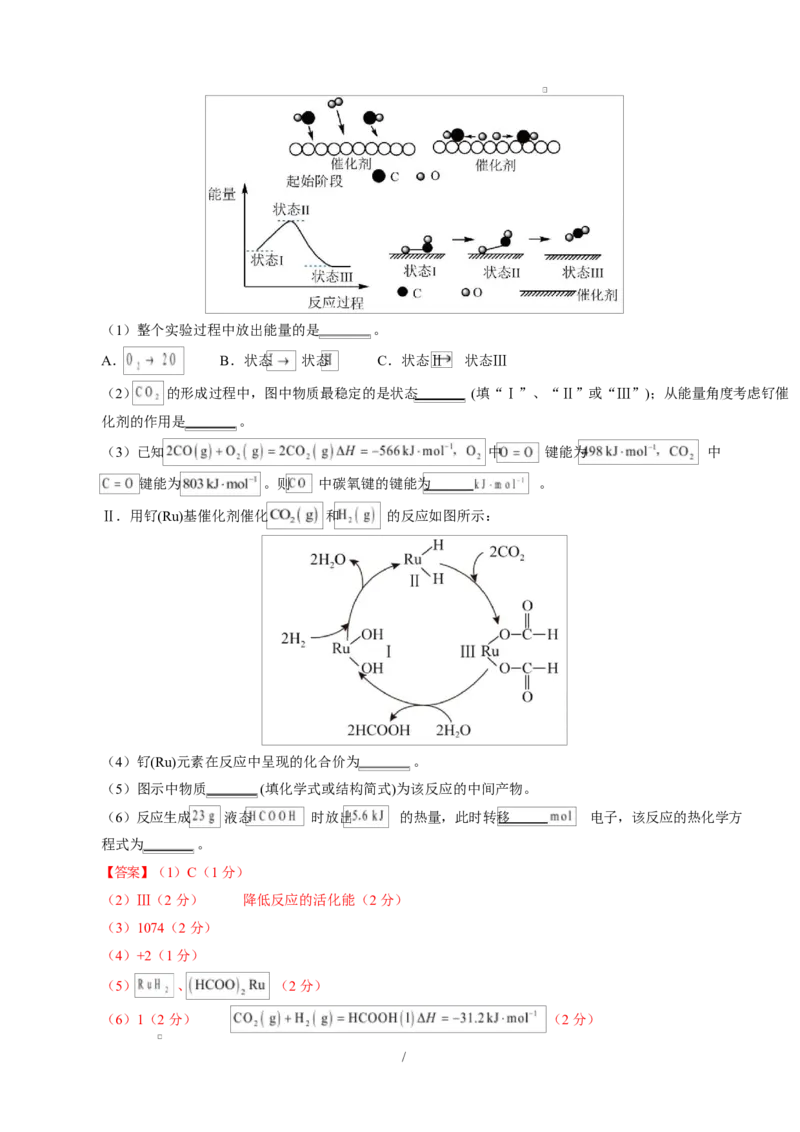
Ⅰ.研究人员通过实验在钌催化剂表面成功观察到 与 形成化学键生成 的过程,起始阶段及反
应过程如下图:
/(1)整个实验过程中放出能量的是 。
A. B.状态 状态 C.状态Ⅱ 状态Ⅲ
(2) 的形成过程中,图中物质最稳定的是状态 (填“Ⅰ”、“Ⅱ”或“Ⅲ”);从能量角度考虑钌催
化剂的作用是 。
(3)已知 中 键能为 中
键能为 。则 中碳氧键的键能为 。
Ⅱ.用钌(Ru)基催化剂催化 和 的反应如图所示:
(4)钌(Ru)元素在反应中呈现的化合价为 。
(5)图示中物质 (填化学式或结构简式)为该反应的中间产物。
(6)反应生成 液态 时放出 的热量,此时转移 电子,该反应的热化学方
程式为 。
【答案】(1)C(1 分)
(2)Ⅲ(2 分) 降低反应的活化能(2 分)
(3)1074(2 分)
(4)+2(1 分)
(5) 、 (2 分)
(6)1(2 分) (2 分)
/【解析】(1)a. O 2O,化学键断裂需要吸收能量,a 不符合题意;
2
b.状态Ⅰ 状态Ⅱ,反应物分子变成活化分子需要吸收能量,b 不符合题意;
c.状态Ⅱ 状态Ⅲ,活化分子变成生成物分子放出能量,c 符合题意;
故选 c;
(2)能量越低越稳定,状态Ⅲ的能量最低,所以 CO 的形成过程中,图中物质最稳定的是状态Ⅲ;从
2
能量角度考虑钌催化剂的作用是降低反应的活化能;
(3)反应热=反应物键能和-产物键能和,即
,则 E(
)=1074kJ⋅mol−1;
(4)H 和 O 的电负性大于钌,根据结构简式可判断 Ru 元素在该反应呈现的化合价为+2 价;
(5)图为催化 CO(g)和 H(g)的反应生成 HCOOH,物质Ⅰ在合成甲酸的过程中物质的量没有改变,
2 2
只是改变了反应机理,所以物质Ⅰ为该反应的催化剂,Ⅱ、Ⅲ为中间产物,故答案为: 、
;
(6)根据整个流程可知,反应生成 液态 时放出 的热量,CO 和 H 为反应物,产
2 2
物为 HCOOH,23gHCOOH 的物质的量为 =0.5mol,所以生成 1mol 液态 HCOOH 放出 31.2kJ
能量,热化学方程式为 H(g)+CO (g)=HCOOH(l) △H=-31.2kJ·mol-1;结合热化学方程式可知,当生成
2 2
0.5mol 甲酸时,有 0.5mol 氢气参加反应,每个氢气参加反应转移 2 个电子,则 0.5mol 氢气参加反应转
移 1mol 电子,故答案为:1; 。
/