文档内容
哈三中2025-2026学年度上学期
高三学年第一次验收考试 化学 试卷
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Cl 35.5 Cu 64
一、单选题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有
一项符合题目要求。
1.下列应用不涉及氧化还原反应的是
A.Na O 用作呼吸面具的供氧剂
2 2
B.工业上电解熔融状态的Al O 制备铝单质
2 3
C.常温下,铁遇浓硫酸钝化
D.用(NH ) SO 溶液除去铜器表面的铜锈
4 2 4
2.画中有“化”,多彩中华。下列叙述正确的是
A.岩彩画的颜料石青为蓝铜矿[主要成分Cu (CO ) (OH) ]加工制成,该物质属于碱
3 3 2 2
B.油画颜料调和剂所用核桃油,属于有机高分子
C.竹胎漆画颜料贝壳的主要成分为碳酸钙
D.水墨画墨汁以桐油制烟黑的过程中发生了完全燃烧
3.下列符号表征或说法正确的是
A.HF电离:HF=F−+ H+ B.Br原子基态核外电子排布式为[Ar]4s24p5
C.SO 分子构型:直线形 D.氢化钠电子式:
2
4.次氯酸钠是一种广泛使用的漂白剂、消毒剂。下列关于次氯酸钠说法错误的是
A.实验室可用氯气与热的NaOH溶液反应得到NaClO
B.NaClO的稳定性强于HClO,因此更容易保存
C.适当调低NaClO溶液的pH,可增强其氧化性
D.向NaClO溶液中通入少量CO ,反应的离子方程式:ClO-+CO +H O=HClO+HCO-
2 2 2 3
5.下列各组中的离子,能在溶液中大量共存的是
A.NH+ 、Na+、[Al(OH) ]−、NO− B.Al3+、H+、Cl−、S O2−
4 4 3 2 3
C.Mg2+、K+、I−、SO2− D.Cu2+、Fe2+、CO2− 、Br−
4 3
6.下列装置符合规范且能达到实验目的的是
D.蒸发结晶获得无
A.试剂存放 B.实验室制蒸馏水 C.干燥NH
3
水FeCl
3
化学试题 第1页(共8页)
{#{QQABRQYAggCoQAAAABgCAwFqCgGQkBGCCYoGRBAcMAAASBFABCA=}#}7.我国学者把游离态氮固定在碳上(示踪反应如下),制得的[N=C=N]2﹣离子可用于合成
核酸的结构单元。阿伏加德罗常数的值为N ,下列说法正确的是
A
15N +C(石墨)+2LiH 一定条件 Li [15N=C=15N]+H
2 2 2
A.22.4 L 15N 含有的中子数为16N
2 A
B.28 g 15N 中含有孤电子对数为2N
2 A
C.1 mol [N=C=N]2−中含有的π键数为2N
A
D.生成1 mol H 时,总反应转移的电子数为2N
2 A
8.室温下,下列关于颜色变化的说法中,实验过程及现象能验证相应实验结论的是
实验过程及现象 实验结论
向石蕊溶液中加入CaO 粉末,溶液先变为蓝 溶液褪色是因为CaO 具有强氧
2 2
A
色,后变为无色 化性,将石蕊氧化
B 向溴水中加入花生油,振荡后静置,溴水褪色 花生油将溴水中的溴萃取
向酸性KMnO 溶液中滴入草酸,振荡后溶液
4
C 草酸具有漂白性
褪色
用pH试纸测定常温下浓度均为0.1 mol/L的 次氯酸钠溶液显碱性,次氯酸是
D
NaCl、NaClO溶液的pH 弱酸
9.下列解释事实的离子方程式错误的是
A.用酸化的KI淀粉溶液检验加碘盐中的IO- :IO- +5I−+6H+=3I +3H O
3 3 2 2
B.用CuSO 溶液除去乙炔中的H S:Cu2++S2− =CuS↓
4 2
C.向NaClO溶液中通入过量SO :SO +ClO−+H O=2H++SO2− +Cl−
2 2 2 4
D.向NH Al(SO ) 溶液中加入少量NaOH溶液:Al3++3OH-=Al(OH) ↓
4 4 2 3
10.价类二维图是学习化学的重要工具和模型,硫元素的部分价类二维图如图所示。下
列说法正确的是
A.可存在!!"!#!$!%!&的转化关系
B.实验室常用盐酸清洗附着于试管内壁的b物质
C.将铁丝插入e的稀溶液中可得到c
D.c使高锰酸钾溶液和品红溶液褪色的原理相同
化学试题 第2页(共8页)
{#{QQABRQYAggCoQAAAABgCAwFqCgGQkBGCCYoGRBAcMAAASBFABCA=}#}11.由原子序数递增的X、Y、Z、W、M五种短周期主族元素形成的一种化合物可用作
分析试剂和环氧树脂固化剂,其结构如图所示。已知Y、Z、W、M同周期,且Y、Z相
邻,W、M相邻,原子序数X+Y=Z,Z原子的最外层电子数是内层电子数的二倍。下列
说法正确的是
A.非金属性顺序:Z<Y<W<M
B.M的最高价氧化物对应的水化物为强酸
C.W的单质有两种常见的同素异形体
D.Z的氢化物分子间可以形成氢键
12.已知CuCl是一种难溶于水的白色固体,酸性溶液中发生反应:2CuCl=CuCl +Cu。
2
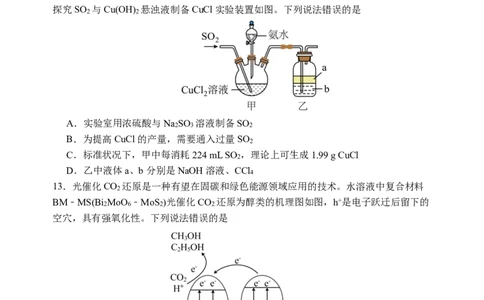
探究SO 与Cu(OH) 悬浊液制备CuCl实验装置如图。下列说法错误的是
2 2
A.实验室用浓硫酸与Na SO 溶液制备SO
2 3 2
B.为提高CuCl的产量,需要通入过量SO
2
C.标准状况下,甲中每消耗224 mL SO ,理论上可生成1.99 g CuCl
2
D.乙中液体a、b分别是NaOH溶液、CCl
4
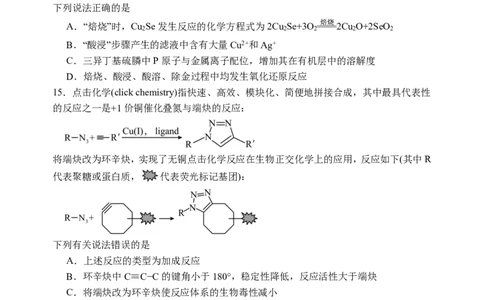
13.光催化CO 还原是一种有望在固碳和绿色能源领域应用的技术。水溶液中复合材料
2
BM﹣MS(Bi MoO ﹣MoS )光催化CO 还原为醇类的机理图如图,h+是电子跃迁后留下的
2 6 2 2
空穴,具有强氧化性。下列说法错误的是
A.H O在富集空穴的MoS 材料上发生氧化反应
2 2
B.不论还原产物是C H OH还是CH OH,等质量CO 被固定后的产氧量相同
2 5 3 2
C.在Bi MoO 材料上,消耗标准状况下2.24 L CO 时,转移0.4 mol电子
2 6 2
D.光催化过程的总反应是2CO +3H O=C H OH+3O 和2CO +4H O=2CH OH+3O
2 2 2 5 2 2 2 3 2
化学试题 第3页(共8页)
{#{QQABRQYAggCoQAAAABgCAwFqCgGQkBGCCYoGRBAcMAAASBFABCA=}#}14.K PtCl 可用于镀铂以及作铂催化剂、不灭墨水和铂镜等。某科研小组从阳极泥(成分
2 6
为Cu Se、Ag Se、Au、Pt)中提取K PtCl 的工艺流程如图所示。
2 2 2 6
已知:三异丁基硫膦的结构简式为 ,“焙烧”时Cu Se转化为Cu O。
2 2
下列说法正确的是
A.“焙烧”时,Cu Se发生反应的化学方程式为2Cu Se+3O 2Cu O+2SeO
2 2 2 2 2
B.“酸浸”步骤产生的滤液中含有大量Cu2+和Ag+
C.三异丁基硫膦中P原子与金属离子配位,增加其在有机层中的溶解度
D.焙烧、酸浸、酸溶、除金过程中均发生氧化还原反应
15.点击化学(click chemistry)指快速、高效、模块化、简便地拼接合成,其中最具代表性
的反应之一是+1价铜催化叠氮与端炔的反应:
将端炔改为环辛炔,实现了无铜点击化学反应在生物正交化学上的应用,反应如下(其中R
代表聚糖或蛋白质, 代表荧光标记基团):
下列有关说法错误的是
A.上述反应的类型为加成反应
B.环辛炔中C≡C−C的键角小于180°,稳定性降低,反应活性大于端炔
C.将端炔改为环辛炔使反应体系的生物毒性减小
D.碳原子更多的环炔都能替代环辛炔发生无催化的生物正交化学反应
化学试题 第4页(共8页)
{#{QQABRQYAggCoQAAAABgCAwFqCgGQkBGCCYoGRBAcMAAASBFABCA=}#}二、非选择题:本题共4小题,共55分。
16.(16分)
钒具有广泛用途。黏土钒矿中,钒以+3、+4、+5价的化合物存在,还包括钾、镁的
铝硅酸盐,以及SiO 、Fe O 。采用以下工艺流程可由黏土钒矿制备NH VO 。
2 3 4 4 3
该工艺条件下,溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
金属离子 Fe3+ Fe2+ Al3+ Mn2+
开始沉淀pH 1.9 7.0 3.0 8.1
完全沉淀pH 3.2 9.0 4.7 10.1
回答下列问题:
(1)“酸浸氧化”需要加热,其原因是_________。
(2)“酸浸氧化”中,VO+和VO2+被氧化成VO+ ,同时还有_________离子被氧化。写出
2
VO+转化为VO+ 反应的离子方程式_________。
2
(3)“中和沉淀”中,钒水解并沉淀为V O ·xH O,随滤液②可除去金属离子K+、Mg2+、
2 5 2
Na+、_________,以及部分的_________。
(4)“沉淀转溶”中,V O ·xH O转化为钒酸盐溶解,滤渣③的主要成分是_________。
2 5 2
(5)“调pH”中有沉淀生成,生成沉淀反应的化学方程式是_________。
(6)“沉钒”中析出NH VO 晶体时,需要加入过量NH Cl,其原因是_________。
4 3 4
化学试题 第5页(共8页)
{#{QQABRQYAggCoQAAAABgCAwFqCgGQkBGCCYoGRBAcMAAASBFABCA=}#}17.(12分)
某化学兴趣小组设计了利用MnO 和H SO 生成MnS O ,再与Na CO 反应制备
2 2 3 2 6 2 3
Na S O ·2H O的方案:
2 2 6 2
(1)采用下图所示装置制备SO ,仪器a的名称为_________;步骤I中采用冰水浴是为
2
了_________。
(2)步骤Ⅱ应分数次加入MnO ,原因是_________。
2
(3)写出生成MnS O 的化学方程式_________。
2 6
(4)步骤Ⅳ生成MnCO 沉淀,判断Mn2+已沉淀完全的操作是_________。
3
(5)将步骤Ⅴ中正确操作或现象的标号填入相应括号中。
A.蒸发皿中出现少量晶体
B.使用漏斗趁热过滤
C.利用蒸发皿余热使溶液蒸干
D.用玻璃棒不断搅拌
E.等待蒸发皿冷却
化学试题 第6页(共8页)
{#{QQABRQYAggCoQAAAABgCAwFqCgGQkBGCCYoGRBAcMAAASBFABCA=}#}18.(13分)
卤素的许多化合物是重要化工原料。回答下列问题:
(1)1774年,舍勒在研究软锰矿(主要成分是MnO )的过程中,将它与浓盐酸混合加
2
热,产生了一种黄绿色气体。实验室沿用舍勒的方法制取Cl 的化学方程式为________。
2
(2)“84消毒液”的有效成分为NaClO,不可与酸性清洁剂混用的原因是________(用离
子方程式表示)。
(3)Cl O为淡棕黄色气体,是次氯酸的酸酐,实验室中可用潮湿的Na CO 与少量氯气
2 2 3
反应制得,上述制备Cl O的化学方程式为_________。
2
(4)ClO 常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。
2
①一种有效成分为NaClO 、NaHSO 、NaHCO 的“二氧化氯泡腾片”,能快速溶于水、溢
2 4 3
出大量气泡,得到ClO 溶液,上述过程中生成ClO 的反应属于歧化反应,每生成1 mol
2 2
ClO 消耗NaClO 的量为_______mol;实验室中多余的ClO 可用含H O 的NaOH溶液吸
2 2 2 2 2
收,生成NaClO 溶液,在此吸收反应中,氧化剂与还原剂的物质的量之比为________,
2
其氧化产物是________。
②某小组拟以“
m(ClO2)
”作为衡量ClO 的“产率”指标。若取NaClO 样品6.0 g,通过反应
2 3
m(NaClO3)
和吸收获得250.0 mL ClO 溶液,取此溶液25.0 mL与20.0 mL 0.500 mol/L (NH ) Fe(SO )
2 4 2 4 2
溶液恰好完全反应,试计算ClO 的“产率”________(保留一位小数)。
2
(5)食盐中含有一定量的镁、铁等杂质。某学习小组对加碘食盐进行如下实验:取一定量
某加碘食盐(还可能含有KIO 、MgCl 、FeCl ),用适量蒸馏水溶解,并加稀盐酸酸化,将
3 2 3
所得溶液分为2份。第一份试液中滴加KSCN溶液后显红色,证明该碘盐中含________(用
化学式表示);第二份试液中加亚硫酸钠溶液,试液显淡黄色,用 CCl 萃取,下层溶液显
4
紫红色,生成该有色物质的离子方程式为________。
化学试题 第7页(共8页)
{#{QQABRQYAggCoQAAAABgCAwFqCgGQkBGCCYoGRBAcMAAASBFABCA=}#}19.(14分)
H的盐酸盐是一种镇吐药物,H的合成路线之一如下(略去部分试剂和条件)。
已知:
回答下列问题:
(1)A→B的反应所需试剂为_________。
(2)C中官能团的名称是_________、_________。
(3)C→D的反应类型为_________。
(4)写出D→E的反应方程式_________。
(5)X部分加氢还原得到Z(C H O ),写出能同时满足下列条件的Z的同分异构体的结
6 10 2
构简式_________(任写一种)。
①1 mol Z最多能消耗4 mol新制Cu(OH)
2
②Z分子中含有手性碳原子
(6)药物K的合成路线如下:
已知:Y含有羰基,按照!!"的方法合成I。
I的结构简式为_________,第①步的化学反应方程式为_________。
化学试题 第8页(共8页)
{#{QQABRQYAggCoQAAAABgCAwFqCgGQkBGCCYoGRBAcMAAASBFABCA=}#}