文档内容
邯郸市2025届高三年级第三次调研监测
化 学
本试卷满分100分,考试用时75分钟。
注意事项:
1 .答题前,考生务必将自己的姓名、考生号、考场号、座位号填写在答题卡上。
2 .回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂
黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在
答题卡上。写在本试卷上无效。
3 .考试结束后,将本试卷和答题卡一并交回。
4 .本试卷主要考试内容:高考全部内容。
5 .可能用到的相对原子质量:H 1 C12 N14 0 16 F 19 Na 23 Mg 24
P31 S32 Cl 35; 5 Fe 56 Sb 122
一、选择题:本题共14小题,每小题3分,共42分。每小题只有一个选项符合题意。
L磁山文化,因首先在邯郸市武安磁山发现而得名。磁山文化是仰韶文化的源头之一。磁山文
化最具代表性的器物是陶盂及陶支架、石磨盘及磨棒。磁山是世界上粟、家鸡和核桃等的最
早发现地。下列说法错误的是
A制作陶器的陶土的主要成分为硅酸盐
B.粟中含有脂肪、蛋白质和淀粉,这三者均为天然有机高分子
C.家鸡是餐桌上常见的肉食之一,鸡肉中含有丰富的蛋白质
D.核桃中富含硬脂酸、油酸和亚油酸,此三种酸均为十八碳酸
2,钻的一种配合物Na3[Co(NO2)6:]在分析化学中常用来检验K+,原理为2K++Na+4-
[Co(NO2)6丁一弱酸性或中性 KNatXXNOz”:]。(亮黄色)。下列化学用语表述正确的是
A.中子数为33的钻原子濯Co
B. Na3[Co(NO2)6]中钻元素的化合价为+3价,配位数为3
C. NOF中N原子的杂化轨道类型为sp2,其空间结构为V形
D.基态钾原子最外层的电子云图为
3.下列有关物质的性质与用途具有对应关系的是
选项 用途 性质
A 常用甲苯除去家具表面的油漆斑点 甲苯易挥发
B 水玻璃(NazSiOs水溶液)作防火剂 Na2SiO3溶液显碱性
C 氨气可用作制冷剂 氨气易液化且液氨汽化时吸收大量的热
D 用浓硫酸和NaCl固体制备少量HC1 浓硫酸具有酸性
【高三化学第1页(共8页)】4 .X、Y、Z、W、R、Q是原子序数依次增大的短周期主族元素,其中基态X原子核外电子只有一
种自旋取向,YX3的VSEPR模型为平面三角形,X与Q形成的化合物能刻蚀玻璃。下列说
法正确的是
A. Y、Z、W三种元素中,W的最高价含氧酸酸性最强
B.X分别与Z、W形成的化合物中,前者的沸点一定低于后者
C.与R同周期且第一电离能大于R的元素有2种
D.只由X、W、R三种元素形成的化合物一定为共价化合物
5 .下列反应的离子方程式书写正确的是
A.用稀硝酸清洗试管壁上的银镜:Ag+2H++N0「==Ag+ +NO2 f +H20
B.向冷的石灰乳中通入Ch制漂白粉:Clz+20H—^==Cr+C10-+H20
C.用醋酸除水壶中的水垢(CaCO3):2H++CaCO3 =Ca2+ +C02 f +H20
0H
COOH
D.用碳酸氢钠溶液检验水杨酸中的竣基: + HC07 + H20
+CCU
6 .环丙烷可作为全身麻醉剂,环己烷是重要的有机溶剂。已知某些有机化合物的反应方程式
如下:
Ni
MI+H2菽…
③O+H?袅〜X。
下列说法错误的是
A.可通过核磁共振仪鉴别环丙烷与丙烯
B.烷煌和环烷烧中,C原子的杂化方式相同,均属于饱和燃
C.从上述反应可以看出,最容易发生开环加成反应的环烷煌是环戊烷
D.环丁烷与HBr在一定条件下的反应方程式为<>+HBr段
7 .有机物M的合成路线如下,下列说法错误的是
C. X、Y、Z所含官能团种类相同 D. M具有对映异构体8 .下列实验方案能达到实验目的的是
、夹子
垫有石
棉绒的
caac0 3
固体
C.制备CO2气体,该 D.用酸性KMnO,溶液测定
A.混合乙醇和浓硫酸 B,制取无水MgCl2
装置可随制随停 FeCl2溶液中Fe2+的浓度
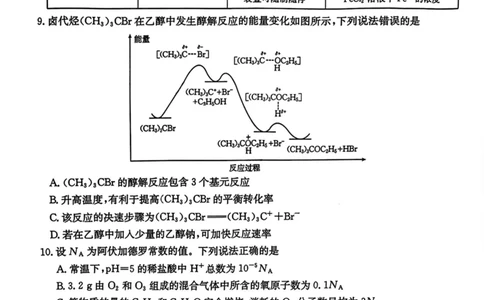
9 .卤代煌(CH3)3CBr在乙醇中发生醇解反应的能量变化如图所示,下列说法错误的是
A. (CH3)3CBr的醇解反应包含3个基元反应
B.升高温度,有利于提高(CHsbCBr的平衡转化率
C.该反应的决速步骤为(CH3)3CBr=(CH3)3C++B-
D.若在乙醇中加入少量的乙醇钠,可加快反应速率
10.设Na为阿伏加德罗常数的值。下列说法正确的是
A.常温下,pH=5的稀盐酸中H+总数为10-5Na
B. 3・2 g由O2和O3组成的混合气体中所含的氧原子数为0. 1Na
C.等物质的量的弓风和C2H6。完全燃烧,消耗的02分子数目均为3Na
D. 2. 4 g Mg在过量的空气中燃烧,生成的产物有MgO、Mg3N2,转移的电子数为2NA
11 .一种高效除去废水中的PO厂的电化学装置如图所示。已知常温下,K5P(FePO1 = 1.3X
10-22,K8pEFe(OH)3]=2. 8X10~39o 下列说法正确的是
A若以铅蓄电池为电源,则a极应与Pb电极相连 02 广|电诿芈1
B,阳极发生的电极反应为4Fe2++O2+4H++4PO7 = '一「卬里、
4FePO4 I +2氏0
R-; pot ■■
C.开始电解前应先调节pH约为2,若pH>4,该电解原理除去 青£,酸性废水与二
por的效率更高
D.电路中有0. 3 mol电子通过时,理论上最多生成的FePO4的质量为22. 65 g12 .铁被誉为“第一金属”,铁及其化合物在生活中有广泛应用,下列说法错误的是
已知:图甲为氧化亚铁晶体结构(晶胞边长为a nm),图乙为氮化铁晶体结构(底边长为
b nm,高为 c run,a=j3=9O°,y=120°)0
A离子半径:Fe2+>Fe3+
B.FeCl3的晶体类型为分子晶体
C.在FeO晶体中,与Fe2+紧邻且等距离的Fe?+数目为6
舞照
D.p(FeN)”(FeO)=
阅读下列材料,完成1344小题,
事实证明,配离子在水中存在解禽平衡,而且,各种配离子的解离能力相差很大。如难溶于
水的AgCl可在浓盐酸中形成AgCl「布解,溶液一稀释,AgCE就解离,出现了 AgCl,而
[FeCCN”了-的水溶液中几乎检验不出CW的存在。已知:①M"+?nX—->|>14)"一"〉一
(配离子)K稳。②K熄{京!1924丁-} = 5.0旅1016,1<稳{0^(。\06丁一} = 1.0义:1035,
K«{[Ag(CN)2]-}=1.0X1021o
13 .下列说法错误的是
A.第一电离能:ON>C1
B. CN一作为配体时,配位原子为C
C. [FeCCN为广的钾盐常用于检验Fe3+的存在
D.K稳越大,说明在水中形成配离子的趋势越大,配离子越稳定
14 .常温下,溶液中CN一分别与三种金属离子形成配离子[Zn(CN) j-、[Ag(CN)2:T、
[Fe(CN)6:T,平衡时与一Igc(CN-)的关系如图所示,其中I表示的是
cl配岗十)
I意儒常与Tgc(CN—)变化的关系。
10
I
0 口
(
+
-10
褪
-20
-lgc(CN-)
a
s
z
(
卜
槌
联
阳
ao
J
-30下列说法错误的是
A.其中ni表示的是1g 市鬻%亍与一lg c(CN— ,变化的关系
B.当I对应的相关离子浓度处于P点时,金属配离子的解离速率小于生成速率
C.当平衡体系中出现 c {CZn(CN)4]2~} =c (ZP )时,c (CN-)
D.当II和ID对应相关离子的混合液处于Q点,达到平衡时,%=3.5
二、非选择题:本题共4小题,共58分。
15 . (14分)三氯氧磷(POCh)是一种重要的化工原料。某小组以P^C12和S02为原料,先制取
PCh,后制备POCh。实验装置如图:
鼠
蜿I
部
已知:
A
物质 PCI3 RCh POC13 SOC12
沸点/c 76.1 160 105.8 78.8
其他 遇水均剧烈水解
螭
回答下列问题:
(D仪器a的名称为 o
(2)装置D的作用是 o
(3)装置B除生成POC13外还有SOC12生成,写出反应的化学方程式:。
(4)装置C中装有浓硫酸,其目的是 o实验室欲提纯POCh,可采用的方
法是 0
(5)POC13纯度测定:测定样品中杂质SOC12的含量即可得出POC13的纯度(假设杂质仅含
有 SO。)。
步骤1:准确称量提纯后的m g样品。
步骤2:将称量好的样品放入盛有280 mL NaOH溶液(过量)的锥形瓶中,密封,充分反
应(SOCI2 +4NaOH -Na2 so3 +2NaCl+2H2 O)后冷却,再将锥形瓶中的溶液全部转
移到500 mL容量瓶中,洗涤锥形瓶2〜3次,洗涤液一并转入容量瓶中,静置至室温,定
容,摇匀,得到溶液X。
步骤3:准确量取50. 00 mL溶液X于250 mL碘量瓶中,加入两滴指示剂,用2 mol - L-1
的盐酸中和过量的NaOH溶液至恰好完全。
【高三化学 第5页(共8页)]步骤4:准确加入% mLc】 mol - L-1碘标准溶液,充分反应后,用淀粉溶液作指示剂,用
C2 mol・L_1的Na2S2O3溶液滴定过量的碘,反应为I2+2Na2S2O3 -+
2NaIe平行测定四次,反应消耗Na282c)3溶液的平均体积为匕mL0
①实验室常用溶质质量分数为36. 5%,密度为1.19 g - cm-3的浓盐酸来配制2 mol • L-1
的盐酸,则该操作中除需要使用250 mL容量瓶、量筒和烧杯外,还需要的玻璃仪器
有 O
②则样品中POC13的质量分数为(用含c】、C2、Vi、V2、m的代数式表示);下列
情况会导致POCh的质量分数偏高的是(填标号)。
A与NaOH反应时,未密封锥形瓶导致有部分气体逸出
B.实际N^SaOa溶液浓度偏高
C.步骤2定容时俯视刻度线
16 . (15分)NaSbF6(六氟镁酸钠)是光化学反应的催化剂。我国科学家开发的一种以睇矿(主要
含Sb2C)3、Sb2S3,还含少量FgC^CuS'SbzOs等)为原料制备NaSbF6的工艺流程如图
所示。
NaOH'NaBOs溶液胆矶 X修。2 氢氟酸
镒矿T 彳出陛驾珅Tl->lWl->NaSbO3 - 3H2O晶体 现堡作■» NaSbFe
滤渣1 浪渣2
已知:①常温下,K£CuS)=6. 3X1076、 k/Cu(OH)21=2. 1X10-2。。
②“滤液”中主要含有NaSbOz、Na2s以及NaOH三种溶质。
回答下列问题:
⑴锚矿含有的五种元素61)壬6、。1、0、5)中位于元素周期表p区的有 种,基态Sb
原子的价电子排布式为 O
⑵“浸出”时Sb2s3可与NaOH反应生成硫代亚睇酸盐(Na3sbs3)和亚锦酸盐(NasSbOs),
写出反应的离子方程式:;SbSr只能在碱性介质中存在,通酸则生成
硫代亚储酸(不稳定,与亚硫酸类似,会分解),写出Na3sbs3与稀硫酸反应的离子方程
式:O
(3)“滤渣1"的成分是(填化学式)。
(4)“精制”的目的是除去溶液中的S?一。常温下,向“滤液”中加入胆矶,生成CuS和
Cu(OH)2沉淀,若此时溶液的pH为10,则溶液中剩余c(S2、=mol・L"
(5)锦矿粉中Sb的质量分数为20%,整个流程中损失率为5%,则10 t睇矿粉理论上能制备
NaSbF6的质量为(保留两位有效数字)£
(6)工业上还可以通过电解含Na3sbs3、Na2S、NaOH的溶液制备金属Sb,电解过程中,阳极
上发生的电极反应为。
【高三化学第6页(共8页)】17 .(14分)尿素[CCKNHzM是第一种由无机物人工合成的有机物。根据所学知识,回答下列
问题:
(D已知:一定温度下,由元素的最稳定的单质生成1 mol纯物质的热效应称为该物质的摩
尔生成烙,化学反应的婚变(AbOnAFf(生成物的摩尔生成焙总和)一(反应物的摩
尔生成培总和)。
物质 NH3(g) CO2(g) 乩 0(g) CO(NH2)2(s)
摩尔生成婚/(kJ・mor1) -46.11 -393. 5 -241. 8 -333. 51
则 2NH3(g)+CO2(g)-CO(NH2)2(s) + H2O(g) △”=kJ • moL,该反
应在(填“高温”“低温”或“任意温度”)下能自发进行。
(2)1 ℃,某恒容密闭容器中,只发生反应2NH3(g)+CO2(g)—CO(NH2)2(s)+H2O(g),下
列说法正确的是(填标号)。
A.若混合气体的质量不再随时间变化而改变,则该反应达到平衡
B.若氏0(g)的质量不再随时间变化而改变,则该反应达到平衡
C.每断裂0. 3 mol N—H键,同时生成0. 2 mol H—0键
D.每消耗 2. 24 L NH3(g),同时生成 0. 05 mol CO(NH2)2(s)
(3)氨基甲酸筱(H2NCOONH4)是以氨气和二氧化碳为原料合成尿素的中间产物,
2NH3 (g) +C02 (g)^H2NCOONH4 (s) △H]V0。在恒温条件下,将足量纯净的氨
基甲酸钱置于容器中[只发生:H2NCOONH4 (s)-2NH3 (g) +CO2(g)],先关闭K3,
打开K】和K2,开启真空泵抽气至测压仪数值接近0后关闭Ki,关闭尺,缓慢开启K3,
以维持“口 ”字形管两边液面始终相平。读取并记录该过程的压强数值(如图)。
①0〜5 min内,用分压变化表示”(NH3)= kPa - min-10该反应的平衡常数
/=kPa30
②相同温度下,投入足量的氨基甲酸铁固体后,欲使平衡时/>(NH3)<2 kPa,可提前在
真空恒容容器中充入一定量的C02,则提前充入的C02压强至少为 kPa。
(4)科学家开发催化电极材料,实现电催化C02和硝酸盐
在常温常压下合成尿素。电解质溶液为一定浓度
KNO3溶液,在电极上生成CO(NH2)2,模拟装置如图
所示。
①a极电极反应式为 o
KNO籀液 质子交换膜
②每生成 30. 0 g CO(NH2)2,有 mol H+ 由 b
极向a极迁移。18. (15分)化合物G是某化工生产中的重要中间体,其合成路线如下:
D E F G
已知:Me表示一CH3,Et表示一C2H5。回答下列问题:
(1) CH2=CHCOOCH3的化学名称为,B分子中含氧官能团的名称为 o
(2)若实验中未进行B—>C转化,即B直接与EtMgBr反应,可能生成分子式为C16H26。3 密
的副产物,贝。该副产物的结构简式为。
撵
(3)E-F的反应类型为 o
(4)按氮原子所连短基数目分析,Et3N可归类为(填“伯胺”“仲胺”或“叔胺
Me3N的碱性弱于EtsN,试解释其原因 o
(5)G有同时满足下列条件的同分异构体,写出一种该同分异构体的结构简式:o
①除苯环外不含其他环状结构;②能发生银镜反应;③含有对称的t—Bu(叔丁基)o
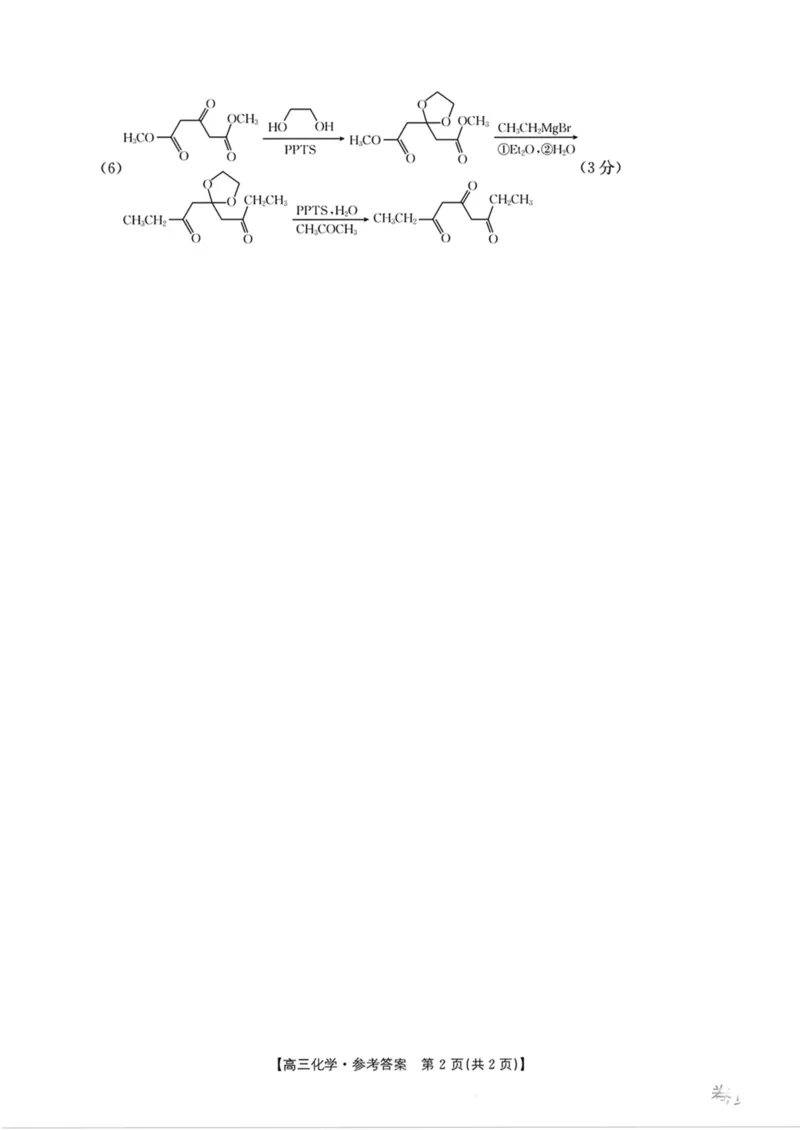
(6)烧基卤化镁在有机合成中的广泛应用,极大地推动了有机化学的发展。写出以
引
Z° OCH3
H3C0_^_\_^ 、CH3CH2MgBr 和 HOCH2cH20H 为原 料制备
涮
O O
CH2cH3 噌
CH3cH2 的合成路线流程图(无机试剂和有机溶剂任用,合成路线
0 0
陶
流程图示例见本题题干)。
【高三化学第8页(共8页)】邯郸市2025届高三年级第三次调研监测
化学参考答案
l.B 2.C 3. C 4. A 5.D 6. C 7. C 8. C 9. B 10. D 11. D 12. C 13. A 14. B
15. (D三颈烧瓶(或三口烧瓶,1分)
(2)吸收SO2X12等尾气,防止污染空气(答到吸收尾气或防止污染空气或防止空气中的水
蒸气进入均可,2分)
(3)PC13+C12+SO2 ===POC13+SOC12(2 分)
(4)干燥气体,同时便于控制气体流速和反应体积比(2分);蒸镭(1分)
(5)①玻璃棒、胶头滴管(2分)
②---------------~~」-%(2 分);A(2 分)
m
16. (1)3(1 分);5s25P3(2分)
(2)Sb2s3+6OH-.SbS^-l SbOf+3H2O(2 分);2sbs 打+6H+----。+3H2Sf
(H3sbs3未拆写不扣分,未写“本““心”不扣分,2分)
(3)Fe2O3 和 CuS(2 分)
(4)3X10-24(2 分)
(5)4. 0(2 分)
(6)S2--2e--S(或 40H一一4e---- O" 卜2H2。,任写一个即可,2 分)
17. (1)-89. 59(1 分);低温(1 分)
(2)AB(2 分)
(3)① 1.6(2 分);256(2 分)
②63(2分)
(4)(DCO2+2NOr + 18H+ + 16e~==CO(NH2)2+7H2O(2 分)
②8(2分)
18. (1)丙烯酸甲酯(2分);埃基(答酮基或酮谈基都给分)、酯基(2分)
(3)加成反应(只写“加成”也给分,1分)
(4)叔胺(1分);三乙胺中的乙基比三甲胺中的甲基具有更强的供电子效应,导致三乙胺中
氮原子的电子密度更高,从而使其碱性更强(2分)
CHO
h
⑸ Q [或 分]
(CH3)3C C(CH3)3 (CH3)3C %(产国)3
【高三化学•参考答案 第1页(共2页)】()
(3分)
【高三化学•参考答案第2页(共2页)】