文档内容
专题 08 化学反应速率与化学平衡
考点 三年考情(2022-2024) 命题趋势
◆化学反应速率:2024安徽卷、2024江
选择题中对于化学反应速率和化学平衡内容
苏卷、2024甘肃卷、2023广东卷、2023
的考查不算太多,这是因为在主观题中,化
山东卷、2023辽宁卷、2023浙江卷、
学反应速率和化学平衡才是考查的重头戏。
2022广东卷、2022北京卷、2022河北
随着新高考单科卷的实行,选择题题量大
考点1 化学反 卷、2022浙江卷
增,有关化学反应速率和化学平衡试题的考
应速率与化学 ◆化学平衡:2024黑吉辽卷、2024山东
查在选择题中开始有所增加,考查的核心知
平衡 卷、2024江苏卷、2024浙江卷、2024湖
识还是有关化学反应速率的比较、计算和影
南卷、2023北京卷、2023湖南卷、2023
响因素的判断,化学平衡常数、转化率、物
山东卷、2022天津卷、2022重庆卷、
质的浓度的计算,以及平衡移动原理的分析
2022江苏卷、2022浙江卷、2022北京
等,常结合坐标图像或表格进行考查。
卷、2022辽宁卷、2022湖南卷
考法01 化学反应速率
1. (2024·安徽卷)室温下,为探究纳米铁去除水样中SeO2-的影响因素,测得不同条件下SeO2-浓度随时间
4 4
变化关系如下图。
实验序号 水样体积/mL 纳米铁质量/mg 水样初始pH
① 50 8 6② 50 2 6
③ 50 2 8
下列说法正确的是
A. 实验①中,0~2小时内平均反应速率v(SeO 2-)=2.0mol·L-1·h-1
4
B. 实验③中,反应的离子方程式为:2Fe+SeO 2-+8H+=2Fe3++Se+4H O
4 2
C. 其他条件相同时,适当增加纳米铁质量可加快反应速率
D. 其他条件相同时,水样初始pH越小,SeO2-的去除效果越好
4
【答案】C
【解析】A. 实验①中,0~2小时内平均反应速率 ,A
不正确;
B. 实验③中水样初始 =8,溶液显弱碱性,发生反应的离子方程式中不能用 配电荷守恒,B不正确;
C. 综合分析实验①和②可知,在相同时间内,实验①中 浓度的变化量大,因此,其他条件相同时,
适当增加纳米铁质量可加快反应速率,C正确;
D. 综合分析实验③和②可知,在相同时间内,实验②中 浓度的变化量大,因此,其他条件相同时,
适当减小初始 , 的去除效果越好,但是当初始 太小时, 浓度太大,纳米铁与 反应速
率加快,会导致与 反应的纳米铁减少,因此,当初始 越小时 的去除效果不一定越好,D
不正确;
综上所述,本题选C。
2. (2024·江苏卷)下列说法正确的是
A. 豆科植物固氮过程中,固氮酶能提高该反应的活化能
B. 与 反应中,Ag催化能提高生成 的选择性
C. 制 反应中, 能加快化学反应速率
D. 与 反应中, 能减小该反应的焓变
【答案】C
【解析】A. 固氮酶是豆科植物固氮过程的催化剂,能降低该反应的活化能,A错误;
B.根据题意,催化剂有选择性,如C H 与O 反应用Ag催化生成 (环氧乙烷)、用CuCl /PdCl
2 4 2 2 2
催化生成CHCHO,则判断Ag催化不能提高生成CHCHO的选择性,B错误;
3 3
C. MnO 是HO 制O 反应的催化剂,能加快化学反应速率,C正确;
2 2 2 2
D. VO 是SO 与O 反应的催化剂,能加快反应速率,但不能改变该反应的焓变,D错误;
2 5 2 2
故选C。3. (2024·甘肃卷)下列措施能降低化学反应速率的是
A. 催化氧化氨制备硝酸时加入铂 B. 中和滴定时,边滴边摇锥形瓶
C. 锌粉和盐酸反应时加水稀释 D. 石墨合成金刚石时增大压强
【答案】C
【解析】A.催化剂可以改变化学反应速率,一般来说,催化剂可以用来加快化学反应速率,故催化氧化
氨制备硝酸时加入铂可以加快化学反应速率,A项不符合题意;
B.中和滴定时,边滴边摇锥形瓶,可以让反应物快速接触,可以加快化学反应速率,B项不符合题意;
C.锌粉和盐酸反应时加水稀释会降低盐酸的浓度,会降低化学反应速率,C项符合题意;
D.石墨合成金刚石,该反应中没有气体参与,增大压强不会改变化学反应速率,D项不符合题意;
故选C。
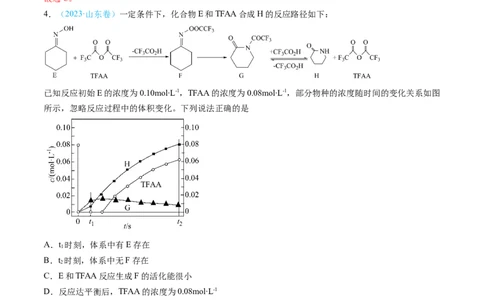
4.(2023·山东卷)一定条件下,化合物E和TFAA合成H的反应路径如下:
已知反应初始E的浓度为0.10mol∙L-1,TFAA的浓度为0.08mol∙L-1,部分物种的浓度随时间的变化关系如图
所示,忽略反应过程中的体积变化。下列说法正确的是
A.t 时刻,体系中有E存在
1
B.t 时刻,体系中无F存在
2
C.E和TFAA反应生成F的活化能很小
D.反应达平衡后,TFAA的浓度为0.08mol∙L-1
【答案】AC
【分析】一定条件下,化合物E和TFAA合成H的反应路径中,共发生三个反应:
①E+TFAA F ②F G ③G H+TFAA
t 之后的某时刻,H为0.02 mol∙L-1,此时TFAA的浓度仍为0,则表明0.10mol∙L-1E、起始时的
1
0.08mol∙L-1TFAA、G分解生成的0.02 mol∙L-1 TFAA全部参加反应,生成0.10mol∙L-1F;在t 时刻,H为
2
0.08mol∙L-1,TFAA为0.06mol∙L-1,G为0.01 mol∙L-1,则F为0.01 mol∙L-1。
【解析】A.t 时刻,H的浓度小于0.02 mol∙L-1,此时反应③生成F的浓度小于0.02 mol∙L-1,参加反应①的
1H的浓度小于0.1 mol∙L-1,则参加反应E的浓度小于0.1 mol∙L-1,所以体系中有E存在,A正确;
B.由分析可知,t 时刻,H为0.08mol∙L-1,TFAA为0.06mol∙L-1,G为0.01 mol∙L-1,则F为0.01 mol∙L-1,
2
所以体系中有F存在,B不正确;
C.t 之后的某时刻,H为0.02 mol∙L-1,此时TFAA的浓度仍为0,表明此时E和TFAA完全反应生成F,
1
所以E和TFAA生成F的反应速率快,反应的活化能很小,C正确;
D.在t 时刻,H为0.08mol∙L-1,TFAA为0.06mol∙L-1,G为0.01 mol∙L-1,F为0.01 mol∙L-1,只有F、G全部
2
转化为H和TFAA时,TFAA的浓度才能为0.08mol∙L-1,而G H+TFAA为可逆反应,所以反应达平衡后,
TFAA的浓度一定小于0.08mol∙L-1,D不正确;
故选AC。
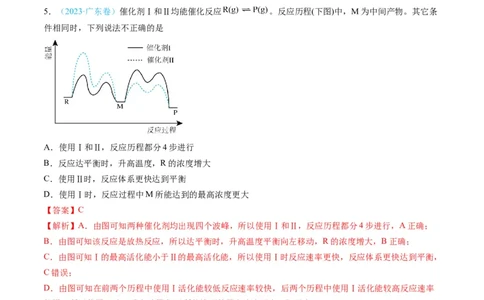
5.(2023·广东卷)催化剂Ⅰ和Ⅱ均能催化反应 。反应历程(下图)中,M为中间产物。其它条
件相同时,下列说法不正确的是
A.使用Ⅰ和Ⅱ,反应历程都分4步进行
B.反应达平衡时,升高温度,R的浓度增大
C.使用Ⅱ时,反应体系更快达到平衡
D.使用Ⅰ时,反应过程中M所能达到的最高浓度更大
【答案】C
【解析】A.由图可知两种催化剂均出现四个波峰,所以使用Ⅰ和Ⅱ,反应历程都分4步进行,A正确;
B.由图可知该反应是放热反应,所以达平衡时,升高温度平衡向左移动,R的浓度增大,B正确;
C.由图可知Ⅰ的最高活化能小于Ⅱ的最高活化能,所以使用Ⅰ时反应速率更快,反应体系更快达到平衡,
C错误;
D.由图可知在前两个历程中使用Ⅰ活化能较低反应速率较快,后两个历程中使用Ⅰ活化能较高反应速率
较慢,所以使用Ⅰ时,反应过程中M所能达到的最高浓度更大,D正确;
故选C。
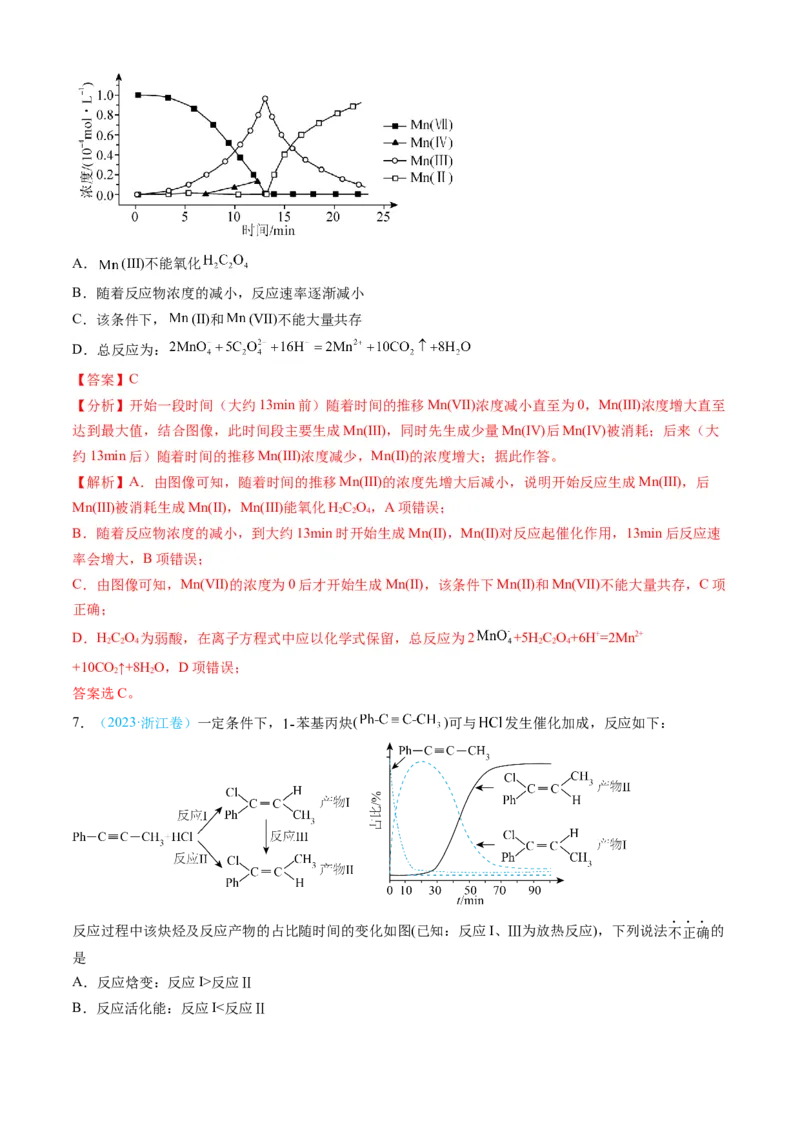
6.(2023·辽宁卷)一定条件下,酸性 溶液与 发生反应, (Ⅱ)起催化作用,过程中不同
价态含 粒子的浓度随时间变化如下图所示。下列说法正确的是A. (Ⅲ)不能氧化
B.随着反应物浓度的减小,反应速率逐渐减小
C.该条件下, (Ⅱ)和 (Ⅶ)不能大量共存
D.总反应为:
【答案】C
【分析】开始一段时间(大约13min前)随着时间的推移Mn(Ⅶ)浓度减小直至为0,Mn(Ⅲ)浓度增大直至
达到最大值,结合图像,此时间段主要生成Mn(Ⅲ),同时先生成少量Mn(Ⅳ)后Mn(Ⅳ)被消耗;后来(大
约13min后)随着时间的推移Mn(Ⅲ)浓度减少,Mn(Ⅱ)的浓度增大;据此作答。
【解析】A.由图像可知,随着时间的推移Mn(Ⅲ)的浓度先增大后减小,说明开始反应生成Mn(Ⅲ),后
Mn(Ⅲ)被消耗生成Mn(Ⅱ),Mn(Ⅲ)能氧化HC O,A项错误;
2 2 4
B.随着反应物浓度的减小,到大约13min时开始生成Mn(Ⅱ),Mn(Ⅱ)对反应起催化作用,13min后反应速
率会增大,B项错误;
C.由图像可知,Mn(Ⅶ)的浓度为0后才开始生成Mn(Ⅱ),该条件下Mn(Ⅱ)和Mn(Ⅶ)不能大量共存,C项
正确;
D.HC O 为弱酸,在离子方程式中应以化学式保留,总反应为2 +5H C O+6H+=2Mn2+
2 2 4 2 2 4
+10CO ↑+8H O,D项错误;
2 2
答案选C。
7.(2023·浙江卷)一定条件下, 苯基丙炔( )可与 发生催化加成,反应如下:
反应过程中该炔烃及反应产物的占比随时间的变化如图(已知:反应I、Ⅲ为放热反应),下列说法不正确的
是
A.反应焓变:反应I>反应Ⅱ
B.反应活化能:反应I<反应ⅡC.增加 浓度可增加平衡时产物Ⅱ和产物I的比例
D.选择相对较短的反应时间,及时分离可获得高产率的产物Ⅰ
【答案】C
【解析】A.反应I、Ⅲ为放热反应,相同物质的量的反应物,反应I放出的热量小于反应Ⅱ放出的热量,
反应放出的热量越多,其焓变越小,因此反应焓变:反应I>反应Ⅱ,故A正确;
B.短时间里反应I得到的产物比反应Ⅱ得到的产物多,说明反应I的速率比反应Ⅱ的速率快,速率越快,
其活化能越小,则反应活化能:反应I<反应Ⅱ,故B正确;
C.增加HCl浓度,平衡正向移动,但平衡时产物Ⅱ和产物I的比例可能降低,故C错误;
D.根据图中信息,选择相对较短的反应时间,及时分离可获得高产率的产物Ⅰ,故D正确。
综上所述,答案为C。
8.(2022·广东卷)在相同条件下研究催化剂I、Ⅱ对反应 的影响,各物质浓度c随反应时间t的
部分变化曲线如图,则
A.无催化剂时,反应不能进行
B.与催化剂Ⅰ相比,Ⅱ使反应活化能更低
C.a曲线表示使用催化剂Ⅱ时X的浓度随t的变化
D.使用催化剂Ⅰ时, 内,
【答案】D
【解析】A.由图可知,无催化剂时,随反应进行,生成物浓度也在增加,说明反应也在进行,故A错误;
B.由图可知,催化剂I比催化剂II催化效果好,说明催化剂I使反应活化能更低,反应更快,故B错误;
C.由图可知,使用催化剂II时,在0~2min 内Y的浓度变化了2.0mol/L,而a曲线表示的X的浓度变化
了2.0mol/L,二者变化量之比不等于化学计量数之比,所以a曲线不表示使用催化剂II时X浓度随时间t
的变化,故C错误;
D.使用催化剂I时,在0~2min 内,Y的浓度变化了4.0mol/L,则 (Y) = = =2.0
, (X) = (Y) = 2.0 =1.0 ,故D正确;
答案选D。
9.(2022·北京卷)CO 捕获和转化可减少CO 排放并实现资源利用,原理如图1所示。反应①完成之后,
2 2
以N 为载气,以恒定组成的N、CH 混合气,以恒定流速通入反应器,单位时间流出气体各组分的物质的
2 2 4
量随反应时间变化如图2所示。反应过程中始终未检测到CO,在催化剂上有积碳。
2下列说法不正确的是
A.反应①为CaO+CO =CaCO ;反应②为CaCO +CH CaO+2CO+2H
2 3 3 4 2
B.t~t,n(H )比n(CO)多,且生成H 速率不变,可能有副反应CH C+2H
1 3 2 2 4 2
C.t 时刻,副反应生成H 的速率大于反应②生成H 速率
2 2 2
D.t 之后,生成CO的速率为0,是因为反应②不再发生
3
【答案】C
【解析】A.由题干图1所示信息可知,反应①为CaO+CO =CaCO ,结合氧化还原反应配平可得反应②为
2 3
,A正确;
B.由题干图2信息可知,t~t,n(H )比n(CO)多,且生成H 速率不变,且反应过程中始终未检测到CO,
1 3 2 2 2
在催化剂上有积碳,故可能有副反应 ,反应②和副反应中CH 和H 的系数比均为1:2,
4 2
B正确;
C.由题干反应②方程式可知,H 和CO的反应速率相等,而t 时刻信息可知,H 的反应速率未变,仍然
2 2 2
为2mmol/min,而CO变为1~2mmol/min之间,故能够说明副反应生成H 的速率小于反应②生成H 速率,
2 2
C错误;
D.由题干图2信息可知,t 之后,CO的速率为0,CH 的速率逐渐增大,最终恢复到1,说明生成CO的
3 4
速率为0,是因为反应②不再发生,而后副反应逐渐停止反应,D正确;
答案选C。
10.(2022·河北卷)恒温恒容条件下,向密闭容器中加入一定量X,发生反应的方程式为① ;②
。反应①的速率 ,反应②的速率 ,式中 为速率常数。图甲为该体系中X、
Y、Z浓度随时间变化的曲线,图乙为反应①和②的 曲线。下列说法错误的是A.随 的减小,反应①、②的速率均降低
B.体系中
C.欲提高Y的产率,需提高反应温度且控制反应时间
D.温度低于 时,总反应速率由反应②决定
【答案】AB
【分析】由图中的信息可知,浓度随时间变化逐渐减小的代表的是X,浓度随时间变化逐渐增大的代表的
是Z,浓度随时间变化先增大后减小的代表的是Y;由图乙中的信息可知,反应①的速率常数随温度升高
增大的幅度小于反应②的。
【解析】A.由图甲中的信息可知,随c(X)的减小,c(Y) 先增大后减小,c(Z)增大,因此,反应①的速率
随c(X)的减小而减小,而反应②的速率先增大后减小,A说法错误;
B.根据体系中发生的反应可知,在Y的浓度达到最大值之前,单位时间内X的减少量等于Y和Z的增加
量,因此,v (X)= v (Y) +v(Z),但是,在Y的浓度达到最大值之后,单位时间内Z的增加量等于Y和X
的减少量,故v (X) + v (Y) = v(Z),B说法错误;
C.升高温度可以可以加快反应①的速率,但是反应①的速率常数随温度升高增大的幅度小于反应②的,
且反应②的的速率随着Y的浓度的增大而增大,因此,欲提高Y的产率,需提高反应温度且控制反应时间,
C说法正确;
D.由图乙信息可知,温度低于T 时,k>k,反应②为慢反应,因此,总反应速率由反应②决定,D说法
1 1 2
正确;
综上所述,本题选AB。
11.(2022·浙江卷)在恒温恒容条件下,发生反应A(s)+2B(g) 3X(g),c(B)随时间的变化如图中曲线
甲所示。下列说法不正确的是
A.从a、c两点坐标可求得从a到c时间间隔内该化学反应的平均速率
B.从b点切线的斜率可求得该化学反应在反应开始时的瞬时速率
C.在不同时刻都存在关系:2v(B)=3v(X)D.维持温度、容积、反应物起始的量不变,向反应体系中加入催化剂,c(B)随时间变化关系如图中曲线
乙所示
【答案】C
【解析】A.图象中可以得到单位时间内的浓度变化,反应速率是单位时间内物质的浓度变化计算得到,
从a、c两点坐标可求得从a到c时间间隔内该化学反应的平均速率,选项A正确;
B.b点处的切线的斜率是此时刻物质浓度除以此时刻时间,为反应物B的瞬时速率,选项B正确;
C.化学反应速率之比等于化学方程式计量数之比分析,3v(B)=2v(X),选项C不正确;
D.维持温度、容积不变,向反应体系中加入催化剂,平衡不移动,反应速率增大,达到新的平衡状态,
平衡状态与原来的平衡状态相同,选项D正确;
答案选C。
考法02 化学平衡
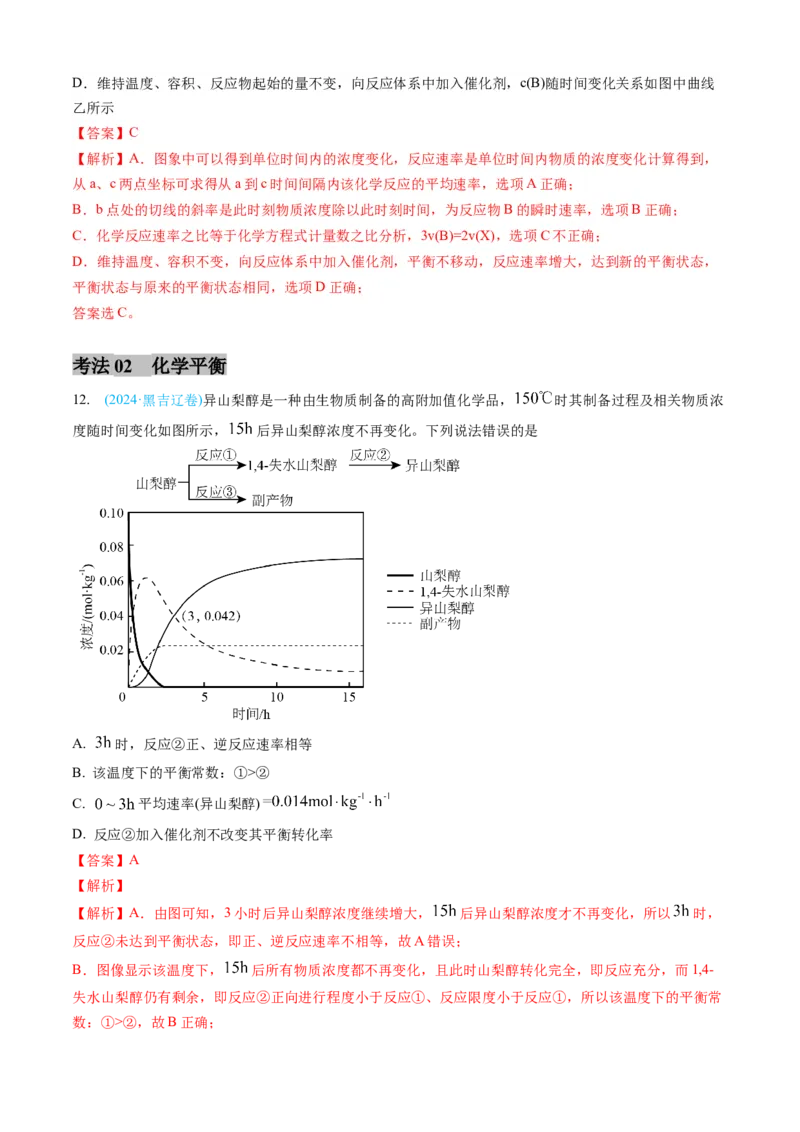
12. (2024·黑吉辽卷)异山梨醇是一种由生物质制备的高附加值化学品, 时其制备过程及相关物质浓
度随时间变化如图所示, 后异山梨醇浓度不再变化。下列说法错误的是
A. 时,反应②正、逆反应速率相等
B. 该温度下的平衡常数:①>②
C. 平均速率(异山梨醇)
D. 反应②加入催化剂不改变其平衡转化率
【答案】A
【解析】
【解析】A.由图可知,3小时后异山梨醇浓度继续增大, 后异山梨醇浓度才不再变化,所以 时,
反应②未达到平衡状态,即正、逆反应速率不相等,故A错误;
B.图像显示该温度下, 后所有物质浓度都不再变化,且此时山梨醇转化完全,即反应充分,而1,4-
失水山梨醇仍有剩余,即反应②正向进行程度小于反应①、反应限度小于反应①,所以该温度下的平衡常
数:①>②,故B正确;C.由图可知,在 内异山梨醇的浓度变化量为0.042mol/kg,所以平均速率(异山梨醇)=
,故C正确;
D.催化剂只能改变化学反应速率,不能改变物质平衡转化率,所以反应②加入催化剂不改变其平衡转化
率,故D正确;
故答案为:A。
13. (2024·山东卷)逆水气变换反应: 。一定压力下,按 ,
物质的量之比 投料, , 温度时反应物摩尔分数随时间变化关系如图所示。已
知该反应的速率方程为 , , 温度时反应速率常数k分别为 。下列说法错
误的是
A.
B. 温度下达平衡时反应速率的比值:
C. 温度不变,仅改变体系初始压力,反应物摩尔分数随时间的变化曲线不变
D. 温度下,改变初始投料比例,可使平衡时各组分摩尔分数与 温度时相同
【答案】CD
【解析】
【分析】由图可知,T 比T 反应速率速率快,则T >T ;T 温度下达到平衡时反应物的摩尔分数低于T 温
1 2 1 2 1 2
度下平衡时;由于起始CO 与H 的物质的量之比为1∶1,则达到平衡时CO 和H 的摩尔分数相等。
2 2 2 2
【解析】A.根据分析,T 比T 反应速率速率快,反应速率常数与温度有关,结合反应速率方程知k>
1 2 1
k,A项正确;
2
B.反应的速率方程为v=kc0.5(H )c(CO),则 ,T 温度下达到平衡时反应物的
2 2 1
摩尔分数低于T 温度下平衡时,则 ,B项正确;
2
C.温度不变,仅改变体系初始压力,虽然平衡不移动,但反应物的浓度改变,反应速率改变,反应达到平衡的时间改变,反应物摩尔分数随时间的变化曲线变化,C项错误;
D.T 温度下,改变初始投料比,相当于改变某一反应物的浓度,达到平衡时H 和CO 的摩尔分数不可能
2 2 2
相等,故不能使平衡时各组分摩尔分数与T 温度时相同,D项错误;
1
答案选CD。
14. (2024·江苏卷)二氧化碳加氢制甲醇的过程中的主要反应(忽略其他副反应)为:
①
②
、 下,将一定比例 、 混合气匀速通过装有催化剂的绝热反应管。装置及L、L、
1 2
L…位点处(相邻位点距离相同)的气体温度、CO和 的体积分数如图所示。下列说法正确的是
3
A. L 处与L 处反应①的平衡常数K相等
4 5
B. 反应②的焓变
C. L 处的 的体积分数大于L 处
6 5
D. 混合气从起始到通过L 处,CO的生成速率小于 的生成速率
1
【答案】C
【解析】A.L 处与L 处的温度不同,故反应①的平衡常数K不相等,A错误;
4 5
B.由图像可知,L-L 温度在升高,该装置为绝热装置,反应①为吸热反应,所以反应②为放热反应,
1 3
ΔH<0,B错误;
2
C.从L 到L,甲醇的体积分数逐渐增加,说明反应②在向右进行,反应②消耗 CO,而 CO 体积分数没
5 6
有明显变化,说明反应①也在向右进行,反应①为气体分子数不变的反应,其向右进行时,n(H O) 增大,
2
反应②为气体分子数减小的反应,且没有HO的消耗与生成,故 n总减小而n(H₂O)增加,即HO的体积
2 2
分数会增大,故L 处的 HO的体积分数大于L 处,C正确;
6 2 5
D.L 处CO 体的积分数大于 CHOH,说明生成的 CO 的物质的量大于CHOH,两者反应时间相同,说
1 3 3
明CO的生成速率大于 CHOH的生成速率,D错误;
3
故选C。
15. (2024·浙江卷6月)二氧化碳氧化乙烷制备乙烯,主要发生如下两个反应:
I.II.
向容积为 的密闭容器中投入 和 ,不同温度下,测得 时(反应均未平衡)的
相关数据见下表,下列说法不正确的是
温度( ) 400 500 600
乙烷转化率( ) 2.2 9.0 17.8
乙烯选择性( ) 92.6 80.0 61.8
注:乙烯选择性
A. 反应活化能:
B. 时, 反应I的平均速率为:
C. 其他条件不变,平衡后及时移除 ,可提高乙烯的产率
D. 其他条件不变,增大投料比 投料,平衡后可提高乙烷转化率
【答案】D
【解析】A.由表可知,相同温度下,乙烷在发生转化时,反应Ⅰ更易发生,则反应活化能:Ⅰ<Ⅱ,A正
确;
B.由表可知,500℃时,乙烷的转化率为9.0%,可得转化的乙烷的总物质的量为2mol×9.0%=0.18mol,而
此温度下乙烯的选择性为80%,则转化为乙烯的乙烷的物质的量为0.18mol×80%=0.144mol,根据方程式可
得 , 生 成 乙 烯 的 物 质 的 量 为 0.144mol , 则 反 应 I 的 平 均 速 率 为 :
,B正确;
C.其他条件不变,平衡后及时移除 ,反应Ⅰ正向进行,可提高乙烯的产率,C正确;
D.其他条件不变,增大投料比 投料,平衡后CO 转化率提高,C H 转化率降低,D
2 2 6
错误;
答案选D。
16. (2024·湖南卷)恒压下,向某密闭容器中充入一定量的 和 ,发生如下反应:
主反应:
副反应:
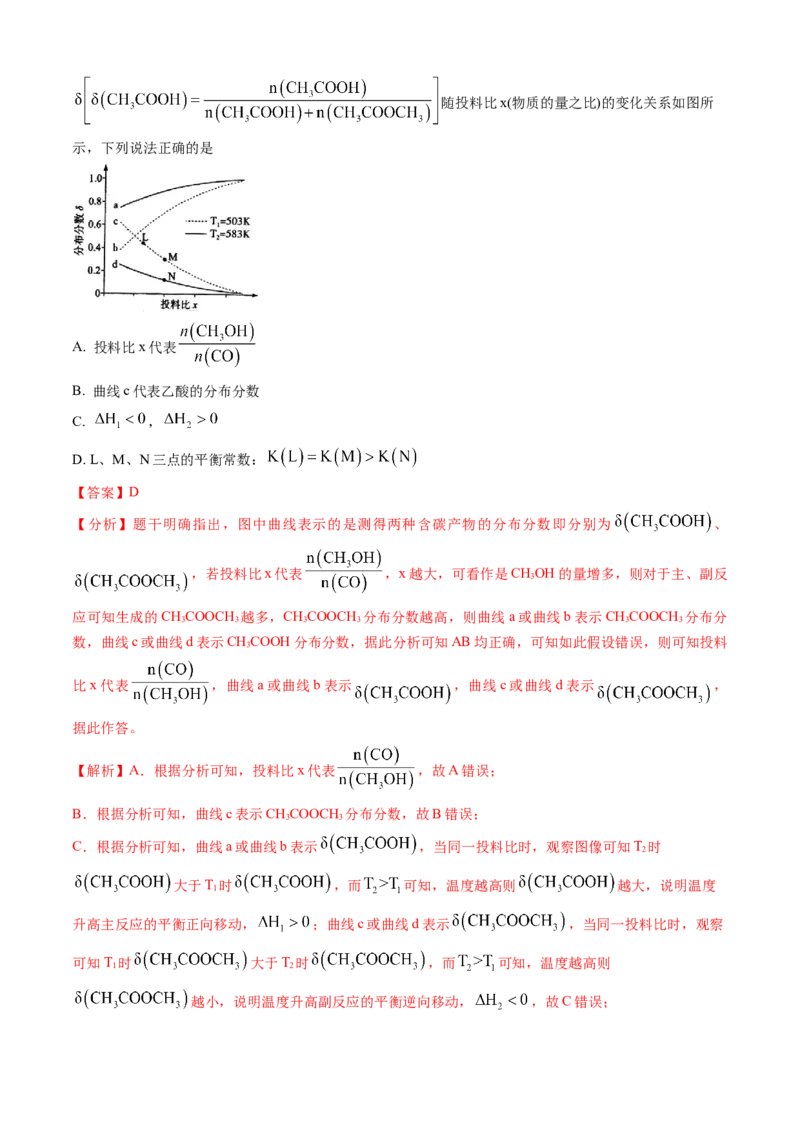
在不同温度下,反应达到平衡时,测得两种含碳产物的分布分数随投料比x(物质的量之比)的变化关系如图所
示,下列说法正确的是
A. 投料比x代表
B. 曲线c代表乙酸的分布分数
C. ,
D. L、M、N三点的平衡常数:
【答案】D
【分析】题干明确指出,图中曲线表示的是测得两种含碳产物的分布分数即分别为 、
,若投料比x代表 ,x越大,可看作是CHOH的量增多,则对于主、副反
3
应可知生成的CHCOOCH 越多,CHCOOCH 分布分数越高,则曲线a或曲线b表示CHCOOCH 分布分
3 3 3 3 3 3
数,曲线c或曲线d表示CHCOOH分布分数,据此分析可知AB均正确,可知如此假设错误,则可知投料
3
比x代表 ,曲线a或曲线b表示 ,曲线c或曲线d表示 ,
据此作答。
【解析】A.根据分析可知,投料比x代表 ,故A错误;
B.根据分析可知,曲线c表示CHCOOCH 分布分数,故B错误;
3 3
C.根据分析可知,曲线a或曲线b表示 ,当同一投料比时,观察图像可知T 时
2
大于T 时 ,而 可知,温度越高则 越大,说明温度
1
升高主反应的平衡正向移动, ;曲线c或曲线d表示 ,当同一投料比时,观察
可知T 时 大于T 时 ,而 可知,温度越高则
1 2
越小,说明温度升高副反应的平衡逆向移动, ,故C错误;D.L、M、N三点对应副反应 ,且 ,升高温度平衡逆向移动,
,故D正确;
故答案选D。
17.(2023·北京卷)下列事实能用平衡移动原理解释的是
A. 溶液中加入少量 固体,促进 分解
B.密闭烧瓶内的 和 的混合气体,受热后颜色加深
C.铁钢放入浓 中,待不再变化后,加热能产生大量红棕色气体
D.锌片与稀 反应过程中,加入少量 固体,促进 的产生
【答案】B
【解析】A.MnO 会催化 HO 分解,与平衡移动无关,A项错误;
2 2 2
B.NO 转化为NO 的反应是放热反应,升温平衡逆向移动, NO 浓度增大,混合气体颜色加深,B项正
2 2 4 2
确;
C.铁在浓硝酸中钝化,加热会使表面的氧化膜溶解,铁与浓硝酸反应生成大量红棕色气体,与平衡移动
无关,C项错误;
D.加入硫酸铜以后,锌置换出铜,构成原电池,从而使反应速率加快,与平衡移动无关,D项错误;
故选B。
18.(2023·湖南卷)向一恒容密闭容器中加入 和一定量的 ,发生反应:
。 的平衡转化率按不同投料比 随温度的变化曲线
如图所示。下列说法错误的是
A.
B.反应速率:
C.点a、b、c对应的平衡常数:
D.反应温度为 ,当容器内压强不变时,反应达到平衡状态
【答案】B
【解析】A.一定条件下,增大水的浓度,能提高CH 的转化率,即x值越小,CH 的转化率越大,则
4 4,故A正确;
B.b点和c点温度相同,CH 的起始物质的量都为1mol,b点x值小于c点,则b点加水多,反应物浓度
4
大,则反应速率: ,故B错误;
C.由图像可知,x一定时,温度升高CH 的平衡转化率增大,说明正反应为吸热反应,温度升高平衡正向
4
移动,K增大;温度相同,K不变,则点a、b、c对应的平衡常数: ,故C正确;
D.该反应为气体分子数增大的反应,反应进行时压强发生改变,所以温度一定时,当容器内压强不变时,
反应达到平衡状态,故D正确;
答案选B。
19.(2023·山东卷)在含HgI (g)的溶液中,一定c(I-)范围内,存在平衡关系: ;
2
; ; ; ,平衡常
数依次为 。已知 、 , 、 随 的变化关
系如图所示,下列说法错误的是
A.线 表示 的变化情况
B.随 增大, 先增大后减小
C.
D.溶液中I元素与 元素的物质的量之比始终为
【答案】B
【分析】由题干反应方程式 可知,K= ,则有c(Hg2+)= ,则有
1
lgc(Hg2+)=lgK +lgc(HgI )-2lgc(I-),同理可得:lgc(HgI+)=lgK +lgc(HgI )-lgc(I-), =lgK +lgc(HgI )+
1 2 2 2 3 2
lgc(I-), ==lgK+lgc(HgI )+ 2lgc(I-),且由 可知K= 为一定值,
4 2 0故可知图示中 曲线1、2、3、4即L分别代表 、 、
、 ,据此分析解题。
【解析】A.由分析可知,线 表示 的变化情况,A正确;
B.已知 的化学平衡常数K= ,温度不变平衡常数不变,故随 增大,
0
始终保持不变,B错误;
C.由分析可知,曲线1方程为:lgc(Hg2+)=lgK +lgc(HgI )-2lgc(I-),曲线2方程为:
1 2
lgc(HgI+)=lgK +lgc(HgI )-lgc(I-)即有①b= lgK+lgc(HgI )-2a,②b= lgK+lgc(HgI )-a,联合①②可知得:
2 2 1 2 2 2
,C正确;
D.溶液中的初始溶质为HgI ,根据原子守恒可知,该溶液中I元素与 元素的物质的量之比始终为 ,
2
D正确;
故答案为:B。
20.(2022·天津卷)向恒温恒容密闭容器中通入2mol 和1mol ,反应
达到平衡后,再通入一定量 ,达到新平衡时,下列有关判断错误的是
A. 的平衡浓度增大 B.反应平衡常数增大
C.正向反应速率增大 D. 的转化总量增大
【答案】B
【解析】A.平衡后,再通入一定量 ,平衡正向移动, 的平衡浓度增大,A正确;
B.平衡常数是与温度有关的常数,温度不变,平衡常数不变,B错误;
C.通入一定量 ,反应物浓度增大,正向反应速率增大,C正确;
D.通入一定量 ,促进二氧化硫的转化, 的转化总量增大,D正确;
故选B。
21.(2022·重庆卷)两种酸式碳酸盐的分解反应如下。某温度平衡时总压强分别为p1和p2。
反应1:NH HCO (s) NH (g)+HO(g)+CO(g) p=3.6×104Pa
4 3 3 2 2 1
反应2:2NaHCO (s) NaCO(s)+HO(g)+CO(g) p=4×103Pa
3 2 3 2 2 2
该温度下,刚性密闭容器中放入NH HCO 和NaCO 固体,平衡后以上3种固体均大量存在。下列说法错
4 3 2 3
误的是A.反应2的平衡常数为4×106Pa2 B.通入NH ,再次平衡后,总压强增大
3
C.平衡后总压强为4.36×105Pa D.缩小体积,再次平衡后总压强不变
【答案】B
【解析】A.反应2的平衡常数为 ,A正确;
B.刚性密闭容器,温度不变平衡常数不变,再次达平衡后,容器内各气体分压不变,总压强不变,B错
误;
C. , ,
, ,所以总压强为:
,C正确;
D.达平衡后,缩小体积,平衡逆向移动,温度不变,平衡常数不变,再次平衡后总压强不变,D正确;
故选B。
22.(2022·江苏卷)乙醇-水催化重整可获得 。其主要反应为
,
,在 、 时,若仅考
虑上述反应,平衡时 和CO的选择性及 的产率随温度的变化如图所示。
CO的选择性 ,下列说法正确的是
A.图中曲线①表示平衡时 产率随温度的变化
B.升高温度,平衡时CO的选择性增大
C.一定温度下,增大 可提高乙醇平衡转化率
D.一定温度下,加入 或选用高效催化剂,均能提高平衡时 产率
【答案】B
【分析】根据已知反应① ,反应②,且反应①的热效应更大,温度升高的时候对反应①影响更
大一些,根据选择性的含义,升温时CO选择性增大,同时CO 的选择性减小,所以图中③代表CO的选
2
择性,①代表CO 的选择性,②代表H 的产率,以此解题。
2 2
【解析】A.由分析可知②代表H 的产率,故A错误;
2
B.由分析可知升高温度,平衡时CO的选择性增大,故B正确;
C.一定温度下,增大 ,可以认为开始时水蒸气物质的量不变,增大乙醇物质的量,乙醇的平
衡转化率降低,故C错误;
D.加入 或者选用高效催化剂,不会影响平衡时 产率,故D错误;
故选B。
23.(2022·江苏卷)用尿素水解生成的 催化还原 ,是柴油机车辆尾气净化的主要方法。反应为
,下列说法正确的是
A.上述反应
B.上述反应平衡常数
C.上述反应中消耗 ,转移电子的数目为
D.实际应用中,加入尿素的量越多,柴油机车辆排放的尾气对空气污染程度越小
【答案】B
【解析】A.由方程式可知,该反应是一个气体分子数增大的反应,即熵增的反应,反应△S>0,故A错
误;
B.由方程式可知,反应平衡常数 ,故B正确;
C.由方程式可知,反应每消耗4mol氨气,反应转移12mol电子,则反应中消耗1mol氨气转移电子的数
目为3mol×4× ×6.02×1023=3×6.02×1023,故C错误;
D.实际应用中,加入尿素的量越多,尿素水解生成的氨气过量,柴油机车辆排放的氨气对空气污染程度
增大,故D错误;
故选B。
24.(2022·浙江卷)恒温恒容的密闭容器中,在某催化剂表面上发生氨的分解反应:
,测得不同起始浓度和催化剂表面积下氨浓度随时间的变化,如下表所示,下
列说法不正确的是A.实验①, ,
B.实验②, 时处于平衡状态,
C.相同条件下,增加氨气的浓度,反应速率增大
D.相同条件下,增加催化剂的表面积,反应速率增大
【答案】C
【解析】A.实验①中,0~20min,氨气浓度变化量为2.40 10-3mol/L-2.00 10-3mol/L=4.00 10-4mol/L,
v(NH )= =2.00 10-5mol/(L·min),反应速率之比等于化学计量数之比,v(N )= v(NH )=1.00
3 2 3
10-5mol/(L·min),A正确;
B.催化剂表面积大小只影响反应速率,不影响平衡,实验③中氨气初始浓度与实验①中一样,实验③达
到平衡时氨气浓度为4.00 10-4mol/L,则实验①达平衡时氨气浓度也为4.00 10-4mol/L,而恒温恒容条件下,
实验②相对于实验①为减小压强,平衡正向移动,因此实验②60min时处于平衡状态,x<0.4,即x≠0.4,B
正确;
C.实验①、实验②中0~20min、20min~40min氨气浓度变化量都是4.00 10-4mol/L,实验②中60min时反
应达到平衡状态,实验①和实验②催化剂表面积相同,实验①中氨气初始浓度是实验②中氨气初始浓度的
两倍,实验①60min时反应未达到平衡状态,相同条件下,增加氨气浓度,反应速率并没有增大,C错误;
D.对比实验①和实验③,氨气浓度相同,实验③中催化剂表面积是实验①中催化剂表面积的2倍,实验
③先达到平衡状态,实验③的反应速率大,说明相同条件下,增加催化剂的表面积,反应速率增大,D正
确;
答案选C。
25.(2022·北京卷)某 多孔材料孔径大小和形状恰好将 “固定”,能高选择性吸附 。废
气中的 被吸附后,经处理能全部转化为 。原理示意图如下。
已知:
下列说法不正确的是A.温度升高时不利于 吸附
B.多孔材料“固定” ,促进 平衡正向移动
C.转化为 的反应是
D.每获得 时,转移电子的数目为
【答案】D
【分析】废气经过MOFs材料之后,NO 转化成NO 被吸附,进而与氧气和水反应生成硝酸,从该过程中
2 2 4
我们知道,NO 转化为NO 的程度,决定了整个废气处理的效率。
2 2 4
【解析】A.从 可以看出,这个是一个放热反应,升高温度之后,平衡逆向移动,
导致生成的NO 减少,不利于NO 的吸附,A正确;
2 4 2
B.多孔材料“固定” ,从而促进 平衡正向移动,B正确;
C.NO 和氧气、水反应生成硝酸,其方程式为 ,C正确;
2 4
D.在方程式 中,转移的电子数为4e-,则每获得 ,转移的电子数为
0.4mol,即个数为 ,D错误;
故选D。
26.(2022·辽宁卷)某温度下,在 恒容密闭容器中 发生反应2X(s) Y(g)+2Z(g),有关数据
如下:
时间段/ 产物Z的平均生成速率/
0~2 0.20
0~4 0.15
0~6 0.10
下列说法错误的是
A. 时,Z的浓度大于
B. 时,加入 ,此时
C. 时,Y的体积分数约为33.3%
D. 时,X的物质的量为
【答案】B
【解析】A.反应开始一段时间,随着时间的延长,反应物浓度逐渐减小,产物Z的平均生成速率逐渐减
小,则 内Z的平均生成速率大于 内的,故 时,Z的浓度大于 ,A正确;
B. 时生成的Z的物质的量为 , 时生成的Z的物质的量为
,故反应在 时已达到平衡,设达到平衡时生了 ,列三段
式:根据 ,得 ,则Y的平衡浓度为 ,Z的平衡浓度为 ,平衡常数
, 时Y的浓度为 ,Z的浓度为 ,加入 后Z的浓
度变为 , ,反应正向进行,故 ,B错误;
C.反应生成的Y与Z的物质的量之比恒等于1∶2,反应体系中只有Y和Z为气体,相同条件下,体积之
比等于物质的量之比, ,故Y的体积分数始终约为33.3%,C正确;
D.由B项分析可知 时反应处于平衡状态,此时生成Z为 ,则X的转化量为 ,初始X
的物质的量为 ,剩余X的物质的量为 ,D正确;
故答案选B。
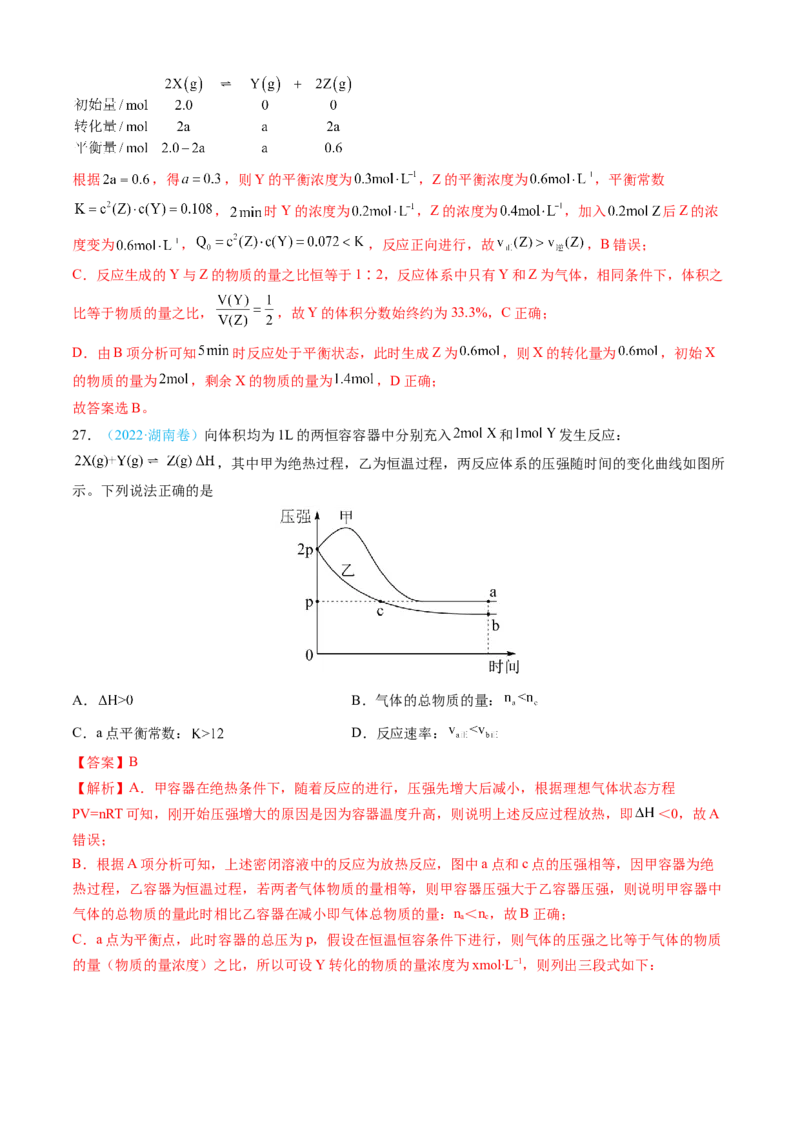
27.(2022·湖南卷)向体积均为1L的两恒容容器中分别充入 和 发生反应:
,其中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间的变化曲线如图所
示。下列说法正确的是
A. B.气体的总物质的量:
C.a点平衡常数: D.反应速率:
【答案】B
【解析】A.甲容器在绝热条件下,随着反应的进行,压强先增大后减小,根据理想气体状态方程
PV=nRT可知,刚开始压强增大的原因是因为容器温度升高,则说明上述反应过程放热,即 <0,故A
错误;
B.根据A项分析可知,上述密闭溶液中的反应为放热反应,图中a点和c点的压强相等,因甲容器为绝
热过程,乙容器为恒温过程,若两者气体物质的量相等,则甲容器压强大于乙容器压强,则说明甲容器中
气体的总物质的量此时相比乙容器在减小即气体总物质的量:n<n,故B正确;
a c
C.a点为平衡点,此时容器的总压为p,假设在恒温恒容条件下进行,则气体的压强之比等于气体的物质
的量(物质的量浓度)之比,所以可设Y转化的物质的量浓度为xmol∙L−1,则列出三段式如下:,则有 ,计算得到x=0.75,那么化学平衡常数
K= ,又甲容器为绝热条件,等效为恒温条件下升温,平衡逆向移动,则平衡
常数减小即平衡常数K<12,故C错误;
D.根据图像可知,甲容器达到平衡的时间短,温度高,所以达到平衡的速率相对乙容器的快,即V >V
a正 b
,故D错误。
正
综上所述,答案为B。
28.(2022·广东卷)恒容密闭容器中, 在不同温度下达平衡时,
各组分的物质的量(n)如图所示。下列说法正确的是
A.该反应的
B.a为 随温度的变化曲线
C.向平衡体系中充入惰性气体,平衡不移动
D.向平衡体系中加入 ,H 的平衡转化率增大
2
【答案】C
【解析】A.从图示可以看出,平衡时升高温度,氢气的物质的量减少,则平衡正向移动,说明该反应的
正反应是吸热反应,即ΔH>0,故A错误;
B.从图示可以看出,在恒容密闭容器中,随着温度升高氢气的平衡时的物质的量减少,则平衡随着温度
升高正向移动,水蒸气的物质的量增加,而a曲线表示的是物质的量不随温度变化而变化,故B错误;
C.容器体积固定,向容器中充入惰性气体,没有改变各物质的浓度,平衡不移动,故C正确;
D.BaSO 是固体,向平衡体系中加入BaSO,不能改变其浓度,因此平衡不移动,氢气的转化率不变,故
4 4
D错误;
故选C。
29.(2022·江苏卷)乙醇-水催化重整可获得 。其主要反应为
,
,在 、 时,若仅考虑上述反应,平衡时 和CO的选择性及 的产率随温度的变化如图所示。
CO的选择性 ,下列说法正确的是
A.图中曲线①表示平衡时 产率随温度的变化
B.升高温度,平衡时CO的选择性增大
C.一定温度下,增大 可提高乙醇平衡转化率
D.一定温度下,加入 或选用高效催化剂,均能提高平衡时 产率
【答案】B
【分析】根据已知反应① ,反应②
,且反应①的热效应更大,温度升高的时候对反应①影响更
大一些,根据选择性的含义,升温时CO选择性增大,同时CO 的选择性减小,所以图中③代表CO的选
2
择性,①代表CO 的选择性,②代表H 的产率,以此解题。
2 2
【解析】A.由分析可知②代表H 的产率,故A错误;
2
B.由分析可知升高温度,平衡时CO的选择性增大,故B正确;
C.一定温度下,增大 ,可以认为开始时水蒸气物质的量不变,增大乙醇物质的量,乙醇的平
衡转化率降低,故C错误;
D.加入 或者选用高效催化剂,不会影响平衡时 产率,故D错误;
故选B。
30.(2022·海南卷)某温度下,反应CH=CH (g)+HO(g) CHCHOH(g)在密闭容器中达到平衡,下列
2 2 2 3 2
说法正确的是
A.增大压强, ,平衡常数增大
B.加入催化剂,平衡时 的浓度增大
C.恒容下,充入一定量的 ,平衡向正反应方向移动
D.恒容下,充入一定量的 , 的平衡转化率增大【答案】C
【解析】A.该反应是一个气体分子数减少的反应,增大压强可以加快化学反应速率,正反应速率增大的
幅度大于逆反应的,故v > v ,平衡向正反应方向移动,但是因为温度不变,故平衡常数不变,A不正
正 逆
确;
B.催化剂不影响化学平衡状态,因此,加入催化剂不影响平衡时CHCHOH(g)的浓度,B不正确;
3 2
C.恒容下,充入一定量的HO(g),HO(g)的浓度增大,平衡向正反应方向移动,C正确;
2 2
D.恒容下,充入一定量的CH=CH (g),平衡向正反应方向移动,但是CH=CH (g)的平衡转化率减小,
2 2 2 2
D不正确;
综上所述,本题选C。
31.(2022·浙江卷)AB型强电解质在水中的溶解(可视作特殊的化学反应)表示为AB(s)=An+(aq)+Bn-(aq),
其焓变和熵变分别为ΔH和ΔS。对于不同组成的AB型强电解质,下列说法正确的是
A.ΔH和ΔS均大于零
B.ΔH和ΔS均小于零
C.ΔH可能大于零或小于零,ΔS大于零
D.ΔH和ΔS均可能大于零或小于零
【答案】D
【解析】强电解质溶于水有的放热,如硫酸铜等;有的吸热,如碳酸氢钠等,所以在水中溶解对应的ΔH
可能大于零或小于零。熵表示系统混乱程度。体系越混乱,则熵越大。AB型强电解质固体溶于水,存在
熵的变化。固体转化为离子,混乱度是增加的,但离子在水中存在水合过程,这样会引发水的混乱度的变
化,让水分子会更加规则,即水的混乱度下降,所以整个溶解过程的熵变ΔS,取决于固体转化为离子的熵
增与水合过程的熵减两个作用的相对大小关系。若是前者占主导,则整个溶解过程熵增,即ΔS>0,反之,
熵减,即ΔS<0。综上所述,D项符合题意。故选D。