文档内容
2025届湖北省部分高中协作体高三年级三月联考一模考试
高三化学试题
本试卷共8页,19题,全卷满分100分,考试用时75分钟。
★祝考试顺利★
注意事项:
1、答题前,请将自己的姓名、准考证号、考场号、座位号填写在试卷和答
题卡上,并将准考证号条形码粘贴在答题卡上的制定位置。
2、选择题的作答:每小题选出答案后,用 2B铅笔把答题卡上对应题目的
答案标号涂黑,写在试卷、草稿纸和答题卡上的非答题区域均无效。
3、非选择题作答:用黑色签字笔直接答在答题卡对应的答题区域内,写在
试卷、草稿纸和答题卡上的非答题区域均无效。
4、考试结束后,请将答题卡上交。
一、选择题:本题共15小题,每题3分,共45分,每小题仅有一项是符
合题意。
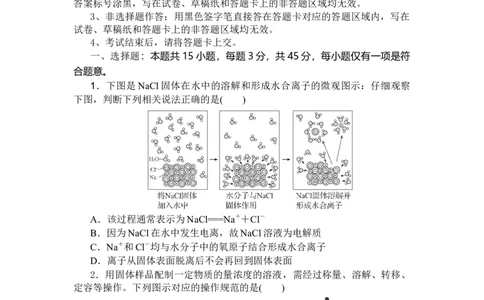
1.下图是NaCl固体在水中的溶解和形成水合离子的微观图示:仔细观察
下图,判断下列相关说法正确的是( )
→ →
A.该过程通常表示为NaCl===Na++Cl-
B.因为NaCl在水中发生电离,故NaCl溶液为电解质
C.Na+和Cl-均与水分子中的氧原子结合形成水合离子
D.离子从固体表面脱离后不会再回到固体表面
2.用固体样品配制一定物质的量浓度的溶液,需经过称量、溶解、转移、
定容等操作。下列图示对应的操作规范的是( )
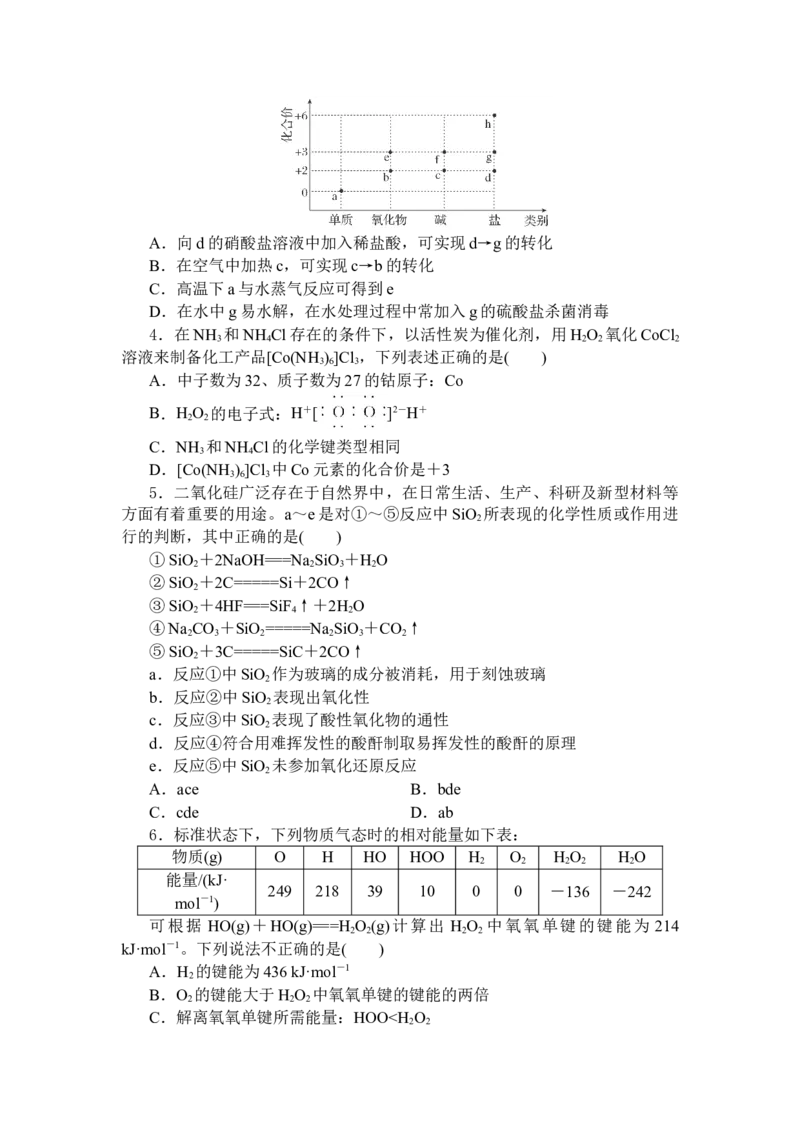
3. 铁元素的“价—类”二维图如下图所示。下列有关说法正确的是( )A.向d的硝酸盐溶液中加入稀盐酸,可实现d→g的转化
B.在空气中加热c,可实现c→b的转化
C.高温下a与水蒸气反应可得到e
D.在水中g易水解,在水处理过程中常加入g的硫酸盐杀菌消毒
4.在NH 和NH Cl存在的条件下,以活性炭为催化剂,用H O 氧化CoCl
3 4 2 2 2
溶液来制备化工产品[Co(NH ) ]Cl ,下列表述正确的是( )
3 6 3
A.中子数为32、质子数为27的钴原子:Co
B.H O 的电子式:H+[ ]2-H+
2 2
C.NH 和NH Cl的化学键类型相同
3 4
D.[Co(NH ) ]Cl 中Co元素的化合价是+3
3 6 3
5.二氧化硅广泛存在于自然界中,在日常生活、生产、科研及新型材料等
方面有着重要的用途。a~e是对①~⑤反应中SiO 所表现的化学性质或作用进
2
行的判断,其中正确的是( )
①SiO +2NaOH===Na SiO +H O
2 2 3 2
②SiO +2C=====Si+2CO↑
2
③SiO +4HF===SiF ↑+2H O
2 4 2
④Na CO +SiO =====Na SiO +CO ↑
2 3 2 2 3 2
⑤SiO +3C=====SiC+2CO↑
2
a.反应①中SiO 作为玻璃的成分被消耗,用于刻蚀玻璃
2
b.反应②中SiO 表现出氧化性
2
c.反应③中SiO 表现了酸性氧化物的通性
2
d.反应④符合用难挥发性的酸酐制取易挥发性的酸酐的原理
e.反应⑤中SiO 未参加氧化还原反应
2
A.ace B.bde
C.cde D.ab
6.标准状态下,下列物质气态时的相对能量如下表:
物质(g) O H HO HOO H O H O H O
2 2 2 2 2
能量/(kJ·
249 218 39 10 0 0 -136 -242
mol-1)
可根据 HO(g)+HO(g)===H O (g)计算出 H O 中氧氧单键的键能为 214
2 2 2 2
kJ·mol-1。下列说法不正确的是( )
A.H 的键能为436 kJ·mol-1
2
B.O 的键能大于H O 中氧氧单键的键能的两倍
2 2 2
C.解离氧氧单键所需能量:HOO8 时,
NH VO 的 产 量 明 显 降 低 , 原 因 是
4 3
_______________________________________。
19.(14分)氢溴酸在医药和石化工业上有广泛用途。如图是模拟工业制
备氢溴酸粗品并精制的流程:根据上述流程回答下列问题:
(1)混合①中发生反应的化学方程式为_______________________________
_____________________________________________________________________
____________________________________________。
(2)混合①中使用冰水的目的是_____________________________________
_____________________________________________________________________
____________________________________。
(3)操作Ⅱ和操作Ⅲ的名称分别是___________、____________。操作Ⅲ一般
适用于分离_______________(填字母)混合物。
a.固体和液体 b.固体和固体
c.互不相溶的液体 d.互溶的液体
(4)混合②中加入Na SO 的目的是__________________________________
2 3
____________________________________________________________________
_____________________________________________________________________
______________________________________。
(5) 纯净的氢溴酸应为无色液体,但实际
工业生产中制得的氢溴酸(工业氢溴酸)带有淡淡的黄色,于是甲和乙同学设计
了如下简单实验加以探究:甲同学假设工业氢溴酸呈淡黄色是因为含有 Fe3+,
则用于证明该假设所用的试剂为________________,若假设成立,可观察到的
现象为_________________________ _______________________。乙同学假设工
业 氢 溴 酸 呈 淡 黄 色 是 因 为 __________
_____________________________________________________________________
_________________________________________________________________,其
用于证明该假设所用的试剂为____________。
高三化学试题答案
一、选择题:本题共15小题,每题3分,共45分,每小题仅有一项是符合题意。
1.解析:A A.NaCl为强电解质,在水中完全电离,该过程通常表示为
NaCl===Na++Cl-,A正确;B.NaCl 在水中完全电离,氯化钠为强电解质,但是得到的氯化钠溶液为混合物,不是电解质,B错误;C.从图示知,Na+与水分
子中的氧原子结合形成水合离子,Cl-与水分子中的氢原子结合形成水合离子,
C错误;D.NaCl 溶解时钠离子和氯离子从固体表面脱离进入溶液中,同时钠离
子和氯离子受 NaCl表面的氯离子和钠离子的吸引回到固体表面,D错误。
2.解析:B A项,托盘天平使用时应“左物右码”,图为“左码右物”,
错误;B项,用玻璃棒搅拌加速溶解,正确;C项,移液时不能将烧杯中的溶
液直接倒入容量瓶,应用玻璃棒引流,错误;D项,胶头滴管应在容量瓶口垂
直正上方,不能伸入瓶口,错误。
4. 解析:A 根据图中信息,a 为 Fe,b 为 FeO,e 为 Fe O ,c 为
2 3
Fe(OH) ,f为Fe(OH) ,d为亚铁盐,g为铁盐,h为高铁酸盐;Fe与水蒸气反
2 3
应不能得到Fe O ,C项错误;在空气中加热 Fe(OH) ,Fe(OH) 会被O 氧化为
2 3 2 2 2
Fe(OH) ,最终生成Fe O ,不能得到FeO,B项错误;Fe2+、NO、H+会发生氧
3 2 3
化还原反应:3Fe2++NO+4H+===3Fe3++NO↑+2H O,可实现Fe2+→Fe3+的
2
转化,A项正确;Fe3+水解,Fe3++3H OFe(OH) +3H+,生成Fe(OH) 胶粒
2 3 3
可吸附杂质净水,不能杀菌消毒,D项错误。
4.解析:D A项,中子数为32,质子数为27的钴元素,质量数为27+
32=59,表示为Co,错误;B项,H O 为共价化合物,电子式为H
2 2
H,错误;C项,NH 中只存在共价键,NH Cl中既存在离子键又存在共价键,
3 4
二者化学键类型不同,错误;D项,[Co(NH ) ]Cl 中,NH 整体为0价,Cl元
3 6 3 3
素为-1价,所以Co元素的化合价为+3,正确。
5.解析:B 通常用氢氟酸来刻蚀玻璃,与之对应的反应是③,反应①中
SiO 表现出酸性氧化物的通性,a、c判断错误;反应②是一个置换反应,其中
2
二氧化硅被还原,表现出氧化性,b判断正确;反应④是一个复分解反应,用
难挥发的二氧化硅制取易挥发的二氧化碳,d判断正确;反应⑤中碳的化合价
由0价变为-4价和+2价,硅和氧的化合价都没有改变,因此二氧化硅没有参
加氧化还原反应,e判断正确。
6.解析:C 由气态时 H、H 的相对能量可知,H 的键能为 218 kJ·mol-
2 2
1×2=436 kJ·mol-1,A项正确;由表格中数据可知O 的键能为249 kJ·mol-1×2
2
=498 kJ·mol-1,而H O 中氧氧单键的键能为 214 kJ·mol-1,214 kJ·mol-1×2<
2 2498 kJ·mol-1,B项正确;HOO中解离氧氧单键所需能量为 249 kJ·mol-1+39
kJ·mol-1-10 kJ·mol-1=278 kJ·mol-1,H O 中解离氧氧单键所需能量为 214
2 2
kJ·mol-1,C项错误;ΔH=-136 kJ·mol-1-(-242 kJ·mol-1)-249 kJ·mol-1=
-143 kJ·mol-1,D项正确。
7.解析:B 催化电极b上发生还原反应,为阴极,连接电源的负极,A
项 正 确 ; 阴 极 的 电 极 反 应 为 + 6e - + 6H + ===
+2H O,生成水,c(H SO )减小,B项错误;阳极区发生反
2 2 4
应6Ni2+-6e-+12H O===6NiO(OH)+18H+、6NiO(OH)+
2
+ 12H + === + 10H O + 6Ni2 + , 总 反 应 为
2
-6e-+2H O=== +6H+,C项正确;
2
由 电 极 反 应 及 各 电 极 上 转 移 电 子 数 相 等 , 可 得 关 系 式
,故每消耗 1 mol 对硝基苯酚
同时生成1 mol 2,5-呋喃二甲酸,D项正确。
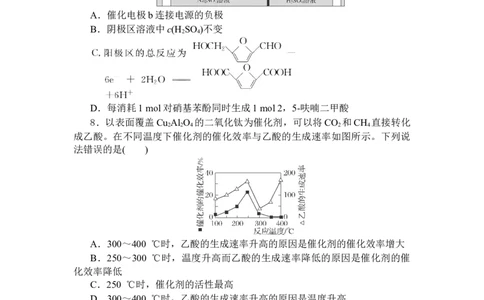
8.解析:A 图中250 ℃时催化剂的催化效率最大,催化剂活性最高,故
C正确;催化剂可加快反应速率,温度太高使催化剂失去活性,则250~300 ℃
时,温度升高而乙酸的生成速率降低的主要原因是催化剂的催化效率降低,故
B正确;300~400 ℃时,乙酸生成速率与催化效率变化不同,催化剂的催化效
率降低,乙酸的生成速率增大,故A错误;300~400 ℃时,催化剂的催化效
率降低,则乙酸的生成速率升高的原因是温度升高,故D正确。
9.解析:C 根据化学方程式NH COONH (s)2NH (g)+CO (g)可知,生
2 4 3 2
成的气体的物质的量之比始终是2∶1,所以气体的平均相对分子质量始终不变
故不能作为达到平衡状态的判断依据,A项错误;从表中数据可以看出,随着
温度升高,气体的总浓度增大,平衡正向移动,则该反应的正反应为吸热反应,
ΔH>0,反应中固体变为气体,混乱度增大,ΔS>0,根据ΔG=ΔH-TΔS可知反
应在高温下正向自发进行,B项错误;压缩容器体积,气体压强增大,平衡逆向移动,氨基甲酸铵固体的质量增加,C项正确;反应中生成的氨和二氧化碳
的浓度之比为 2∶1,总浓度为 2.4×10-3 mol·L-1,所以氨的浓度为 1.6×10-
3mol·L-1,D项错误。
10.解析:D 根据电离方程式,电离出的c(H+)=c(B-),即K (HB)==
a
≈1.1×10-3,K (HB)的数量级为10-3,A错误;恰好完全反应时得到NaB溶液,
a
溶液显碱性,故可采用酚酞作为指示剂,D正确;b点时混合溶液恰好为中性
由于NaB为强碱弱酸盐,故此时酸有剩余,V <10,C、B错误。
1
11.解析:B 碘化银溶解是吸热的,温度越高电离出的离子越多,图像中
c(I-):a>b,故T>20 ℃,A错误;K 属于平衡常数的一种,只受温度影响,在
sp
相同温度下,曲线上的各点溶度积相同,温度越高,溶度积越大,因此,AgI
的溶度积K (AgI):c=d=e8时,生成V O或VO。
2
答案:(1)CaO+O +V O =====Ca(VO )
2 2 3 3 2
(2)Ca(VO ) +4H+===Ca2++2VO+2H O (3)调节溶液的pH,并提供Ca2+形成
3 2 2
Ca (VO ) 沉淀 (4) (5)当pH>8时,钒的主要存在形式不是VO
3 4 2
19.(14分)
解析:(1)SO 具有还原性,Br 具有氧化性,二者能发生反应:SO +Br +
2 2 2 2
2H O===2HBr+H SO 。(2)降低体系温度,可以增大SO 气体在水中的溶解度,
2 2 4 2同时防止溴挥发。(3)操作Ⅱ是分离固体和溶液,采用过滤的方法;操作Ⅲ是分
离相互溶解的液体,采用蒸馏的方法。(4)Na SO 具有还原性,可以将溴单质还
2 3
原为溴离子,从而除去粗品中未反应完的溴。(5)考查Fe3+、Br 的检验方法。
2
答案:(1)SO +Br +2H O===2HBr+H SO (2)降低体系温度,增加SO 气体
2 2 2 2 4 2
在水中的溶解度,防止溴挥发,使反应完全 (3)过滤 蒸馏 d (4)除去粗品
中未反应完的溴 (5)KSCN溶液 溶液变成红色 含有Br CCl
2 4