文档内容
绝密★考试结束前
2025-2026 学年第一学期天域全国名校协作体联考
高三年级化学学科 试题
考生须知:
1.本卷共8页满分100分,考试时间90分钟。
2.答题前,在答题卷指定区域填写班级、姓名、考场号、座位号及准考证号并填涂相应数字。
3.所有答案必须写在答题纸上,写在试卷上无效。
4.考试结束后,只需上交答题纸。
5.可能用到的相对原子质量:Be-9 B-11 O-16 Cl-35.5 Cr-52 Co-59 As-75 Br-80 Ag-108
选择题部分
一、选择题(本大题共16题,每小题3分,共48分。每小题列出的四个备选项中只有一个是符合
题目要求的,不选、多选、错选均不得分)
1.下列物质属于非极性分子的是
A.CH Cl B.H O C.P D.O
2 2 2 2 4 3
2.下列化学用语正确的是
A.中子数为10的氧原子:16O B.SO2-的VSEPR模型:
3
C.基态As原子的简化电子排布式:[Ar]4s24p3 D. 丙炔的键线式:
3.化学与生产生活密切相关,下列说法不
.
正
.
确
.
的是
A.利用硝酸铵和水合碳酸钠的反应可制冷敷袋,该反应能发生的原理是熵增
B.二氧化硅可用作牙膏的摩擦剂,说明它难溶于水
C.La-Ni合金在一定条件下能吸放氢气,故可用作储氢合金
D.氢氟酸呈酸性,故可用于刻蚀玻璃器皿
4.太阳能转化为电能时,要用到Si、GaP、GaAs等半导体材料。下列说法正确的是
A.原子半径:r(As)<r(Ga) B.第二电离能:I (Si)>I (P)
2 2
C.热稳定性:AsH >PH D.酸性:H PO <H SiO
3 3 3 4 2 3
5.物质结构决定性质,影响物质用途。下列结构或性质不
.
能
.
解释其用途的是
选项 结构或性质 用途
某种氮化硼结构与石墨类似,但电子
A 该氮化硼可用于制作导电材料
基本上定域在氮上
硅胶(SiO₂·nH₂O)具有多孔结构,比
B 硅胶可用作食品干燥剂
表面积大,吸附能力强
C 乳酸分子中含有羧基和羟基 乳酸可用于制备可降解塑料
甲醛分子中含有醛基(-CHO),具有
D 甲醛可用于动物标本制作的防腐剂
还原性和杀菌性
1
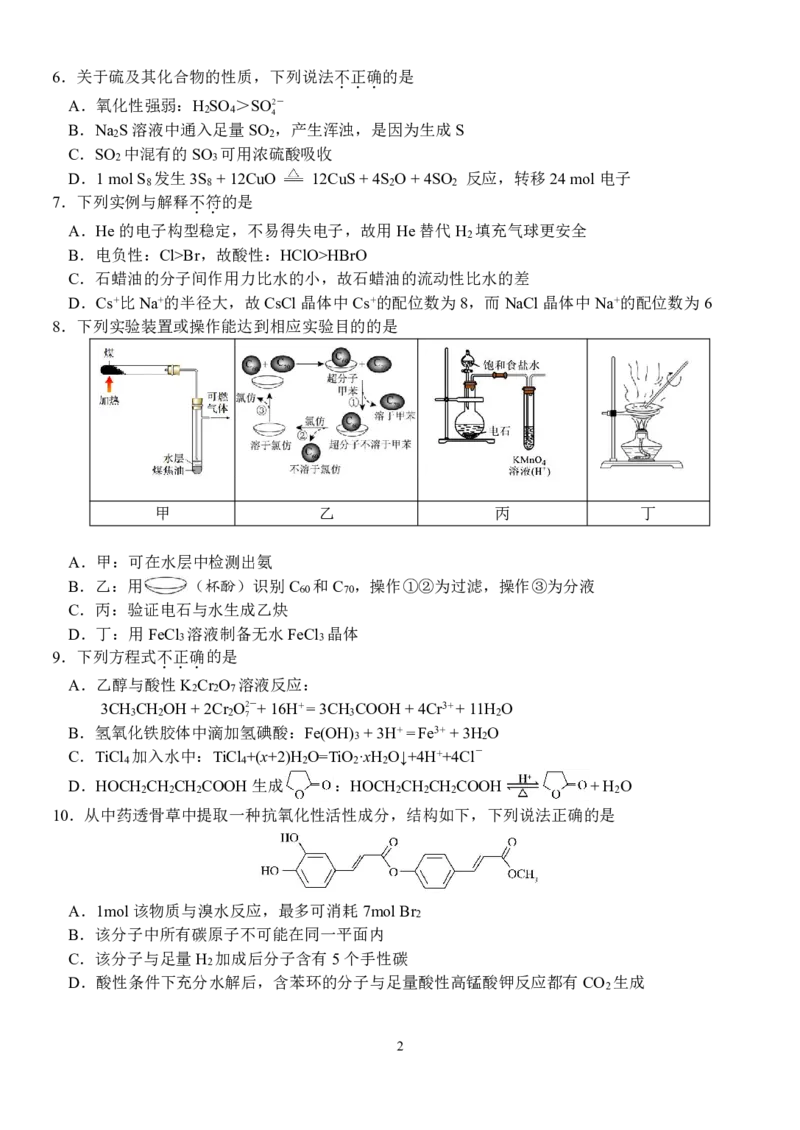
{#{QQABKYK05ggQkpSACB6qVUG0CgkQsIKiJQoMRQCcuAYCiAFIBAA=}#}6.关于硫及其化合物的性质,下列说法不
.
正
.
确
.
的是
A.氧化性强弱:H SO >SO2-
2 4 4
B.Na S溶液中通入足量SO ,产生浑浊,是因为生成S
2 2
C.SO 中混有的SO 可用浓硫酸吸收
2 3
D.1molS 发生3S +12CuO 12CuS+4S O+4SO 反应,转移24mol电子
8 8 2 2
7.下列实例与解释不
.
符
.
的是
A.He的电子构型稳定,不易得失电子,故用He替代H 填充气球更安全
2
B.电负性:Cl>Br,故酸性:HClO>HBrO
C.石蜡油的分子间作用力比水的小,故石蜡油的流动性比水的差
D.Cs+比Na+的半径大,故CsCl晶体中Cs+的配位数为8,而NaCl晶体中Na+的配位数为6
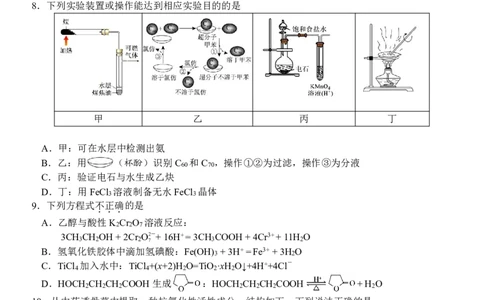
8.下列实验装置或操作能达到相应实验目的的是
甲 乙 丙 丁
A.甲:可在水层中检测出氨
B.乙:用 (杯酚)识别C 和C ,操作①②为过滤,操作③为分液
60 70
C.丙:验证电石与水生成乙炔
D.丁:用FeCl 溶液制备无水FeCl 晶体
3 3
9.下列方程式不
.
正
.
确
.
的是
A.乙醇与酸性K Cr O 溶液反应:
2 2 7
3CH CH OH+2Cr O2-+16H+=3CH COOH+4Cr3++11H O
3 2 2 7 3 2
B.氢氧化铁胶体中滴加氢碘酸:Fe(OH) +3H+=Fe3++3H O
3 2
C.TiCl 加入水中:TiCl +(x+2)H O=TiO ·xH O↓+4H++4Cl-
4 4 2 2 2
D.HOCH CH CH COOH生成 :HOCH CH CH COOH +H O
2 2 2 2 2 2 2
10.从中药透骨草中提取一种抗氧化性活性成分,结构如下,下列说法正确的是
A.1mol该物质与溴水反应,最多可消耗7molBr
2
B.该分子中所有碳原子不可能在同一平面内
C.该分子与足量H 加成后分子含有5个手性碳
2
D.酸性条件下充分水解后,含苯环的分子与足量酸性高锰酸钾反应都有CO 生成
2
2
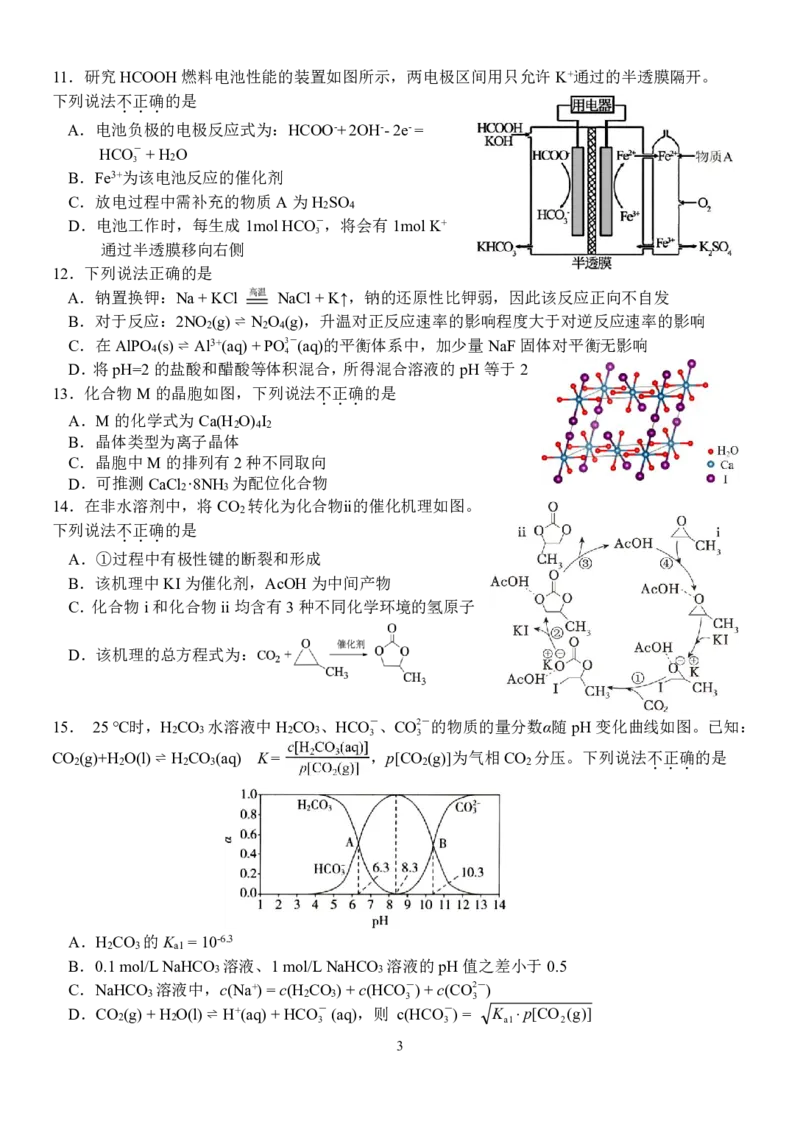
{#{QQABKYK05ggQkpSACB6qVUG0CgkQsIKiJQoMRQCcuAYCiAFIBAA=}#}11.研究HCOOH燃料电池性能的装置如图所示,两电极区间用只允许K+通过的半透膜隔开。
下列说法不正确的是
...
A.电池负极的电极反应式为:HCOO-+2OH--2e-=
HCO-+H O
3 2
B.Fe3+为该电池反应的催化剂
C.放电过程中需补充的物质A为H SO
2 4
D.电池工作时,每生成1molHCO-,将会有1molK+
3
通过半透膜移向右侧
12.下列说法正确的是
A.钠置换钾:Na+KCl NaCl+K↑,钠的还原性比钾弱,因此该反应正向不自发
B.对于反应:2NO (g)⇌ N O (g),升温对正反应速率的影响程度大于对逆反应速率的影响
2 2 4
C.在AlPO (s)⇌ Al3+(aq)+PO3-(aq)的平衡体系中,加少量NaF固体对平衡无影响
4 4
D.将pH=2的盐酸和醋酸等体积混合,所得混合溶液的pH等于2
13.化合物M的晶胞如图,下列说法不
.
正
.
确
.
的是
A.M的化学式为Ca(H O) I
2 4 2
B.晶体类型为离子晶体
C.晶胞中M的排列有2种不同取向
D.可推测CaCl ·8NH 为配位化合物
2 3
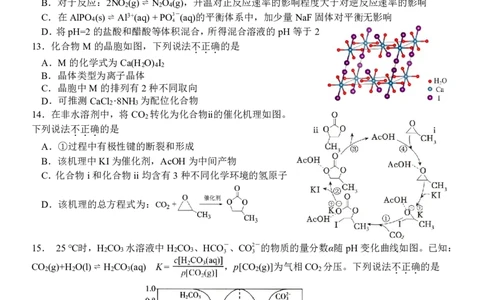
14.在非水溶剂中,将CO 转化为化合物ⅱ的催化机理如图。
2
下列说法不正确的是
...
A.①过程中有极性键的断裂和形成
B.该机理中KI为催化剂,AcOH为中间产物
C.化合物i和化合物ii均含有3种不同化学环境的氢原子
D.该机理的总方程式为:
15. 25℃时,H CO 水溶液中H CO 、HCO -、CO2-的物质的量分数α随pH变化曲线如图。已知:
2 3 2 3 3 3
CO 2 (g)+H 2 O(l)⇌ H 2 CO 3 (aq) K= ,p[CO 2 (g)]为气相CO 2 分压。下列说法不 . 正 . 确 . 的是
A.H CO 的K =10-6.3
2 3 a1
B.0.1mol/LNaHCO 溶液、1mol/LNaHCO 溶液的pH值之差小于0.5
3 3
C.NaHCO 溶液中,c(Na+)=c(H CO )+c(HCO-)+c(CO2-)
3 2 3 3 3
D.CO (g)+H O(l)⇌ H+(aq)+HCO-(aq),则 c(HCO-)= K p[CO (g)]
2 2 3 3 a1 2
3
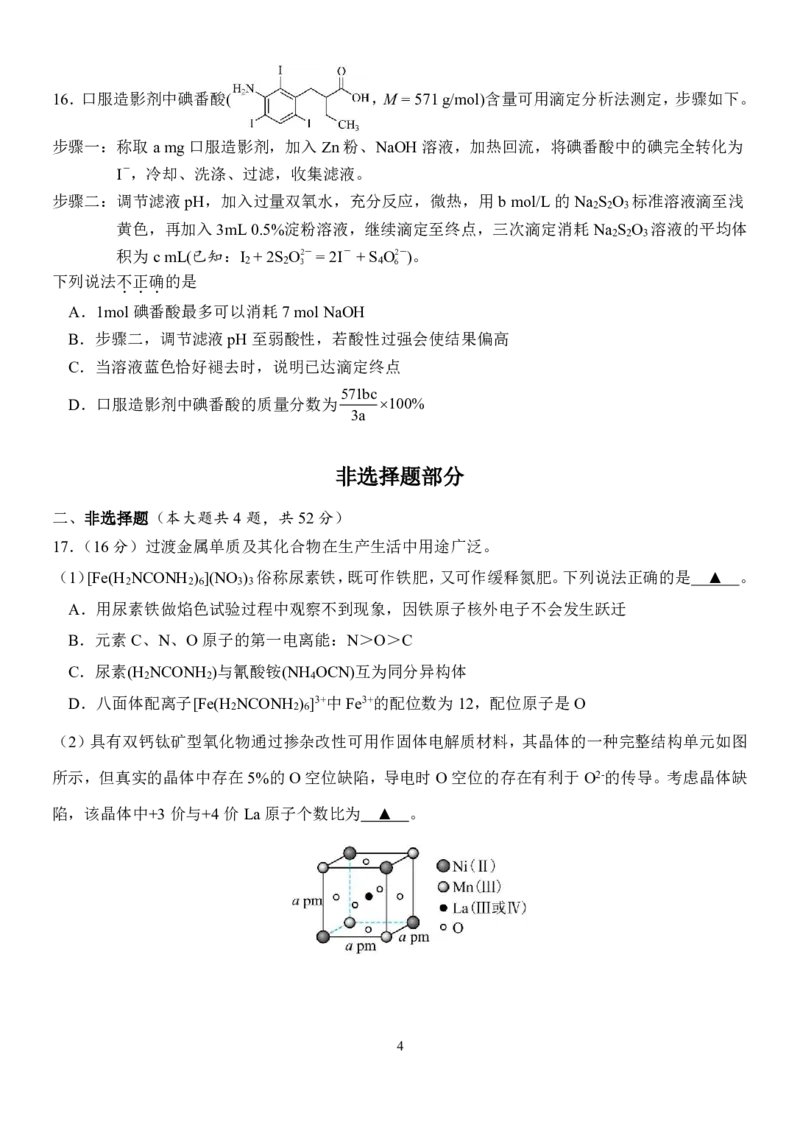
{#{QQABKYK05ggQkpSACB6qVUG0CgkQsIKiJQoMRQCcuAYCiAFIBAA=}#}16.口服造影剂中碘番酸( ,M=571g/mol)含量可用滴定分析法测定,步骤如下。
步骤一:称取amg口服造影剂,加入Zn粉、NaOH溶液,加热回流,将碘番酸中的碘完全转化为
I-,冷却、洗涤、过滤,收集滤液。
步骤二:调节滤液pH,加入过量双氧水,充分反应,微热,用bmol/L的Na S O 标准溶液滴至浅
2 2 3
黄色,再加入3mL0.5%淀粉溶液,继续滴定至终点,三次滴定消耗Na S O 溶液的平均体
2 2 3
积为cmL(已知:I +2S O2-=2I- +S O2-)。
2 2 3 4 6
下列说法不正确的是
...
A.1mol碘番酸最多可以消耗7molNaOH
B.步骤二,调节滤液pH至弱酸性,若酸性过强会使结果偏高
C.当溶液蓝色恰好褪去时,说明已达滴定终点
571bc
D.口服造影剂中碘番酸的质量分数为 100%
3a
非选择题部分
二、非选择题(本大题共4题,共52分)
17.(16分)过渡金属单质及其化合物在生产生活中用途广泛。
(1)[Fe(H NCONH ) ](NO ) 俗称尿素铁,既可作铁肥,又可作缓释氮肥。下列说法正确的是 ▲ 。
2 2 6 3 3
A.用尿素铁做焰色试验过程中观察不到现象,因铁原子核外电子不会发生跃迁
B.元素C、N、O原子的第一电离能:N>O>C
C.尿素(H NCONH )与氰酸铵(NH OCN)互为同分异构体
2 2 4
D.八面体配离子[Fe(H NCONH ) ]3+中Fe3+的配位数为12,配位原子是O
2 2 6
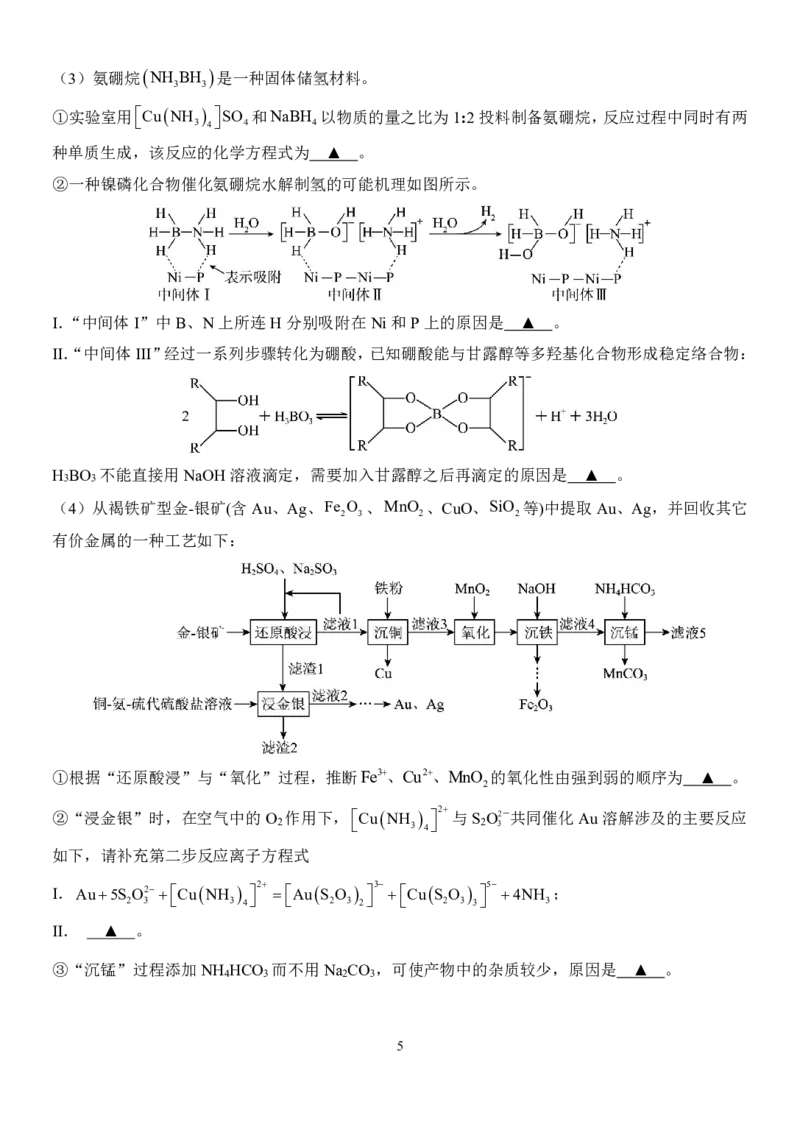
(2)具有双钙钛矿型氧化物通过掺杂改性可用作固体电解质材料,其晶体的一种完整结构单元如图
所示,但真实的晶体中存在5%的O空位缺陷,导电时O空位的存在有利于O2-的传导。考虑晶体缺
陷,该晶体中+3价与+4价La原子个数比为 ▲ 。
4
{#{QQABKYK05ggQkpSACB6qVUG0CgkQsIKiJQoMRQCcuAYCiAFIBAA=}#}(3)氨硼烷NH BH 是一种固体储氢材料。
3 3
①实验室用
CuNH
3
4
SO
4
和NaBH
4
以物质的量之比为1:2投料制备氨硼烷,反应过程中同时有两
种单质生成,该反应的化学方程式为 ▲ 。
②一种镍磷化合物催化氨硼烷水解制氢的可能机理如图所示。
I.“中间体I”中B、N上所连H分别吸附在Ni和P上的原因是 ▲ 。
II.“中间体III”经过一系列步骤转化为硼酸,已知硼酸能与甘露醇等多羟基化合物形成稳定络合物:
H BO 不能直接用NaOH溶液滴定,需要加入甘露醇之后再滴定的原因是 ▲ 。
3 3
(4)从褐铁矿型金-银矿(含Au、Ag、Fe O 、MnO 、CuO、SiO 等)中提取Au、Ag,并回收其它
2 3 2 2
有价金属的一种工艺如下:
①根据“还原酸浸”与“氧化”过程,推断Fe3、Cu2、MnO 的氧化性由强到弱的顺序为 ▲ 。
2
②“浸金银”时,在空气中的O 作用下,CuNH 2 与S O2-共同催化Au溶解涉及的主要反应
2 3 4 2 3
如下,请补充第二步反应离子方程式
I.Au5S O2CuNH 2 AuS O 3 CuS O 5 4NH ;
2 3 3 4 2 3 2 2 3 3 3
II. ▲ 。
③“沉锰”过程添加NH HCO 而不用Na CO ,可使产物中的杂质较少,原因是 ▲ 。
4 3 2 3
5
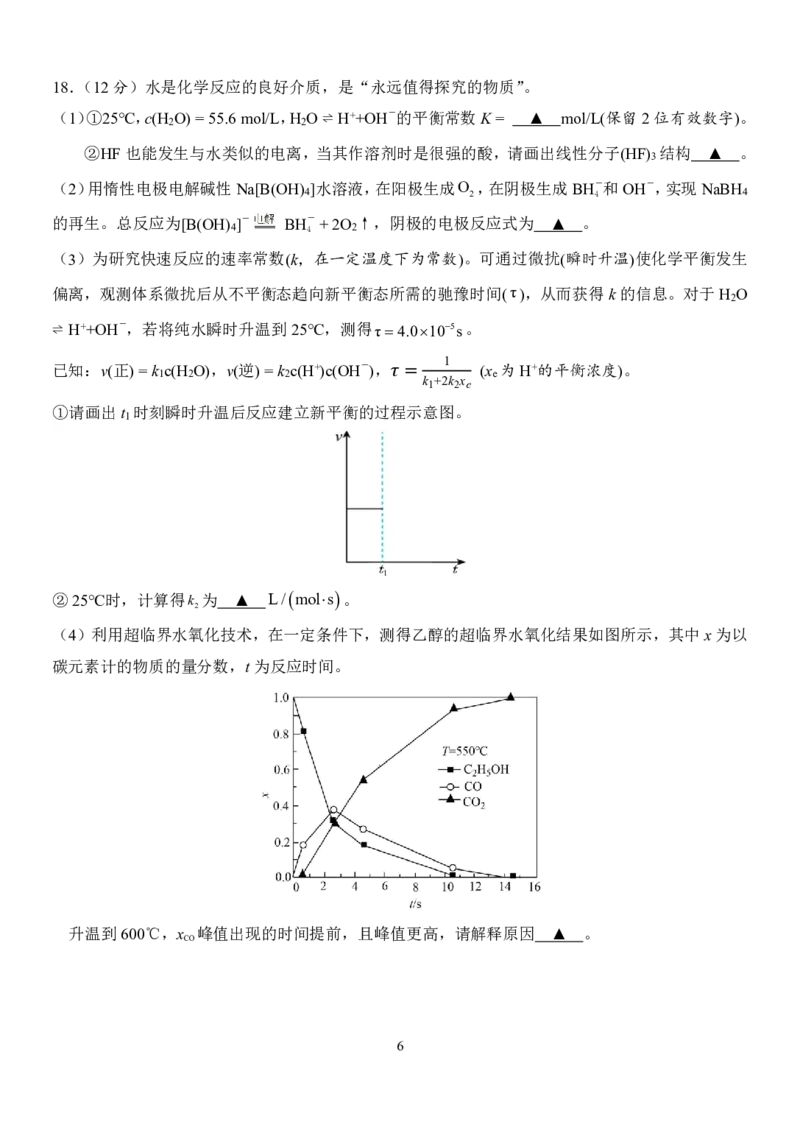
{#{QQABKYK05ggQkpSACB6qVUG0CgkQsIKiJQoMRQCcuAYCiAFIBAA=}#}18.(12分)水是化学反应的良好介质,是“永远值得探究的物质”。
(1)①25℃,c(H O)=55.6mol/L,H O⇌ H++OH-的平衡常数K= ▲ mol/L(保留2位有效数字)。
2 2
②HF也能发生与水类似的电离,当其作溶剂时是很强的酸,请画出线性分子(HF) 结构 ▲ 。
3
(2)用惰性电极电解碱性Na[B(OH) ]水溶液,在阳极生成O ,在阴极生成BH-和OH-,实现NaBH
4 2 4 4
的再生。总反应为[B(OH) ]- BH-+2O ↑,阴极的电极反应式为 ▲ 。
4 4 2
(3)为研究快速反应的速率常数(k,在一定温度下为常数)。可通过微扰(瞬时升温)使化学平衡发生
偏离,观测体系微扰后从不平衡态趋向新平衡态所需的驰豫时间(τ),从而获得k的信息。对于H O
2
⇌ H++OH-,若将纯水瞬时升温到25℃,测得τ4.0105s。
1
已知:v(正)=k c(H O),v(逆)=k c(H+)c(OH-), (x 为H+的平衡浓度)。
1 2 2 e
k1+2k2xe
①请画出t 时刻瞬时升温后反应建立新平衡的过程 =示意图。
1
②25℃时,计算得k 为 ▲ L/mols。
2
(4)利用超临界水氧化技术,在一定条件下,测得乙醇的超临界水氧化结果如图所示,其中x为以
碳元素计的物质的量分数,t为反应时间。
升温到600℃,x 峰值出现的时间提前,且峰值更高,请解释原因 ▲ 。
CO
6
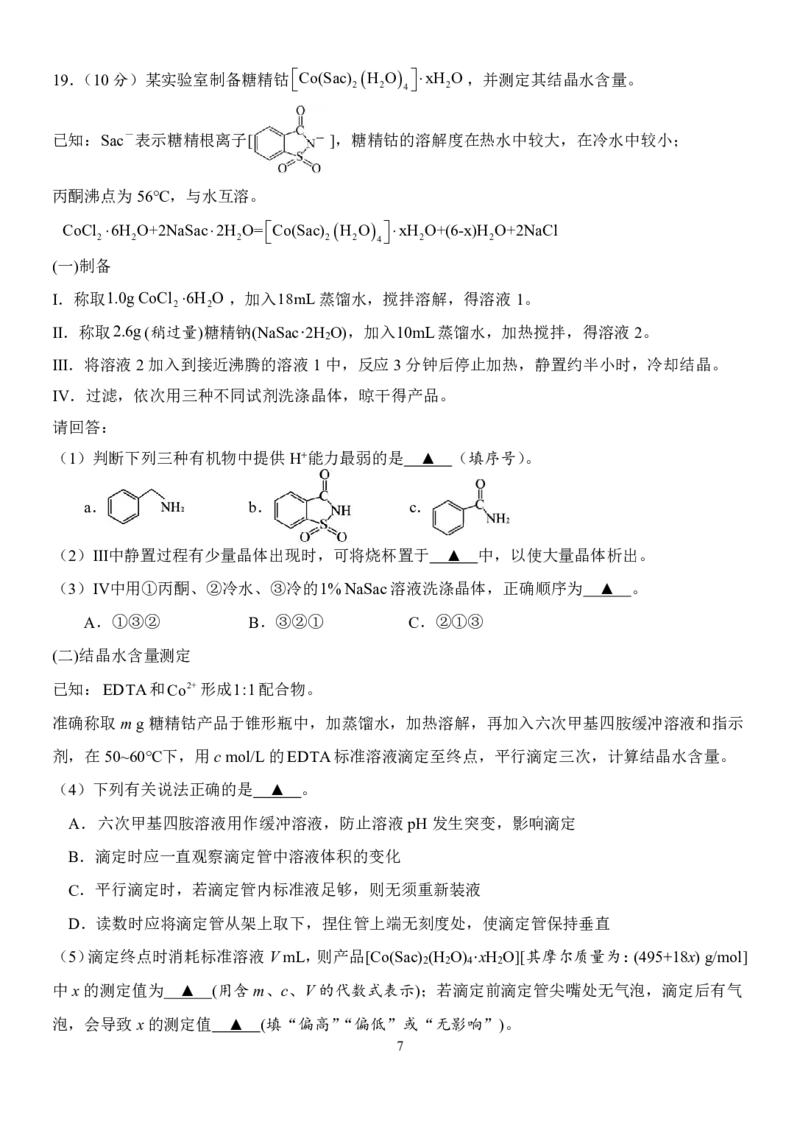
{#{QQABKYK05ggQkpSACB6qVUG0CgkQsIKiJQoMRQCcuAYCiAFIBAA=}#}19.(10分)某实验室制备糖精钴
Co(Sac)
2
H
2
O
4
xH
2
O,并测定其结晶水含量。
已知:Sac一表示糖精根离子[ ],糖精钴的溶解度在热水中较大,在冷水中较小;
丙酮沸点为56℃,与水互溶。
CoCl 6H O+2NaSac2H O=Co(Sac) H O xH O+(6-x)H O+2NaCl
2 2 2 2 2 4 2 2
(一)制备
I.称取1.0g CoCl 6H O ,加入18mL蒸馏水,搅拌溶解,得溶液1。
2 2
Ⅱ.称取2.6g(稍过量)糖精钠(NaSac·2H O),加入10mL蒸馏水,加热搅拌,得溶液2。
2
Ⅲ.将溶液2加入到接近沸腾的溶液1中,反应3分钟后停止加热,静置约半小时,冷却结晶。
Ⅳ.过滤,依次用三种不同试剂洗涤晶体,晾干得产品。
请回答:
(1)判断下列三种有机物中提供H+能力最弱的是 ▲ (填序号)。
a. b. c.
(2)Ⅲ中静置过程有少量晶体出现时,可将烧杯置于 ▲ 中,以使大量晶体析出。
(3)Ⅳ中用①丙酮、②冷水、③冷的1% NaSac溶液洗涤晶体,正确顺序为 ▲ 。
A.①③② B.③②① C.②①③
(二)结晶水含量测定
已知:EDTA和Co2+形成1:1配合物。
准确称取mg糖精钴产品于锥形瓶中,加蒸馏水,加热溶解,再加入六次甲基四胺缓冲溶液和指示
剂,在50~60℃下,用cmol/L的EDTA标准溶液滴定至终点,平行滴定三次,计算结晶水含量。
(4)下列有关说法正确的是 ▲ 。
A.六次甲基四胺溶液用作缓冲溶液,防止溶液pH发生突变,影响滴定
B.滴定时应一直观察滴定管中溶液体积的变化
C.平行滴定时,若滴定管内标准液足够,则无须重新装液
D.读数时应将滴定管从架上取下,捏住管上端无刻度处,使滴定管保持垂直
(5)滴定终点时消耗标准溶液VmL,则产品[Co(Sac) (H O) ·xH O][其摩尔质量为:(495+18x)g/mol]
2 2 4 2
中x的测定值为 ▲ (用含m、c、V的代数式表示);若滴定前滴定管尖嘴处无气泡,滴定后有气
泡,会导致x的测定值 ▲ (填“偏高”“偏低”或“无影响”)。
7
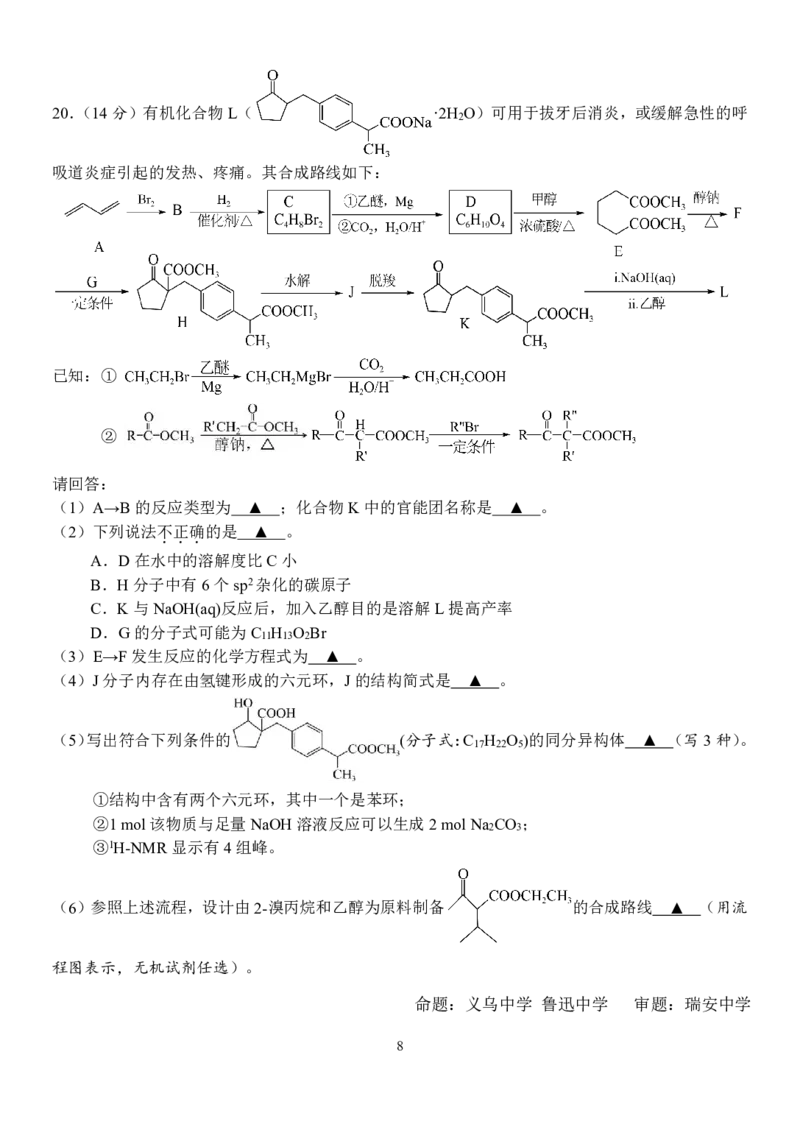
{#{QQABKYK05ggQkpSACB6qVUG0CgkQsIKiJQoMRQCcuAYCiAFIBAA=}#}20.(14分)有机化合物L( ·2H O)可用于拔牙后消炎,或缓解急性的呼
2
吸道炎症引起的发热、疼痛。其合成路线如下:
已知:①
②
请回答:
(1)A→B的反应类型为 ▲ ;化合物K中的官能团名称是 ▲ 。
(2)下列说法不 . 正 . 确 . 的是 ▲ 。
A.D在水中的溶解度比C小
B.H分子中有6个sp2杂化的碳原子
C.K与NaOH(aq)反应后,加入乙醇目的是溶解L提高产率
D.G的分子式可能为C H O Br
11 13 2
(3)E→F发生反应的化学方程式为 ▲ 。
(4)J分子内存在由氢键形成的六元环,J的结构简式是 ▲ 。
(5)写出符合下列条件的 (分子式:C H O )的同分异构体 ▲ (写3种)。
17 22 5
①结构中含有两个六元环,其中一个是苯环;
②1mol该物质与足量NaOH溶液反应可以生成2molNa CO ;
2 3
③1H-NMR显示有4组峰。
(6)参照上述流程,设计由2-溴丙烷和乙醇为原料制备 的合成路线 ▲ (用流
程图表示,无机试剂任选)。
命题:义乌中学 鲁迅中学 审题:瑞安中学
8
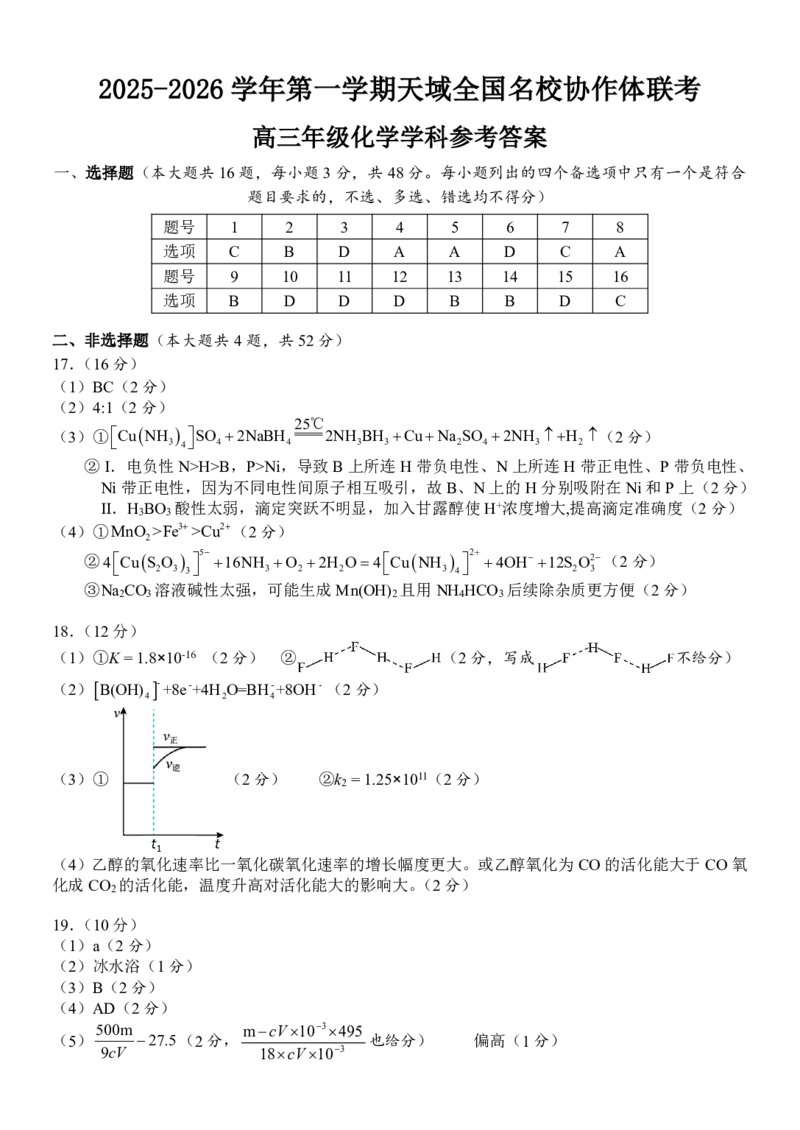
{#{QQABKYK05ggQkpSACB6qVUG0CgkQsIKiJQoMRQCcuAYCiAFIBAA=}#}2025-2026 学年第一学期天域全国名校协作体联考
高三年级化学学科参考答案
一、选择题(本大题共16题,每小题3分,共48分。每小题列出的四个备选项中只有一个是符合
题目要求的,不选、多选、错选均不得分)
题号 1 2 3 4 5 6 7 8
选项 C B D A A D C A
题号 9 10 11 12 13 14 15 16
选项 B D D D B B D C
二、非选择题(本大题共4题,共52分)
17.(16分)
(1)BC(2分)
(2)4:1(2分)
25℃
(3)①
CuNH
3
4
SO
4
2NaBH
4
2NH
3
BH
3
CuNa
2
SO
4
2NH
3
H
2
(2分)
②I.电负性N>H>B,P>Ni,导致B上所连H带负电性、N上所连H带正电性、P带负电性、
Ni带正电性,因为不同电性间原子相互吸引,故B、N上的H分别吸附在Ni和P上(2分)
II.H BO 酸性太弱,滴定突跃不明显,加入甘露醇使H+浓度增大,提高滴定准确度(2分)
3 3
(4)①MnO >Fe3>Cu2(2分)
2
②4CuS O 5 16NH O 2H O4CuNH 2 4OH12S O2(2分)
2 3 3 3 2 2 3 4 2 3
③Na CO 溶液碱性太强,可能生成Mn(OH) 且用NH HCO 后续除杂质更方便(2分)
2 3 2 4 3
18.(12分)
(1)①K=1.8×10-16 (2分) ② (2分,写成 不给分)
(2)B(OH) - +8e-+4H O=BH-+8OH- (2分)
4 2 4
(3)① (2分) ②k =1.25×1011(2分)
2
(4)乙醇的氧化速率比一氧化碳氧化速率的增长幅度更大。或乙醇氧化为CO的活化能大于CO氧
化成CO 的活化能,温度升高对活化能大的影响大。(2分)
2
19.(10分)
(1)a(2分)
(2)冰水浴(1分)
(3)B(2分)
(4)AD(2分)
500m mcV103495
(5) 27.5(2分, 也给分) 偏高(1分)
9cV 18cV103
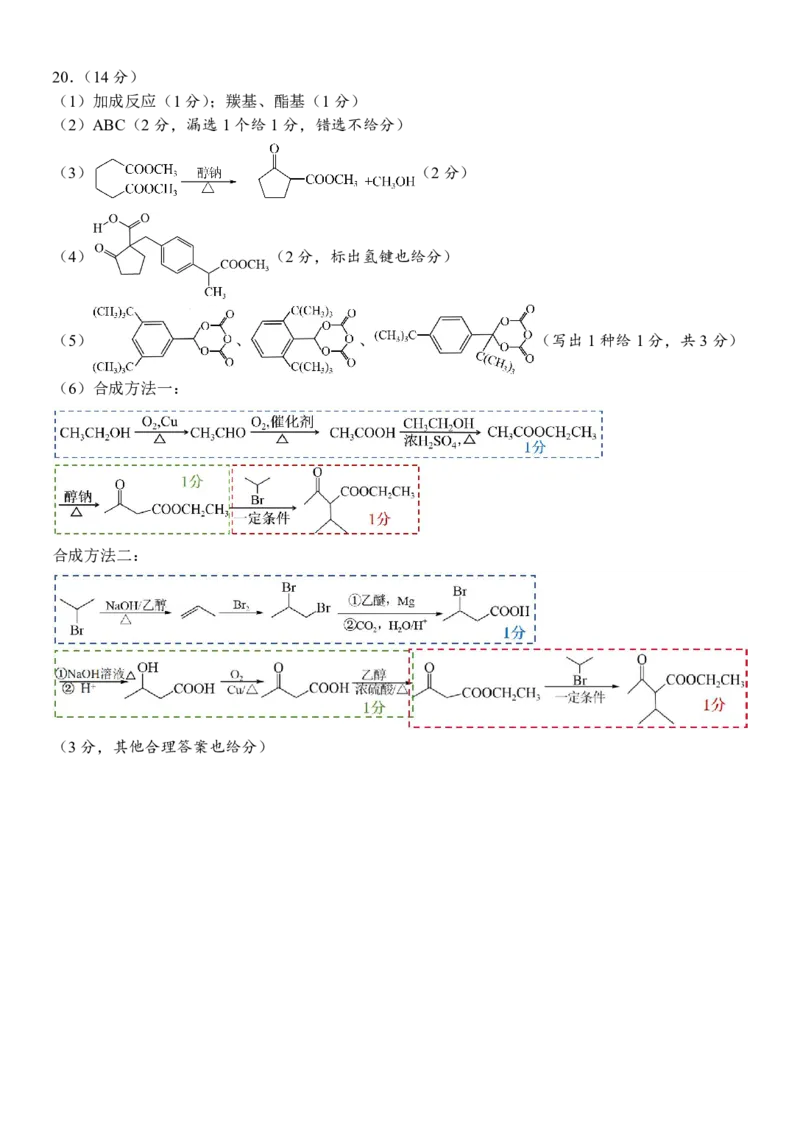
{#{QQABKYK05ggQkpSACB6qVUG0CgkQsIKiJQoMRQCcuAYCiAFIBAA=}#}20.(14分)
(1)加成反应(1分);羰基、酯基(1分)
(2)ABC(2分,漏选1个给1分,错选不给分)
(3) (2分)
(4) (2分,标出氢键也给分)
(5) 、 、 (写出1种给1分,共3分)
(6)合成方法一:
合成方法二:
(3分,其他合理答案也给分)
{#{QQABKYK05ggQkpSACB6qVUG0CgkQsIKiJQoMRQCcuAYCiAFIBAA=}#}