文档内容
湖北省黄冈中学 2025 届高三第二次模拟考试
化学试卷
命题教师:李青 方圆 审题教师:邓丽娟
考试时间:2025年5月18日下午14:30-17:05 试卷满分:100分
可能用到的相对原子质量:H 1 O 16 P 31 S 32 K 39 Co 59
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有
一项是符合题目要求的。
1.古往今来,化学出现在生产生活的方方面面。下列有关说法不正确的是
A.我国《汉书》中记载“高奴县有洧水,可燃”,“洧水”指的是酒精
B.19世纪,苯酚曾作为外用消毒剂广泛用于手术前的器械消毒
C.导电高分子材料可用于制造移动电子设备开关、轻便的彩色显示屏
D.高分子分离膜是一种可用于药物提纯、血液透析的功能高分子材料
2.我国科研团队近期开发出一种新型钠离子电池,其正极材料为普鲁士白(化学式为
Na₂Fe[Fe(CN)₆]),具有低成本、高稳定性和环境友好性。下列相关叙述错误的是
A.普鲁士白材料在空气中长期存放会变质
B.使用普鲁士白的钠离子电池相比锂离子电池更符合可持续发展理念,因其原料储
量丰富且成本相对低廉
C.普鲁士白可作为智能窗的变色材料,其显色原理是Fe²⁺/Fe³⁺价态互变
D.废弃的普鲁士白在高温煅烧处理下分解为Fe O₃、NaCN等,从而实现无害化处理
2
3.关于物质的分离和提纯,下列说法错误的是
A.重油经过减压蒸馏可以得到液化石油气和润滑油
B.提纯苯甲酸的步骤有加热溶解、趁热过滤、冷却结晶
C.使用酸性KMnO 溶液检验2-溴丙烷消去产物要先用水洗气
4
D.从青蒿中分离出青蒿素的方法是萃取和柱色谱法
4.下列图示或化学用语表述错误的是
COOH
A.
NH2
的系统命名:1-羧基-2-苯乙胺
B.PO 分子的球棍模型:
4 10
C.NaH的电子式:
D.HSe分子的价层电子对互斥模型:
2
5.下列对有关物质结构或性质的描述不正确的是
A.纯物质晶体颗粒小于200nm时,晶粒越小,熔点越高
B.分子空间结构与其稳定性有关,例如椅式C H 比船式C H 稳定
6 12 6 12
C.等离子体是一种特殊的气体,可存在于日光灯的灯管里、蜡烛的火焰里和极光里
湖北省黄冈中学2025届高三第二次模拟考试化学试卷共 8 页第 1 页D.下图为六个硅氧四面体(六元环)形成的简单阴离子,其化学式为
6.胆固醇的结构如下图,下列有关说法错误的是
A.手性碳原子有8个
B.同分异构体中不可能有芳香醛
C.红外光谱中出现了 以上的吸收峰
D.总胆固醇是血脂四项检查指标之一,合理的饮食结构有助于控制胆固醇水平
7.下列方程式书写正确的是
A.甲醛与过量的银氨溶液反应:
HCHO + 2[Ag(NH)]OH HCOONH + 2Ag↓ + 3NH + H O
3 2 4 3 2
B.硬脂酸甘油酯在碱性条件下水解:
3C H COONa
17 33
C.在牙膏中添加氟化物,能起到预防龋齿的原理:
Ca (PO )OH(s)+F-(aq) Ca (PO )F(s)+OH-(aq)
5 4 3 5 4 3
D.铁发生吸氧腐蚀的正极电极反应式:2Fe2++2HO+O+4e⁻= 2Fe(OH) ↓
2 2 2
8.物质结构决定物质性质。下列性质差异与结构因素匹配错误的是
选项 性质描述 结构因素
A AgCl难溶于水而AgF易溶于水 Ag+强极化能力、半径:Cl->F-
B (CH)CHCH NH NO 熔点低于NH NO 阳离子体积
3 2 2 3 3 4 3
C NH 键角大于NF 键的极性
3 3
D 频繁烫发会对头发产生一定的损害 蛋白质中二硫键(-S-S-)的破坏与重
排
9.短周期主族元素X、Y、Z、W、Q的原子序数依次增大,分布于三个不同周期。已知:
①X的原子半径最小;②Z的单质可与热水反应,其氧化物广泛用作耐火材料;③W
的最高价氧化物对应水化物具有两性;④ Z、Q的最外层电子数之和等于Y的原子序
湖北省黄冈中学2025届高三第二次模拟考试化学试卷共 8 页第 2 页数。下列说法正确的是
A.Z的第一电离能小于W的第一电离
B.简单离子半径: W > Z > X
C.工业上通过电解W的氯化物制备W单质
D.Y的简单气态氢化物稳定性强于Q
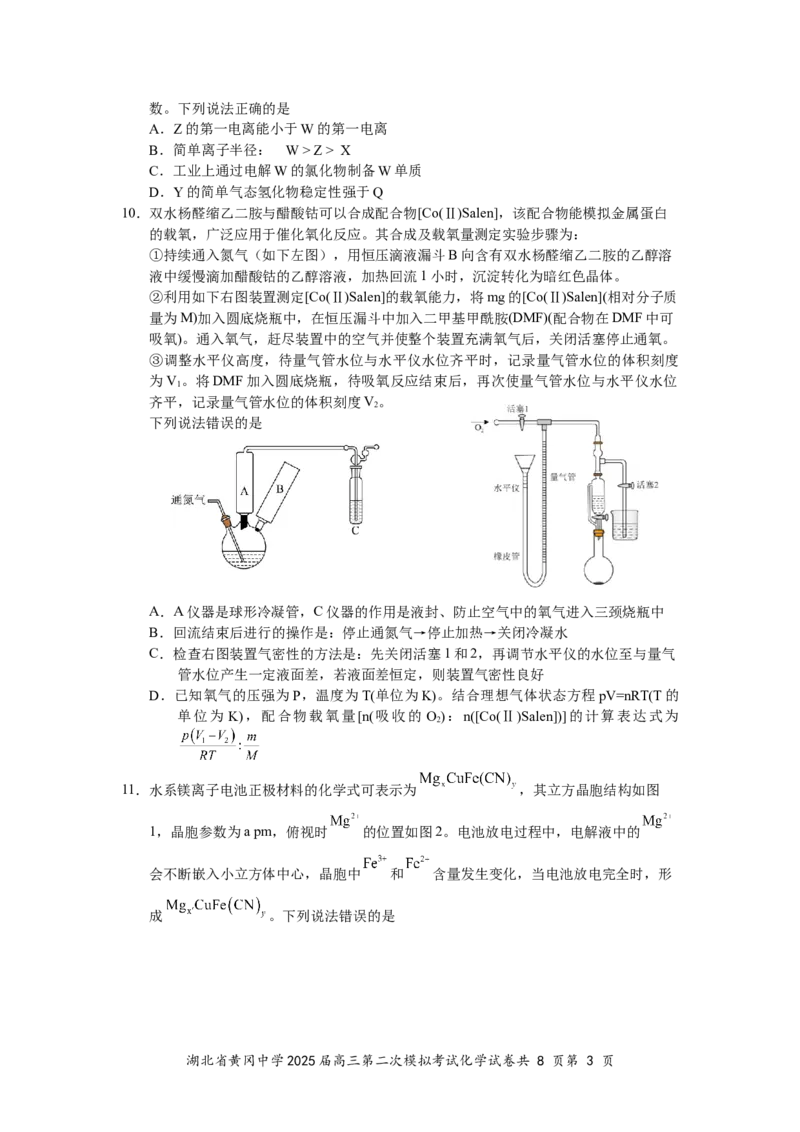
10.双水杨醛缩乙二胺与醋酸钴可以合成配合物[Co(Ⅱ)Salen],该配合物能模拟金属蛋白
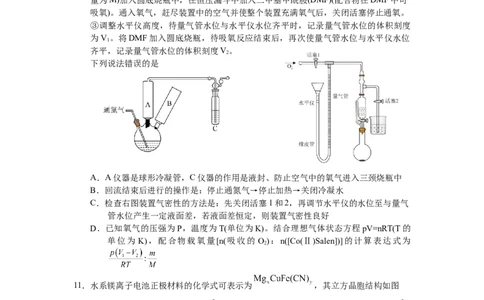
的载氧,广泛应用于催化氧化反应。其合成及载氧量测定实验步骤为:
①持续通入氮气(如下左图),用恒压滴液漏斗B向含有双水杨醛缩乙二胺的乙醇溶
液中缓慢滴加醋酸钴的乙醇溶液,加热回流1小时,沉淀转化为暗红色晶体。
②利用如下右图装置测定[Co(Ⅱ)Salen]的载氧能力,将mg的[Co(Ⅱ)Salen](相对分子质
量为M)加入圆底烧瓶中,在恒压漏斗中加入二甲基甲酰胺(DMF)(配合物在DMF中可
吸氧)。通入氧气,赶尽装置中的空气并使整个装置充满氧气后,关闭活塞停止通氧。
③调整水平仪高度,待量气管水位与水平仪水位齐平时,记录量气管水位的体积刻度
为V 。将DMF加入圆底烧瓶,待吸氧反应结束后,再次使量气管水位与水平仪水位
1
齐平,记录量气管水位的体积刻度V。
2
下列说法错误的是
A.A仪器是球形冷凝管,C仪器的作用是液封、防止空气中的氧气进入三颈烧瓶中
B.回流结束后进行的操作是:停止通氮气→停止加热→关闭冷凝水
C.检查右图装置气密性的方法是:先关闭活塞1和2,再调节水平仪的水位至与量气
管水位产生一定液面差,若液面差恒定,则装置气密性良好
D.已知氧气的压强为P,温度为T(单位为K)。结合理想气体状态方程pV=nRT(T的
单位为 K),配合物载氧量[n(吸收的 O):n([Co(Ⅱ)Salen])]的计算表达式为
2
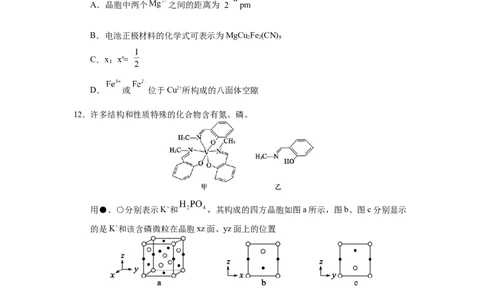
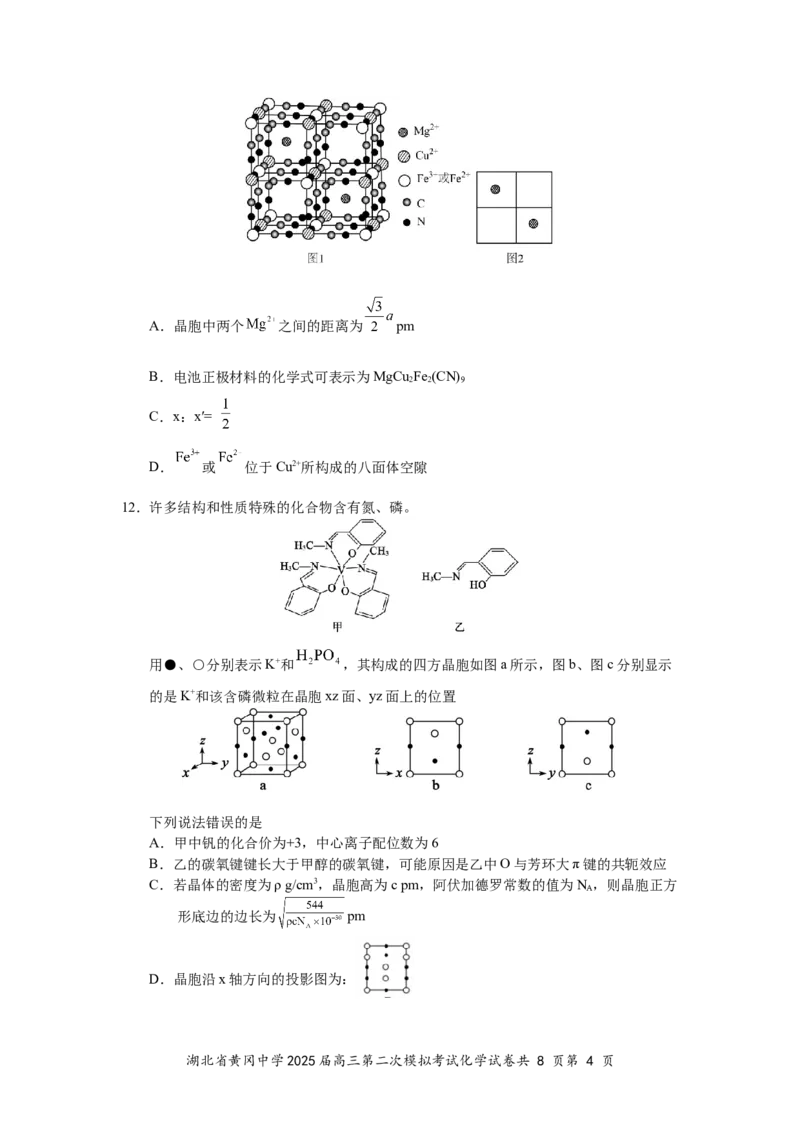
11.水系镁离子电池正极材料的化学式可表示为 ,其立方晶胞结构如图
1,晶胞参数为a pm,俯视时 的位置如图2。电池放电过程中,电解液中的
会不断嵌入小立方体中心,晶胞中 和 含量发生变化,当电池放电完全时,形
成 。下列说法错误的是
湖北省黄冈中学2025届高三第二次模拟考试化学试卷共 8 页第 3 页A.晶胞中两个 之间的距离为 pm
B.电池正极材料的化学式可表示为MgCu Fe (CN)
2 2 9
C.x:x′=
D. 或 位于Cu2+所构成的八面体空隙
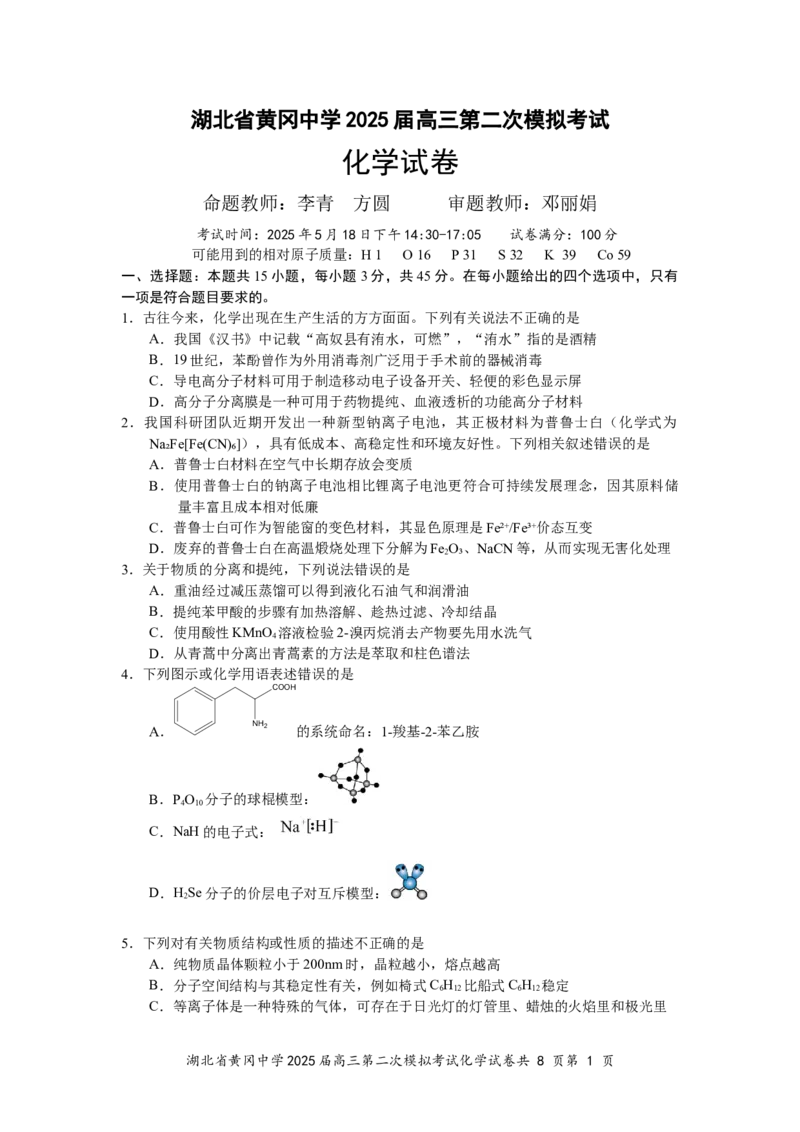
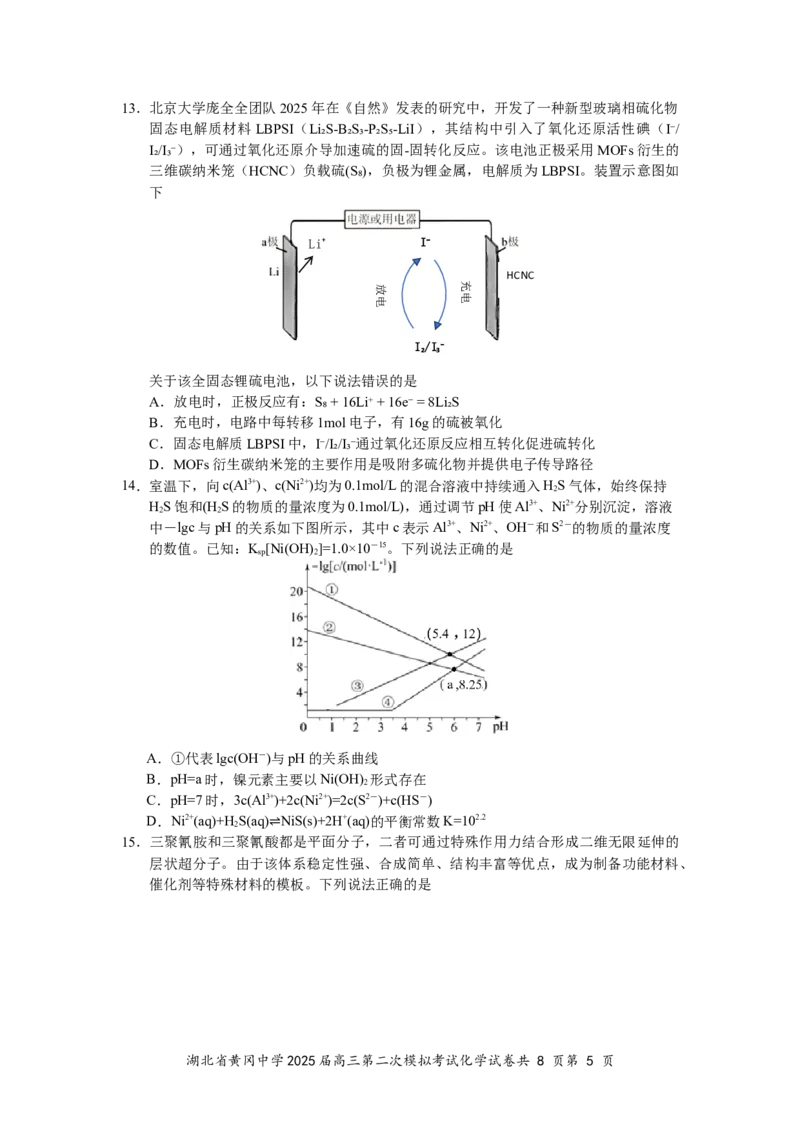
12.许多结构和性质特殊的化合物含有氮、磷。
用●、○分别表示K+和 ,其构成的四方晶胞如图a所示,图b、图c分别显示
的是K+和该含磷微粒在晶胞xz面、yz面上的位置
下列说法错误的是
A.甲中钒的化合价为+3,中心离子配位数为6
B.乙的碳氧键键长大于甲醇的碳氧键,可能原因是乙中O与芳环大π键的共轭效应
C.若晶体的密度为ρ g/cm3,晶胞高为c pm,阿伏加德罗常数的值为N ,则晶胞正方
A
形底边的边长为 pm
D.晶胞沿x轴方向的投影图为:
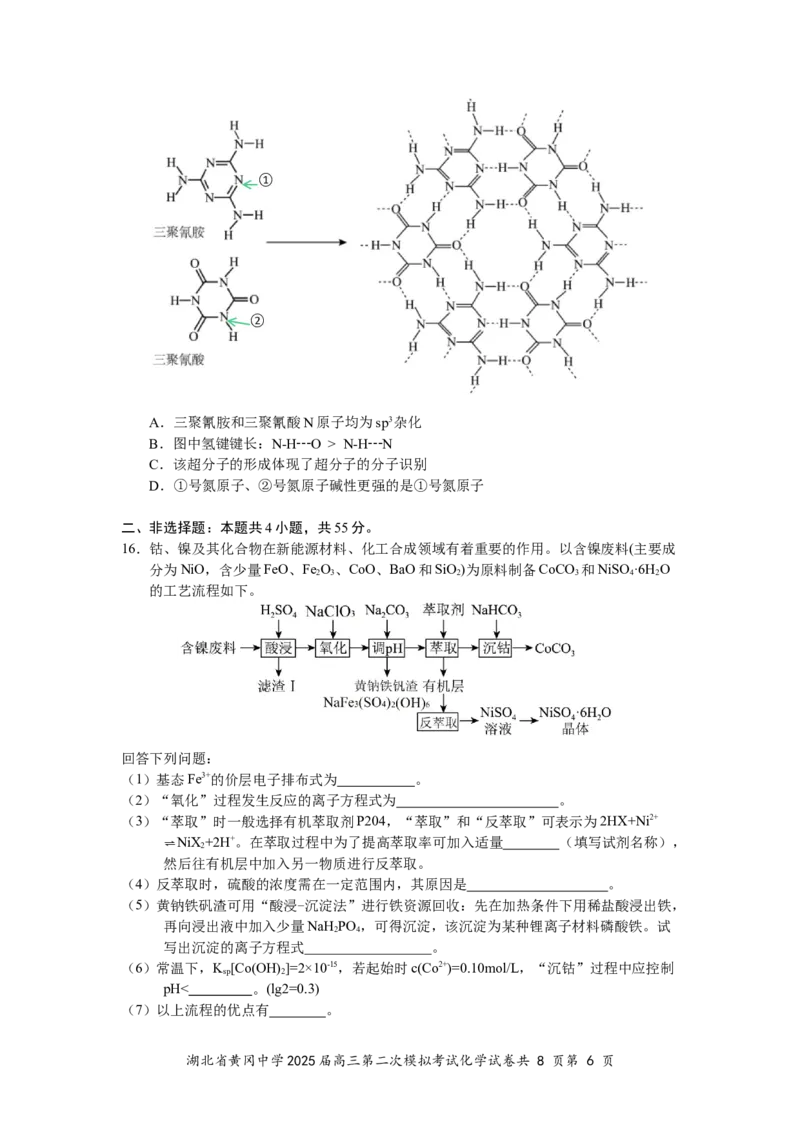
湖北省黄冈中学2025届高三第二次模拟考试化学试卷共 8 页第 4 页13.北京大学庞全全团队2025年在《自然》发表的研究中,开发了一种新型玻璃相硫化物
固态电解质材料LBPSI(Li₂S-B₂S₃-P₂S₅-LiI),其结构中引入了氧化还原活性碘(I⁻/
I₂/I₃⁻),可通过氧化还原介导加速硫的固-固转化反应。该电池正极采用MOFs衍生的
三维碳纳米笼(HCNC)负载硫(S₈),负极为锂金属,电解质为LBPSI。装置示意图如
下
Li+ I⁻
HCNC
I₂/I₃⁻
湖北省黄冈中学2025届高三第二次模拟考试化学试卷共 8 页第 5 页
放电
充电
关于该全固态锂硫电池,以下说法错误的是
A.放电时,正极反应有:S₈ + 16Li⁺ + 16e⁻ = 8Li₂S
B.充电时,电路中每转移1mol电子,有16g的硫被氧化
C.固态电解质LBPSI中,I⁻/I₂/I₃⁻通过氧化还原反应相互转化促进硫转化
D.MOFs衍生碳纳米笼的主要作用是吸附多硫化物并提供电子传导路径
14.室温下,向c(Al3+)、c(Ni2+)均为0.1mol/L的混合溶液中持续通入HS气体,始终保持
2
HS饱和(H S的物质的量浓度为0.1mol/L),通过调节pH使Al3+、Ni2+分别沉淀,溶液
2 2
中-lgc与pH的关系如下图所示,其中c表示Al3+、Ni2+、OH-和S2-的物质的量浓度
的数值。已知:K [Ni(OH) ]=1.0×10-15。下列说法正确的是
sp 2
A.①代表lgc(OH-)与pH的关系曲线
B.pH=a时,镍元素主要以Ni(OH) 形式存在
2
C.pH=7时,3c(Al3+)+2c(Ni2+)=2c(S2-)+c(HS-)
D.Ni2+(aq)+H S(aq) NiS(s)+2H+(aq)的平衡常数K=102.2
2
15.三聚氰胺和三聚氰酸都是平面分子,二者可通过特殊作用力结合形成二维无限延伸的
⇌
层状超分子。由于该体系稳定性强、合成简单、结构丰富等优点,成为制备功能材料、
催化剂等特殊材料的模板。下列说法正确的是①
②
A.三聚氰胺和三聚氰酸N原子均为sp3杂化
B.图中氢键键长:N-H┄O > N-H┄N
C.该超分子的形成体现了超分子的分子识别
D.①号氮原子、②号氮原子碱性更强的是①号氮原子
二、非选择题:本题共4小题,共55分。
16.钴、镍及其化合物在新能源材料、化工合成领域有着重要的作用。以含镍废料(主要成
分为NiO,含少量FeO、Fe O、CoO、BaO和SiO)为原料制备CoCO 和NiSO ·6H O
2 3 2 3 4 2
的工艺流程如下。
回答下列问题:
(1)基态Fe3+的价层电子排布式为 。
(2)“氧化”过程发生反应的离子方程式为 。
(3)“萃取”时一般选择有机萃取剂P204,“萃取”和“反萃取”可表示为2HX+Ni2+
NiX+2H+。在萃取过程中为了提高萃取率可加入适量 (填写试剂名称),
⇌ 2
然后往有机层中加入另一物质进行反萃取。
(4)反萃取时,硫酸的浓度需在一定范围内,其原因是 。
(5)黄钠铁矾渣可用“酸浸-沉淀法”进行铁资源回收:先在加热条件下用稀盐酸浸出铁,
再向浸出液中加入少量NaH PO ,可得沉淀,该沉淀为某种锂离子材料磷酸铁。试
2 4
写出沉淀的离子方程式__________________。
(6)常温下,K [Co(OH) ]=2×10-15,若起始时c(Co2+)=0.10mol/L,“沉钴”过程中应控制
sp 2
pH< 。(lg2=0.3)
(7)以上流程的优点有 。
湖北省黄冈中学2025届高三第二次模拟考试化学试卷共 8 页第 6 页A.资源高效回收利用,低能耗,符合绿色化学原则
B.分步除杂,选择性高
C.工艺成熟,操作简便
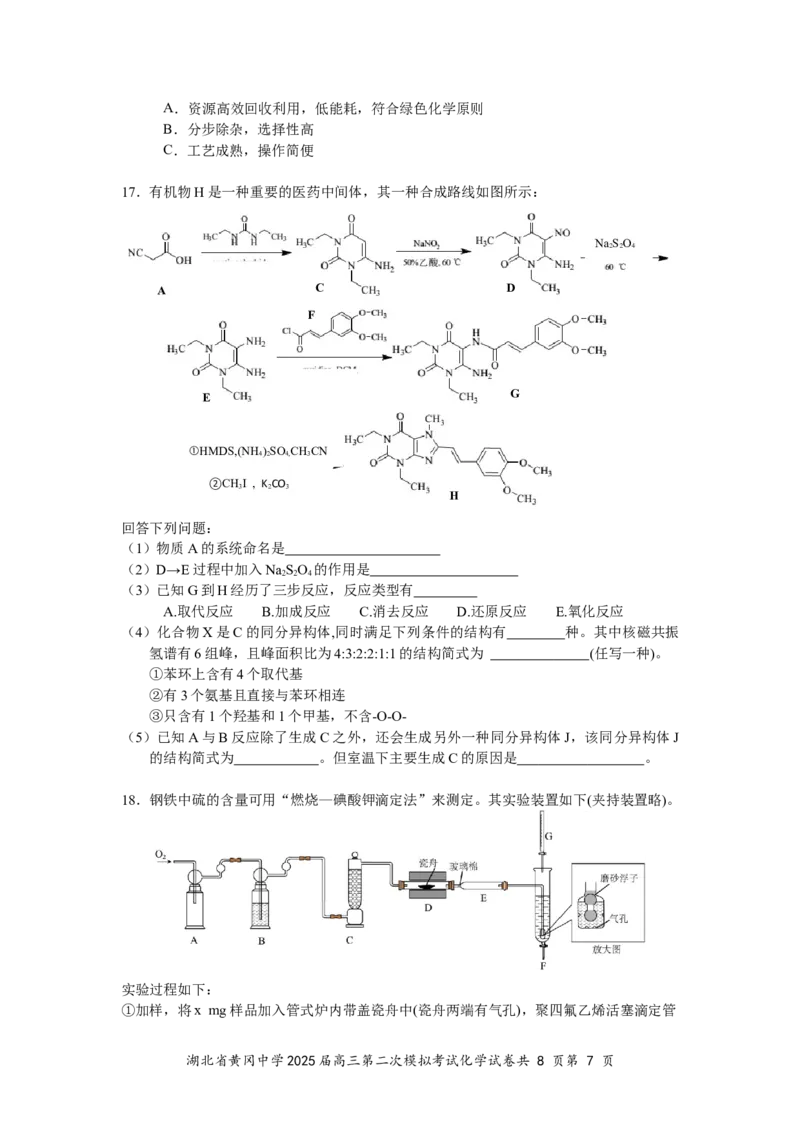
17.有机物H是一种重要的医药中间体,其一种合成路线如图所示:
NaSO
2 2 4
A C D
F
E G
①HMDS,(NH
4
)
2
SO
4,
CH
3
CN
②CH
3
I , K
2
CO
3
H
回答下列问题:
(1)物质A的系统命名是
(2)D→E过程中加入NaSO 的作用是
2 2 4
(3)已知G到H经历了三步反应,反应类型有
A.取代反应 B.加成反应 C.消去反应 D.还原反应 E.氧化反应
(4)化合物X是C的同分异构体,同时满足下列条件的结构有 种。其中核磁共振
氢谱有6组峰,且峰面积比为4:3:2:2:1:1的结构简式为 (任写一种)。
①苯环上含有4个取代基
②有3个氨基且直接与苯环相连
③只含有1个羟基和1个甲基,不含-O-O-
(5)已知A与B反应除了生成C之外,还会生成另外一种同分异构体J,该同分异构体J
的结构简式为 。但室温下主要生成C的原因是 。
18.钢铁中硫的含量可用“燃烧—碘酸钾滴定法”来测定。其实验装置如下(夹持装置略)。
实验过程如下:
①加样,将x mg样品加入管式炉内带盖瓷舟中(瓷舟两端有气孔),聚四氟乙烯活塞滴定管
湖北省黄冈中学2025届高三第二次模拟考试化学试卷共 8 页第 7 页G内预装c(KIO ):c(KI)略小于1:5的KIO 碱性标准溶液,吸收管F内盛有盐酸酸化的淀
3 3
粉水溶液。向F内滴入适量KIO 碱性标准溶液,发生反应
3
KIO +5KI+6HCl=3I +6KCl+3H O,使溶液显浅蓝色;
3 2 2
②燃烧:一定流速下通入O,一段时间后,加热并使样品燃烧;
2
③滴定:当F内溶液浅蓝色消退时(发生反应SO +I +2H O=HSO +2HI),立即用KIO 碱
2 2 2 2 4 3
性标准溶液滴定至浅蓝色复现。随SO 不断进入F,滴定过程中溶液颜色“消退-变蓝”
2
不断快速变换,直至终点。
(1)配制KIO 标准溶液时,c(KIO ):c(KI)略小于1:5的原因是 。
3 3
(2)装置B中的浓硫酸和装置C中的PO 的作用是 。装置F中通气管末端多
2 5
孔玻璃泡内置一密度小于水的磨砂浮子(见放大图),放大图中装置的目的是
(请写出两点)。
(3)该滴定到达终点的颜色变化是 。实际操作中,终点常出现溶液蓝色
反复(消退-变蓝)的现象,可能原因是 。
(4)滴定消耗0.001mol•L-1 KIO 碱性标准溶液VmL,样品中硫的质量分数是
3
。
(5)若钢铁中含有硫酸盐(如FeSO ),对硫含量测定的干扰体现在
4
。
19.工业上利用CO 和H 催化合成甲醇,既可减少温室气体排放,又能制备清洁能源。主
2 2
要反应如下:
主反应Ⅰ :CO 2 (g)+3H 2 (g) ⇌ CH 3 OH(g)+H 2 O(g) ΔH 1
副反应Ⅱ :CO(g)+H(g) CO(g)+H O(g) ΔH = +41.2 kJ·mol⁻¹
2 2 2 2
请回答下列问题:
⇌
(1)根据以下信息,求反应Ⅰ的ΔH= 。
1
①已知以下燃烧焓数据(ΔH,单位kJ·mol⁻¹):
物质 H CO CHOH(l)
2 3
燃烧热 ΔH/kJ·mol⁻¹ -285.8 -283.0 -726.6
②H O(l) = H O(g) ΔH=+44.0 kJ·mol⁻¹
2 2
③CH OH(l) = CHOH(g) ΔH= +37.4 kJ·mol⁻¹
3 3
(2)在 5 L 密闭容器中,充入 2 mol CO 和8 mol H ,发生反应Ⅰ和Ⅱ。平衡时测得
2 2
CHOH为1.0 mol,CO为0.5 mol。
3
①计算CO 的总转化率 ;
2
②求反应Ⅰ的平衡常数Kc 。(保留两位有效数字)
(3)研究反应Ⅰ的速率方程,实验数据如下:
实验 c(CO)/mol·L ¹ c(H)/mol·L ¹ 初始速率/mol·L⁻¹·min⁻¹
2 2
1 0.5 1.0 0.05
2 1.0 ⁻ 1.0 ⁻ 0.10
3 1.0 2.0 0.80
已知速率方程的表达式为v = k·cm(CO)·cn(H ),根据表格数据,计算m= ,n= ;
2 2
(4)工业上利用CO 加氢制甲醇时,催化剂的选择直接影响反应路径和产物分布。某研究
2
团队测试了两种催化剂(Cat.A和Cat.B)在不同温度下的CO 转化率及产物选择性,
2
经过相同反应时间测得如下实验数据:
编号 温度 催化剂 CO 总转化率 CHOH选择性 CO选择性(%)
2 3
(℃) (%) (%)
1 200 Cat.A 65 80 20
2 250 Cat.A 60 65 35
湖北省黄冈中学2025届高三第二次模拟考试化学试卷共 8 页第 8 页3 300 Cat.A 55 40 60
4 200 Cat.B 50 30 70
5 250 Cat.B 70 15 85
6 300 Cat.B 85 5 95
请回答下列问题:
①对比实验1和4可发现:在相同温度下,催化剂Cat.A对CO 转化为CHOH的选择性
2 3
比Cat.B的要高,试用碰撞理论解释其原因____________________________。
②分析Cat.A在200℃→300℃升温过程中,CHOH选择性从80%降至40%的原因
3
。
湖北省黄冈中学2025届高三第二次模拟考试化学试卷共 8 页第 9 页