文档内容
专题31 分子结构与性质
1.【2023年山东卷】下列分子属于极性分子的是
A. B. C. D.
【答案】B
【解析】A.CS 中C上的孤电子对数为 (4-2 2)=0, 键电子对数为2,价层电子对数为2,CS 的空间
2 2
构型为直线形,分子中正负电中心重合×,CS×属于非σ极性分子,A项不符合题意;B.NF 中N上的孤
2 3
电子对数为 (5-3 1)=1, 键电子对数为3,价层电子对数为4,NF 的空间构型为三角锥形,分子
3
× × σ
中正负电中心不重合,NF 属于极性分子,B项符合题意;C.SO 中S上的孤电子对数为 (6-
3 3
3 2)=0, 键电子对数为3,价层电子对数为3,SO 的空间构型为平面正三角形,分子中正×负电中心
3
重×合,SOσ属于非极性分子,C项不符合题意;D.SiF 中Si上的孤电子对数为 (4-4 1)=0, 键电
3 4
子对数为4,价层电子对数为4,SiF 的空间构型为正四面体形,分子中正负电中心×重合×,SiF 属σ于非
4 4
极性分子,D项不符合题意;答案选B。
2.【2023年辽宁卷】下列化学用语或表述正确的是
A.BeCl 的空间结构:V形 B.P 中的共价键类型:非极性键
2 4
C.基态Ni原子价电子排布式:3d10 D.顺—2—丁烯的结构简式:
【答案】B
【解析】A.BeCl 的中心原子为Be,根据VSEPR模型可以计算,BeCl 中不含有孤电子对,因此BeCl 为
2 2 2
直线型分子,A错误;B.P 分子中相邻两P原子之间形成共价键,同种原子之间形成的共价键为非
4
极性共价键,P 分子中的共价键类型为非极性共价键,B正确;C.Ni原子的原子序数为28,其基态
4
原子的价电子排布为3d84s2,C错误;D.顺-2-丁烯的结构中两个甲基在双键的同一侧,其结构简式为
,D错误;故答案选B。
3.【2023年1月浙江卷】共价化合物 中所有原子均满足8电子稳定结构,一定条件下可发生反应:
,下列说法不正确的是
A. 的结构式为 B. 为非极性分子C.该反应中 的配位能力大于氯 D. 比 更难与 发生反应
【答案】D
【解析】A.由双聚氯化铝分子中所有原子均满足8电子稳定结构可知,分子的结构式为
,故A正确;B.由双聚氯化铝分子中所有原子均满足8电子稳定结构可知,
分子的结构式为 ,则双聚氯化铝分子为结构对称的非极性分子,故B正确;
C.由反应方程式可知,氨分子更易与具有空轨道的铝原子形成配位键,配位能力大于氯原子,故C
正确;D.溴元素的电负性小于氯元素,原子的原子半径大于氯原子,则铝溴键弱于铝氯键,所以双
聚溴化铝的铝溴键更易断裂,比双聚氯化铝更易与氨气反应,故D错误;故选D。
4.【2023年湖北卷】下列有关物质结构和性质的说法错误的是
A.含有手性碳原子的分子叫做手性分子
B.邻羟基苯甲醛的沸点低于对羟基苯甲醛的沸点
C.酰胺在酸或碱存在并加热的条件下可发生水解反应
D.冠醚(18-冠-6)的空穴与K+尺寸适配,两者能通过弱相互作用形成超分子
【答案】A
【解析】A.有手性异构体的分子被称为手性分子,当分子中存在两个或两个以上的手性碳原子时,会出
现内消旋体,这种含有内消旋体的分子不是手性分子,A错误;B.邻羟基苯甲醛中含有分子内氢键,
分子内氢键可以降低物质的熔沸点,因此邻羟基苯甲醛的熔沸点低于对羟基苯甲醛的熔沸点,B正确;
C.酰胺在酸性条件下反应生成羧酸和胺,在碱性条件下反应生成羧酸盐和氨气,二者均为水解反应,
C正确;D.超分子是由两种或两种以上的分子通过分子间作用力形成的分子聚集体,分子间作用力
是弱相互作用,冠醚(18-冠-6)的空穴大小为260~320pm,可以适配K+(276pm)、Rb+(304pm),冠醚与
离子之间形成配位键,通过弱相互作用形成超分子,D正确;故答案选A。
5.【2023年湖北卷】物质结构决定物质性质。下列性质差异与结构因素匹配错误的是
选项 性质差异 结构因素
A 沸点:正戊烷(36.1℃)高于新戊烷(9.5℃) 分子间作用力
B 熔点: (1040℃)远高于 (178℃升华) 晶体类型
C 酸性: ( )远强于 ( ) 羟基极性
D 溶解度(20℃): (29g)大于 (8g) 阴离子电荷
【答案】D
【解析】A.正戊烷和新戊烷形成的晶体都是分子晶体,由于新戊烷支链多,对称性好,分子间作用力小,
所以沸点较低,故A正确;B.AlF 为离子化合物,形成的晶体为离子晶体,熔点较高,AlCl 为共价
3 3化合物,形成的晶体为分子晶体,熔点较低,则 熔点远高于 ,故B正确;C.由于电负性
F>H,C-F键极性大于C-H键,使得羧基上的羟基极性增强,氢原子更容易电离,酸性增强,故C正
确;D.碳酸氢钠在水中的溶解度比碳酸钠小的原因是碳酸氢钠晶体中HCO 间存在氢键,与晶格能
大小无关,即与阴离子电荷无关,故D错误;答案选D。
6.【2023年湖北卷】价层电子对互斥理论可以预测某些微粒的空间结构。下列说法正确的是
A. 和 的VSEPR模型均为四面体
B. 和 的空间构型均为平面三角形
C. 和 均为非极性分子
D. 与 的键角相等
【答案】A
【解析】A.甲烷分子的中心原子的价层电子对为4,水分子的中心原子价层电子对也为4,所以他们的
VSEPR模型都是四面体,A正确;B.SO 的孤电子对为1,CO 的孤电子对为0,所以SO 的空
间构型为三角锥形,CO 的空间构型为平面三角形,B错误,C.CH 为正四面体结构,为非极性分
4
子,SF 中心原子有孤电子对,为极性分子,C错误;D.XeF 和XeO 分子中,孤电子对不相等,孤
4 2 2
电子对越多,排斥力越大,所以键角不等,D错误;故选A。
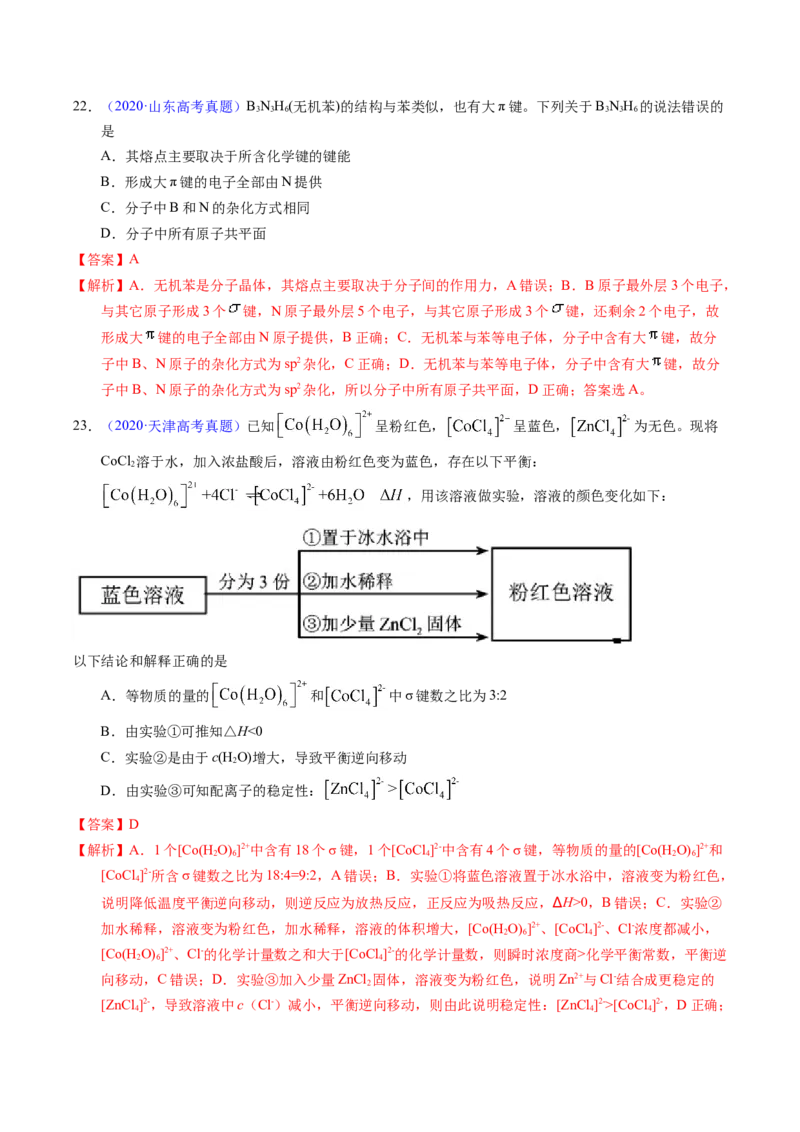
7.【2023年湖北卷】中科院院士研究发现,纤维素可在低温下溶于NaOH溶液,恢复至室温后不稳定,
加入尿素可得到室温下稳定的溶液,为纤维素绿色再生利用提供了新的解决方案。下列说法错误的是
A.纤维素是自然界分布广泛的一种多糖
B.纤维素难溶于水的主要原因是其链间有多个氢键
C.NaOH提供 破坏纤维素链之间的氢键
D.低温降低了纤维素在NaOH溶液中的溶解性
【答案】D
【解析】A.纤维素属于多糖,大量存在于我们吃的蔬菜水果中,在自然界广泛分布,A正确;B.纤维素
大分子间和分子内、纤维素和水分子之间均可形成氢键以及纤维素链段间规整紧密的结构使纤维素分
子很难被常用的溶剂如水溶解,B正确;C.纤维素在低温下可溶于氢氧化钠溶液,是因为碱性体系
主要破坏的是纤维素分子内和分子间的氢键促进其溶解,C正确;D.由题意可知低温提高了纤维素
在NaOH溶液中的溶解性,D错误;故选D。
8.(2021·山东真题)关于CHOH、NH 和(CH)NNH 的结构与性质,下列说法错误的是
3 2 4 3 2 2A.CHOH为极性分子 B.NH 空间结构为平面形
3 2 4
C.NH 的沸点高于(CH)NNH D.CHOH和(CH)NNH 中C、O、N杂化方式均相同
2 4 3 2 2 3 3 2 2
【答案】B
【解析】A.甲醇可看成是甲烷中的一个氢原子被羟基取代得到的,为四面体结构,是由极性键组成的极
性分子,A正确;B.NH 中N原子的杂化方式为sp3,不是平面形,B错误;C.NH 分子中连接N
2 4 2 4
原子的H原子数多,存在氢键的数目多,而偏二甲肼((CH)NNH)只有一端可以形成氢键,另一端
3 2 2
的两个甲基基团比较大,影响了分子的排列,沸点较NH 的低,C正确;D.CHOH为四面体结
2 4 3
构,-OH结构类似于水的结构,(CH)NNH 的结构简式为 ,两者分子中C、O、N杂化方
3 2 2
式均为sp3,D正确;故选B。
9.【2022年天津卷】下列物质沸点的比较,正确的是
A. B.HF>HCl
C. D.
【答案】B
【解析】A.甲烷和乙烷组成结构相似,相对分子质量越大,范德华力越大,沸点越高,因此沸点
,故A错误;B.HF存在分子间氢键,因此沸点HF>HCl,故B正确;C.
组成结构相似,相对分子质量越大,范德华力越大,沸点越高,因此沸点 ,故C错误;D.
相同碳原子的烷烃,支链越多,沸点越低,因此 ,故D错误。综上所述,
答案为B。
10.【2022年天津卷】利用反应 可制备NH。下列叙述正确的是
2 4
A.NH 分子有孤电子对,可做配体
3
B.NaCl晶体可以导电
C.一个NH 分子中有4个σ键
2 4
D.NaClO和NaCl均为离子化合物,他们所含的化学键类型相同
【答案】A
【解析】A.NH 中N原子的孤电子对数= =1,可以提供1对孤电子对,可以做配体,A正确;
3
B.导电需要物质中有可自由移动的离子或电子,NaCl晶体中没有自由移动的电子或者离子,故不能
导电,B错误;C.单键属于σ键,双键中含有1个σ键和1个π键,三键中含有1个σ键和2个π键;
NH 的结构式为 ,分子中含有5个σ键,C错误;D.NaClO含有离子键和共价键,
2 4
NaCl只含有离子键,都是离子化合物,但所含的化学键类型不同,D错误;故选A。
11.【2022年天津卷】一定条件下,石墨转化为金刚石吸收能量。下列关于石墨和金刚石的说法正确的是A.金刚石比石墨稳定
B.两物质的碳碳 键的键角相同
C.等质量的石墨和金刚石中,碳碳 键数目之比为4∶3
D.可以用X射线衍射仪鉴别金刚石和石墨
【答案】D
【解析】A.石墨转化为金刚石吸收能量,则石墨能量低,根据能量越低越稳定,因此石墨比金刚石稳定,
故A错误;B.金刚石是空间网状正四面体形,键角为109°28′,石墨是层内正六边形,键角为120°,
因此碳碳 键的键角不相同,故B错误;C.金刚石是空间网状正四面体形,石墨是层内正六边形,
层与层之间通过范德华力连接,1mol金刚石有2mol碳碳 键,1mol石墨有1.5mol碳碳 键,因此等
质量的石墨和金刚石中,碳碳 键数目之比为3∶4,故C错误;D.金刚石和石墨是两种不同的晶体
类型,因此可用X射线衍射仪鉴别,故D正确。综上所述,答案为D。
12.(2021·海南真题)SF 可用作高压发电系统的绝缘气体,分子呈正八面体结构,如图所示。有关SF
6 6
的说法正确的是
A.是非极性分子 B.键角 都等于90°
C. 与 之间共用电子对偏向S D. 原子满足8电子稳定结构
【答案】A
【解析】A.结构对称、正负电荷重心重合的分子为非极性分子,SF 分子呈正八面体结构,S 原子位于正
6
八面体的中心,该分子结构对称、正负电荷重心重合,所以为非极性分子,A正确;B.SF 是结构对
6
称、正负电荷重心重合的分子,故键角 不都等于90°,B错误;C.由于F的电负性比S的大,S
与F之间共用电子对偏向F,C错误;D.中心元素价电子数+化合价的绝对值=8时该分子中所有原子
都达到8电子稳定结构,但氢化物除外,该化合物中S元素化合价+价电子数=6+6=12,则S原子不是
8电子稳定结构,D错误;故答案为:A。
13.(2021·海南真题)关于 性质的解释合理的是
选项 性质 解释
A 比 容易液化 分子间的范德华力更大
B 熔点高于 键的键能比 大
C 能与 以配位键结合 中氮原子有孤电子对
D 氨水中存在 是离子化合物
【答案】C【解析】A. 和 都属于同一主族是氢化物,分子晶体的沸点与其相对分子质量成正比,但氨气中
含有氢键, PH 不含氢键,氢键的存在导致氨气的沸点升高,故A错误;B. 熔点高于 ,是
3
因为氨气中含有氢键,氢键的存在导致氨气的熔点升高,不是 键的键能比 大,故B错误;
C. 中氮原子有孤电子对,使 和 以配位键结合形成[Ag(NH)]+,故C正确;D.
3 2
是共价化合物,是弱碱,在水溶液中部分电离出 和OH-,故D错误;答案选C。
14.【2022年上海卷】二氧化碳在一定条件下可以转化为乙酸,下列有关二氧化碳性质的说法正确的是
A.为共价化合物B.为电解质 C.为折线形分子 D.含非极性共价键
【答案】A
【解析】A.二氧化碳的结构式为 ,只含共价键,为共价化合物,故A正确;B.二氧化碳自身
不能电离,为非电解质,故B错误;C.二氧化碳为直线形分子,故C错误;D.二氧化碳分子中含
有碳氧双键,为极性共价键,故D错误;选A。
15.(2021·湖北真题)下列有关N、P及其化合物的说法错误的是
A.N的电负性比P的大,可推断NCl 分子的极性比PCl 的大
3 3
B.N与N的π键比P与P的强,可推断N≡N的稳定性比P≡P的高
C.NH 的成键电子对间排斥力较大,可推断NH 的键角比PH 的大
3 3 3
D.HNO 的分子间作用力较小,可推断HNO 的熔点比HPO 的低
3 3 3 4
【答案】A
【解析】A.P和Cl的电负性差值比N和Cl的电负性差值大,因此PCl 分子的极性比NCl 分子极性大,A
3 3
项错误;B.N与N的 键比P与P的强,故 的稳定性比 的高,B项正确;C.N的电负性
比P大,NH 中成键电子对距离N比PH 中成键电子对距离P近,NH 中成键电子对间的斥力大,因
3 3 3
此NH 的键角比PH 的大,C项正确;D.相对分子质量:HNO0,B错误;C.实验②
加水稀释,溶液变为粉红色,加水稀释,溶液的体积增大,[Co(H O) ]2+、[CoCl ]2-、Cl-浓度都减小,
2 6 4
[Co(H O) ]2+、Cl-的化学计量数之和大于[CoCl ]2-的化学计量数,则瞬时浓度商>化学平衡常数,平衡逆
2 6 4
向移动,C错误;D.实验③加入少量ZnCl 固体,溶液变为粉红色,说明Zn2+与Cl-结合成更稳定的
2
[ZnCl ]2-,导致溶液中c(Cl-)减小,平衡逆向移动,则由此说明稳定性:[ZnCl ]2->[CoCl ]2-,D正确;
4 4 4答案选D。
24.(2020·山东高考真题)下列关于C、Si及其化合物结构与性质的论述错误的是
A.键能 、 ,因此C H 稳定性大于Si H
2 6 2 6
B.立方型SiC是与金刚石成键、结构均相似的共价晶体,因此具有很高的硬度
C.SiH 中Si的化合价为+4,CH 中C的化合价为-4,因此SiH 还原性小于CH
4 4 4 4
D.Si原子间难形成双键而C原子间可以,是因为Si的原子半径大于C,难形成 键
【答案】C
【解析】A.因键能C—C>Si—Si、C—H>Si—H,H 的键能总和大于Si H,键能越大越稳定,H 的稳
2 6 2 6 2 6
定性大于Si H,A正确;B.SiC的成键和结构与金刚石类似均为原子晶体,金刚石的硬度很大,类
2 6
比可推测SiC的硬度和很大,B正确;C.SiH 中Si的化合价为-4价,C的非金属性强于Si,则C的
4
氧化性强于Si,则Si的阴离子的还原性强于C的阴离子,则SiH 的还原性较强,C错误;D.Si原子
4
的半径大于C原子,在形成化学键时纺锤形的p轨道很难相互重叠形成π键,故Si原子间难形成双键,
D正确;故选C。
25.(2018·上海高考真题)下列有关二氧化碳的描述正确的是( )
A.含有非极性键 B.是直线形分子
C.属于极性分子 D.结构式为C=O=O
【答案】B
【解析】A.二氧化碳分子中碳原子和氧原子形成极性共价键,不含有非极性共价键,错误;B.二氧化碳
分子中中心原子的价层电子对数为 ,不含有孤对电子,为sp杂化,空间构型为直线形,
是直线形分子,正确;C.二氧化碳为直线形分子,二氧化碳分子是对称结构,正负电中心重合,是
非极性分子,错误;D.二氧化碳分子的中心原子是C,故其结构简式应为O=C=O,错误;答案选
B。
26.(2015·上海高考真题)下列有关物质性质的比较,错误的是
A.溶解度:小苏打 < 苏打 B.密度:溴乙烷 > 水
C.硬度:晶体硅 < 金刚石 D.碳碳键键长:乙烯 > 苯
【答案】D
【解析】A.在碳酸钠饱和溶液中通入二氧化碳生成碳酸氢钠,可观察到溶液变浑浊,说明碳酸钠溶解度
大于碳酸氢钠,正确;B.卤代烃的密度比水大,则溴乙烷的密度大于水,正确;C.晶体硅与金刚石
都为原子晶体C-C>Si-Si,原子晶体中,键长越短,键能越大,则硬度越大,正确;D.苯中碳碳键
介于单键和双键之间,碳碳键键长:乙烯<苯,错误;故选D。