文档内容
专题41 反应热计算——键能
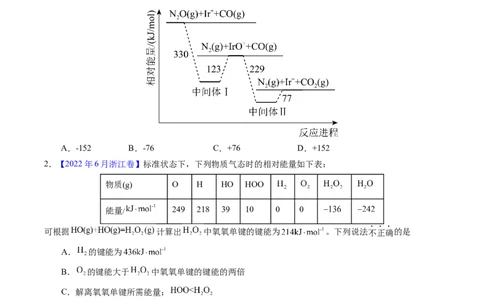
1.【2021年重庆卷】“天朗气清,惠风和畅。”研究表明,利用Ir+可催化消除大气污染物NO和CO,
2
简化中间反应进程后,相对能量变化如图所示。已知CO(g)的燃烧热 H = -283 kJ·mol-1,则
2NO(g)=2N (g) + O(g)的反应热 H (kJ·mol-1)为
2 2 2 ∆
∆
A.-152 B.-76 C.+76 D.+152
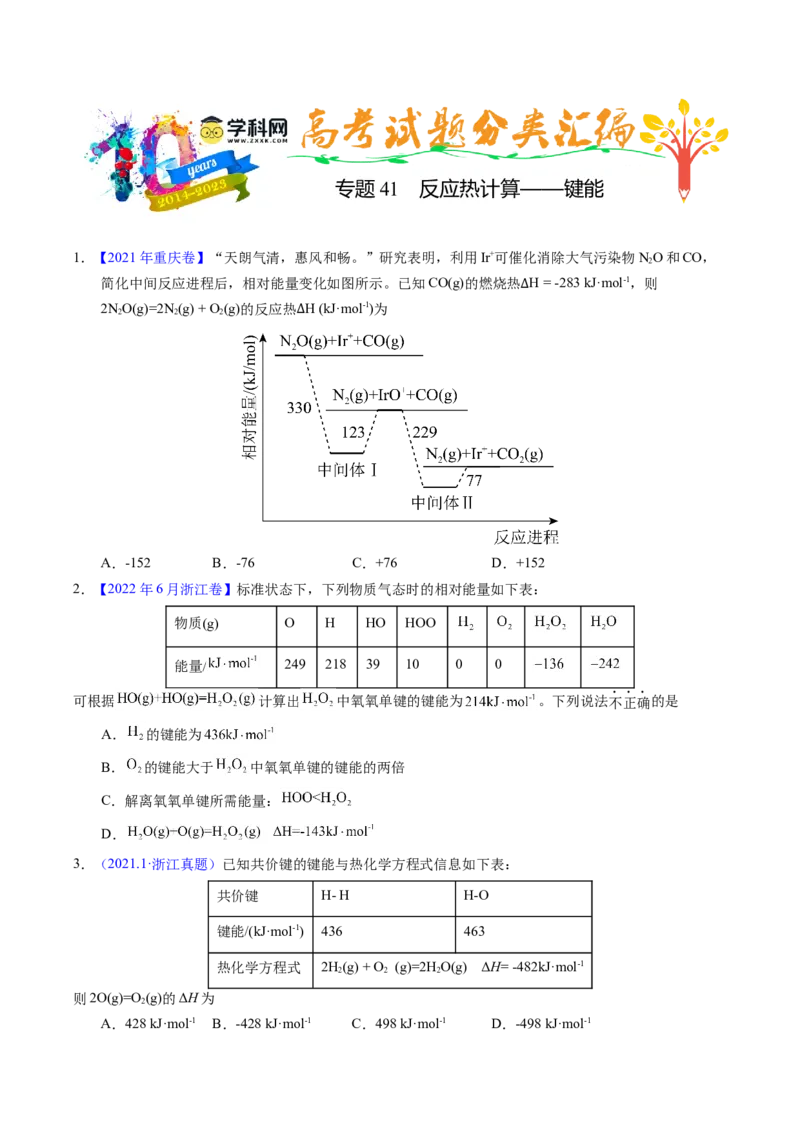
2.【2022年6月浙江卷】标准状态下,下列物质气态时的相对能量如下表:
物质(g) O H HO HOO
能量/ 249 218 39 10 0 0
可根据 计算出 中氧氧单键的键能为 。下列说法不正确的是
A. 的键能为
B. 的键能大于 中氧氧单键的键能的两倍
C.解离氧氧单键所需能量:
D.
3.(2021.1·浙江真题)已知共价键的键能与热化学方程式信息如下表:
共价键 H- H H-O
键能/(kJ·mol-1) 436 463
热化学方程式 2H(g) + O (g)=2HO(g) ΔH= -482kJ·mol-1
2 2 2
则2O(g)=O (g)的ΔH为
2
A.428 kJ·mol-1 B.-428 kJ·mol-1 C.498 kJ·mol-1 D.-498 kJ·mol-14.(2010·湖南高考真题)己知: 与 反应的 ; 与
反应的 。则 在水溶液中电离的 等于
A. B.
C. D.
5.(2016·海南高考真题)油酸甘油酯(相对分子质量884)在体内代谢时可发生如下反应:C H O(s)
57 104 6
+80O (g)=57CO(g)+52HO(l)。已知燃烧1kg该化合物释放出热量3.8×104kJ。油酸甘油酯的燃烧热
2 2 2
△H为
A.3.8×104kJ·mol-1 B.-3.8×104kJ·mol-1
C.3.4×104kJ·mol-1 D.-3.4×104kJ·mol-1
6.(2019·海南高考真题)根据图中的能量关系,可求得 的键能为( )
A. B. C. D.
7.(2015·海南高考真题)已知丙烷的燃烧热△H=-2215kJ·mol-1,若一定量的丙烷完全燃烧后生成1.8g水,
则放出的热量约为( )
A.55 kJ B.220 kJ C.550 kJ D.1108 kJ
8.(2014·重庆高考真题)已知: ;
, 、 和 键的键能 分
别为436、496和462,则a为( )
A. B. C. D.
9.(2008·海南高考真题)白磷与氧可发生如下反应:P+5O =P O 。已知断裂下列化学键需要吸收的能
4 2 4 10
量分别为:P—P akJ·mol—1、P—O bkJ·mol—1、P=O ckJ·mol—1、O=O dkJ·mol—1。
根据图示的分子结构和有关数据估算该反应的△H,其中正确的是( )
A.(6a+5d-4c-12b)kJ·mol—1
B.(4c+12b-6a-5d)kJ·mol—1
C.(4c+12b-4a-5d)kJ·mol—1D.(4a+5d-4c-12b)kJ·mol—1
10.(2009·全国高考真题)已知:2H(g)+ O (g)=2HO(l) ΔH=-571.6kJ· mol-1
2 2 2
CH(g)+ 2O (g)=CO(g)+2HO(l) ΔH=-890kJ· mol-1
4 2 2 2
现有H 与CH 的混合气体112L(标准状况),使其完全燃烧生成CO 和HO(l),若实验测得反应放热
2 4 2 2
3695kJ,则原混合气体中H 与CH 的物质的量之比是( )
2 4
A.1∶1 B.1∶3 C.1∶4 D.2∶3
11.(2009·海南高考真题)已知: (1)Fe O(s)+ C(s)= CO(g)+2Fe(s),ΔH=+234.1kJ•mol-1
2 3 2
则 的ΔH是( )
A.-824.4 kJ•mol-1 B.-627.6kJ•mol-1 C.-744.7kJ•mol-1 D.-169.4kJ•mol-1
12.(2013·重庆高考真题)已知:P(s)+6Cl(g)=4PCl (g) ΔH=akJ·mol-1
4 2 3
P(s)+10Cl(g)=4PCl (g) ΔH= bkJ·mol-1
4 2 5
P 具有正四面体结构,PCl 中P-Cl键的键能为ckJ·mol-1,PCl 中P-Cl键的键能为1.2ckJ·mol-1
4 5 3
下列叙述正确的是( )
A.P-P键的键能大于P-Cl键的键能
B.可求Cl(g)+PCl (g)=PCl (s)的反应热ΔH
2 3 5
C.Cl-Cl键的键能 kJ·mol-1
D.P-P键的键能为 kJ·mol-1
13.(2013·福建高考真题)某科学家利用二氧化铈(CeO)在太阳能作用下将HO、CO 转变成H、
2 2 2 2
CO。其过程如下:
mCeO (m-x)CeO ·xCe+xO ,(m-x)CeO ·xCe+xH O+ xCO mCeO + xH + xCO
2 2 2 2 2 2 2 2
下列说法不正确的是
A.该过程中CeO 没有消耗
2
B.该过程实现了太阳能向化学能的转化
C.右图中△H=△H+△H
1 2 3
D.以CO和O 构成的碱性燃料电池的负极反应式为CO+4OH--2e-=CO 2-+2H O
2 3 2
14.(2010·全国高考真题)下面均是正丁烷与氧气反应的热化学方程式(25°,101kPa):①
②
③
④
由此判断,正丁烷的燃烧热是
A.-2878kJ/mol B.-2658kJ/mol C.-1746kJ/mol D.-1526kJ/mol
15.(2007·重庆高考真题)已知1 g氢气完全燃烧生成水蒸气时放出热量121 kJ,且氧气中1 mol O=O键
完全断裂时吸收热量496 kJ,水蒸气中1mol H-O键形成时放出热量463 kJ,则氢气中1mol H-H键断
裂时吸收热量为
A.920 kJ B.557 kJ C.436 kJ D.188 kJ
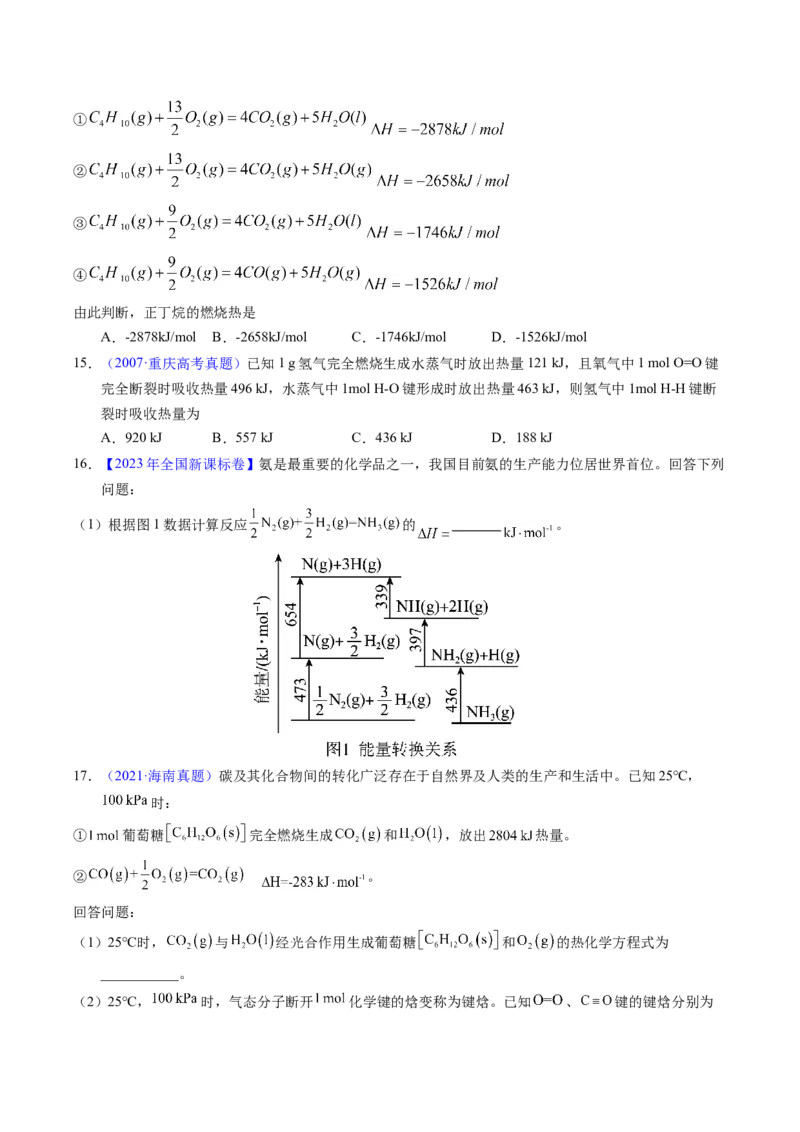
16.【2023年全国新课标卷】氨是最重要的化学品之一,我国目前氨的生产能力位居世界首位。回答下列
问题:
(1)根据图1数据计算反应 的 。
17.(2021·海南真题)碳及其化合物间的转化广泛存在于自然界及人类的生产和生活中。已知25℃,
时:
① 葡萄糖 完全燃烧生成 和 ,放出 热量。
② 。
回答问题:
(1)25℃时, 与 经光合作用生成葡萄糖 和 的热化学方程式为
___________。
(2)25℃, 时,气态分子断开 化学键的焓变称为键焓。已知 、 键的键焓分别为、 , 分子中碳氧键的键焓为___________ 。
18.(2021·湖北真题)丙烯是一种重要的化工原料,可以在催化剂作用下,由丙烷直接脱氢或氧化脱氢制
备。
反应Ⅰ(直接脱氢):C H(g)=C H(g)+H(g)△H=+125kJ·mol-1
3 8 3 6 2 1
反应Ⅱ(氧化脱氢):C H(g)+ O(g)=C H(g)+HO(g)△H=-118kJ·mol-1
3 8 2 3 6 2 2
(1)已知键能:E(C—H)=416kJ·mol-1,E(H—H)=436kJ·mol-1,由此计算生成1mol碳碳π键放出的能量为
___kJ。
19.【2022年海南卷】某空间站的生命保障系统功能之一是实现氧循环,其中涉及反应:
回答问题:
(1)已知:电解液态水制备 ,电解反应的 。由此计算 的燃烧热(焓)
_______ 。
20.(2021·湖南真题)氨气中氢含量高,是一种优良的小分子储氢载体,且安全、易储运,可通过下面两
种方法由氨气得到氢气。
方法I:氨热分解法制氢气
相关化学键的键能数据
化学键
键能 946 436.0 390.8
一定温度下,利用催化剂将 分解为 和 。回答下列问题:
(1)反应 _______ ;
21.(2021·广东真题)我国力争于2030年前做到碳达峰,2060年前实现碳中和。CH 与CO 重整是CO
4 2 2
利用的研究热点之一。该重整反应体系主要涉及以下反应:
a)CH(g)+CO (g) 2CO(g)+2H(g) ∆H
4 2 2 1
b)CO(g)+H(g) CO(g)+HO(g) ∆H
2 2 2 2
c)CH(g) C(s)+2H(g) ∆H
4 2 3
d)2CO(g) CO(g)+C(s) ∆H
2 4
e)CO(g)+H(g) HO(g)+C(s) ∆H
2 2 5
(1)根据盖斯定律,反应a的∆H=_______(写出一个代数式即可)。
1
22.(2020·浙江高考真题)研究 氧化 制 对资源综合利用有重要意义。相关的主要化学反
应有:
ⅠⅡ
Ⅲ
Ⅳ
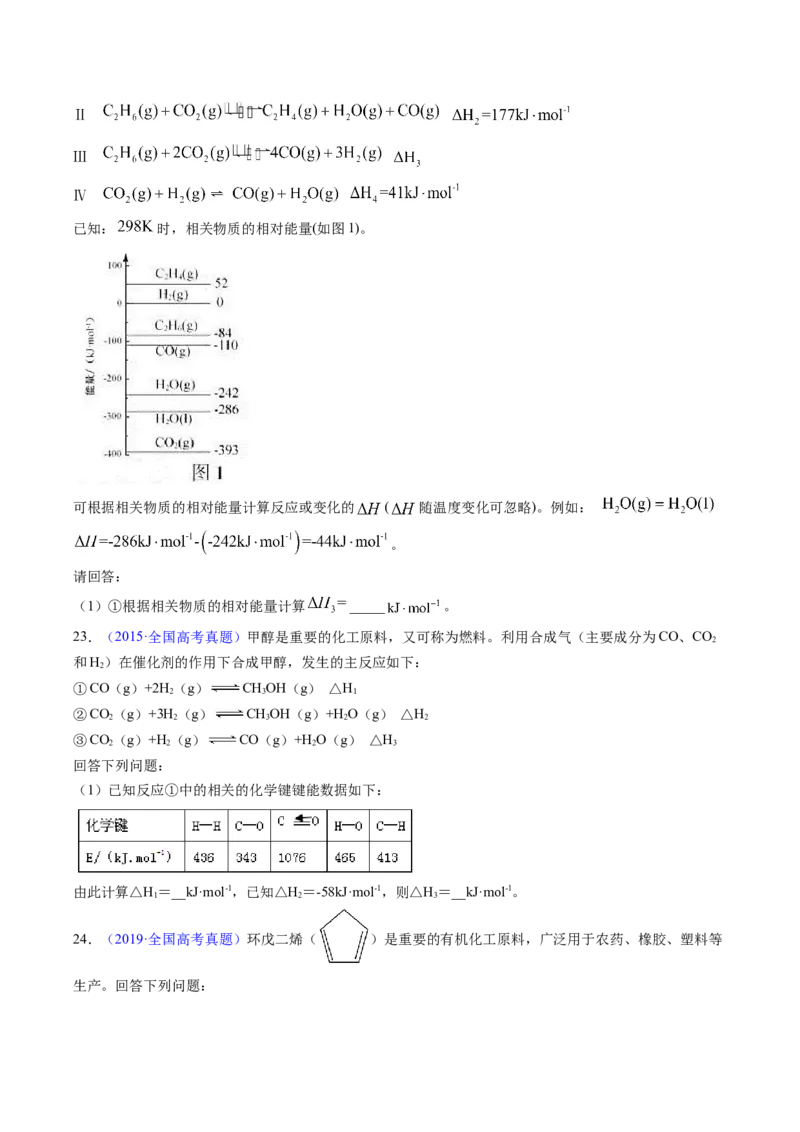
已知: 时,相关物质的相对能量(如图1)。
可根据相关物质的相对能量计算反应或变化的 ( 随温度变化可忽略)。例如:
。
请回答:
(1)①根据相关物质的相对能量计算 _____ 。
23.(2015·全国高考真题)甲醇是重要的化工原料,又可称为燃料。利用合成气(主要成分为CO、CO
2
和H)在催化剂的作用下合成甲醇,发生的主反应如下:
2
①CO(g)+2H (g) CHOH(g) △H
2 3 1
②CO(g)+3H (g) CHOH(g)+H O(g) △H
2 2 3 2 2
③CO(g)+H (g) CO(g)+H O(g) △H
2 2 2 3
回答下列问题:
(1)已知反应①中的相关的化学键键能数据如下:
由此计算△H=__kJ·mol-1,已知△H=-58kJ·mol-1,则△H=__kJ·mol-1。
1 2 3
24.(2019·全国高考真题)环戊二烯( )是重要的有机化工原料,广泛用于农药、橡胶、塑料等
生产。回答下列问题:(1)已知: (g)= (g)+H(g) ΔH=100.3 kJ·mol −1 ①
2 1
H(g)+ I (g)=2HI(g) ΔH=﹣11.0 kJ·mol −1 ②
2 2 2
对于反应: (g)+ I (g)= (g)+2HI(g) ③ ΔH=___________kJ·mol −1。
2 3
25.(2020·浙江高考真题)100 mL 0.200 mol⋅L-1CuSO 溶液与1.95g锌粉在量热计中充分反应。测得
4
反应前温度为20.1℃,反应后最高温度为30.1℃。
已知:反应前后,溶液的比热容均近似为4.18J⋅g-1
⋅℃
-1、溶液的密度均近似为1.00g⋅cm-3,忽略溶
液体积、质量变化和金属吸收的热量。请计算:
(1)反应放出的热量Q=_____J。
(2)反应Zn(s)+CuSO (aq)=ZnSO (aq)+Cu(s)的ΔH=______kJ⋅mol-1(列式计算)。
4 4